


2. 贵州省人民医院干医科,贵州 贵阳 550002
2. General Ward, Guizhou Provincial People's Hospital, Guiyang 550002, China
微血管内皮细胞具有多种重要的生理功能,其功能失调和损伤在诸多病征中扮演了重要角色[1-2]。许多因素会导致内皮细胞损伤,其中补体旁路的过度激活会引起微血管内皮细胞的炎症反应,上调黏附分子、炎症介质等表达,进而介导炎症和组织损伤[3-5]。绿原酸是中药民族药中常见的成分,具有抗炎等多种活性,除本身具有药理活性外,其代谢产物咖啡酸、阿魏酸也是其发挥药理活性的重要物质基础[6]。目前尚不清楚绿原酸及其代谢产物咖啡酸、阿魏酸对补体旁路激活导致的微血管内皮细胞炎症反应是否有干预作用。本文基于代谢组学角度研究了绿原酸及其代谢产物咖啡酸、阿魏酸对补体旁路激活引起的微血管内皮细胞炎症反应的干预作用。
1 材料与方法 1.1 材料人微血管内皮细胞株(HMEC)由本实验室传代培养,RPMI 1640培养基为美国Gibco公司产品,胎牛血清为杭州四季青生物工程材料有限公司产品;人ICAM-1 (intracellular adhesion molecular-1)、IL-6 (interleukin-6)、IL-8 (interleukin-8) ELISA检测试剂盒购自武汉博士德生物工程有限公司;人t-PA (tissue plasminogen activator)、PAI-1(plasminogen activator inhibitor-1)检测试剂盒购自美国Assaypro公司;绿原酸(chlorogenic acid,CGA)、咖啡酸(caffeic acid,CA)、阿魏酸(ferulic acid,FA)购自美国Sigma公司;眼镜蛇毒因子(cobra venom factor,CVF)由本实验室制备,其分离纯化和检测方法参照文献[7];正常人血清(normal human serum,NHS)由本实验室健康志愿者献血制备,混合血清分装后于-80℃冻存,经补体活性检测,备用;灭活人血清(inactive normal human serum,INHS)由NHS于56 ℃水浴灭活30 min制备;其余试剂均为符合实验要求的分析纯。
1.2 主要仪器Forma 3111 CO2培养箱和Revco超低温冰箱(美国Thermo公司);Nikon TS100倒置相差显微镜(日本Nikon公司);Molecular Devices Spectra MAX-190连续波长酶标仪(美国MD公司);5810R冷冻离心机(德国Eppendorf公司);Elix纯水系统和Milli-Q超纯水系统(美国Millipore公司)。
1.3 方法 1.3.1 细胞培养人微血管内皮细胞株HMEC由本实验室传代培养,用含10%胎牛血清的RPMI 1640培养基于37 ℃,5% CO2和饱和湿度培养箱进行培养,收集对数生长期的细胞进行实验。
1.3.2 补体旁路激活产物的制备参照文献[7]方法,将CVF (6.5×104 U·L-1)与NHS等比例混合,37℃水浴30 min,制备NHS的CVF激活产物(CVF-activated complement,CAC)。实验同时制备CVF与INHS的混合孵育物作为对照。
1.3.3 CAC对HMEC表达黏附分子的影响将HMEC以1×104 cells·well-1接种于96孔细胞培养板,培养24 h后弃上清,加入140 μL无血清RPMI1640培养基,再加入60μL CAC至200 μL,分别取1、6、12、24 h孵育上清离心后,按照试剂盒说明书测定ICAM-1。实验设置CVF与INHS的混合孵育物作为对照。
1.3.4 CAC对HMEC表达炎症因子的影响将HMEC以1×105 cells·well-1接种于24孔细胞培养板,培养24 h后弃上清,后续操作同1.3.3,分别孵育12、24、48 h, 取上清离心后,按试剂盒说明书步骤测定IL-6、IL-8。
1.3.5 CAC对HMEC表达纤溶相关蛋白分子的影响将HMEC以1×104 cells·well-1接种于96孔细胞培养板,培养24 h后弃上清,后续操作同1.3.3,取1、6、12、24 h上清离心后,按照试剂盒说明书测定t-PA、PAI-1。
1.3.6 CGA、CA和FA对CAC刺激HMEC表达ICAM-1、t-PA、PAI-1的影响将HMEC以1×104 cells·well-1接种于96孔细胞培养板,培养24 h后弃上清,加入不同浓度CGA、CA、FA的无血清RPMI 1640培养基140 μL预处理细胞1 h,再加入60 μL CAC,孵育不同时间,取6h时间组的培养上清用于检测ICAM-1,取12 h时间组的上清检测t-PA和PAI-1。
1.3.7 CGA、CA和FA对CAC刺激HMEC表达IL-6、IL-8的影响将HMEC以1×105 cells·well-1,接种于24孔细胞培养板,培养24h后弃上清,后续操作同1.3.6,孵育48 h取上清离心后测定IL-6、IL-8。
1.3.8 统计学分析实验数据以x±s表示,采用SPSS 19.0软件进行单因素方差分析,组间多重比较采用LSD法。
2 结果 2.1 CAC对HMEC表达黏附分子、炎症介质、纤溶功能分子的影响CAC作用于HMEC后导致了ICAM-1的表达上调,在6 h时间点检测到表达的高峰,与之前的结果类似[7];IL-6浓度随作用时间延长逐渐升高,在48 h时间点其浓度明显升高(P < 0.01);而IL-8的浓度在24h时间点检测到明显的升高(P < 0.05),到48 h时,与对照组相比,其表达进一步上调(P < 0.01);纤溶功能分子t-PA、PAI-1的表达均持续上调(P < 0.05或P < 0.01),其中在1h时间点的t-PA/PAI-1比值有一个明显的上调,与之前的结果类似[8]。上述结果表明本研究成功复制了CAC诱导的HMEC炎症反应模型。
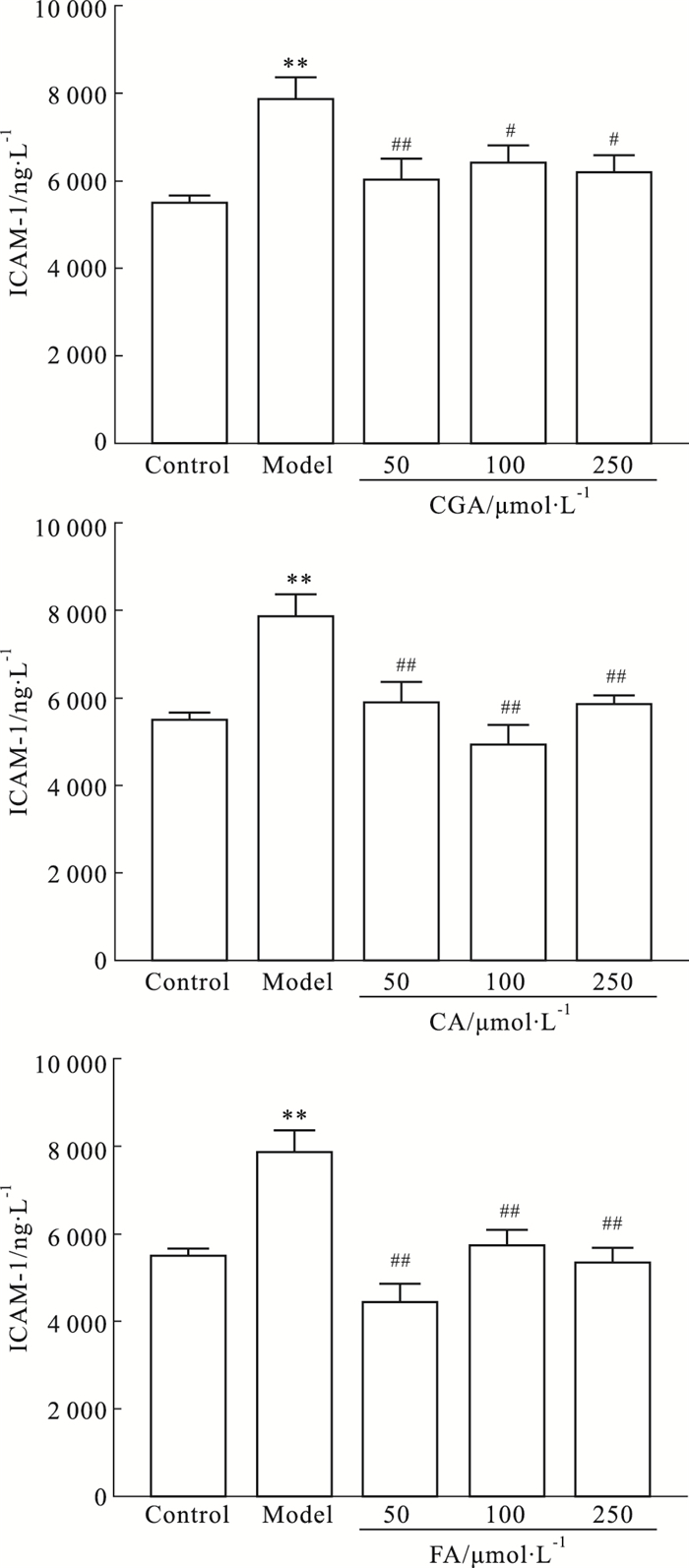
2.2 CGA、CA和FA对HMEC表达黏附分子、炎症介质及纤溶功能分子的影响 2.2.1 CGA、CA和FA对HMEC表达ICAM-1的影响结果显示,50、100和250 μmol·L-1的CGA、CA和FA均能有效抑制ICAM-1的表达,与模型组相比差异有显著性(P < 0.05或P < 0.01), Fig 1。
|
| Fig 1 Effect of CGA, CA, and FA with different concentrations on ICAM-1 expression of HMEC induced by CAC for 6 h (n=3) **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs model |
结果表明,50、100和250 μmol·L-1的CGA、FA预处理内皮细胞后,可降低IL-6的表达,其中250 μmol·L-1时,与模型组相比差异有统计学意义(P < 0.05或P < .01),而不同浓度的CA对IL-6的表达均有明显的抑制作用(P < 0.01), 见Fig 2。

|
| Fig 2 Effect of CGA, CA, and FA with different concentrations on IL-6 expression of HMEC induced by CAC for 48 h (n=3) **P < 0.01, *P < 0.05 vs control; #P < 0.05, ##P < 0.01 vs model |
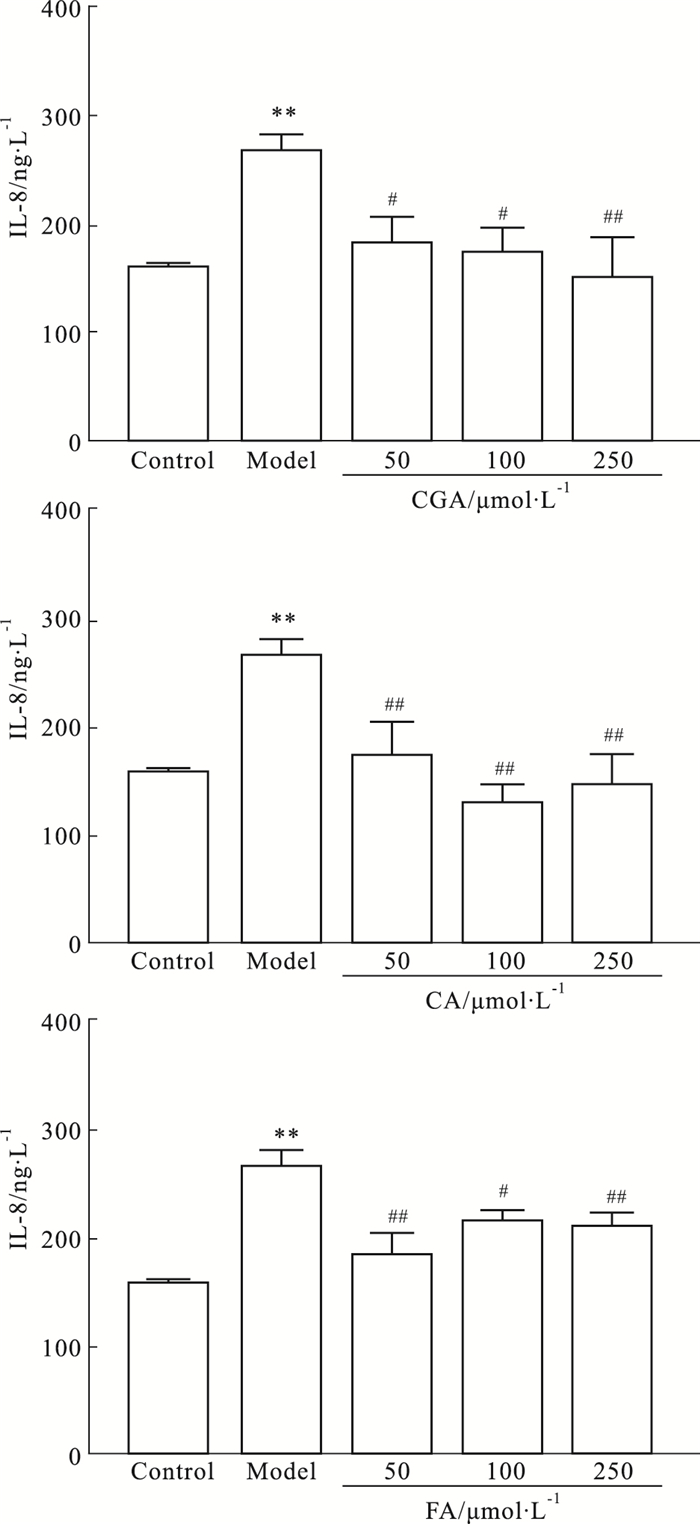
结果表明,HMEC经50、100和250 μmol·L-1的CGA、CA和FA预处理后,其IL-8的表达明显下调,与模型组相比差异有统计学意义(P < 0.05或P < 0.01),见Fig 3。
|
| Fig 3 Effect of CGA, CA, and FA with different concentrations on IL-8 expression of HMEC induced by CAC for 48 h (n=3) **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs model |
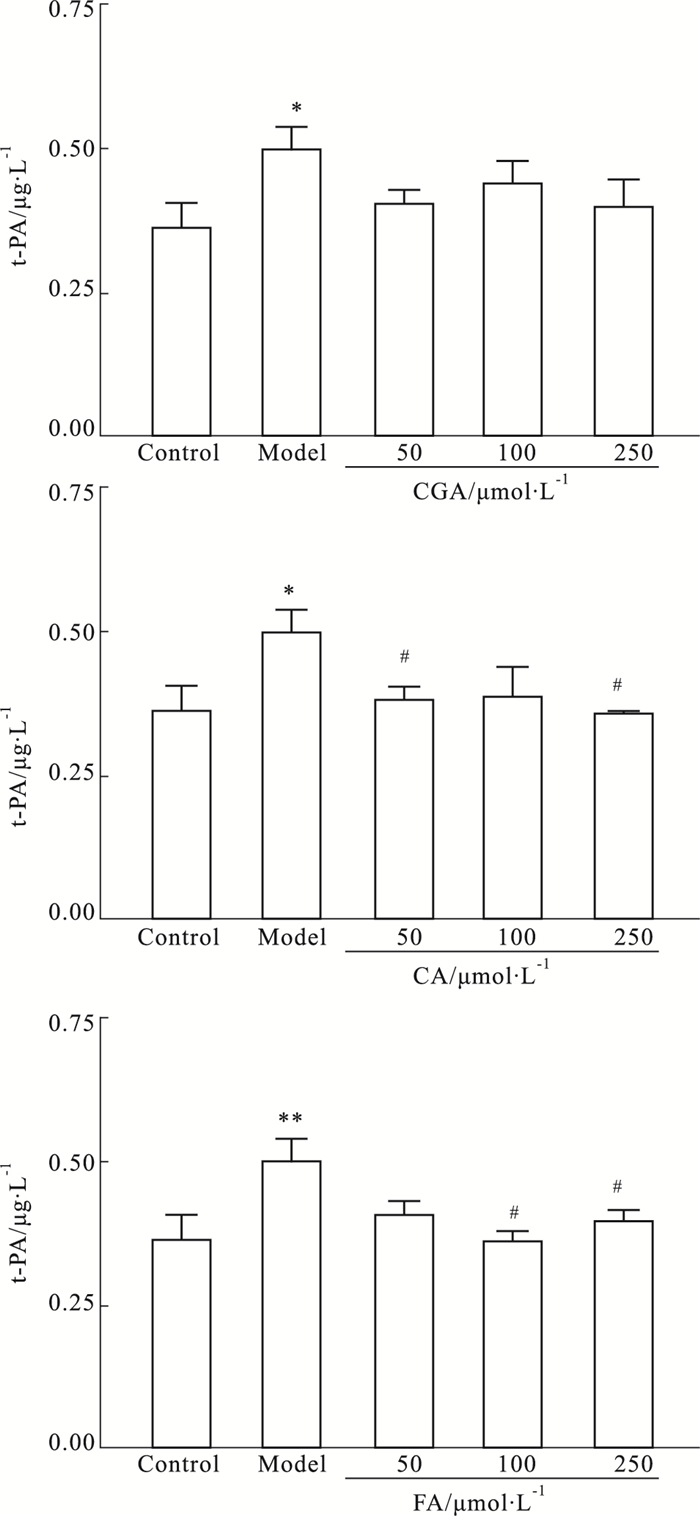
结果显示,50、100和250 μmol·L-1的CGA、CA和FA对t-PA的表达有抑制作用,其中,CA的作用相对较明显,见Fig 4。
|
| Fig 4 Effect of CGA, CA, and FA with different concentrations on t-PA expression of HMEC induced by CAC for 12 h (n=4) *P < 0.05, **P < 0.01 vs control, #P≤0.05 vs model |
不同浓度的CGA、CA和FA对PAI-1的表达均有抑制作用,其中,在50、100 μmol·L-1时,与模型组相比差异均有统计学意义(P < 0.05或P < 0.01),见Fig 5。

|
| Fig 5 Effect of CGA, CA, and FA with different concentrations on PAI-1 expression of HMEC induced by CAC for 12 h (n=4) **P < 0.01 vs control, #P < 0.05, ##P < 0.01 vs model |
补体旁路途径在机体天然防御系统中具有重要的生理功能,但在诸多病理情况下,补体旁路的过度激活会引发炎症和损伤,其中补体旁路激活诱导的微血管内皮细胞炎症反应在炎症启动和放大的环节中扮演了重要角色。CGA作为一种在食材和药材中较为常见的多酚类化合物,具有抗炎、抗氧化等多种药理活性[6]。其代谢产物CA、FA等也是其发挥药理活性的重要物质基础。因此,本文从代谢组学的角度,研究了CGA、CA和FA对补体旁路激活诱导微血管内皮细胞炎症反应的干预作用,以期从新的角度认识和挖掘CGA及其代谢产物CA、FA的药理药效作用。
CAC的刺激会导致HMEC出现活化和后续的炎症反应[7-9]。在本研究中可以看到,HMEC受到CAC刺激后,ICAM-1、IL-6、IL-8、t-PA和PAI-1的表达均出现上调。其中,ICAM-1在6 h时达到峰值,IL-8和IL-6的上调分别在24h和48h检测点出现明显变化,而衡量纤溶功能的t-PA/PAI-1比值在1 h时有明显上调。ICAM-1是介导中性粒细胞和内皮细胞黏附、聚集、浸润的重要黏附分子,IL-6和IL-8则是重要的炎症介质,而t-PA和PAI-1以及t-PA/PAI-1比值的变化则与炎症中的纤溶凝血功能异常密切相关。它们在炎症的发展中扮演了重要角色。上述分子的表达上调提示了HMEC在受到CAC刺激后,出现了炎性反应状态。
采用CGA、CA和FA对上述炎症反应的干预实验表明,50、100、250 μmol·L-1的CGA、CA、FA对ICAM-1、IL-6、IL-8、t-PA和PAI-1的上调表达具有不同程度的抑制作用。其中,CGA、CA、FA对ICAM-1和IL-8的抑制作用最为明显。而综合各指标来看,CA的干预作用最好,其次为FA。本研究表明了CGA、CA、FA对补体旁路激活导致的HMEC炎症反应有一定的干预作用,而它们在干预作用上的差别则为进一步开展机制研究提供了线索和依据。CGA、CA、FA具有多样的生物学活性,本研究的结果进一步丰富和拓展了对CGA、CA、FA药理药效作用的认识和理解。
本研究表明了天然活性分子绿原酸、咖啡酸和阿魏酸对补体旁路激活导致的微血管内皮细胞炎症反应有一定的干预作用,为进一步深入挖掘绿原酸、咖啡酸和阿魏酸的药理药效作用及调控机制提供了参考依据。
( 致谢: 本文实验是在贵州省中国科学院天然产物化学重点实验室药理与生物活性研究中心孙黔云研究员实验室完成。 )
| [1] | Rajendran P, Rengarajan T, Thangavel J, et al. The vascular endothelium and human diseases[J]. Int J Biol Sci, 2013, 9 (10). |
| [2] | Ramli J, CalderonArtero P, Block RC, Mousa SA. Novel therapeutic targets for preserving a healthy endothelium: strategies for reducing the risk of vascular and cardiovascular disease[J]. Cardiol J, 2011, 18 (4): 352-63. |
| [3] | 孙黔云. 眼镜蛇毒因子在生命科学中的应用[J]. 生命科学, 2016, 28 (1) : 22-6. Sun Q Y. Application of cobra venom factor in life sciences[J]. Chin Bull Life Sci, 2016, 28 (1): 22-6. |
| [4] | Bosmann M, Ward PA. Role of C3, C5 and anaphylatoxin receptors in acute lung injury and in sepsis[J]. Adv Exp Med Biol, 2012, 946 : 147-59. doi:10.1007/978-1-4614-0106-3 |
| [5] | Takano T, Elimam H, Cybulsky AV. Complement-mediated cellular injury[J]. Semin Nephrol, 2013, 33 (6): 586-601. doi:10.1016/j.semnephrol.2013.08.009 |
| [6] | Wu C, Luan H, Zhang X, et al. Chlorogenic acid protects against atherosclerosis in ApoE-/- mice and promotes cholesterol efflux from RAW264.7 macrophages[J]. PLoS One, 2014, 9 (9): e95452. doi:10.1371/journal.pone.0095452 |
| [7] | 孙黔云, 李敏, 叶巧玲, 李红玲. 补体旁路激活导致内皮细胞的活化和损伤[J]. 中国药理学通报, 2012, 28 (7) : 925-9. Sun Q Y, Li M, Ye Q L, Li H L. Endothelial cell activation and injury induced by complement alternative pathway[J]. Chin Pharma Bull, 2012, 28 (7): 925-9. |
| [8] | 路青瑜, 李敏, 孙黔云. 补体旁路激活致内皮细胞纤溶凝血相关分子表达变化及干预研究[J]. 中国药理学通报, 2015, 31 (8) : 1142-6. Lu Q Y, Li M, Sun Q Y. Expression of coagulation-and fibrinolysis-related molecules of endothelial cells induced by activated complement alternative pathway and intervention[J]. Chin Pharmacol Bull, 2015, 31 (8): 1142-6. |
| [9] | 李红玲, 孙黔云, 李敏, 石京山. 补体旁路激活产物刺激内皮细胞NF-κB、p38MAPK、JAK2通路活化及抑制剂的干预研究[J]. 中国细胞生物学学报, 2013, 35 (6) : 836-41. Li H L, Sun Q Y, Li M, Shi J S. Activation of NF-κB, p38MAPK, and JAK2 in endothelial cells induced by activated complement alternative pathway and intervention by inhibitors[J]. Chin J Cell Biol, 2013, 35 (6): 836-41. |

