


急性肾损伤(acute kidney injury,AKI)是一种常见临床急症,以肾功能迅速下降为临床特点,最终导致急性肾衰竭(acute renal failure,ARF),甚至引起其他器官衰竭。AKI的启动方式很多,如缺血/再灌注、手术对比剂的应用、服用药物不当、横纹肌溶解症、感染等[1-2]。近年来,AKI的发病率不断升高,住院患者AKI发病率达1%~5%,并迅速增长。一旦AKI发生,患者病死率明显增加,重症致死率高达50%以上。据全球肾脏病改善预后委员会指南(kidney disease improving global outcomes,KDIGO)中的数据显示,重症监护室(intensive care unit,ICU)中成人AKI的发病率在16%~67%之间,而成人和儿童中AKI的致死率不断升高[3]。在临床治疗过程中,发生AKI后,患者虽进行肾脏治疗使其功能得到了一定改善,但很难实现完全恢复的治疗目标。AKI的发病率和致死率一直居高不下,并呈逐年增长趋势,给社会经济和公共健康造成了巨大的影响。
尽管科学家一直致力于研发潜在的AKI治疗药物,如红细胞生成素(erythropoietin)、活性C反应蛋白(activated protein C)、他汀类药物、胱冬肽酶抑制剂(caspase inhibitors)及骨髓间充质干细胞(mesenchymal stem cells,MSC)等[4-5],然而很多药物还在基础实验中,尚未用于临床。随着回归自然热潮的兴起,来自于自然界的活性天然产物备受关注[6]。在我国,中草药研究和应用已有几千年的历史,因具有毒副作用小、治疗靶点多和价格低廉等优点,其实用性、有效性和科学性毋庸置疑,如今中药作为补充和替代治疗药物在世界上倍受关注和认可。本文对近年来AKI的发病机制和中药预防和治疗AKI的研究进展作一简要的综述。
1 AKI发病机制AKI是一组临床综合征,按照病因作用于肾组织的不同部位,可分为肾前性、肾后性、肾性。肾前性AKI主要与血容量减少、心输出量减少、肾血管严重收缩、肾动脉机械闭锁等引起的肾脏灌流不足有关;肾后性AKI是指肾盂到尿道任一水平引起的尿道梗阻所导致的AKI;肾性AKI通常指肾实质或肾血管疾病相关性AKI。临床上,AKI的发病机制各异。
1.1 缺血/再灌注损伤与AKI缺血/再灌注损伤(ischemia reperfusion injury,IRI)是临床AKI的重要发病机制,常见于器官移植手术、中毒性休克、弥散性血管内凝血和急性失血等过程中,尤其在器官移植中几乎不可避免,是影响移植肾早期功能恢复和移植排斥反应的主要原因。肾脏为高灌注器官,肾脏缺血后,再灌注时产生大量的ROS,并引发一连串的细胞反应,最终导致肾缺血/再灌注损伤。临床和动物模型研究表明,IRI与大量活性氧产生、细胞内Ca2+超载、炎症反应、细胞凋亡等介导的肾损伤有着密不可分的关系。
1.1.1 大量ROS产生ROS是具有很高生物活性的氧分子,如氧离子(O2-)、含氧自由基、过氧化物(如过氧化氢)等。根据来源不同,分为外源性和内源性。外源性ROS来源于外源性氧化剂(酮类、硝基类等)或外源性刺激因素(药物氧化、光照、电离、热辐射冲击等);内源性ROS来源于生物体细胞内的有氧代谢过程中(黄嘌呤氧化酶代谢、活性中性粒细胞等)[7]。肾组织缺血后再灌注时,机体内产生大量ROS是导致IRI的主要原因之一,具体机制如下:ROS对生物膜造成损害,使其流动性降低、通透性增强,进而导致生物膜功能性障碍(如细胞膜破裂、线粒体膜肿胀溶解、溶酶体膜溶解破裂等);ROS增加引起核酸损伤,可能由于ROS攻击核酸碱基或攻击糖苷键,DNA链断裂,引起细胞功能受损;ROS诱发细胞凋亡,导致细胞内Ca2+迁移,胞质内Ca2+浓度增加,加剧了AKI的发生[8]。
1.1.2 细胞内Ca2+超载细胞内Ca2+超载是缺血/再灌注导致AKI的重要因素,ROS促进Ca2+内流,诱发细胞内Ca2+浓度增加,而Ca2+激活蛋白水解酶和磷脂酶A2促使ROS破坏作用增强,二者相互协同,互相影响,导致肾组织损伤加重[9]。肾脏组织发生缺血后,再灌注期间,Na+,K+-ATP 酶活性降低,促进H+增加,Na+内流,激活Na+/Ca2+互换系统,加重细胞质内Ca2+堆积,导致细胞内离子分布不均衡,影响调控功能,线粒体通透性增强,膜电位下降,促使其功能受损,导致ATP合成受到抑制,能量合成障碍,促发级联损伤反应。此外,胞质内Ca2+浓度升高,激活Ca2+/Mg2+依赖性核酸内切酶,DNA链发生断裂,细胞功能受损,诱导细胞凋亡[10]。由此可见,在肾缺血/再灌注过程中,细胞内Ca2+超载与大量ROS的产生两者之间相互促进,成为加剧肾脏组织急性损伤的关键影响因素。
1.1.3 炎症反应炎症级联反应是缺血/再灌注后导致肾组织功能急性衰退的又一主要原因。缺血/再灌注后可激活炎症细胞、肾内皮细胞,使细胞因子[白细胞介素、趋化性细胞因子、肿瘤坏死因子(tumor necrosis factor,TNF)等]、黏附因子(包括整合素家族、钙黏蛋白家族和免疫球蛋白家族等)的表达增加[11]。TNF-α是触发众多细胞因子启动、乃至全身炎症反应的关键性因子,可直接诱导白细胞介素-1(interleukin-1,IL-1)、白细胞介素-6 (interleukin-6,IL-6)、白细胞介素-8 (interleukin-8,IL-8)等炎症细胞因子大量释放,触发炎症级联反应;同时,也促进黏附因子表达增高,使炎症细胞与内皮细胞间的黏附作用增强,中性粒细胞浸润,白细胞活化并致炎,肥大细胞释放大量炎症介质(嗜酸粒细胞趋化因子、前列腺素D2、白三烯和一些细胞因子等),级联反应将信号一步一步放大,最终造成细胞生理功能紊乱,炎症蔓延[12]。
1.1.4 细胞凋亡缺血/再灌注过程中,肾单位中大量肾小管上皮细胞凋亡,进而发生细胞坏死,这是导致肾脏组织最终发生脏器性功能衰竭的重要原因。凋亡发生时,线粒体外膜破坏,调控线粒体的凋亡信号分子TNF-α、Bax、caspase等诱导细胞凋亡的基因高表达,体内重要的抗凋亡基因Bcl-2表达降低,诱导细胞凋亡[13];Ca2+超载导致的DNA链断裂降解,并诱发肾组织细胞功能性损伤,也参与了缺血/再灌注过程中的细胞凋亡反应;ROS短期内的爆发使线粒体内膜发生脂质过氧化,导致线粒体内膜通透性增加,膜电位下降,使凋亡诱导因子释放,直接或间接地诱导细胞凋亡;同时,炎症因子和黏附因子也会进一步加剧细胞凋亡的发生[14]。因此,肾缺血/再灌注过程中细胞凋亡的发生与大量ROS释放、Ca2+超载、炎症反应等过程相互协同,加剧肾脏组织功能性急性损伤。
1.2 大手术与AKIAKI常见于重大手术(如肝移植手术、冠脉搭桥手术等)和危重症,主要原因是缺乏早期诊断AKI的措施[15-16]。其中,冠脉搭桥手术等心脏手术是导致严重AKI的主要原因,患有急性冠状动脉综合征或是心脏瓣膜病的患者心室功能受损,可能减少心输出量,导致肾灌注受损。肾脏灌流不足是AKI最初的诱因,导致代谢旺盛的肾髓质血流量减少,造成区域性缺氧和低灌注,由于管状缺血和损伤会导致肾小管上皮细胞损伤。术前患者如果不进行AKI预防措施,麻醉等因素甚至会致使心脏失去自动调控功能。而进行肝脏移植手术的患者无论是术前还是术后,AKI的发病机制仍是一个复杂、多层面、颇具争议性的话题,不仅增加患者的医疗费用,且降低患者的生存率。对于原位肝移植手术患者,诱发AKI的因素有很多,如术前因素(肝衰竭、肝肾综合征、腹水),术中因素(失血、低血压、高渗透性高钠血症),术后因素(早期移植物功能障碍、败血症、使用免疫抑制药物和放射造影剂、重复手术)[17]。肝移植手术后早期AKI预测具有滞后性和不准确性,导致患者术后严重肾功能不全,这也是造成患者术后生存率下降,死亡率升高的原因之一[18]。
1.3 横纹肌溶解症与AKI横纹肌溶解症(rhabdomyolysis,RM)是指因多种因素破坏横纹肌细胞膜完整性,内容物漏出入血,包括肌红蛋白、醛缩酶、小分子物质等,其中肌红蛋白对于肾脏的直接损伤是导致AKI的最直接原因[19]。横纹肌的病因多样而复杂,包括获得性病因(过量运动、缺血、代谢紊乱、自身免疫等)和遗传性相关的病因(肌酸磷酸化酶缺陷等)。在病理生理学机制上主要有缺血损伤和ATP耗竭、肌浆网钙调节受损、低钾、组织氧化应激。当出现横纹肌溶解所致AKI病理为急性肾小管坏死,发生机制包括肾小管堵塞、小管氧化物损伤、肾缺血(包括血管收缩及低血容量)[20]。
1.4 脓毒症与AKI脓毒症(sepsis)是因感染引起的全身炎症反应。脓毒症引发系统性细胞因子-趋化因子响应,有可能导致肾脏终末器官损伤。急性肾小管坏死(acute tubular necrosis,ATN)一般是由缺血/再灌注损伤和细胞因子介导的炎症反应共同驱动的脓毒症引起的[21]。在脓毒症发生过程中,肾小管细胞损伤是由于AKI的传播蔓延,肾小管细胞凋亡,胞内线粒体功能异常导致的氧化应激以及局部微循环障碍是系统性脓毒症的应答反应,在脓毒症AKI的病理过程中发挥了重要作用,这是脓毒症肾损伤(sepsis-associated AKI,SA-AKI)的潜在机制。肾脏因调节人体内环境稳定而需消耗大量能量,而脓毒症患者肾脏细胞中线粒体功能异常,导致ATP生成障碍,引起整个机体处于高危状态[22]。
1.5 药物与AKI肾脏是人体的主要排泄器官,大多数药物主要经肾排泄,药物的使用甚至滥用有可能导致药源性AKI,主要源于肾脏具有以下特点:组织血流丰富、耗氧量大、血流量不足、肾髓质逆流倍增机制、肾小管的作用(肾小管重吸收以及pH变化导致药物沉积)、肾小球的结构(与药物接触面积大以及滤过屏障导致大分子药物滞留)等[23]。发病机制包括:直接肾毒性、免疫炎症反应、梗阻性病变、血流动力学影响及代谢紊乱等。主要病理现象包括:肾性-肾小管毒性(氨基糖苷类、两性霉素B、对比剂、抗病毒药、顺铂、可卡因、马兜铃酸等);肾性-间质性肾炎(青霉素、磺胺类、环丙沙星、万古霉素、四环素、利福平、质子泵抑制剂、抗惊厥药物、西咪替丁、利尿剂、可卡因等);肾后性-晶体沉积(阿昔洛韦、磺胺嘧啶、磷甲酸、氨苯蝶啶、麻黄碱等);肾性-肾小球疾病(氨苄西林、利福平、锂盐、青霉胺、肼苯哒嗪、水银、海洛因、干扰素、环孢素、他克莫司等);渗透性病变(静脉免疫球蛋白、淀粉、甘露醇、对比剂等)。这些药源性肾损伤临床表现轻重不一,使用这些药物时需遵循临床用药原则,严格观察用药后不良反应,出现先兆症状应立即采取措施,以避免由于药物的使用或滥用导致AKI。
2 AKI的中药干预目前,仍缺乏有效的AKI预防和治疗药物,欧洲危重病协会肾病学预防和治疗AKI常用的方法有扩容、利尿、血管活性药物的使用、激素的使用、代谢干预、肾脏替代治疗以及血液净化治疗[24]。关于AKI的肾脏替代治疗已有些进展,但死亡率仍居高不下。中药因其自身特点和优势,在预防和治疗AKI 方面具有广阔的应用前景。
2.1 中药复方中药复方是依据君臣佐使原则,选择多味中药(两种或两种以上)按照一定的比例进行配伍而制成方剂。中药复方的优点在于多味中药相互配合、协同作用,降低毒副作用,提高生物利用度,应对疾病的病程和性质复杂多变,提高疗效。陈秀兰等[25]用由黄芪、益智仁、山药、丹参、淫羊藿、太子参、杜仲、芡实、当归、鸡内金10味中药组成的固精丹治疗庆大霉素诱导的AKI,发现该复方通过抗氧化、稳定细胞膜的功能来缓解AKI。张国欣等[26]将由黄芪、益母草、香草、大黄、丹参、冬虫夏草、黄精等中药组成的参黄草合剂应用于临床治疗早期AKI以及庆大霉素诱导的大鼠AKI实验中,发现该中药复方可明显改善肾小管损伤,减轻水肿,使患者尿酶恢复正常,缓解早期肾损伤。孙艳玲等[27]用由红参、附片等中药组成的参附注射液治疗肾缺血/再灌注诱导的大鼠AKI,发现其通过抗脂质过氧化来减轻缺血/再灌注诱导的AKI。严彬等[28]发现由人参、黄芪、川芎、赤勺、田七等中药组成的补气活血中药通过降低血清和肾组织中NO含量,缓解缺血/再灌注诱导的AKI。蔡琪等[29]发现由黄芪、当归等药材组成的黄芪当归合剂可明显降低肾缺血/再灌注大鼠血清肌酐水平,减轻肾组织病变,从而达到治疗缺血/再灌注诱导的AKI的药理学作用。钱风华等[30]发现由生地、黄连、黄芩、丹皮、石膏、栀子、甘草、竹叶、玄参、犀角、连翘、芍药、知母、桔梗等中药组成的清瘟败毒饮,能提高脓毒症患者的AKI治疗效果。
2.2 中药提取物中药提取物是以动、植物等中药材为原料,采用提取分离方法将药材中的有效成分提取出来,定向获取和浓集,最大程度保留有效成分或有效部位,在不改变其有效成分结构的前提下而形成的产品。现代研究发现,许多中药提取物在抗AKI方面具有明显的疗效。相关中药提取物及分子作用机制见Tab 1。
| 中药提取物 | 动物模型 | 可能的分子机制 |
| 胡黄连 | 肾缺血/再灌注损伤大鼠 | 抑制肾脏ICAM-1、MCP-1表达,其作用与其抗氧化、抑制炎症反应有关,改善肾功能 |
| 虎杖 | 肾缺血/再灌注损伤大鼠 | 抑制肾组织中ICAM-1表达,减少血清中TNF-α的含量 |
| 莲子 | 肾缺血/再灌注损伤大鼠 | 抗自由基损伤和减轻脂质过氧化、抗血栓形成来减轻缺血/再灌注对肾组织细胞的损害 |
| 木芙蓉叶 | 肾缺血/再灌注损伤大鼠 | 抑制TNF-α等炎症细胞因子的生成及活性 |
| 人工虫草 | 庆大霉素诱导AKI | 减轻肾损伤,促进修复再生 |
| 山药 | 对乙酰氨基酚诱导AKI | 抑制肾损伤,降低血清BUN、Cr水平,改善肾功能 |
| 五味子 | 肾缺血/再灌注损伤大鼠 | 抗自由基损伤和减轻脂质过氧化 |
| 银杏叶 | 氯化汞诱导AKI | 能明显诱导肾内HO-1的表达,增强肾组织抗氧化能力 |
| 艾氏天芥菜 | 顺铂诱导AKI | 降低MDA水平,升高SOD、CAT水平,缓解肾小管坏死,改善肾功能 |
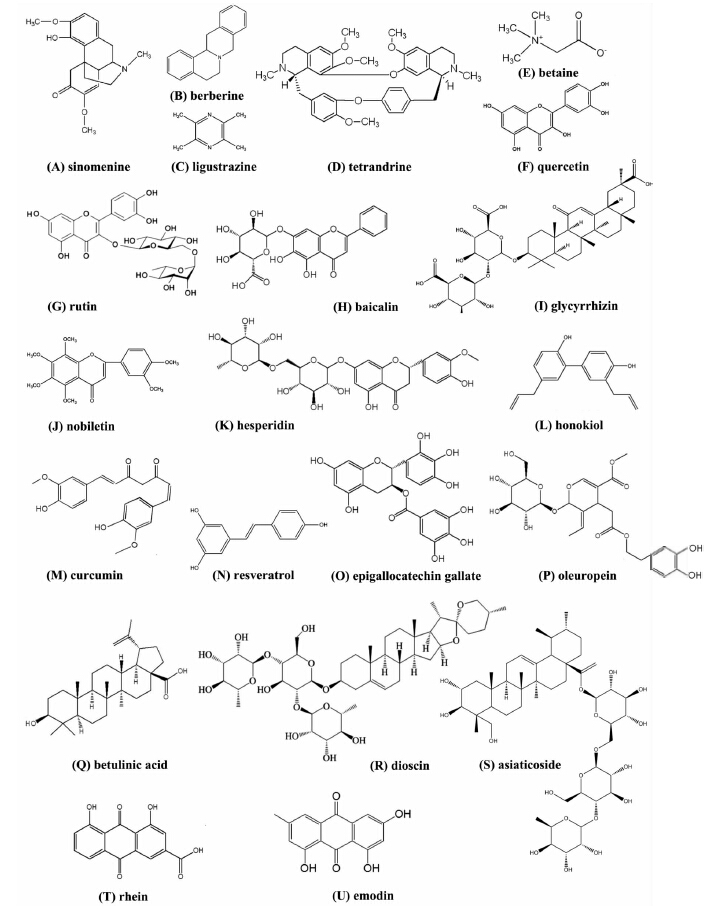
从中药中寻找有效成分是研制治疗AKI的新药的一条重要途径。近年来,中药有效成分在防治肾病方面取得了较大进展。自然界中防治肾损伤的成分有很多,如生物碱类、黄酮类、皂苷类等,相关中药有效成分及分子作用机制见Tab 2,化合物的结构图见Fig 1。
| 成分分类 | 活性成分 | 来源 | 动物模型 | 可能的分子机制 |
| 生物碱类 | 青藤碱(sinomenine)(Fig 1A) | 防已科植物青藤的根和茎,蝙蝠葛叶等 | 梗阻性黄疸急性肾损伤大鼠 | 通过抗氧化作用和抑制转化生长因子-β1(transforming growth factor-β1,TGF-β1)的表达发挥保护作用 |
| 小檗碱(berberine)(Fig 1B) | 小檗科等四个科十个属的许多植物 | 肾缺血/再灌注急性肾损伤大鼠 | 通过抑制氧化应激反应和细胞凋亡来发挥肾脏保护作用 | |
| 川芎嗪(ligustrazine)Fig 1C | 伞形科植物川芎、姜科植物温莪术、大戟科植物痛风麻风树根茎 | 对比剂诱导的急性肾损伤大鼠 | 通过抑制p38丝裂原激活的蛋白激酶(p38 MAPK)和叉头转录因子1(forkhead box O1,FoxO1)信号通路来抑制肾功能紊乱和肾小管细胞凋亡 | |
| 粉防己碱(tetrandrine)Fig 1D | 防己科植物粉防己的块根 | 急性缺血性肾损伤大鼠 | 通过调节肾小管上皮细胞的凋亡水平发挥保护作用 | |
| 甜菜碱(betaine)Fig 1E | 天然植物的根、茎、叶及果实的甜菜糖 | 顺铂诱导的急性肾损伤大鼠 | 可抑制TNF-α和核转录因子kappa B (NF-κB)的表达,以及半胱氨酸天冬氨酸蛋白酶3(caspase-3)的活化,来发挥抑制炎症和凋亡,提高抗氧化能力,缓解急性肾损伤 | |
| 黄酮类 | 槲皮素(quercetin)Fig 1F | 存在于多种植物中,是银杏叶总黄酮的主要成分 | 肾缺血/再灌注急性肾损伤大鼠 | 通过活化AMPK介导的自噬信号通路,发挥抗急性肾损伤的生物学活性 |
| 芦丁(rutin)Fig 1G | 存在于多种植物中 | 肾缺血/再灌注肾损伤大鼠 | 通过抗氧化及抗自由基作用发挥肾损伤保护作用 | |
| 黄芩苷(baicalin)Fig 1H | 唇形科植物黄芩的根茎中 | 肾缺血/再灌注肾损伤大鼠 | 通过减少氧化应激和组织学损伤,改善肾脏功能,抑制促炎反应和管状细胞凋亡,减少Toll样受体2 (TLR2)、Toll样受体4 (TLR4)、髓样分化因子(MyD88)、NF-κB蛋白水平的表达,并减少caspase-3活化,缓解急性肾损伤 | |
| 甘草酸苷(glycyrrhizin) Fig 1I | 中药甘草 | 肾缺血/再灌注肾损伤大鼠 | 通过抑制caspase-3的活化和促炎因子的爆发,发挥抑制炎症反应和肾脏细胞凋亡的作用 | |
| 川陈皮素(nobiletin)Fig 1J | 芸香科川橘果皮、酸橙果皮、柑橘叶茎等 | 顺铂诱导的急性肾损伤大鼠 | 通过抑制凋亡通路的激活和DNA损伤,减轻肾小管损伤,具有抗炎、抗氧化、抗凋亡的生物学活性 | |
| 橙皮苷(hesperidin)Fig 1K | 芸香科柑桔属植物甜橙、柠檬等 | 顺铂诱导的急性肾损伤大鼠 | 通过缓解氧化应激和脂质过氧化反应,减少白细胞浸润和促炎因子的表达,抑制caspase-3活化和DNA损伤,同时增加肾脏中NO的产生,改善肾功能 | |
| 酚类 | 和厚朴酚(honokiol)Fig 1L | 中药厚朴 | 盲肠结扎穿孔引起脓毒症并进一步诱导的急性肾损伤大鼠 | 可以减少NO和一氧化氮合酶(inducible NO synthetase,iNOS) 的生成,缓解大鼠肾损伤程度 |
| 姜黄素(curcumin)Fig 1M | 草本植物姜黄根茎中 | 顺铂诱导急性肾损伤大鼠 | 可以明显降低血清BUN、Cr和MDA,缓解白细胞浸润、肾组织功能障碍和氧化应激反应 | |
| 白藜芦醇(resveratrol)Fig 1N | 虎杖、花生、葡萄、决明等植物性食物或药物中 | 造影剂诱导的人肾小管上皮细胞(HK-2)细胞毒性 | 通过减少DNA碎片,减轻氧化DNA损伤,增加抗凋亡蛋白和生存素的产生,抑制ROS的生成,发挥体外抗急性肾损伤的效果[BHG6*2] | |
| 表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG) Fig 1O | 茶叶 | 肾缺血/再灌注急性肾损伤大鼠 | EGCG可明显改善肾脏功能障碍、组织学变化和TNF-α的表达,抑制促炎因子的产生和caspase-3活化,从而缓解急性肾损伤 | |
| 萜类 | 橄榄苦苷(oleuropein)Fig 1P | 橄榄树叶子 | 顺铂诱导急性肾损伤小鼠 | 通过抑制细胞外信号调节激酶(ERK)信号通路,抑制急性肾损伤小鼠肾脏组织凋亡反应的发生 |
| 白桦脂酸(betulinic acid)Fig 1Q | 白桦树等植物 | CLP模型诱导脓毒症诱发的急性肾损伤大鼠 | 通过对抗炎症反应和氧化应激,抑制NF-κB、IL-6、IL-10等促炎因子的生成,缓解急性肾损伤 | |
| 皂苷类 | 薯蓣皂苷(dioscin)Fig 1R | 穿山龙、山药等植物 | 肾缺血/再灌注急性肾损伤大鼠 | 通过上调HSP70来发挥抑制TLR4/MyD88 炎症信号通路,抑制促炎因子产生和NF-κB的核易位,从而缓解大鼠肾缺血/再灌注急性损伤〖BHG3〗 |
| 积雪草苷(asiaticoside)Fig 1S | 伞形科植物积雪草 | 脓毒症诱导的急性肾损伤小鼠 | 可明显降低脓毒症小鼠血清BUN和Cr,通过抑制血清IL-6和iNOS蛋白的表达来发挥药理学活性〖BHG4*2〗 | |
| 蒽醌类 | 大黄酸(rhein)Fig 1T | 蓼科植物药用大黄、掌叶大黄的根茎、唐古特大黄 | 内毒素诱导的急性肾损伤大鼠 | 通过减少NF-κB激活,抑制NF-κB信号通路相关蛋白的表达和磷酸化,阻碍NF-κB p65的转录,从而发挥疗效 |
| 大黄素(emodin)Fig 1U | 蓼科植物虎杖的干燥根茎和根、掌叶大黄的根茎 | 内毒素诱导的急性肾损伤大鼠 | 通过抑制LPS诱导的TLR2、NF-κB、TNF-α、IL-1β和IL-6 mRNA表达水平,下调TLR2介导的NF-κB信号通路来发挥免疫炎症调节功能 |
|
| Fig 1 Typical chemical structure of natural products |
天然产物在防治AKI方面具有明显疗效,且副作用相对较少,越来越得到医患的重视。近年来,对各类中药从单纯的疗效观察,到作用机制分析、药物作用靶点的寻找,研究水平日趋深入。特别是将蛋白质组学技术应用于新药研发后,可借助其对分子网络机制中的复杂调控关系找到药物作用的新靶点。通过对中药复方、中药提取物或其中的单一有效成分进行多层次、多环节、多靶点的研究,建立天然产物作用于AKI特异性的靶点识别体系,进一步指导及预见中药材或制剂中抗AKI有效成分的发现和分离。因此,在未来的研究中,中药的研究将以中医药理论为指导思想,结合现代化方法和技术,克服传统中药的不足,为抗AKI中药的应用开辟新的局面。
| [1] | 张燕妮, 谢席胜. 急性肾损伤发病机制研究新进展[J]. 临床肾脏病杂志, 2014, 14 (2) : 125-8. Zhang Y N, Xie X S. New progress in the pathogenesis of acute kidney injury[J]. J Clin Nephrol, 2014, 14 (2): 125-8. |
| [2] | Waikar S S, Liu K D, Chertow G M. The incidence and prognostic significance of acute kidney injury[J]. Curr Opin Nephrol Hypertens, 2007, 16 (3): 227-36. doi:10.1097/MNH.0b013e3280dd8c35 |
| [3] | Medve L, Antek C, Paloczi B, et al. Epidemiology of acute kidney injury in Hungarian intensive care units: a multicenter, prospective, observational study[J]. BMC Nephrol, 2011, 12 : 43. doi:10.1186/1471-2369-12-43 |
| [4] | 许庆有, 贾晓明, 丁英钧, 等. 依普利酮对环孢素A急性肾损伤小管上皮细胞坏死及再生作用[J]. 中国药理学通报, 2010, 26 (7) : 906-9. Xu Q Y, Jia X M, Ding Y J, et al. Effect of eplerenone on necrosis and regeneration of tubular epithelial cells in acute cyclosporine nepharotoxicity[J]. Chin Pharmacol Bull, 2010, 26 (7): 906-9. |
| [5] | 罗景慧, 杨迎暴, 安田日出夫, 等. N-乙酰半胱氨酸影响p-38有丝分裂原活化蛋白激酶对顺铂诱导急性肾损伤的保护作用[J]. 中国药理学通报, 2011, 27 (2) : 229-33. Luo J H, Yang Y B, Hideo Y, et al. Protective effect of N-acetylcysteine on cisplatin-induced acute kidney injury related to p38 MAPK pathway in rats[J]. Chin Pharmacol Bull, 2011, 27 (2): 229-33. |
| [6] | 沈龙海, 安泳潼, 杨庆尧, 等. 中国被毛孢菌丝体提取物抗肾损伤作用体内外实验研究[J]. 中国药理学通报, 2011, 27 (11) : 1537-40. Shen L H, An Y T, Yang Q Y, et al. In vitro and in vivo study of Hirsutella sinensis extract on kidney injury[J]. Chin Pharmacol Bull, 2011, 27 (11): 1537-40. |
| [7] | Sing I. Biochemistry of peroxisomes in health and disease[J]. Mol Cell Biochem, 1997, 167 (1-2): 1-29. |
| [8] | Abogresha N M, Greish S M, Abdelaziz E Z, et al. Remote effect of kidney ischemia-reperfusion injury on pancreas: role of oxidative stress and mitochondrial apoptosis[J]. Arch Med Sci, 2016, 12 (2): 252-62. |
| [9] | Yamashita J, Itoh M, Kuro T, et al. Pre- or post-ischemic treatment with a novel Na+/Ca2+ exchange inhibitor, κB-R7943, shows real renal protective effects in rats with ischemic acute renal failure[J]. J Pharmacol Exp Ther, 2001, 296 (2): 412-9. |
| [10] | Tucci S Jr, Borelli-Bovo T J, Cologna A J, et al. Calcium channel blocker and renal mitochondrial function in warm renal ischemia[J]. Int Braz J Urol, 2005, 31 (4): 384-9. |
| [11] | Friedewald J J, Rabb H. Inflammatory cells in ischemic acute renal failure[J]. Kidney Int, 2004, 66 : 486-91. doi:10.1111/j.1523-1755.2004.761_3.x |
| [12] | Yu Y, Li M, Su N, et al. Honokiol protects against renal ischemia/reperfusion injury via the suppression of oxidative stress, iNOS, inflammation and STAT3 in rats[J]. Mol Med Rep, 2016, 13 (2): 1353-60. |
| [13] | Li J, Gui Y, Ren J, et al. Metformin protects against cisplatin-induced tubular cell apoptosis and acute kidney injury via AMPKα-regulated autophagy induction[J]. Sci Rep, 2016, 6 : 23975. doi:10.1038/srep23975 |
| [14] | Zhao H, Liu Z, Shen H, et al. Glycyrrhizic acid pretreatment prevents sepsis-induced acute kidney injury via suppressing inflammation, apoptosis and oxidative stress[J]. Eur J Pharmacol, 2016, 781 : 92-9. doi:10.1016/j.ejphar.2016.04.006 |
| [15] | Karapanagiotou A, Kydona C, Dimitriadis C, et al. Acute kidney injury after orthotopic liver transplantation[J]. Transplant Proc, 2012, 44 (9): 2727-9. doi:10.1016/j.transproceed.2012.09.096 |
| [16] | Stafford-Smith M. Evidence-based renal protection in cardiac surgery[J]. Semin Cardiothorac Vasc Anesth, 2005, 9 (1): 65-76. doi:10.1177/108925320500900107 |
| [17] | Cabezuelo J B, Ramlrez P, Rlos A, et al. Risk factors of acute renal failure after liver transplantation[J]. Kidney Int, 2006, 69 (6): 1073-80. doi:10.1038/sj.ki.5000216 |
| [18] | Saner F, Cicinnati V, Sotiropoulos G, et al. Strategies to prevent or reduce acute and chronic kidney injury in liver transplantation[J]. Liver Int, 2012, 32 (2): 179-88. doi:10.1111/liv.2011.32.issue-2 |
| [19] | Bosch X, Poch E, Grau J M. Rhabdomyolysis and acute kidney injury[J]. N Engl J Med, 2009, 361 (1): 62-72. doi:10.1056/NEJMra0801327 |
| [20] | Shanu A, Groebler L, Kim H B, et al. Selenium inhibits renal oxidation and inflammation but not acute kidney injury in an animal model of rhabdomyolysis[J]. Antioxid Redox Signal, 2013, 18 (7): 756-69. doi:10.1089/ars.2012.4591 |
| [21] | Langenberg C, Bagshaw S M, May C N, et al. The histopathology of septic acute kidney injury: a systematic review[J]. Crit Care, 2008, 12 (2): R38. doi:10.1186/cc6823 |
| [22] | Langenberg C, Bellomo R, May C, et al. Renal blood flow in sepsis[J]. Crit Care, 2004, 9 (4): R363-74. |
| [23] | 李嵘, 王永星. 药物性肾损害[J]. 世界最新医学信息文摘, 2015, 15 (25) : 98. Li R, Wang Y X. Drug induced kidney injury[J]. World Latest Med Inf, 2015, 15 (25): 98. |
| [24] | Patschan D, Müller G A. Acute kidney injury[J]. J Inj Violence Res, 2015, 7 (1): 19-26. |
| [25] | 陈秀兰, 郭丽, 张予阳, 等. 固精丹对庆大霉素急性肾损伤的防治作用及机制研究[J]. 中成药, 2007, 29 (6) : 801-5. Chen X L, Guo L, Zhang Y Y, et al. Effect and mechanism of Gujingdan on acute renal injury induced by gentamicin[J]. Chin Tradit Patent Med, 2007, 29 (6): 801-5. |
| [26] | 张国欣, 王秀芬, 张萍, 等. 参黄草合剂治疗早期肾损伤的临床研究[J]. 中国中医药信息杂志, 2002, 9 (12) : 16-7. Zhang G X, Wang X F, Zhang P, et al. The clinical study of the Shenhuangcao-mixture treating early renal injury[J]. Chin J Inf TCM, 2002, 9 (12): 16-7. |
| [27] | 孙艳玲, 刘先义. 参附注射液对大鼠肾缺血/再灌注损伤的防治作用[J]. 中国临床药理学与治疗学, 2005, 10 (8) : 943-6. Sun Y L, Liu X Y. Preventive and therapeutic effects of Shenfu injection in rats with renal ischemia reperfusion[J]. Chin J Clin Pharmacol Ther, 2005, 10 (8): 943-6. |
| [28] | 严彬, 王建华, 王旭东, 等. 补气活血中药对肾缺血/再灌注损伤模型大鼠的保护作用研究[J]. 中国药房杂志, 2005, 16 (9) : 658-60. Yan B, Wang J H, Wang X D, et al. Study on the protective effect of traditional Chinese medicine that invigorating vital energy and promoting blood flow on model of renal ischemical/reperfusion injury of rats[J]. China Pharm, 2005, 16 (9): 658-60. |
| [29] | Cai Q, Li X M, Wang H Y. Astragali and Angelica protect the kidney against ischemia and reperfusion injury and accelerate recovery[J]. Chin Med J, 2001, 114 (2): 119-23. |
| [30] | 钱风华, 郭健, 孙芳园, 等. 清瘟败毒饮治疗脓毒症急性肾损伤60例[J]. 河南中医, 2015, 35 (6) : 1392-4. Qian F H, Guo J, Sun F Y, et al. Sixty cases of kidney damage due to sepsis treated with decoction for eliminating pestilence and sepsis[J]. Henan Tradit Chin Med, 2015, 35 (6): 1392-4. |

