


2. 上海中医药大学附属龙华医院,上海 200032
2. Longhua Hospital Affiliated to Shanghai University of Traditional Chinese Medicine, Shanghai 200032, China
MSCs是一种易于扩增、具有分化为各种不同细胞潜能的干细胞,也是一种优良的种子细胞。它可分化为:脂肪细胞、成骨细胞、成软骨细胞、生肌细胞、甚至神经细胞等[1]。维生素D,目前认为它是一种前类固醇激素。作为激素分子的作用机制是[2]:1, 25(OH)2D3从血清维生素D结合蛋白或其他转运蛋白中分离出来,进入细胞内,与维生素D受体(vitamin D receptor, VDR)结合后,通过基因调节的方式发挥防治骨质疏松症、儿童佝偻病、成人软骨症、关节痛等作用。作为体内MSCs分化的重要调节因子[3-5],本文综述了维生素D通过Wnt信号通路、Wnt5a/ROR2轴、BMP/TGF-β/Samd信号通路、ROS/ERK信号通路调控MSCs成骨分化的分子作用。
2 维生素D通过Wnt信号通路促进MSCs成骨分化Wnt蛋白最早是由Nusse在1982年通过果蝇基因与小鼠的INT-1基因组合而来。Wnt蛋白家族富含L-半胱氨酸,在进化中高度保守[6-7]。目前已经知道细胞膜外Wnt蛋白共有19个成员,其中Wnt1、Wnt3a、Wnt4、Wnt7a、Wnt7b等参与Wnt/β-catenin信号途径,又称Wnt经典途径,这些蛋白与LRP/FZD结合而发挥协同作用,激活Wnt/β-catenin经典通路[8]。Wnt4、Wnt5a、Wnt5b、Wnt11等参与Wnt/Ca2+和Wnt/PCP通路,又称非经典Wnt途径,这些信号分子能与Frizzled结合而激活异源三聚体G-蛋白,提高细胞内钙水平和建立细胞极性、骨架重排等作用[9]。
2.1 维生素D通过Wnt经典途径促进MSCs成骨分化临床与分子生物学研究资料已经证实VDR在维生素D生物学作用中具有极其重要的意义,活性维生素D主要是通过与VDR结合发挥其生物学作用[10]。在肾脏中,1, 25(OH)2D3作为VDR的配体,激素-受体复合物对钙磷代谢产生影响,导致矿物质在骨中沉积和重塑。在骨组织中,1, 25(OH)2D3通过Wnt经典途径促进MSCs成骨分化[11]。近年来,许多科学家利用VDR(-/-)小鼠来研究维生素D对MSCs分化的影响。有研究显示[12-14],1, 25(OH)2D3与VDR结合后释放的因子使Wnt信号通路的抑制因子DKK1、SFRP2活性降低,Wnt受体LRP5表达量增高,同时MSCs分化为成骨细胞的能力恢复正常。另外,Cianferotti等[12]发现相比于野生型小鼠,VDR(-/-)小鼠MSCs分化为脂肪细胞的数量增加,抑制因子DKK1和SFRP2活性增加,LRP5表达量降低。DKKs、SFRPs可以阻碍Wnt蛋白与其受体LRP结合[15],运用基因工程的手段使编码DKK1的一个等位基因突变,另一个等位基因正常表达,进而使DKK1表达降低,低表达的DKK1增加了骨形成,然而在大鼠颅骨成骨细胞中的DKK1过表达会增加脂肪细胞的分化。因此1, 25(OH)2D3可能通过降低DKK1和SFRP2的活性,上调LRP5来激活Wnt信号通路,促进MSCs的成骨分化。
2.2 维生素D通过Wnt5a/ROR2轴促进MSCs成骨分化Wnt5a是Wnt家族成员之一。Wong等[16]根据Wnt家族成员对小鼠细胞C57MG转化能力的高低将Wnt分为2组,其中高转化能力组Wnt可激活β-catentin依赖性通路;弱或无转化功能的Wnt包括Wnt5a等,不依赖β-catentin介导的转录激活,Wnt5a和FZD2可调节细胞内Ca2+的浓度和流向,从而激活Ca2+依赖性的一些通路,在某些特定情况下,Wnt5a也可以激活经典信号通路,调节骨代谢[17]。有研究发现[18],1, 25(OH)2D3可以干扰Wnt5a/ROR2轴,促进MSCs分化为成骨细胞。Wnt5a与不同的受体结合后,激活或抑制Wnt经典信号通路。Wnt5a与ROR2结合会通过非GSK3依赖途径阻碍β-catentin的表达,从而抑制Wnt通路,阻滞MSCs向成骨细胞分化[19]。Wnt5a激活经典途径还是非经典途径,不是由Wnt5a本身决定,而是在某种细胞的背景下,由相应受体的表达情况决定[20]。Tornero-Esteban等[21-22]通过对人的MSC细胞培养实验发现,1, 25(OH)2D3可以与Wnt5a竞争性结合ROR2,迅速上调PKC,CaMKII活性。活化的PKC,CaMKII会激活Wnt5a与FZD4或FZD2、FZD5结合,产生活化因子,激活Wnt信号通路,促进MSCs向成骨细胞分化。
3 维生素D通过BMP/TGF-β/Samd信号通路促进MSCs成骨分化TGF-β家族的受体有Ⅰ、Ⅱ型2种,为受体丝氨酸/苏氨酸激酶形成的异源二聚体。与之相对应的信号通路也有2种,一种称之为TGF-β信号通路,另一种称之为BMP信号通路。这两条信号通路的配体分别与细胞膜上的Ⅰ、Ⅱ型受体结合,然后再通过Samds向细胞核内传递信号[23-24]。其中I型受体又被称为激活素受体样激酶(activin receptor -like kinase, ALKs),包括了ALK1和ALK5等7个激活素受体样激酶,在Ⅱ型受体(TβRⅡ、BMPRⅡ等)下游发挥作用[25]。
3.1 维生素D通过BMP/Samd信号通路促进MSCs分化为成骨细胞在MSCs成骨分化过程中,异三聚复合物P-Smad1/5/8-Smad4、Runx2、Osx[26-27]被认为是重要的调控因子。研究发现[28],在体外培养的SLE病人的MSC中加入维生素D类似物(EB1089)后,MSCs成骨分化能力增强。众所周知,Smad信号通路是介导TGF-β从细胞表面到细胞核的关键,而EB1089可以上调P-Smad1/5/8活性,引起P-Smad1/5/8-Smad4表达增强,P-Smad1/5/8-Smad4转位到细胞核与靶基因上的增强子序列结合,上调Runx2和Osx活性,进而促进MSC成骨分化。另有研究发现[29],体外诱导MSCs分化时,1, 25(OH)2D3能明显上调MSC成骨分化的特异性标志物Ocn表达和ALP活性。Honda等[29]用TB、m4T5、m8T11等不同的混合培养液对小鼠骨髓的MSCs进行体外培养后发现,含有100 μg·L-1 BMP-2的TB、12.5 μg·L-1 BMP-2的m4T5和1, 25(OH)2D3的m8T11均能上调Ocn与ALP活性,促进MSCs向成骨细胞分化。但当分别加入抑制剂Noggin(阻碍BMPs与受体的结合),Dorsomorphin(抑制BMP介导的Smad活性)对小鼠骨髓的MSCs进行培养后发现,在都含有Noggin的TB和m4T5中,MSCs向成骨细胞分化的程度降低,而在含有Noggin的m8T11中,Ocn、Runx2、Osx和ALP活性仍较高,MSCs向成骨细胞分化明显;在都含有Dorsomorphin的TB、m4T5和m8T11中,MSCs向成骨细胞分化的程度明显降低。因此1, 25(OH)2D3可能会激活BMP-2或与BMP-2在BMP/Samd信号通路中有相似作用。
3.2 维生素D通过TGF-β/Samd信号通路促进MSCs分化为成骨细胞组蛋白H3K9ac和H3K9me2也是MSCs成骨分化的重要调控因子。Tan等[30]运用全基因组表达启动子微阵列芯片技术发现,在人的髂骨骨髓MSCs成骨分化过程中,H3K9ac减少,H3K9me2增加。随后又对人的髂骨骨髓MSCs进行成骨诱导体外培养,通过基因芯片技术分析后发现,VDR在H3K9ac和H3K9me2影响MSCs成骨分化过程中起着反式抑制作用,1, 25(OH)2D3与VDR结合可以促进蛋白的甲基化靶点(H3K9)的脱乙酰作用和二甲基化作用,脱乙酰基和二甲基化的H3K9,下调H3K9ac,上调H3K9me2,进而下调TGF-β信号通路THBS1、PITX2、ID1、RBL1、INHBA的表达[31],促进MSCs的成骨分化。综上,维生素D可以通过BMP/TGF-β/Samd信号通路促进MSCs分化为成骨细胞。
4 维生素D通过ROS/ERK信号通路促进MSCs成骨分化活性氧(reactive oxygen species, ROS)是MSCs分化的重要调节者,而激活ERK和p38 MAPK信号转导可以促进大鼠MSCs增值[32],可见ROS和ERK在骨稳态维持过程中起着重要作用。研究发现[33-37],1, 25(OH)2D3可以上调人MSCs中CYP27B1(1-OHase),使25(OH)D3转化为活性维生素D-1, 25(OH)2D3,过转化的1, 25(OH)2D3通过抑制过氧化氢酶上调ROS表达,同时下调MSCs中CYP24A1(24-OHase),阻滞25(OH)D、1, 25(OH)2D3由24-OHase催化而失活[38-40]。在体外培养的人椎骨MSCs中加入1, 25(OH)2D3后ROS表达上调,ROS作为特定的信号分子,能够直接使目标蛋白氧化,随着氧化作用的积累,ROS通过模仿生长因子受体-配体的交互作用直接激活下游ERK,活化的ERK使Runx2磷酸化,引起Runx2过表达,进而促进MSCs的成骨分化[37]。
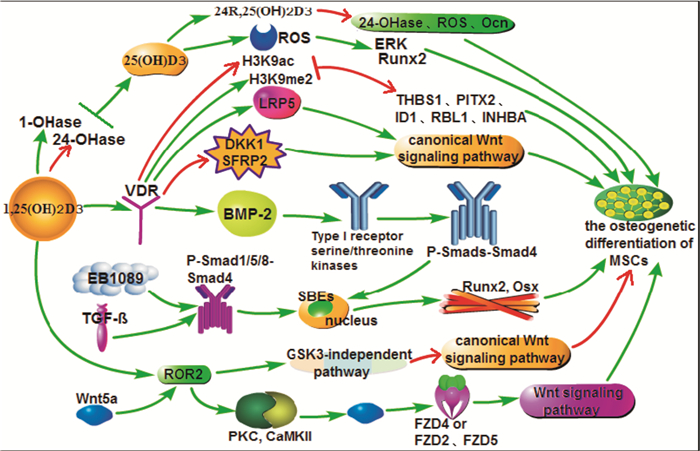
5 结语MSCs是有多向分化潜能的干细胞,能在体外增殖,维持非分化状态并具有分化成骨、软骨、脂肪、纤维及骨髓基质等中胚层组织的潜能,对骨骼的发育和代谢平衡具有十分重要的作用,是目前研究及关注较多的种子细胞之一。随着年龄的增长和绝经后骨质疏松症的发生、发展,骨髓腔内的成骨细胞减少,脂肪细胞增多,因此促进MSCs成骨分化是目前治疗骨质疏松症的新途径。维生素D通过不同的信号通路促进MSCs分化为成骨细胞(Fig 1),系统探讨其分子作用机制,为开发治疗骨质疏松新药、建立新方法奠定了理论基础。
|
| Fig 1 Molecular signaling pathway of regulatory effects of vitamin D on osteogenic differentiation of MSCs |
| [1] | Backesjo C M, Li Y, Lindgren U, Haldosén L A. Activation of Sirtl decreases adipocyte formation during ostcoblast differentiation of mesenchymal stem cells[J]. J Bone Miner Res, 2006, 21 (7): 993-1002. doi:10.1359/jbmr.060415 |
| [2] | Lam N N, Triliana R, Sawyer R K, et al. Vitamin D receptor overexpression in osteoblasts and osteocytes prevents bone loss during vitamin D-deficiency[J]. J Steroid Biochem Mol Biol, 2014, 144 Pt A : 128-31. |
| [3] | Doroudi M, Olivares-Navarrete R, Hyzy S L, et al. Signaling components of the 1alpha, 25(OH)2D3-dependent Pdia3 receptor complex are required for Wnt5a calcium-dependent signaling[J]. Biochim Biophys Acta, 2014, 1843 (11): 2365-75. doi:10.1016/j.bbamcr.2014.06.006 |
| [4] | Yoshikawa Y, Yoshizawa T, Domae E, et al. RNA interference-mediated knockdown of Smad1 inhibits receptor activator of nuclear factor kappaB ligand expression induced by BMP-2 in primary osteoblasts[J]. Arch Oral Biol, 2015, 60 (9): 1319-26. doi:10.1016/j.archoralbio.2015.06.001 |
| [5] | Li M, Zhao Y, Hao H, et al. Mesenchymal stem cell-conditioned medium improves the proliferation and migration of keratinocytes in a diabetes-like microenvironment[J]. Int J Low Extrem Wounds, 2015, 14 (1): 73-86. doi:10.1177/1534734615569053 |
| [6] | 潘京华, 黄浩, 查振刚. 间充质干细胞向成骨细胞分化中的Wnt信号通路[J]. 中国组织工程研究, 2013, 17 (40) : 7144-9. Pan J H, Huang H, Zha Z G. Wnt signaling pathways in osteogenic differentiation of mesenchymal stem cells[J]. Chin J Tissue Eng Res, 2013, 17 (40): 7144-9. |
| [7] | Chun J S, Oh H. Wnt signaling in cartilage development and degeneration[J]. BMB Rep, 2008, 41 (7): 485-94. doi:10.5483/BMBRep.2008.41.7.485 |
| [8] | Shahi P, Seethammagari M R, Valdez J M, et al. Wnt and Notch pathways have interrelated opposing roles on prostate progenitor cell proliferation and differentiation[J]. Stem Cells, 2011, 29 (4): 678-88. doi:10.1002/stem.v29.4 |
| [9] | 昝昀, 安荣泽, 王兆杰. Wnt信号通路与软骨细胞分化[J]. 科学咨询, 2015, 29 : 54-6. Zan Y, An R Z, Wang Z J. Wnt signaling pathway and chondrocyte differentiation[J]. Scientific Consult, 2015, 29 : 54-6. |
| [10] | 郑敏, 刘强. 维生素D及维生素D受体的研究进展[J]. 医学综述, 2013, 19 (21) : 3965-7. Zheng M, Liu Q. The progress in the studies of vitamin D and vitamin D receptor[J]. Med Recapitulate, 2013, 19 (21): 3965-7. |
| [11] | 李晨睿, 孟志远, 牛银波, 等. 黄芩苷通过Wnt/β-catenin信号通路对大鼠骨髓间充质干细胞成骨分化的促进作用[J]. 中国药理学通报, 2015, 31 (7) : 919-24. Li C R, Meng Z Y, Niu Y B, et al. Effect of Baicalin on the osteogenic differentiation of rat bone marrow mesenchymal stem cells by Wnt/β-catenin signaling pathway[J]. Chin Pharmacol Bull, 2015, 31 (7): 919-24. |
| [12] | Cianferotti L, Demay M B. VDR-mediated inhibition of DKK1 and SFRP2 suppresses adipogenic differentiation of murine bone marrow stromal cells[J]. J Cell Biochem, 2007, 101 (1): 80-8. doi:10.1002/(ISSN)1097-4644 |
| [13] | 黄启钊. FGFs/FGFR3与1, 25(OH)2D3/VDR信号通路的交互作用及其在软骨发育中的作用及意义研究[D].西安:第三军医大学, 2014. Huang Q Z. Preliminary research on the crosstalk between FGFs/FGFR3 and 1, 25(OH)2D3/VDR signaling pathway during chondrogenesis[D]. Xi'an:Network Center of Third Military Medical University, 2014. |
| [14] | De P F, Dick-de-Paula I, Bornstein S, et al. VDR haploinsufficiency impacts body composition and skeletal acquisition in a gender-specific manner[J]. Calcif Tissue Int, 2011, 89 (3): 179-91. doi:10.1007/s00223-011-9505-1 |
| [15] | Morvan F, Boulukos K, Clement-Lacroix P, et al. Deletion of a single allele of the Dkk1 gene leads to an increase in bone formation and bone mass[J]. J Bone Miner Res, 2006, 21 (6): 934-45. doi:10.1359/jbmr.060311 |
| [16] | Wong G T, Gavin B J, McMahon A P. Differential transformation of mammary epithelial cells by Wnt genes[J]. Mol Cell Biol, 1994, 14 (9): 6278-86. doi:10.1128/MCB.14.9.6278 |
| [17] | 卜海激, 朱明华. Wnt5a作用及信号转导通路研究进展[J]. 中华病理学杂志, 2015, 44 (7) : 535-8. Bu H J, Zhu M H. Research progress of function and signal transduction pathway of Wnt5a[J]. Chin J Pathol, 2015, 44 (7): 535-8. |
| [18] | Guan S, Wang Z, Xin F, Xin H. Wnt5a is associated with the differentiation of bone marrow mesenchymal stem cells in vascular calcification by connecting with different receptors[J]. Mol Med Rep, 2014, 10 (4): 1985-91. |
| [19] | Cai S X, Liu A R, He H L, et al. Stable genetic alterations of β-catenin and ROR2 regulate the Wnt pathway, affect the fate of MSCs[J]. J Cell Physiol, 2014, 229 (6): 791-800. doi:10.1002/jcp.v229.6 |
| [20] | Torii K, Nishizawa K, Kawasaki A, et al. Anti-apoptotic action of Wnt5a in dermal fibroblasts is mediated by the PKA signaling pathways[J]. Cell Signal, 2008, 20 (7): 1256-66. doi:10.1016/j.cellsig.2008.02.013 |
| [21] | Tornero-Esteban P, Peralta-Sastre A, Herranz E, et al. Altered expression of Wnt signaling pathway components in osteogenesis of mesenchymal stem cells in osteoarthritis patients[J]. PLoS One, 2015, 10 (9): e0137170. doi:10.1371/journal.pone.0137170 |
| [22] | Chen J X, Olivares-Navarrete R, Wang Y, et al. Protein-disulfide isomerase-associated 3(Pdia3) mediates the membrane response to 1, 25-dihydroxyvitamin D3 in osteoblasts[J]. J Biol Chem, 2010, 285 (47): 37041-50. doi:10.1074/jbc.M110.157115 |
| [23] | 兰平文, 沈彬. TGF-β/BMP信号通路在骨关节炎软骨细胞退变中的作用机制[J]. 中华关节外科杂志, 2015, 9 (5) : 644-7. Lan P W, Shen B. The role of TGF-beta /BMP signaling pathway in the degeneration of cartilage cells in osteoarthritis[J]. Chin J Joint Surg, 2015, 9 (5): 644-7. |
| [24] | 李晓敏, 张岩. 女贞子及其化合物对骨矿代谢影响的研究进展[J]. 中国药理学通报, 2015, 31 (10) : 1345-8. Li X M, Zhang Y. Research progress of Fructus Ligustri Lucidi and its compounds: effects on bone and mineral metabolism[J]. Chin Pharmacol Bull, 2015, 31 (10): 1345-8. |
| [25] | Heldin C H, Miyazono K, ten Dijke P. TGF-beta signalling from cell membrane to nucleus through SMAD proteins[J]. Nature, 1997, 390 (6659): 465-71. doi:10.1038/37284 |
| [26] | Zhou S H, Glowacki J, Kim S W, et al. Clinical characteristics influence in vitro action of 1, 25-dihydroxyvitamin D3 in human marrow stromal cells[J]. J Bone Miner Res, 2012, 27 (9): 1992-2000. doi:10.1002/jbmr.1655 |
| [27] | Olivares-Navarrete R, Sutha K, Hyzy S L, et al. Osteogenic differentiation of stem cells alters vitamin D receptor expression[J]. Stem Cells Dev, 2012, 21 (10): 1726-35. doi:10.1089/scd.2011.0411 |
| [28] | Xu J J, Sun Y B, Zhang X L, et al. Vitamin D analog EB1089 could repair the defective bone marrow-derived mesenchymal stromal cells in patients with systemic lupus erythematosus[J]. Int J Clin Exp Med, 2015, 8 (1): 916-21. |
| [29] | Honda Y, Ding X, Mussano F, et al. Guiding the osteogenic fate of mouse and human mesenchymal stem cells through feedback system control[J]. Sci Rep, 2013, 3 : 3420. |
| [30] | Tan J, Lu J, Huang W, et al. Genome-wide analysis of histone H3 lysine9 modifications in human mesenchymal stem cell osteogenic differentiation[J]. PLoS One, 2009, 4 (8): e6792. doi:10.1371/journal.pone.0006792 |
| [31] | Pandey R, Guru R K, Mount D W. Pathway miner: extracting gene association networks from molecular pathways for predicting the biological significance of gene expression microarray data[J]. Bioinformatics, 2004, 20 (13): 2156-8. doi:10.1093/bioinformatics/bth215 |
| [32] | Qin S Y, Zhou W, Liu S Y, et al. Icariin stimulates the proliferation of rat bone mesenchymal stem cells via ERK and p38 MAPK signaling[J]. Int J Clin Exp Med, 2015, 8 (5): 7125-33. |
| [33] | 田丽花, 张劼, 黄松, 等. 25(OH)D3、维生素D受体与糖皮质激素性骨质疏松关系的研究[J]. 中国骨质疏松杂志, 2015, 21 (7) : 769-73. Tian L H, Zhang J, Huang S, et al. Study on the relationship of VDR, 25(OH)D3 and glucocorticoid-induced osteoporosis[J]. Chin J Osteoporos, 2015, 21 (7): 769-73. |
| [34] | Geng S, Zhou S H, Bi Z G, Glowacki J. Vitamin D Metabolism in human bone marrow stromal (mesenchymal stem) cells[J]. Metabolism, 2013, 62 (6): 768-77. doi:10.1016/j.metabol.2013.01.003 |
| [35] | Zhou S H, Geng S, Glowacki J. Histone deacetylation mediates the rejuvenation of osteoblastogenesis by the combination of 25(OH)D3 and parathyroid hormone in MSCs from elders[J]. J Steroid Biochem Mol Biol, 2013, 136 : 156-9. doi:10.1016/j.jsbmb.2012.09.002 |
| [36] | Geng S, Zhou S, Glowacki J. Effects of 25-hydroxyvitamin D(3) on proliferation and osteoblast differentiation of human marrow stromal cells require CYP27B1/1α-hydroxylase[J]. J Bone Miner Res, 2011, 26 (5): 1145-53. doi:10.1002/jbmr.298 |
| [37] | Curtis K M, Aenlle K K, Roos B A, Howard G A. 24R, 25-dihydroxyvitamin D 3 promotes the osteoblastic differentiation of human mesenchymal stem cells[J]. Mol Endocrinol, 2014, 28 (5): 644-58. doi:10.1210/me.2013-1241 |
| [38] | Zhou S H, Leboff M S, Waikar S S, Glowacki J. Vitamin D metabolism and action in human marrow stromal cells: Effects of chronic kidney disease[J]. J Steroid Biochem Mol Biol, 2013, 136 : 342-4. doi:10.1016/j.jsbmb.2012.09.009 |
| [39] | Van Driel M, Koedam M, Buurman C J, et al. Evidence for auto/paracrine actions of vitamin D in bone: 1alpha-hydroxylase expression and activity in human bone cells[J]. FASEB J, 2006, 20 (13): 2417-9. doi:10.1096/fj.06-6374fje |
| [40] | Arai M, Shibata Y, Pugdee K, et al. Effects of reactive oxygen species(ROS) on antioxidant system and osteoblastic differentiation in MC3T3-E1 cells[J]. IUBMB Life, 2007, 59 (1): 27-33. doi:10.1080/15216540601156188 |

