


2. 福建医科大学教学医院福建省妇幼保健院;
3. 福建医科大学附属协和医院,福建 福州 350001;
4. 福建中医药大学研究生部,福建 福州 350108
 ,
HUANG Jian2,
CHEN Qing3,
LI Si-han4,
LIN Jian-long1,
ZHONG Guo-dong1,
HUANG Heng-qing1,
LIN Ping1
,
HUANG Jian2,
CHEN Qing3,
LI Si-han4,
LIN Jian-long1,
ZHONG Guo-dong1,
HUANG Heng-qing1,
LIN Ping1

2. Dept of Gynaecology and Obstetrics,Fujian Medical University Teaching Hospital,Fujian Maternity and Child Health Hospital,Fuzhou 350001,China ;
3. Xiehe Hospital Affiliated to Fujian Medical University, Fuzhou 350001, China ;
4. Dept of Postgraduates, Fujian University of Traditional Chinese Medicine, Fuzhou 350108,China
慢性萎缩性胃炎(chronic atrophic gastritis,CAG)是由多种病因引起的胃黏膜慢性炎症病变,以胃黏膜变薄、黏膜固有腺体萎缩、胃酸分泌功能减少为其病理特点,常伴肠上皮化生及假幽门腺化生[1-2]。阻断或延缓CAG进展,对预防胃癌发生具有十分重要的意义。我们之前临床研究证实,健脾清化中药复方能有效逆转CAG患者胃黏膜腺体萎缩[3]。近年来研究发现,胃黏膜组织中Toll样受体4(Toll-like receptor 4,TLR4) 及其下游MyD88依赖途径,在CAG的发病过程中扮演了重要的角色[4-5]。本研究通过建立CAG大鼠模型,分析健脾清化中药复方对CAG大鼠胃黏膜组织学、TLR4及其下游MyD88依赖通路重要分子MyD88、NF-κB、COX-2蛋白表达量,以及炎性因子TNF-α的影响,探讨健脾清化中药复方干预CAG的作用机制。
1 材料 1.1 动物53只健康SPF级Wistar大鼠,上海斯莱克实验动物有限公司,合格证号SCXK(沪):0164377,2012-0002,体质量(110±10) g,♂,4周龄。
1.2 药物健脾清化中药复方(闽药制字Z05104030) 药物组成:白扁豆220 g、茯苓220 g、薏苡仁220 g、茵陈110 g、佩兰66 g、白豆蔻33 g、黄连33 g、厚朴66 g、赤芍110 g,煎液滤过浓缩至500 mL,灭菌瓶装。由福建中医药大学附属第二人民医院药剂室提供。维酶素片(北海阳光药业有限公司,国药准字H45021183,产品批号:121020) 。
1.3 主要试剂与仪器小鼠抗大鼠TLR4(Santa Cruz,sc-293072) ,小鼠抗大鼠MyD88(Santa Cruz,sc-8197) ,小鼠抗大鼠NF-κB(Santa Cruz,sc-373) ,小鼠抗大鼠COX-2(Santa Cruz,sc-23984) ,小鼠抗大鼠β-actin(R&D,937215) ,HRP 标记的兔抗小鼠IgG(北京中杉)。大鼠TNF-α ELISA试剂盒(上海西塘生物科技有限公司)。Primo R台式冷冻离心机(Thermo Fisher);Mini PROTEAN Tetra小型垂直电泳槽(Bio-rad);Mini Trans-BLot小型转印槽(Bio-rad);Dolphin-Chemi凝胶成像系统(WEALTEC);DENLEY DRAGON Wellscan MK 3酶标仪(Thermo公司);图像分析软件(Quantity One Software);高通量组织研磨器(宁波新芝生物科技股份有限公司)。
2 方法 2.1 分组与造模按随机数字表法,将53只Wistar大鼠分为空白组8只,CAG造模组45只。空白组大鼠在正常饲养环境中,正常饮用水以及正常饲料饮食。CAG造模方法参照文献[6]并加以改进:正常饲料饮食,以0.5 g·L-1氨水作为饮用水自由饮用,20 mmol·L-1去氧胆酸钠溶液每日灌胃1次,每次2 mL,60%乙醇每周空腹灌胃2次,每次2 mL,造模时间为12周。12周末,造模组随机处死3只大鼠,取胃组织行病理检查。在判断CAG造模成功后,剔除造模组死亡及随机处死的大鼠共计5只,将余下造模成功的40只大鼠,按随机数字表法分为模型组8只,维酶素组8只,中药低、中、高剂量组各8只。
2.2 给药方法与标本采集依据临床应用剂量换算成大鼠给药剂量,低、中、高剂量组分别按1.5、3.0、6.0 mL·kg-1·d-1剂量灌胃。维酶素组予维酶素0.3 g·kg-1·d-1灌胃。根据大鼠体重将药液用生理盐水稀释至每次4 mL。空白组及CAG模型对照组给予每次4 mL生理盐水灌胃。灌胃共30 d。药物干预结束后,禁食24 h,经麻醉处死后开腹,腹主动脉取血3 mL。取胃后沿胃大弯剪开,以生理盐水清洗胃黏膜表面,展平观察胃黏膜形态结构、色泽。于胃窦部剪取黄豆大组织2块,立即放入液氮中冻存,余下的胃窦部组织迅速置于4%多聚甲醛溶液中。
2.3 HE染色评价大鼠胃窦部病理组织学改变4%多聚甲醛固定24 h,常规石蜡包埋,连续切片5张,片厚4 μm,HE染色,光镜下观察各组病理切片胃黏膜形态变化。
2.4 Western blot法检测大鼠胃窦部TLR4、MyD88、NF-κB、COX-2蛋白表达量取150 mg胃窦部组织,经蛋白裂解后取30 μg总蛋白上样,SDS-PAGE电泳,转至硝酸纤维素膜上,TBST封闭1 h,分别用抗TLR4(1 ∶800) 、MYD88(1 ∶500) 、NF-κB(1 ∶1 000) 、COX-2(1 ∶800) 、β-actin(1 ∶1 000) 的一抗4℃过夜,TBST洗3次;二抗室温孵育1 h。增强的化学荧光素显像并摄片,以Quantity One Software进行图像分析,计算目标条带与内参(β-actin)灰度的比值。
2.5 ELISA法检测大鼠血清中TNF-α含量将大鼠全血3 mL低温冷冻离心,4℃,3 500 r·min-1×15 min,取上清液,按照试剂盒说明书测定步骤进行操作。
2.6 统计学方法数据用x±s表示,采用SPSS 19.0进行统计分析。组间比较符合正态分布,采用单因素方差分析,方差齐者用LSD法,方差不齐用Tamhane′s T3法;不符合正态分布,采用多个独立样本比较的秩和检验。
3 结果 3.1 大鼠死亡情况空白组大鼠实验期间均全部存活。造模组大鼠造模后期死亡2只,中药各剂量干预组大鼠治疗期间无死亡,模型组大鼠治疗期间死亡1只。病理解剖取材可见胃黏膜固有层腺体数量减少,萎缩变薄,有合并异型增生、轻度肠上皮化生。
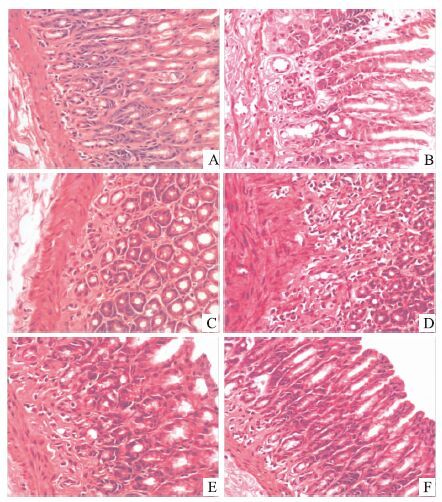
3.2 干预后各组大鼠胃组织病理变化比较空白组大鼠胃上皮细胞排列整齐,腺体形态规则,黏膜厚度正常,细胞呈单层柱状,腺上皮与腺管分界清楚。固有腺及黏膜层毛细血管无扩张,黏膜肌层未见增生及向黏膜层伸入。模型组大鼠见胃黏膜不同程度的萎缩,固有层腺体减少,排列不规则,可伴有不同程度的肠上皮化生及异型增生。中药低、中、高剂量组及维酶素组较模型组有不同程度的改善,以中药高剂量组改善为优,镜下见胃黏膜腺体排列较整齐,数量增多,固有层单个核细胞数量少。见Fig 1。
|
| Fig 1 Pathological images of rat gastric mucosal tissue(×200) A:Blank group;B:Model group;C:Vitacoenzyme-tablet group;D:Low dose of JQCC group;E:Medium dose of JQCC group;F:High dose of JQCC group |
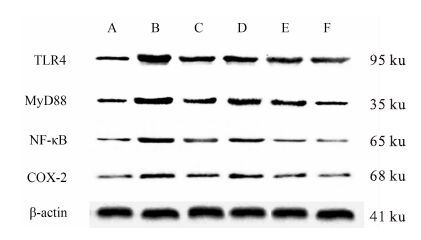
各组灰度值比较显示,与空白组相比,造模后模型组TLR4、MyD88、NF-κB、COX-2蛋白表达量均明显增高(P<0.01) 。药物干预后同模型组比较,不同剂量中药组及维酶素组蛋白表达水平降低(P<0.05或P<0.01) ,特别以中药高剂量组表现明显。见Fig 2、Tab 1。
|
| Fig 2 Expression quantities of TLR4, MyD88, NF-κB, COX-2 from gastric mucosa of rats by Western-blot A:Blank group;B:Model group;C:Vitacoenzyme-tablet group;D:Low dose of JQCC group;E:Medium dose of JQCC group;F:High dose of JQCC group |
| Group | n | TLR4 | MyD88 | NF-κB | COX-2 |
| Control | 8 | 0.472±0.051 | 0.322±0.046 | 0.245±0.031 | 0.253±0.026 |
| Model | 7 | 1.028±0.152** | 0.975±0.152** | 0.807±0.069** | 0.526±0.061** |
| Vitacoenzyme | 8 | 0.788±0.058**△△ | 0.647±0.065**△△ | 0.405±0.028**△△ | 0.382±0.025**△△ |
| JQCC-L | 8 | 0.870±0.093**△ | 0.803±0.120**△ | 0.585±0.063**△△ | 0.491±0.059**## |
| JQCC-M | 8 | 0.754±0.065**△△ | 0.788±0.058**△△ | 0.352±0.013**△△## | 0.305±0.027**△△## |
| JQCC-H | 8 | 0.708±0.091**△△ | 0.468±0.053**△△## | 0.184±0.032**△△## | 0.248±0.018△△## |
| *P<0.05, **P<0.01 vs control;△P<0.05, △△P<0.01 vs model;##P<0.01 vs vitacoenzyme | |||||
与空白组比较,造模后模型组血清中TNF-α浓度明显增高(P<0.01) 。同模型组比较,中药高、中、低剂量组及维酶素组血清中TNF-α浓度均降低(P<0.05或P<0.01) ,且中药高剂量组降低更为明显(P<0.01) 。见Tab 2。
| Group | n | TNF-α/ng·L-1 |
| Control | 8 | 210.3±35.6 |
| Model | 7 | 338.6±58.5** |
| Vitacoenzyme | 8 | 261.4±45.8**△ |
| JQCC-L | 8 | 280.2±44.3**△ |
| JQCC-M | 8 | 263.9±48.7*△ |
| JQCC-H | 8 | 255.2±42.5*△△ |
| *P<0.05, **P<0.01 vs control;△P<0.05, △△P<0.01 vs model | ||
CAG临床上以上腹闷胀痛、反酸、食欲减低等为主要表现,已被列为胃癌的癌前疾病[1]。在CAG发病过程中,TLRs及下游信号通路的激活与CAG病情进展高度相关[5]。TLR4是TLRs家族成员中识别内源性以及外源性配体的最主要受体,其下游通路包括MyD88依赖途径和非MyD88依赖途径[7]。其中MyD88依赖途径是TLR4激活后的主要通路,以启动核转录因子NF-κB的方式介导下游更为广泛的炎性反应[8]。通常情况下,NF-κB以同型或异型二聚体形式存在于胞质,与它的抑制蛋白(IκB)结合在一起。TLRs通路激活可解除NF-κB与IκB的结合,使NF-κB获自由,从胞质移入胞核内,与靶基因上特定的序列结合,引起炎性因子的释放,参与了胃黏膜损伤及病变进展[4]。COX-2(cyclooxygenase-2) 是前列腺素合成的限速酶,与组织损伤、修复、癌变密切相关。在COX-2基因的上游存在NF-κB的作用位点,在NF-κB的作用下COX-2表达增加[9]。Hong等[10]的研究表明,COX-2表达强度在浅表性胃炎、萎缩性胃炎、肠上皮化生、不典型增生以及胃癌中呈递增趋势,提示COX-2的高表达是胃黏膜癌变过程中早期事件且与预后相关。TNF-α是特异性免疫应答与炎性反应之间的一种重要介质[11],可以趋化、激活炎性细胞并使其定位于病变胃黏膜,最终导致胃黏膜组织的炎症和萎缩[12]。NF-κB可以上调TNF-α的基因转录,升高的TNF-α可正反馈再次激活NF-κB,引起级联反应,导致最初的炎性信号进一步扩大[12]。
健脾清化中药复方由白扁豆、茯苓、薏苡仁、茵陈、佩兰、白豆蔻、黄连、厚朴、赤芍组成,目前已被国家中医药管理局十一五脾胃重点专科采纳,作为CAG协定处方应用推广。我们之前的临床研究证实[3],健脾清化中药复方对CAG患者上腹疼痛、上腹闷胀、食欲减低等症状有明显疗效,并可明显逆转胃黏膜组织病理。在本研究中,模型组胃组织中TLR4、MyD88、NF-κB、COX-2蛋白表达量明显增高,血清中TNF-α浓度升高,证实TLR4/MyD88依赖途径的激活参与了CAG的发病过程;经健脾清化中药复方治疗后,胃黏膜萎缩程度改善,且胃组织中TLR4/MyD88依赖途径上的蛋白表达量以及血清中TNF-α浓度均明显下降,提示健脾清化中药复方可能通过抑制TLR4/MyD88的持续活化发挥治疗作用。同时,我们在实验过程中也观察到,中药高剂量组对胃黏膜病变的改善更为明显,对TLR4/MyD88通路的抑制更为明显。
因此我们认为,抑制TLR4/MyD88依赖途径的持续活化,是CAG药物治疗的一个新思路。本研究为进一步研究中药干预对MyD88依赖途径下游靶基因和下游分子的调控机制提供了重要基础。
( 致谢: 本研究在福建中医药大学动物实验中心、福建省中西医结合研究院完成。衷心感谢动物实验中心谢金东老师、福建省中西医结合研究院方翌、张铃实验师的帮忙。 )
| [1] | Fox J G, Wang T C. Inflammation, atrophy, and gastric cancer[J]. J Clin Invest, 2007, 117 (1) : 60-9 doi:10.1172/JCI30111. |
| [2] | 郑君, 林晓春, 陈育尧, 等. 甘草总黄酮抑制慢性萎缩性胃炎大鼠胃黏膜腺体萎缩及机制研究[J]. 中国药理学通报, 2014, 30 (1) : 113-7 . Zheng J, Lin X C, Chen Y Y, et al. Licoflavone suppresses gland atrophy of gastric mucosa and its mechanism in rats with chronic atrophic gastritis[J]. Chin Pharmacol Bull, 2014, 30 (1) : 113-7 . |
| [3] | 黄铭涵, 陈琴, 高尤亮, 等. 清化饮对慢性萎缩性胃炎的疗效及机制研究[J]. 时珍国医国药, 2015, 26 (10) : 2444-6 . Huang M H, Chen Q, Gao Y L, et al. The therapeutic efficacy and mechanism study of Qing huayin in treatment of chronic atrophic gastritis[J]. Lishizhen Med Mat Med Res, 2015, 26 (10) : 2444-6 . |
| [4] | Takeuchi O, Akira S. Pattern recognition receptors and inflammation[J]. Cell, 2010, 140 (6) : 805-20 doi:10.1016/j.cell.2010.01.022. |
| [5] | Khakzad M R, Saffari A, Mohamadpour N, et al. TLR4 and TLR2 expression in biopsy specimens from antral and corporal stomach zones in Helicobacter pylori infections[J]. Rep Biochem Mol Biol, 2014, 3 (1) : 29-37 . |
| [6] | 姒健敏, 吴加国, 曹倩, 等. 鼠慢性萎缩性胃炎模型的建立及致萎缩因素探讨[J]. 中华消化杂志, 2001, 21 (2) : 75-8 . Si J M, Wu J G, Cao Q, et al. Establishment of chronic atrophic gastritis and study of the factors inducing atrophy in a rat model[J]. Chin J Dig, 2001, 21 (2) : 75-8 . |
| [7] | Kfoury A, Virard F, Renno T, et al. Dual function of MyD88 in inflammation and oncogenesis:implications for therapeutic intervention[J]. Curr Opin Oncol, 2014, 26 (1) : 86-91 doi:10.1097/CCO.0000000000000037. |
| [8] | Wang J Q, Jeelall Y S, Ferguson L L, et al. Toll-like receptors and cancer:MyD88 mutation and inflammation[J]. Front Immunol, 2014, 5 : 367 . |
| [9] | Nie M, Pang L, Inoue H, et al. Transcriptional regulation of Cycloo-xygenase 2 by bradyinin and interleukin-1β in human airway smooth muscle cells involvement of different promote relement,transcription factors, and histone H4 acetylation[J]. Mol Cell Biol, 2003, 23 (24) : 9233-44 doi:10.1128/MCB.23.24.9233-9244.2003. |
| [10] | Hong L, Li S, Liu L, et al. The value of MG7-Ag and COX-2 for predicting malignancy in gastric precancerous lesions[J]. Cell Biol Int, 2010, 34 (9) : 873-6 doi:10.1042/CBI20100149. |
| [11] | 李影, 陈镜宇, 张玲玲, 等. 肿瘤坏死因子受体相关因子参与炎症免疫调节的研究进展[J]. 中国药理学通报, 2015, 31 (9) : 1206-11 . Li Y, Chen J Y, Zhang L L, et al. Research advance of tumor necrosis factor receptor-associated factors in inflammatory immune regulation[J]. Chin Pharmacol Bull, 2015, 31 (9) : 1206-11 . |
| [12] | Akira S, Takeda K. Toll-like receptor signalling[J]. Nat Rev Immunol, 2004, 4 (7) : 499-511 doi:10.1038/nri1391. |
文章信息
-
文章历史
- 收稿日期: 2016-05-11
- 修订日期: 2016-05-25