


2. 广东医科大学药学院,广东 东莞 523808;
3. 广东医科大学病原生物学与免疫学研究所;
4. 广东天然药物研究与开发重点实验室,广东 湛江 524023
2. School of Pharmacy, Guangdong Medical University, Dongguan Guangdong 523808, China ;
3. Institute of Immunology and Microbiology ;
4. Guangdong Key Laboratory for Research and Development of Natural Drugs, Guangdong Medical University, Zhanjiang Guangdong 524023, China
含辅酶Q10的红曲胶囊是从中药红曲提取制备而成的一种创新药物,与以往主要含有洛伐他汀及他汀同系物的红曲胶囊不同。目前的观点认为他汀类是红曲胶囊降血脂的主要有效成分,临床研究观察到,长期应用他汀类治疗高脂血症及冠心病,常常出现肝功能损伤等不良反应,但合用辅酶Q10之后这种情况就得到改善[1]。我们在对红曲菌丝体的研究中,发现红曲菌丝体含有辅酶Q10,因此我们从红曲菌丝体中提取辅酶Q10后与红曲的他汀类成分制备成含辅酶Q10的红曲胶囊。本研究采用大鼠去卵巢合并应用D-半乳糖诱导老年性骨质疏松的动物模型,评价该胶囊的抗衰老作用及骨药理学作用,现报道如下。
1 材料与方法 1.1 动物45只SPF级3 mon龄SD大鼠,♀,体质量(231.11±18.96)g。由广东省中山大学实验动物中心提供,实验动物质量合格证号码为:SCXK(粤)2011-0029。
1.2 药物己烯雌酚注射液购于上海通用制药股份有限公司,批号100204;D-半乳糖购于天津市光复精细化工研究所,批号20120928;红曲胶囊由广东医学院医药科技开发中心提供,每粒红曲胶囊含洛伐他汀为1.31 mg,辅酶Q10为6.28 μg。
1.3 仪器与试剂Micro CT仪(viva CT40,SCANCO Medical AG),BioTek Synergy 2多功能酶标仪,Eppendorf高速冷冻离心机,赛多利斯BT 25S电子天平,电感偶合等离子体发射光谱仪(ICP),858 Mini Bionix型材料测试系统(MTS,USA),羟脯氨酸测试盒购于南京建成生物工程研究所,批号:20130109。
1.4 实验方法45只SD大鼠适应性养1周后,根据体质量随机分配为5组,每组9只。① 假手术组(CON):每天灌胃蒸馏水5 mL·kg-1。② 去卵巢组(OVX):双侧去卵巢,每天灌胃蒸馏水5 mL·kg-1。③ 模型组(MOD):双侧去卵巢后,每天皮下注射D-半乳糖100 mg·kg-1。④ 己烯雌酚组(DES):造模后,每天灌胃己烯雌酚30 μg·kg-1。⑤ 红曲胶囊组(RYR):造模后,每天灌胃红曲胶囊0.5颗·kg-1。各组大鼠自由饮水和摄食,并连续灌胃给药60 d。动物每周称体重1次,并按照体重的变化来调整给药的剂量。实验结束时,用戊巴比妥钠(1.5 mL·kg-1)来进行腹腔注射,大鼠麻醉后,右心室彻底抽血以处死大鼠。取左侧股骨检测骨钙、骨磷和羟脯氨酸含量;右侧股骨做三点弯曲试验,之后再进行Micro CT检测。
1.5 观察指标及测定方法 1.5.1 大鼠体重的观察每周称大鼠体重1次,实验第8周在实验结束前停止供应饲料喂养12 h,称重,作为实验结束的最后体重。
1.5.2 大鼠骨钙、骨磷和羟脯氨酸含量的测定左侧股骨精密称重后,置于烤箱80℃烘烤72 h后至恒重,再次精密称重。随后将烘烤干的每份骨标本放入10 mL安培瓶中,加入5 mL 6 mol·L-1的HCL,酒精喷灯火烧密封安瓿瓶口后,再于108℃烤箱中消化24 h,之后取出过滤。取股骨原滤液0.25 mL,加入蒸馏水稀释至5 mL,摇匀后为稀释液。将骨稀释液分为两份:一份取骨稀释液0.25 mL,加入蒸馏水稀释至5 mL,用ICP仪检测骨Ca、P的含量,再根据标准品含量和样品稀释倍数类计算Ca、P的含量;另一份取骨稀释液1 mL,用羟脯氨酸测试盒中调pH值的乙液来调pH值到6~6.8,再加入蒸馏水稀释至10 mL,之后按照测定试剂盒的方法,测定样品的吸光度值,再根据公式计算羟脯氨酸含量。
1.5.3 大鼠骨生物力学检测方法[2]将-80℃保存的股骨常温解冻,用酒精-生理盐水复湿,用858 Mini Bionix型材料测试系统分析右侧股骨的力学性能。把大鼠股骨放在MTS试验机上,用加载速度为0.01 mm·s-1,跨距(L)为15 mm,直径为1 mm的压头测试。试验后,用游标卡尺测量股骨横断面的内外直径。计算骨截面惯性矩,并绘制应力-应变曲线,得到最大载荷(maximum load)、刚度(stiffness)、最大强度(maximum strength)、断裂强度(break strength)、弹性模量(elastic modulus)参数等。
1.5.4 大鼠骨结构的Micro CT检测及分析方法[3]将处理好的股骨下段放入Micro CT仪,对股骨近干骺端进行X-射线扫描。扫描条件为:电压70 kVp,电流114 μA,扫描时间为24.8 min(单层),间隔时间为200 ms,分辨率为中度(medium)。进行角度为180°的投射,对同一样品扫描获得500张不同截面的1024×1024像素的图片,对于股骨选取距生长板远端2 mm,层厚3 mm的骨组织为兴趣区域(ROI)进行三维重建。完成图像二值化,选定ROI内松质骨进行三维可视化呈现。定量分析使用其软件(SCANCO Medical AG),分析参数。参数包括骨体积分数(BV/TV)、骨小梁数量(Tb.N)、骨小梁分离度(Tb.Sp)、骨小梁厚度(Tb.Th)、骨密度(BMD)、结构模型指数(SMI)、连接密度(Conn-Dens)以及各向异性的程度(DA)等。
1.6 统计学分析方法实验数据均用x±s表示,采用SPSS13.0软件进行ANOVA单因素方差分析,若Levene检验方差齐性,则组间采用LSD检验;若方差不齐则采用welch校正后做方差分析,组间采用Dunnett's T3多重检验。
2 结果 2.1 各实验组大鼠体重的变化如Tab 1所示,开始用药前,大鼠体重各组间无统计学意义,各组大鼠体重随着时间的推移而逐渐增加。实验结束时,与CON组相比,OVX、MOD组的大鼠体重均明显增加,分别增加10.83%、9.45%(P<0.01)。与MOD组相比,OVX、DES组体重差别无统计学意义,但RYR组的大鼠体重降低了14.29%(P<0.01)。RYR组的大鼠体重与DES组相比,差异具有统计学意义,RYR组降低了10.45%(P<0.01)。
| Group | 0 wk(g) | 2 wk(g) | 4 wk(g) | 6 wk(g) | 8 wk(g) |
| CON | 230.53±16.32 | 247.27±15.60 | 260.01±13.76 | 264.33±16.12 | 257.12±15.16 |
| OVX | 232.40±23.32 | 252.73±28.19 | 265.25±27.38 | 281.41±23.59 | 284.97±23.34** |
| MOD | 230.77±19.84 | 255.77±18.41 | 267.94±19.30 | 277.40±19.68 | 281.41±21.73** |
| DES | 232.76±18.12 | 242.80±13.11 | 252.39±15.82 | 263.22±17.29 | 269.36±19.09 |
| RYR | 229.07±20.87 | 214.92±15.55**##△△ | 224.98±15.84**##△△ | 236.67±14.38**##△△ | 241.20±13.11##△△ |
| *P<0.05,**P<0.01 vs CON;#P<0.05,##P<0.01 vs MOD;△P<0.05,△△P<0.01 vs DES | |||||
由Tab 2可知,与CON组相比,MOD组的股骨Ca、P、Hyp含量分别降低了12.90%(P<0.05)、12.50%(P<0.01)和9.26%(P<0.05)。而与MOD组相比,RYR组Ca和P含量均明显增加,分别增加了18.52%和28.57%(P<0.01)。此外,与DES组相比,RYR组Ca和P含量明显增加,分别增加了14.28%和28.57%(P<0.01),提示去卵巢合并D-半乳糖可导致大鼠股骨骨矿物和胶原的丢失,红曲胶囊可有效改善此种骨矿物质的丢失。
| Group | BWW/g | BDW/g | Ca/g·g-1 | P/g·g-1 | Hyp/mg·g-1 |
| CON | 0.96±0.08 | 0.61±0.03 | 0.31±0.03 | 0.08±0.01 | 4.21±0.21 |
| OVX | 0.95±0.09 | 0.62±0.05 | 0.27±0.01* | 0.07±0.00** | 4.00±0.09 |
| MOD | 0.97±0.08 | 0.62±0.05 | 0.27±0.02* | 0.07±0.01** | 3.82±0.29* |
| DES | 0.96±0.08 | 0.64±0.05 | 0.28±0.01 | 0.07±0.00** | 4.08±0.12 |
| RYR | 0.95±0.07 | 0.64±0.05 | 0.32±0.01##△△ | 0.09±0.00##△△ | 3.91±0.12* |
| *P<0.05,**P<0.01 vs CON;#P<0.05,##P<0.01 vs MOD;△P<0.05,△△P<0.01 vs DES | |||||
由Tab 3可知,MOD组股骨的生物力学性能指标均较CON组的呈下降趋势,最大载荷、刚度、最大强度、断裂强度、弹性模量,分别降低了8.14%(P<0.05)、14.36%(P<0.05)、16.10%(P<0.01)、15.06%(P<0.05)和16.10%(P<0.05),且该组的斜型断裂面明显比CON组和药物组大鼠要多,提示去卵巢合并D-半乳糖可明显降低大鼠股骨的生物力学性能,容易发生骨折。与MOD组相比,两个药物的各个力学指标均有所增加:DES组中的最大载荷、刚度、最大强度分别增加了8.58%、14.27%和11.97%,差异具有统计学意义(P<0.05);RYR组的最大载荷、刚度、最大强度、断裂强度、弹性模量指标均有所增加,分别增加了3.49%、5.06%、10.92%、10.80%、3.90%,但差别无统计学意义。
| Group | Maximum load/N | Stiffness/N·mm-1 | Maximum strength/MPa | Break strength/MPa | Elastic modulus/MPa |
| CON | 188.59±9.48 | 603.55±75.30 | 253.64±31.42 | 249.93±33.69 | 13494.01±2660.91 |
| OVX | 188.67±17.66# | 570.38±90.85 | 239.77±23.13# | 227.49±38.58 | 11285.50±1625.45* |
| MOD | 173.23±15.57* | 516.91±65.34* | 212.79±22.61** | 212.29±22.94* | 11320.70±2022.21* |
| DES | 188.10±12.04# | 590.76±71.85# | 238.72±30.31# | 236.30±31.42 | 11935.61±2706.92 |
| RYR | 179.28±7.97 | 543.09±77.70 | 236.03±25.58 | 235.21±25.32 | 11762.65±1466.26 |
| *P<0.05,**P<0.01 vs CON;#P<0.05,##P<0.01 vs MOD;△P<0.05,△△P<0.01 vs DES | |||||
CT指标的变化 由Tab 4和Tab 5可知,与CON组相比,MOD组股骨Micro CT指标BV/TV、Tb.N、BMD、Conn-Dens均明显降低,分别降低了72.10%、80.21%、68.45%和77.91%(P<0.01),Tb.Sp、SMI均较CON组明显增加,分别增加了440.91%和47.67%(P<0.01),表明MOD组的大鼠股骨出现极明显严重的结构退变,提示去卵巢合并D-半乳糖对大鼠股骨造成大量的骨丢失,表现出骨质疏松症状。与MOD组相比,OVX组的DA明显降低,降低了5.92%(P<0.05);DES组股骨的BV/TV、Tb.N、Tb.Th、BMD、Conn-Dens均明显增加,分别增加了134.82%(P<0.01)、230.11%(P<0.01)、20.00%(P<0.05)、129.44(P<0.01)和168.03%(P<0.01),Tb.Sp明显降低了68.07%(P<0.01);而RYR组股骨的各项指标趋势与DES组相一致,BV/TV、Tb.N、Tb.Th、BMD、Conn-Dens均明显增加,分别增加了346.49%、425.81%、60.00%、152.51和343.03%(P<0.01),Tb.Sp和SMI均明显降低,分别降低了82.35%和59.84%(P<0.01)。与DES组相比,RYR组的BV/TV、Tb.N、Tb.Th、Conn-Dens明显升高,分别增加了90.14%(P<0.01)、59.28%(P<0.01)、33.33%(P<0.05)、65.29(P<0.01),Tb.Sp、SMI均明显降低,分别降低了44.74%(P<0.05)、58.20%(P<0.01),提示己烯雌酚与红曲胶囊均可明显增加股骨的骨量,改善骨小梁结构的退变。
| Group | BV/TV/% | Tb.N/mm-1 | Tb.Th/mm | Tb.Sp/mm |
| CON | 36.24±9.14 | 4.70±0.59 | 0.12±0.02 | 0.22±0.04 |
| OVX | 10.80±3.98** | 1.09±0.36** | 0.10±0.01 | 1.12±0.34** |
| MOD | 10.11±3.54** | 0.93±0.20** | 0.10±0.01 | 1.19±0.24** |
| DES | 23.74±4.68**## | 3.07±0.86**## | 0.12±0.01# | 0.38±0.11*## |
| RYR | 45.14±8.78**##△△ | 4.89±0.73##△△ | 0.16±0.03*##△ | 0.21±0.05##△ |
| *P<0.05,**P<0.01 vs CON;#P<0.05,##P<0.01 vs MOD;△P<0.05,△△P<0.01 vs DES | ||||
| Group | BMD/mg·cm-2 | Conn-Dens/mm-3 | SMI | DA |
| CON | 334.04±33.74 | 67.55±11.77 | 1.72±0.42 | 1.45±0.07 |
| OVX | 124.99±36.78** | 16.72±7.11** | 2.61±0.43** | 1.52±0.09*# |
| MOD | 105.39±26.47** | 14.92±6.36** | 2.54±0.48** | 1.43±0.08 |
| DES | 241.81±43.20**## | 39.99±10.93**## | 2.44±0.33** | 1.49±0.06 |
| RYR | 266.12±42.29**## | 66.10±12.49##△△ | 1.02±0.59**##△△ | 1.47±0.05 |
| *P<0.05,**P<0.01 vs CON;#P<0.05,##P<0.01 vs MOD;△P<0.05,△△P<0.01 vs DES | ||||
CT二维扫描图 如Fig 1所示,图中A为CON组,该组动物的骨小梁结构较紧密、粗细较均匀、连续性较好;C为MOD模型组,该组动物骨小梁的结构明显稀疏、细小,个别骨小梁呈结节状或钮扣状,而且出现大片无骨小梁的骨髓区;D为DES组,该组的骨小梁较C明显增粗,数目增多,连续性有一定的恢复;E为RYR组,该组的骨小梁分布排列均匀有序,连续性较好,较C在小梁骨的数量、厚度以及分布上均有明显改善。

|
| Fig 1 Micrographs of the vertical section of distal femur in ratsA:CON; B:OVX; C:MOD; D:DES; E:RYR |
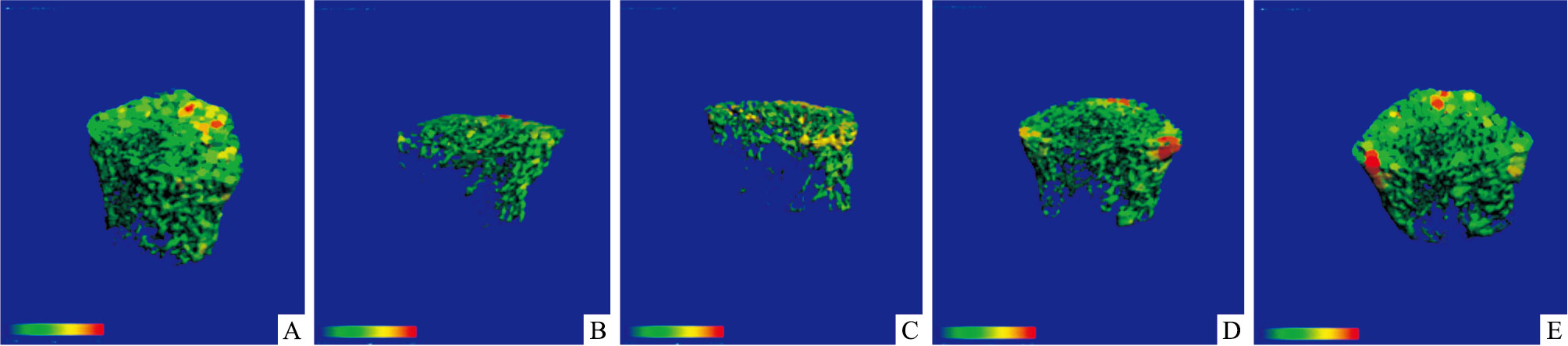
如Fig 2所示,反映骨小梁的厚度分布情况,从绿到红,反映了骨从薄到厚。通过扫描重建所得的三维图像观察到骨结构形态,以及骨小梁的数量变化情况,图中A为CON组,该组动物的骨小梁结构较紧密、粗细较均匀;C为MOD模型组,出现了骨小梁断裂、变短的情况,而且还出现了很大的间隙;D为DES组,该组的骨小梁较C明显增粗,数目增多;E为RYR组,该组的骨小梁分布排列均匀有序,连续性较好,较C在小梁骨的数量以及分布上均有明显改善。
|
| Fig 2 Trabecular thickness images of ROI of distal femur in ratsA:CON; B:OVX; C:MOD; D:DES; E:RYR |
本实验中,双侧去卵巢合并皮下注射D-半乳糖大鼠的体重随着时间推移而逐渐增加,实验结束时,比假手术组大鼠体重明显增加,说明了去卵巢合并D-半乳糖可致大鼠体重明显增加。这可能是由于去卵巢后大鼠雌激素水平降低,引起体内脂质代谢紊乱[4],导致体内脂肪堆积,从而引起实验后大鼠体重的明显增加。研究显示,去卵巢大鼠体内的MDA、H2O2脂质过氧化物含量升高,而CAT、SOD、GSH-Px活性降低[5],即抗氧化水平下降,导致自由基增多。另外D-半乳糖代谢的过程中也会产生过多的自由基,而自由基能诱导脂质体氧化。此外去卵巢后的大鼠通过蛋氨酸负荷后,高同型半胱氨酸血症可影响血管内皮细胞胆固醇的代谢,从而引起脂代谢紊乱[6]。因此去卵巢合并D-半乳糖大鼠雌激素水平降低,出现血脂紊乱,导致体重增加。
对去卵巢合并D-半乳糖大鼠股骨矿物质Ca、P,以及有机质Hyp分析中,我们观察到:与假手术组相比,去卵巢合并D-半乳糖组大鼠股骨的Ca、P和Hyp含量均明显降低,说明去卵巢合并D-半乳糖可导致大鼠股骨骨矿物和胶原的丢失。D-半乳糖可导致大鼠骨矿物质的大量丢失,可能与其产生自由基增加,形成脂质过氧化物,损伤细胞,进而抑制成骨细胞功能有关[7]。
在股骨三点弯曲实验中,我们观察到MOD组股骨的生物力学性能指标均较CON组呈下降趋势,最大载荷、刚度、最大强度、断裂强度、弹性模量均明显降低,且该组的斜型断裂面明显比CON组和药物组大鼠的要多,说明去卵巢合并D-半乳糖大鼠股骨结构力学和材料力学性能均降低,易于发生骨折。去卵巢合并D-半乳糖大鼠的最大载荷、刚度和弹性模量均明显下降,说明去卵巢合并D-半乳糖可破坏大鼠股骨的材料,同时破坏结构力学性能,即很小的力就能使其变形、断裂,提示骨折风险增加。另外,股骨是大鼠的坚硬组织,只有在承受较大的能量冲击时才会损伤或断裂,其损伤的形式分为:横形骨折和斜形骨折,横形骨折是指一条断裂线,而本实验中本组骨标本的断裂面多为斜形骨折,说明骨的质量较差。
Micro CT可以较为方便的测试骨小梁类骨标本的“量”与“质”,而且不受二维骨组织形态计量学中模型假设限制,三维成像与三维测量可直接测定骨形态参数,标本处理简单、无损等。因此,与CON组相比,MOD组股骨Micro CT指标BV/TV、Tb.N、BMD、Conn-Dens均明显降低,Tb.Sp、SMI均明显增加,说明MOD组的大鼠股骨出现极明显严重的结构退变,提示去卵巢合并D-半乳糖对大鼠股骨造成大量的骨丢失,表现出骨质疏松症状。此外MOD组股骨下段Micro CT扫描图中的骨小梁结构明显稀疏、细小,个别骨小梁呈结节状或钮扣状,而且出现大片无骨小梁的骨髓区,Micro CT各项指标说明去卵巢合并D-半乳糖大鼠股骨松质骨的骨量丢失严重,出现严重的结构退变,连接性不好,骨小梁结构形态由板状结构退变成杆状结构,出现典型的骨质疏松症状。
3.2 含辅酶Q10的红曲胶囊对去卵巢合并D-半乳糖大鼠股骨骨质疏松的影响本实验结束时,与MOD组相比,RYR组的大鼠体重明显降低,说明红曲胶囊可减轻去卵巢合并D-半乳糖大鼠的体重,效果比己烯雌酚好。红曲胶囊含有洛伐他汀,他汀类是降血脂药,为HMG-CoA还原酶抑制剂,可阻断HMG-CoA向甲羟戊酸转化从而抑制胆固醇的合成,可降低血浆总胆固醇、低密度脂蛋白胆固醇、ApoB和血浆甘油三酯的水平。另外,红曲胶囊含有辅酶Q10,辅酶Q10具有参与呼吸链电子传递、细胞抗氧化、阻止细胞凋亡、抑制低密度胆固醇氧化、减少动脉粥样硬化损伤,可修复股骨的微观参数和骨生物力学参数等多种生理功能[8]。给予红曲胶囊后,可能是通过降低去卵巢合并D-半乳糖大鼠的CHO和LDL水平,减少了脂肪的堆积,从而使体重减轻。
另外,与MOD组相比,RYR组股骨Ca和P含量均明显增加,提示红曲胶囊可使去卵巢合并D-半乳糖大鼠股骨钙和磷含量增加,表明红曲胶囊可有效预防去卵巢合并D-半乳糖可导致大鼠股骨骨矿物的丢失。孙明等[9]研究红曲对高血脂模型大鼠血液流变学的影响,发现红曲可升高红细胞的变性指数、降低红细胞聚集指数、血小板黏附率等,表明红曲能通过改善血液流变学从而改善微循环。辅酶Q10亦可清除游离自由基、抑制氧化应激反应,还可治疗微循环障碍[10],改善细胞缺氧,减轻细胞损伤。因此,红曲胶囊可能通过清除氧自由基,改善骨髓微循环等而起作用。
通过股骨三点弯曲实验,我们观察到与MOD组相比,RYR组的最大载荷、刚度、最大强度、断裂强度、弹性模量指标均有所增加,但差异无统计学意义。当骨组织受力时,就会引起变形,当受力大于一定阈值时,则骨会折断。弹性载荷、最大载荷和断裂载荷都属于骨结构力学性能,综合反映骨骼在受外力冲击时不同阶段的抵抗能力,与骨的外在结构和内在质量不相关。弹性模量体现骨的内在硬度,反映骨的抗变形能力,属于股骨材料特性,和内在质量相关,与几何结构无关。本实验结果提示,红曲胶囊不可有效提高去卵巢合并D-半乳糖大鼠股骨的结构(弹性载荷、最大载荷、断裂载荷)和材料(弹性模量)力学性能,不能修复骨骼的韧性和硬度,其原因可能是因其不能有效地改善股骨羟脯氨酸的丢失而导致。
从Micro CT扫描结果来看,与MOD组相比,RYR组股骨的BV/TV、Tb.N、Tb.Th、BMD、Conn-Dens均明显增加,Tb.Sp和SMI均明显降低,表明红曲胶囊可明显增加股骨的骨量,改善骨小梁结构的退变。另外,从Micro CT三维图可见,RYR组股骨下段的骨小梁分布排列均匀有序,连续性较好,在骨小梁的数量、厚度以及分布上均有明显改善,提示红曲胶囊可明显增加股骨的骨量,改善骨小梁微观结构的退变,并且效果优于己烯雌酚。
本实验发现,红曲胶囊具有抗去卵巢合并D-半乳糖致大鼠股骨骨量丢失,虽不能有效的改善力学性能,但抗骨丢失效果优于己烯雌酚。雌激素可增加骨密度、促进骨矿化,可预防绝经后女性骨质疏松,因此雌激素替代疗法成为了治疗骨质疏松的新型治疗方案。但随着雌激素疗法的使用及推广出现了大量的副作用。红曲胶囊具有抗骨量丢失,改善骨微结构的作用,因其含有洛伐他汀、辅酶Q10、麦角甾醇等多种有效成分,同时具有降脂、增强免疫力和抑制肿瘤生长等作用[1]。近年来发现,红曲中所含有的洛伐他汀可增加BMP-2表达和分泌,有效增加骨质中雌激素受体α的数量[11],在体外细胞培养过程中可以有效抑制骨髓基质干细胞的成脂分化[12],从而增加骨密度。我们课题组发现[13],洛伐他汀可使CCl4致肝损伤的小鼠增加骨密度,修复骨的显微结构。然而诸多基础和临床研究均发现他汀类药物的成骨潜能,但仍有一部分实验结果未能证实他汀类药物的促骨形成作用[14]。辅酶Q10是一种脂溶性抗氧化剂,能激活人体细胞和细胞能量的营养,具有提高人体免疫力、增强抗氧化、延缓衰老和增强人体活力等功能。而他汀类抑制HMG-CoA还原酶从而阻断人体内的胆固醇合成,同时抑制了辅酶Q10的合成,使体内辅酶Q10的合成减少,导致辅酶Q10在肝、肾、心肌等脏器组织能量供给不足,产生不良反应,如肝脏损伤、肌肉无力等。因此补充辅酶Q10可避免他汀类引起的转氧酶增高,并能增强他汀类的降脂作用。而且近年来发现,辅酶Q10具有潜在的抗骨质疏松作用,可以调节成骨细胞和破骨细胞的分化[15]。
3.3 小结去卵巢合并D-半乳糖可诱导大鼠出现体重增加,股骨骨成分丢失和骨力学降低,出现老年性骨质疏松的症状。而含辅酶Q10的红曲胶囊可使去卵巢合并D-半乳糖大鼠的体重明显减轻,股骨矿物质含量丢失得到恢复;股骨的骨丢失明显减轻,骨微观结构得到明显改善。虽然0.5颗·kg-1的红曲胶囊不能改善股骨力学性能,但在增加松质骨骨小梁数量上比30 μg·kg-1己烯雌酚效果要好。
( 致谢: 本文在广东医科大学药理学教研室、广东天然药物研究与开发重点实验室、上海澎立生物医药技术有限公司完成,在此对以上实验室的老师们表示感谢。 )
| [1] | Xu Q. Atorvastatin combined with coenzyme Q10 treatment of coronary heart disease early cardiac dysfunction Clinical Observation of 35 Cases[J]. Chin J Ethnomed Ethnopharm, 2016, 25 (4) : 95-7 . |
| [2] | Cui W, Liu C L. Biomechanical basis(two)-selection and calculation method of animal bone biomechanical indexes[J]. Chin J Osteop, 1998, 4 (1) : 90-2 . |
| [3] | Follet H, Farlay D, Bala Y, et al. Determinants of microdamage in elderly human vertebral trabecular bone[J]. PLoS One, 2013, 8 (2) : e55232 doi:10.1371/journal.pone.0055232. |
| [4] | Pantaleao T U, Mousovich F, Rosenthal D, et al. Effect of estradiol and leptin levels on thyroid function, food intake and body weight gain in female Wistarrats[J]. Steroids, 2010, 75 (10) : 638-42 doi:10.1016/j.steroids.2010.03.009. |
| [5] | Byun J S, Han Y S, Lee S S. The effects of yellow soybean, black soybean, and sword bean on lipid levels and oxidative stress in ovariectomizedrats[J]. Int J Vitam Nutr Res, 2010, 80 (2) : 97-106 doi:10.1024/0300-9831/a000010. |
| [6] | Shang T, Tian P L. The influence of methionine overload on blood lipids and nitric oxide in ovariectomizedrats[J]. Jilin Med J, 2014, 35 (8) : 1571-2 . |
| [7] | Mody N, Parhami F, Sarafian T A, et al. Oxidative stress modulates osteoblastic differentiation of vascular and bone cells[J]. Free Radic Biol Med, 2001, 31 (4) : 509-19 doi:10.1016/S0891-5849(01)00610-4. |
| [8] | 于琼, 吕思敏, 崔燎, 等. 辅酶Q10对环磷酰胺大鼠股骨的显微结构和生物力学的影响[J]. 中国药理学通报, 2015, 31 (3) : 421-5 . Yu Q, Lyu S M, Cui L, et al. Preventive effects of Co Q10 on trabecular microstructure and biomechanicalproperties of femur in a rat model of cyclophosphamide-induced bone loss[J]. Chin Pharmacol Bull, 2015, 31 (3) : 421-5 . |
| [9] | Sun M, Li X H, Yan W X. Effect of monascus on improving the hemorheology of rats with high blood lipids[J]. J Hyg Res, 2001, 30 (3) : 173-5 . |
| [10] | Zhang G P, Jin H M, Sen C F, et al. An experiment study on the effect of Co Q10 in improving microcirculatory disturbances[J]. J Chin Microcirc, 2005, 9 (1) : 33-5 . |
| [11] | Wang J W, Xu S W, Yang D S, et al. Locally applied simvastatin promotes fracture healing in ovariectomized rat[J]. OsteoporosInt, 2007, 18 (12) : 1641-50 doi:10.1007/s00198-007-0412-2. |
| [12] | Ji R F, Han S F. Modeling and treatment of osteoporosis[J]. China Foreign Med Treat, , 2013, 32 (35) : 197-8 . |
| [13] | 吕思敏, 于琼, 夏海珊, 等. 应用Micro CT观察洛伐他汀和秋水仙碱对CCl4致肝损伤后小鼠骨代谢的影响[J]. 中国药理学通报, 2014, 30 (8) : 1116-22 . Lyu S M, Yu Q, Xia H S, et al. Bone metabolism observation of lovastatin and colchicine in micewith liver injury induced by CCl4 with Micro CT[J]. Chin Pharmacol Bull, 2014, 30 (8) : 1116-22 . |
| [14] | von Stechow D, Fish S, Yahalom D, et al. Does simvastatin stimulate bone formation in vivo[J]. BMC Musculoskelet Disord, 2003, 4 : 8 doi:10.1186/1471-2474-4-8. |
| [15] | Moon H J, Ko W K, Jung M S, et al. Coenzyme Q10 regulates osteoclast and osteoblast differentiation[J]. J Food Sci, 2013, 7 (5) : 785-91 . |

