


活性氧(reactive oxygen species,ROS)是正常细胞代谢的一种副产物,参与多种细胞信号转导过程。当ROS产生过多或清除能力下降,机体氧化还原水平失衡,导致机体发生氧化应激(oxidative stress)损伤[1]。ROS介导的氧化应激参与众多病理生理学过程,是导致组织损伤、机体衰老、疾病和细胞凋亡的一个重要因素。如何通过内源性途径有效地维持细胞内ROS稳态,恢复机体抗氧化平衡已成为许多领域的研究热点。
FOXO3a转录因子属于叉头框转录因子家族(forkhead box,FOX)的O亚族,参与细胞内包括调节细胞周期、促进凋亡、抗氧化应激损伤等在内的多种生物学调控。研究表明,FOXO3a广泛表达于成人的各种组织器官中,包括骨骼肌、心血管系统、神经系统、肾、肝、胰腺和胸腺中。基于FOXO3a维持活性氧稳态方面的重要作用及其广泛表达、内源性等特点,为抗氧化应激损伤的研究开辟了新的途径。
2 FOXO3a的结构基础Kenyon等[2]研究秀丽线虫(C.elegans)突变体时发现,DAF-16基因在高度保守的转导通路中发挥抗氧化应激和促进长寿的作用。而DAF-16基因与哺乳动物FOXO转录因子同源,人们猜想,FOXO转录因子可能同样具有抗氧化应激和促进长寿的作用,引发了对FOXO广泛而深入的研究(Fig 1)。

|
| 图 1 Insulin signaling in mammalian cells and in C. elegans See text for further details.C.elegans DAF-2 and DAF-16 gene homologous to PI3K/Akt and FOXO respectively.DAF-2 possessing DAF-16 inhibition is similar to the PI3K/Akt suppression of FOXO |
哺乳动物的FOXO转录因子家族包含4个成员:FOXO1、FOXO4、FOXO3a和FOXO6,它们都具有由110个氨基酸组成的DNA结合结构域,其中以FOXO3a的分布和功能最为广泛[3]。FOXO3a上的Thr32、Ser253、Ser 315、Ser 644残基等磷酸化位点[4],Lys242、 Lys245氨基酸残基等乙酰化位点[5],可与细胞内的多种信号分子交互作用,从而影响FOXO3a的活性与功能。
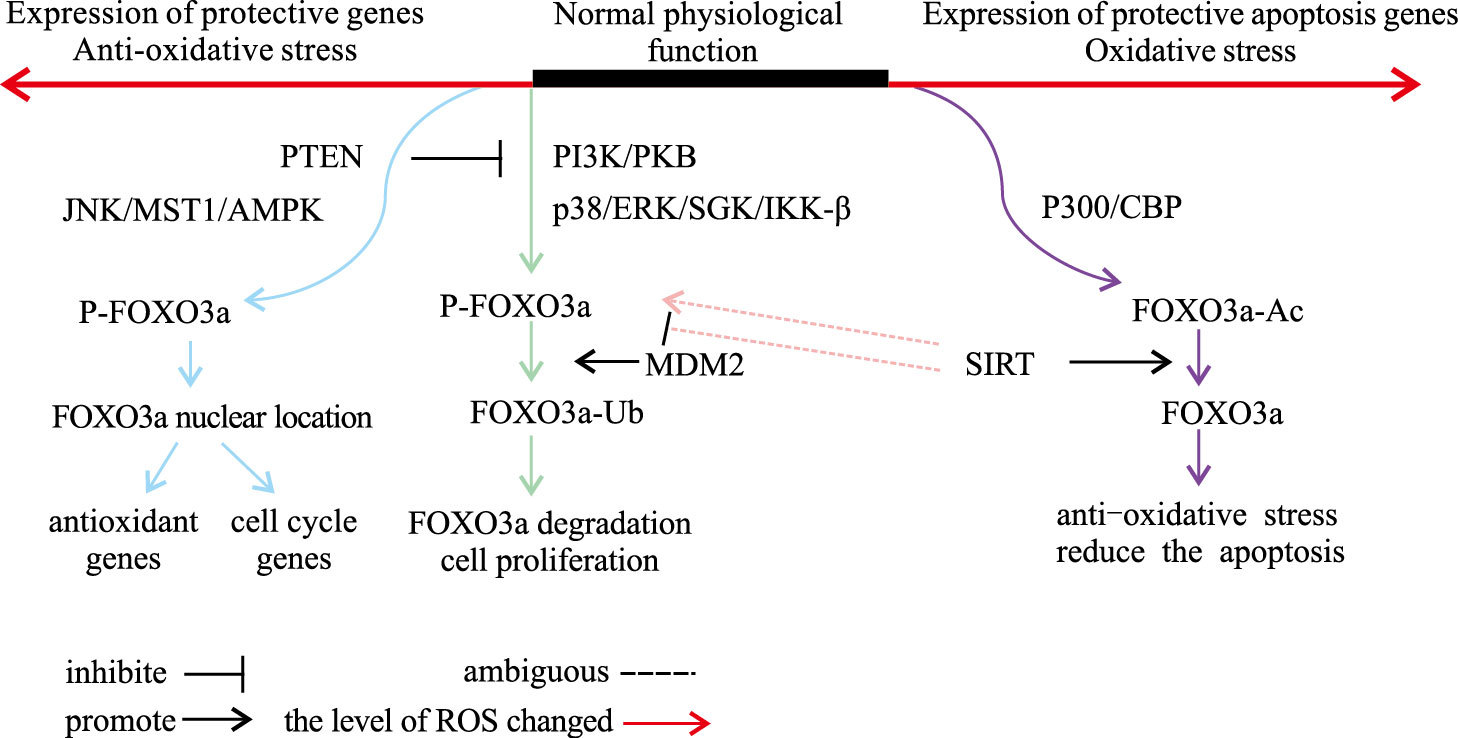
3 氧化应激对FOXO3a的调控作用当机体发生氧化应激时,累积的ROS通过激活多种信号通路,使FOXO3a发生磷酸化/去磷酸化,乙酰化/去乙酰化等翻译后修饰,从而调控FOXO3a的活性与功能。而这一过程是相当复杂,有些甚至是矛盾的。以磷酸化为例,PI3K-AKT通路与p38 MAPK(p38 mitogen-activated kinase)、ERK(extracellular-signal-regulated kinase)、SGK(serum/glucocorticoid regulatedkinase 1)、IKKβ(IkB kinase β)等激酶可使FOXO3a发生磷酸化,抑制其转录活性;而AMPK、JNK(c-Jun N-terminal kinase)、MST1等蛋白激酶则可通过磷酸化作用,增强FOXO3a的转录活性(Fig 2)。
|
| 图 2 Activation or inhibition of FOXO3a through ROS-induced posttranslational modifications |
Coskun等[6]研究发现,在HCT 116和HT-29结肠癌细胞中,PI3K-AKT信号通路在Thr32、Ser253、Ser315位点使FOXO3a发生磷酸化,磷酸化的FOXO3a与14-3-3蛋白结合形成复合物,由胞核转移到胞质,减少其转录活性,抑制细胞凋亡。Dey等[7]在乳腺癌细胞的研究中发现,使用Akt的抑制剂Iturin A,处理MDA-MB-231和 MCF-7 乳腺癌细胞后,减少了FOXO3a的磷酸化,导致FOXO3a的核内聚集,增强了其转录活性。紫铆因(butein)是一种多酚类化合物。在小鼠子宫颈癌模型中,紫铆通过抑制AKT、ERK以及p38 MAPK信号通路,减少FOXO3a的磷酸化,从而激活FOXO3a入核,增强子宫颈癌细胞对铂化合物的敏感性,发挥抗肿瘤活性[8]。p66Shc蛋白在多种组织中介导氧化应激,有研究表明,激活p66Shc 造成的氧化应激反而可增加ERK-1/2、Akt表达,增强对FOXO3a磷酸化作用,抑制FOXO3a的转录活性[9]。
FOXO3a蛋白分子经多种蛋白激酶的磷酸化作用后,与泛素连接酶E3 MDM2结合,作为MDM2的底物泛素化进而降解[10]。以上过程使FOXO3a与下游靶基因隔绝,导致FOXO3a的转录活性受到抑制。
3.1.2 FOXO3a的乙酰化CBP(cAMP binding protein,CBP)/p300(cAMP binding protein p 300)乙酰基转移酶可在叉头区Lys242、Lys245、Lys262等位点直接乙酰化FOXO3a蛋白的赖氨酸,两者以二硫键共价结合,通过这种直接的乙酰化修饰影响FOXO3a转录能力[11]。ROS可通过介导p300/CBP乙酰化作用,促使FOXO3a半胱氨酸与p300/CBP乙酰基转移酶的硫醇形成含二硫键的复合物,从而调节FOXO3a生物学功能[12]。这种氧化还原反应对FOXO3a的直接调节,表明FOXO3a蛋白作为ROS 感受器,也是氧化应激反应的中介者,对于维持胞内氧化还原稳态具有重要作用。
3.2 ROS增强FOXO3a 3.2.1 FOXO3a的磷酸化与去磷酸化心脏微血管内皮细胞的研究表明,高糖刺激引起ROS积累,可通过抑制Akt激活FOXO3a,导致FOXO3a核定位,并与下游基因结合,促进细胞凋亡[13]。PTEN是PKB/Akt抑制因子,在氧化还原反应中具有重要调控作用。研究表明,在CRC(colorectal cancer)细胞中,ROS激活通过PTEN (phosphatase and tensin homologue),抑制PI3K/AKT通路,导致FOXO3a磷酸化减少,FOXO3a转录活性增强,从而诱导Bim等靶基因表达,介导细胞凋亡[14]。
AMPK、JNK(c-Jun N-terminal kinase)、MST1等蛋白激酶可通过磷酸化作用增强FOXO3a功能。ROS积累引起的氧化应激中,JNK、MST1(mammalian sterile 20-like kinase 1)和肿瘤坏死因子(tumor necrosis factor-α ,TNF-α) 等信号分子可使FOXO3a发生磷酸化,使FOXO3a发生核转位,提高其转录活性[15]。在亚砷酸导致的氧化应激中,过量的ROS激活MST1,抑制Akt对FOXO3a的磷酸化作用,促使FOXO3a核定位并进行转录[16]。
3.2.2 FOXO3a的去乙酰化Sirtuins是NAD+依赖的脱乙酰酶家族,其中SIRT1、SIRT3、SIRT5均可通过去乙酰化作用激活FOXO3a,增加FOXO3a的转录活性,在抑制细胞凋亡、抗氧化应激损伤、细胞寿命延长方面发挥重要作用[17]。香烟提取物导致肺上皮细胞的应激中,SIRT5去乙酰化FOXO3a,减少细胞凋亡[18]。同样小胶质细胞中,Sirt3通过去乙酰化作用激活FOXO3a,降低细胞内ROS水平[19],SIRT3介导的FOXO3去乙酰化进一步减少FOXO3磷酸化、泛素化和降解,以此使FOXO3分子稳定[20],但也有研究指出内皮细胞中,SIRT1对FOXO3a的去乙酰化作用导致FOXO3a泛素化及降解,以此拮抗氧化应激介导的细胞凋亡[21]。
4 FOXO3a调控的靶基因FOXO3a被激活后可诱导下游靶基因表达,发挥多种生物学作用。FOXO3a的靶基因包括抗氧化基因、细胞凋亡和细胞周期阻滞基因等。
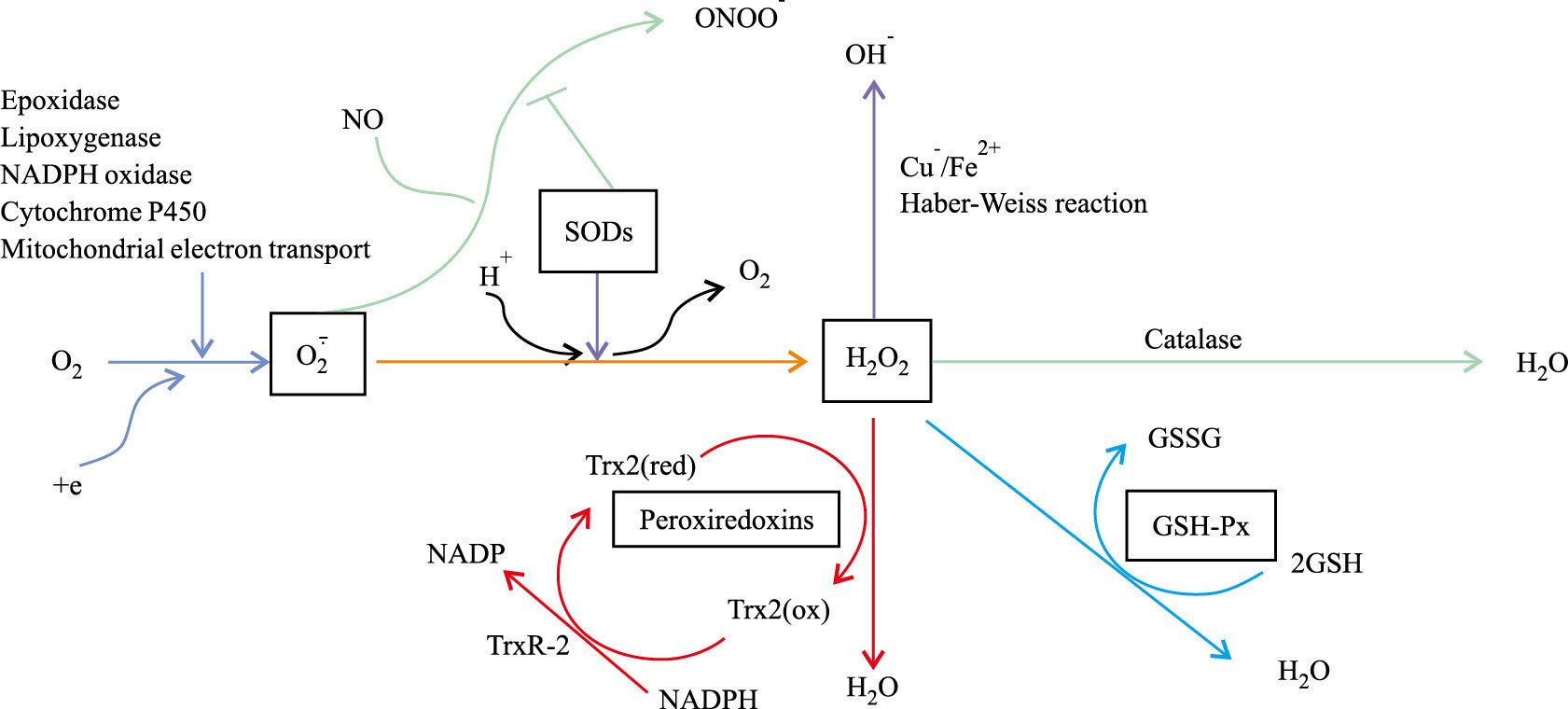
4.1 FOXO3a的靶基因:抗氧化基因正常生理状态下,细胞通过其内的解毒系统来避免内源性ROS产生过多,维持细胞内ROS的稳态,保护细胞免受损伤。ROS产生后的细胞解毒依靠抗氧化酶系统(antioxidant enzymes system)调控作用。抗氧化酶系统包括:超氧化物歧化酶(superoxide dismutases,SODs)、过氧化氢酶(catatlase)、过氧化物酶(peroxidases)等(Fig 3)。
|
| 图 3 FOXO3a target genes coding for antioxidant proteins |
正常状态下,细胞代谢活动中产生的氧自由基能被SODs歧化为氧气(O2)和过氧化氢(H2O2)。SODs在哺乳动物体内广泛存在,包括位于线粒体基质中的MnSOD,位于胞液中的Cu-ZnSOD[22]。研究表明,暴露于过氧化氢的静止期细胞通过激活FOXO3a,直接上调MnSOD的信使RNA和蛋白表达[23]。同时,当FOXO3a的转录活性受到抑制时,MnSOD的表达减少[24]。说明MnSOD的表达受到FOXO3a的调控作用。糖尿病周围神经病变(DPN )小鼠实验中,通心络胶囊可通过抑制MAPK通路提高SOD、GSH-Px活性,有效减低小鼠的氧化应激损伤[25]。Marinkovic等[26]研究发现,FOXO3a具有调控小鼠有核红细胞胞质中的Cu-ZnSOD表达的作用,进一步证明了转录因子FOXO3a在抵抗过氧化物方面发挥着重要的作用。
机体中的多种酶系统参与到了过氧化氢的分解过程,包括过氧化氢酶、谷胱甘肽过氧化物酶(GSH-Px)、抗氧化蛋白(Prxs)等,其中一些也能被FOXO3a调控。强有力的证据证明,PI3K-Akt/PKB信号通路通过调节FOXO3a的活性来增加过氧化氢酶的表达,使过氧化氢(H2O2)分解成水(H2O)和氧气(O2)[27]。值得注意的是过氧化物酶比过氧化氢酶有更高的亲和性,在低水平的H2O2时也能产生同样的效果。谷胱甘肽过氧化物酶(GSH-Px)能催化GSH变为GSSG,使一分子H2O2还原成1分子H2O。Shalini等[28]的研究显示,在caspase-2(-/-)的小鼠肝脏细胞中,FOXO3a的活性被抑制,导致机体的谷胱甘肽过氧化物酶GSH-Px、超氧化物歧化酶SOD表达减少,ROS的清除减少,机体的抗氧化能力减弱,提示FOXO3a可通过调控GSH-Px来发挥抗氧化作用。位于过氧化物酶体、胞液和线粒体上的抗氧化蛋白(Prxs)可将过氧化氢分解成氧气和水。阿霉素(doxorubicin)预处理的H9C2心肌细胞中,ROS表达增加,对FOXO3a磷酸化减少,促进FOXO3a的定位到细胞核中,激活FOXO3a的转录活性,导致Prx Ⅲ表达增加[29]。
4.2 FOXO3a的靶基因:细胞凋亡与细胞周期阻滞基因FOXO3a能增加细胞凋亡基因的表达,如Bim、FasL、TRAIL、PUMA。在结肠癌祖/干细胞中,小分子ONC201/TIC10能够抑制Akt活性。此种情况下,Akt对FOXO3a的磷酸化将减少,可激活FOXO3a的转录活性,FOXO3a定位到细胞核中,促进TRAIL的表达,从而诱导细胞凋亡[30]。同样FOXO3a还能激活细胞周期阻滞蛋白(如p21、p27)表达。p21和p27能与周期蛋白依赖性激酶(cyclin-dependent protein kinases,CDKs)结合,并抑制其活性,从而阻止细胞由G1期向S期转变。S-雌马酚可抑制cyclin B1和CDK1的表达,并通过增加FOXO3a的表达上调,增加p21和p27蛋白表达,使前列腺癌细胞发生细胞周期阻滞,同时可激活Bim和FasL基因表达,从而发挥抗肿瘤活性[31]。FOXO3a参与的细胞周期阻滞和细胞凋亡对于抑制肿瘤细胞具有重要作用,这提示FOXO3a的病理改变可能参与到细胞癌变,使其获得了不死性。
4.3 FOXO3a调控下游靶基因的“长寿理论”de Keizer等[32]认为,鉴于FOXO3a作为一种“长寿基因”,FOXO3a的调控作用需要作出微调以适应不同的ROS水平。不难想象,当细胞遇到较低水平的ROS产生时,倘若FOXO3a直接调控细胞凋亡,随着时间的积累,细胞再生的资源就会消耗殆尽,这显然与长寿不符。另一方面,对于严重的ROS损伤,如果FOXO3a依然调控损伤修复,那么这些受损的细胞就可能出现突变体,引发癌症,从而限制长寿。因此,FOXO3a作为“长寿基因”发挥其功能,不在于单纯的被激活或抑制,而在于调整其能力以适应特定的细胞氧化应激环境。
5 氧化应激相关疾病与FOXO3a在心血管系统中,内皮细胞H2O2积聚导致内皮细胞功能紊乱和动脉粥样硬化。通过激活SIRT1-FOXO3a/PGC-1α信号通路,使锰超氧化物歧化酶(MnSOD)、过氧化氢酶、抗氧化蛋白3和5(Prx3,Prx5)、硫氧还蛋白2(TRX2)、硫氧还蛋白还原酶2(TR2)及解偶联蛋白2(UCP-2)等抗氧化基因表达增加。敲除FOXO3a基因后,即使过表达SIRT1也不能使抗氧化酶表达增加[33]。心脏瓣膜手术后再狭窄主要与抑制心脏微血管内皮细胞(cardiac microvascular endothelial cell,CMECs)增殖和迁移有关,雷帕霉素治疗24 h抑制CMECs的增殖、迁移和一氧化氮(NO)的分泌,同时促进细胞凋亡和活性氧(ROS)的产生。他汀类药物可通过Akt/mTOR(mammalian target of rapamycin)/p70S6K(p70S6 Kinase)/FOXO3a信号通路,降低ROS产生,抑制细胞凋亡,促进增殖和迁移,改善内皮功能,促进血管生成过程[34]。研究发现[35],在衰老的CMECs中过表达FOXO3a,使过氧化氢酶和SOD表达增加,可显著抑制ROS的生成和p27基因的激活,但是这一过程并不能逆转衰老表型。
越来越多的证据表明,氧化应激在骨质疏松的发生发展中起到举足轻重的作用[36]。当骨组织发生氧化应激后,JNK和Mst1结合FOXO3a使其发生磷酸化,促进FOXO3a的核定位。Mst1/FOXO3a可直接诱导细胞凋亡,而JNK可通过磷酸化Mst1增强其介导的前凋亡信号,导致骨质疏松[37]。与之激活方式不同,在Bcl2(-/-)的小鼠体内,Akt的活性受到抑制,导致对FOXO3a的磷酸化减少,激活成骨细胞p53基因表达增加,介导骨质疏松的发生[38]。长期使用糖皮质激素,可诱导机体产生氧化应激,同时诱发骨质疏松[39]。Moriishi等[40]研究发现,FOXO3a既参加了糖皮质激素抑制成骨细胞分化诱发骨质疏松的过程,又能通过细胞凋亡通路增强成骨细胞分化,这两者之间似乎是矛盾的。与以往认为FOXO3a在骨质疏松中诱导细胞凋亡不同,Kim等[41]研究发现,通过激活SIRT1转录因子可使FOXO3a发生去乙酰化,使其下游抗氧化基因表达(如氧化氢酶和HO-1),同时可减少破骨细胞生成和增殖,从而抑制骨质疏松。这提示我们,FOXO3a在骨质疏松中的作用可能是复杂的,有的甚至是矛盾的。
阿尔兹海默症的发生发展也与氧化应激有关。研究发现[42],起初Cdk5(cyclin-dependent kinase 5)可直接磷酸化FOXO3a,促进FOXO3a的核定位,诱导抗氧化酶MnSOD的表达,保护细胞免受氧化应激损伤。进一步暴露于ROS后,FOXO3a则通过上调Bim和FasL基因表达,诱导细胞凋亡。提示在阿尔兹海默症中,FOXO3a介导的抗氧化调控是细胞早期暴露于ROS的结果,当机体的氧化还原反应失调后,FOXO3a会引发凋亡基因的表达。
6 问题与展望明确调控FOXO3a转录因子信号转导通路的组成、作用及其相互关系,无疑是揭示FOXO3a氧化还原调控本质并进行精确干预的重要突破口。FOXO3a作为一种重要的核转录因子,是氧化还原调控多个信号通路的交汇点,在何种内环境、何种机体状态下,FOXO3a发挥何种调控作用尚未得到明确回答。通过深入研究不同病理生理状态下FOXO3a的调控作用及其作用机制,加大基于此通路药物的研发,将会为临床有效治疗机体氧化应激损伤提供新的途径。
| [1] | Poljsak B, šuput D, Milisav I. Achieving the balance between ROS and antioxidants:when to use the synthetic antioxidants[J]. Oxid Med Cell Longev, 2013, 2013 : 956792 . |
| [2] | Kenyon C. The first long-lived mutants: discovery of the insulin/IGF-1pathway for ageing[J]. Philos Trans R Soc Lond B Biol Sci, 2011, 366 (1561) : 9-16 doi:10.1098/rstb.2010.0276. |
| [3] | Zheng F, Wu J, Zhao S, et al. Baicalein increases the expression and reciprocal interplay of RUNX3 and FOXO3a through crosstalk of AMPKα and MEK/ERK1/2 signaling pathways in human non-small cell lung cancer cells[J]. J ExpClin Cancer Res, 2015, 34 (1) : 41-54 . |
| [4] | Simon Taylor, Lam M, Pararasa C, et al. Evaluating the evidence for targeting FOXO3a in breast cancer: a systematic review[J]. Cancer Cell Int, 2015, 15 (1) : 1-9 doi:10.1186/s12935-015-0156-6. |
| [5] | Consolaro F, Ghaem-Maghami S, Bortolozzi R, et al. FOXO3a and posttranslational modifications mediate glucocorticoid sensitivity in B-ALL[J]. Mol Cancer Res, 2015, 13 (12) : 1578-90 doi:10.1158/1541-7786.MCR-15-0127. |
| [6] | Coskun D, Obakan P, Arisan E D, et al. Epibrassinolide alters PI3K/MAPK signaling axis via activating FOXO3a-induced mitochondria-mediated apoptosis in colon cancer cells[J]. Exp Cell Res, 2015, 338 (1) : 10-21 doi:10.1016/j.yexcr.2015.08.015. |
| [7] | Dey G, Bharti R, Dhanarajan G, et al. MarinelipopeptideIturin A inhibits Akt mediated GSK3β and FOXO3a signaling and triggers apoptosis in breast cancer[J]. Sci Rep, 2015, 5 : 10316 doi:10.1038/srep10316. |
| [8] | Zhang L, Yang X, Li X, et al. Butein sensitizes HeLa cells to cisplatin through the AKT and ERK/p38 MAPK pathways by targeting FOXO3a[J]. Int J Mol Med, 2015, 36 (4) : 957-66 . |
| [9] | Perrini S, Tortosa F, Natalicchio A, et al. The p66Shc protein controls redox signaling and oxidation-dependent DNA damage in human liver cells[J]. Am J Physiol Gastrointest Liver Physiol,, 2015, 309 (10) : G826-40 . |
| [10] | Yang Y C, Tang Y A, Shieh J M, et al. DNMT3B overexpression by deregulation of FOXO3a-mediated transcription repression and MDM2 overexpression in lung cancer[J]. J ThoracOncol, 2014, 9 (9) : 1305-15 . |
| [11] | Hagenbuchner J, Ausserlechner M J. Mitochondria and FOXO3: breath or die[J]. Front Physiol, 2013, 4 : 147 . |
| [12] | Dansen T B, Smits L M, van Triest M H, et al. Redox-sensitive cysteines bridge p300/CBP-mediated acetylation and FoxO4 activity[J]. Nat Chem Biol, 2009, 5 (9) : 664-72 doi:10.1038/nchembio.194. |
| [13] | Peng C, Ma J, Gao X, et al. High glucose induced oxidative stress and apoptosis in cardiac microvascular endothelial cells are regulated by FOXO3a[J]. PLoS One, 2013, 8 (11) : e79739 doi:10.1371/journal.pone.0079739. |
| [14] | Luo H, Yang Y, Duan J, et al. PTEN-regulated AKT/FOXO3a/Bim signaling contributes to reactive oxygen species-mediated apoptosis in selenite-treated colorectal cancer cells[J]. Cell Death Dis, 2013, 4 : e481 doi:10.1038/cddis.2013.3. |
| [15] | Wilk A, Urbanska K, Yang S, et al. Factor 3a counteracts high glucose/tumor necrosis factor-α-mediated neuronal damage: implications for human immunodeficiency virus encephalitis[J]. J Neurosci Res, 2011, 89 (2) : 183-98 doi:10.1002/jnr.v89.2. |
| [16] | Yamaguchi Y, Madhyastha H, Madhyastha R, et al. Arsenic acid inhibits proliferation of skin fibroblasts, and increases cellular senescence through ROS mediated MST1-FOXO signaling pathway[J]. J Toxicol Sci, 2016, 41 (1) : 105-13 doi:10.2131/jts.41.105. |
| [17] | Zhang F, Li Z L, Xu X M, et al. Protective effects of icariin-mediated SIRT1/FOXO3 signaling pathway on intestinal ischemia/reperfusion-induced acute lung injury[J]. Mol Med Rep,2015, 1852 (11) : 2442-55 . |
| [18] | Wang Y, Zhu Y, Xing S, et al. SIRT5 prevents cigarette smoke extract-induced apoptosis in lung epithelial cells via deacetylation of FOXO3[J]. Cell Stress Chaperones, 2015, 20 (5) : 805-10 doi:10.1007/s12192-015-0599-7. |
| [19] | Rangarajan P, Karthikeyan A, Lu J, et al. Sirtuin 3 regulates FOXO3a-mediated antioxidant pathway in microglia[J]. Neuroscience, 2015, 311 : 398-414 doi:10.1016/j.neuroscience.2015.10.048. |
| [20] | Tseng A H, Wu L H, Shieh S S, et al. SIRT3 interactions with FOXO3 acetylation, phosphorylation and ubiquitinylation mediate endothelial cell responses to hypoxia[J]. Biochem J, 2014, 464 (1) : 157-68 doi:10.1042/BJ20140213. |
| [21] | Sionov R V, Vlahopoulos S A, Granot Z. Regulation of bim in health and disease[J]. Oncotarget, 2015, 6 (27) : 23058-134 doi:10.18632/oncotarget. |
| [22] | Holzmeister C, Gaupels F, Geerlof A, et al. Differentialinhibition of Arabidopsis superoxidedismutases by peroxynitrite-mediated tyrosine nitration[J]. J Exp Bot, 2015, 66 (3) : 989-99 doi:10.1093/jxb/eru458. |
| [23] | Kops G J, Dansen T B, Polderman P E, et al. Forkhead transcription factor FOXO3a protects quiescent cells from oxidative stress[J]. Nature, 2002, 419 (6904) : 316-21 doi:10.1038/nature01036. |
| [24] | Callaway D A, Riquelme M A, Sharma R, et al. Caspase-2 modulates osteoclastogenesis through down-regulating oxidative stress[J]. Bone, 2015, 76 : 40-8 doi:10.1016/j.bone.2015.03.006. |
| [25] | 王超, 张会欣, 邢邯英, 等. 通心络胶囊抑制 p38 MAPK 磷酸化抑制糖尿病周围神经病变小鼠氧化应激[J]. 中国药理学通报, 2015, 31 (5) : 726-30 . Wang C, Zhang H X, Xing G Y. Tongxinluo capsule inhibits oxidative stress in diabetic peripheral neuropathy mice by inhibiting the activity of p-p38 MAPK[J]. Chin Pharmacol Bull, 2015, 31 (5) : 726-30 . |
| [26] | Marinkovic D, Zhang X, Yalcin S, et al. Foxo3 is required for the regulation of oxidative stress in erythropoiesis[J]. J Clin Invest, 2007, 117 (8) : 2133-44 doi:10.1172/JCI31807. |
| [27] | Glorieux C, Zamocky M, Sandoval J M, et al. Regulation of catalase expression in healthy and cancerous cells[J]. Free Radic Biol Med, 2015, 87 : 84-97 doi:10.1016/j.freeradbiomed.2015.06.017. |
| [28] | Shalini S, Dorstyn L, Wilson C, et al. Impaired antioxidant defence and accumulation of oxidative stress in caspase-2-deficient mice[J]. Cell Death Differ, 2012, 19 (8) : 1370-80 doi:10.1038/cdd.2012.13. |
| [29] | Liu M H, Zhang Y, He J, et al. Upregulation of peroxiredoxin Ⅲ in doxorubicin-induced cytotoxicity and the FOXO3a-dependent expression in H9c2 cardiac cells[J]. Exp Ther Med, 2015, 10 (4) : 1515-20 . |
| [30] | Prabhu V V, Allen J E, Dicker D T, et al. Small-molecule ONC201/TIC10 targets chemotherapy-resistant colorectal cancer stem-like cells in an Akt/FOXO3a/TRAIL-dependent manner[J]. Cancer Res, 2015, 75 (7) : 1423-32 doi:10.1158/0008-5472.CAN-13-3451. |
| [31] | Lu Z, Zhou R, Kong Y, et al. S-equol, a secondary metabolite of natural anticancer isoflavone daidzein, inhibits prostate cancer growth in vitro and in vivo, though activating the Akt/FOXO3a pathway[J]. Curr Cancer Drug Targets, 2015 . |
| [32] | de Keizer P L, Burgering B M, Dansen T B. Forkhead box o as a sensor,mediator, and regulator of redox signaling[J]. Antioxid Redox Signal, 2011, 14 (6) : 1093-106 doi:10.1089/ars.2010.3403. |
| [33] | Olmos Y, Sánchez-Gómez F J, Wild B, et al. SirT1 regulation of antioxidant genes is dependent on the formation of a FOXO3a/PGC-1α complex[J]. Antioxid Redox Signal, 2013, 19 (13) : 1507-21 doi:10.1089/ars.2012.4713. |
| [34] | Pan Q, Xie X, Guo Y, et al. Simvastatin promotes cardiac microvascular endothelial cells proliferation,migration and survival byphosphorylation of p70 S6K and FOXO3a[J]. Cell Biol Int, 2014, 38 (5) : 599-609 doi:10.1002/cbin.v38.5. |
| [35] | Qi X F, Chen Z Y, Xia J B, et al. FOXO3a suppresses the senescence of cardiac microvascular endothelial cells by regulating the ROS-mediated cell cycle[J]. J Mol Cell Cardiol, 2015, 81 : 114-26 doi:10.1016/j.yjmcc.2015.01.022. |
| [36] | Johnson S A, Feresin R G, Soung D Y, et al. Vitamin E suppresses ex vivo osteoclastogenesis in ovariectomized rats[J]. Food Funct, 2016, 7 (3) : 1628-33 doi:10.1039/C5FO01066G. |
| [37] | Almeida M. Unraveling the role of FoxOs in bone-insights from mouse models[J]. Bone, 2011, 49 (3) : 319-27 doi:10.1016/j.bone.2011.05.023. |
| [38] | Moriishi T, Kawai Y, Komori H, et al. Bcl2 deficiency activates FoxO through Akt inactivation and accelerates osteoblast differentiation[J]. PLoS One, 2014, 9 (1) : e86629 doi:10.1371/journal.pone.0086629. |
| [39] | Frenkel B, White W, Tuckermann J. Glucocorticoid-induced osteoporosis[J]. AdvExp Med Biol, 2015, 872 : 179-215 doi:10.1007/978-1-4939-2895-8. |
| [40] | Moriishi T, Komori T. Glucocorticoid and Bone. The inhibition of osteoblast differentiation and induction of osteocyte apoptosis through the regulation of Bcl-2 by glucocorticoids[J]. Clin Calcium, 2015, 24 (9) : 1329-36 . |
| [41] | Kim H N, Han L, Iyer S, et al. Sirtuin1 suppresses osteoclastogenesis by deacetylatingFoxOs[J]. Mol Endocrinol, 2015, 29 (10) : 1498-509 doi:10.1210/me.2015-1133. |
| [42] | Shi C, Viccaro K, Lee H G, et al. Cdk5-FOXO3a axis: initially neuroprotective, eventually neurodegenerative in Alzheimer’s disease models[J]. J Cell Sci, 2016 . |

