


卵巢癌早期即可在腹腔内种植扩散,因其生长隐秘、迅速,约70%的患者初诊时已属晚期,其死亡率在女性生殖系统恶性肿瘤中居首位,严重威胁着女性的生命健康[1]。据肿瘤干细胞学说,人们推定卵巢癌干细胞可能是卵巢癌发生、转移、侵袭、复发和耐药的根本原因,因此,清除肿瘤干细胞是改善卵巢癌治疗效果的策略之一[2-3]。有研究表明,转化生长因子β(transforming growth factor-β,TGF-β)、肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)或两者共同诱导获得肿瘤干细胞特性[4-6]。白杨素(chrysin,ChR)作为一种蜂胶中含量最高的天然黄酮类化合物,近期发现它具有抑制肿瘤干细胞自我更新的作用[7-10]。本文主要检测白杨素是否具有逆转TNF-α处理慢性暴露TGF-β诱导人卵巢癌OVCAR-3细胞系球形成作用,并探讨其作用机制是否涉及抑制核因子-κB(nuclear factor-kappa B,NF-κB)活性。
1 材料与方法 1.1 受试物与试剂白杨素购自美国Sigma 公司,用二甲基亚砜(dimethyl sulfoxide,DMSO)溶解,实验组培养体系中DMSO 的最高终浓度为不影响细胞生长速率的浓度(0.1%)。鼠抗人NF-κB(p65)抗体购自美国Santa Cruz Biotechnology公司;鼠抗人β-actin单克隆抗体购自美国Sigma-Aldrich公司。NF-κB(p65) siRNA依据GenBank(基因登记号. M61909)设计;NF-κB(p65) siRNA和乱序对照siRNA购自上海Invitrogen公司。NF-κB(p65) siRNA序列为:5’-GCCTTAATAGTAGGGTAAGTT-3’。乱序对照siRNA序列为:5’-UUCUCCGAACGUGUCACGUTT-3’。Lipofectamine RNAiMAX购自美国Invitrogen公司。TGF-β和TNF-α购自北京义翘神州生物技术有限公司。
1.2 细胞与球培养人卵巢癌OVCAR-3细胞系细胞购自中国科学院细胞库。按照文献[11-12]所述方法,进行细胞培养和球培养,分别得到单层贴壁生长细胞和非黏附克隆性生长的球(球体直径 ≥ 50.0 μm)细胞。
1.3 球形成率测定实验分组设计为Mock组:完全培养基对照组;TGF-β组: TGF-β(5.0 μg·L-1)处理OVCAR-3细胞12 d;TGF-β+TNF-α组:TGF-β(5.0 μg·L-1)处理OVCAR-3细胞12 d,或者在不同浓度白杨素(5、10、20 μmol·L-1)存在或者缺失情况下,TNF-α(10.0 μg·L-1)联合TGF-β(5.0 μg·L-1)处理24 h。分别收集细胞,并以无血清干细胞条件培养基悬浮细胞,调节细胞密度为1×106·L-1,每孔1.0 mL,接种于24孔超低黏附培养板,培养8 d,计数每孔球数目。球形成率计算公式如下:球形成率/% = 每孔肿瘤球均数/每孔接种活细胞总数(1 000个细胞)×100%。
1.4 Western blot实验提取上述处理的OVCAR-3球细胞的全细胞裂解物,测定蛋白含量。按照文献[8]所述方法,以β-actin作为内参对照,Western blot检测NF-κB(p65)蛋白水平。Alpha Imager 2200软件分别测定NF-κB(p65)蛋白信号与β-actin信号的随机灰度单位,并计算两者比值,数据以x±s表示。
1.5 NF-κBp65 siRNA转染 按照文献[8]方法,用DMEM培养基悬浮卵巢癌OVCAR-3细胞,并调节细胞密度为5×107·L-1,每孔2.0 mL,接种于6孔细胞培养板。培养24 h,细胞达到约50%融合,按照供应商说明书的方法和步骤,用Lipofectamine RNAiMAX试剂将50 nmol·L-1 NF-κB(p65) siRNA或乱序对照siRNA(Control siRNA)转染入细胞。转染24 h后进行相应TGF-β(5.0 μg·L-1)、TNF-α(10.0 μg·L-1)、白杨素处理。
1.6 统计学分析各组实验数据录入SPSS 15.0统计软件建立数据库,数据用x±s表示。采用One Way ANOVA方差分析;首先进行方差齐性检验,在方差齐性时,多组均数比较采用LSD法;在方差不齐时,多组均数间比较采用Tukey’s检验。
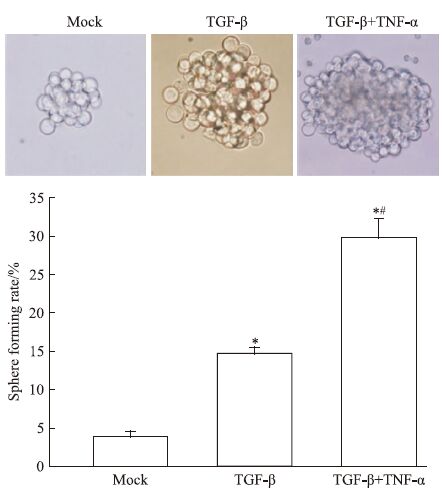
2 结果 2.1 TNF-α诱导TGF-β慢性暴露卵巢癌OVCAR-3细胞球形成干细胞条件培养基超低黏附板悬浮培养OVCAR-3细胞系细胞8 d,形成非黏附克隆性球。用球形成率测定法对比Mock、TGF-β和TNF-α+TGF-β 3组卵巢癌OVCAR-3细胞系球形成率。结果显示,与Mock组相比,TGF-β能增高卵巢癌OVCAR-3细胞系肿瘤球形成率,且TNF-α能进一步增强TGF-β诱导卵巢癌OVCAR-3细胞系球形成能力作用(Fig 1)。
|
| Fig 1 Influence of inflammatory factor TGF-β and TNF-α on rate of tumor sphere formation of ovarian OVCAR-3 cells Treatment with TGF-β and TGF-β plus TNF-α increased the rate of tumor sphere formation of ovarian OVCAR-3 cells. *P<0.05 vs untreated OVCAR-3 cells; #P<0.05 vs OVCAR-3 cells treated with 5.0 μg·L-1 TGF-β alone. |
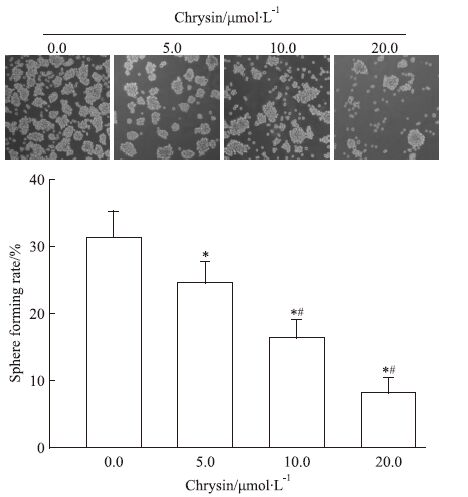
采用不同浓度(5.0、10.0、20.0 μmol·L-1)白杨素处理TGF-β+TNF-α组OVCAR-3细胞,球形成率测定法检测细胞自我更新能力作用。Fig 2结果显示,不同浓度白杨素以浓度依赖方式抑制TGF-β慢性暴露合并TNF-α处理诱导卵巢癌OVCAR-3细胞系球形成作用(P<0.05)。
|
| Fig 2 Effect of chrysin on rate of tumor sphere formation of OVCAR-3 cells induced by inflammatory factor Chrysin suppressed self-renew of ovarian stem-like cells increased by inflammatory factor in a dose dependent manner.*P<0.05 vs OVCAR-3 cells treated without chrysin;#P<0.05 vs OVCAR-3 cells treated with 5.0 μmol·L-1 chrysin. |
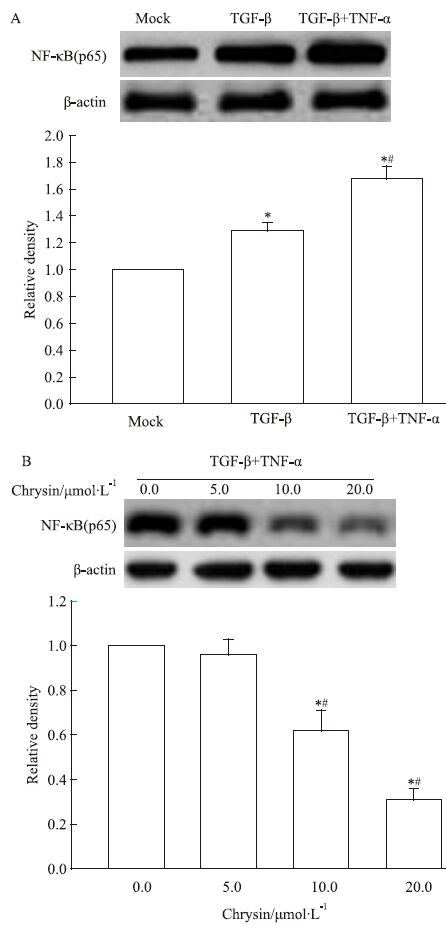
与Mock组相比,TGF-β组和TGF-β+TNF-α组卵巢癌OVCAR-3细胞NF-κB(p65)蛋白表达增强(Fig 3A)。结果说明TGF-β和TNF-α联合处理能有效地激活人卵巢癌OVCAR-3细胞NF-κB经典信号传导通路。不同浓度白杨素(5.0、10.0、20.0 μmol·L-1)孵育TGF-β慢性暴露合并TNF-α处理的卵巢癌OVCAR-3细胞,抗NF-κB(p65)抗体进行Western blot分析。结果如Fig 3B所示,白杨素以浓度依赖方式抑制TNF-α处理合并TGF-β慢性暴露增高卵巢癌OVCAR-3细胞NF-κB(p65)蛋白表达水平(P<0.05)。
|
| Fig 3 Inhibitory effect of chrysin on expression level of NF-κB(p65) in OVCAR-3 cells increased by inflammatory facto A: Comparison of the expression level of NF-κB(p65) in OVCAR-3 cells cultured with or without the inflammatory factor.*P<0.05 vs untreated OVCAR-3 cells;#P<0.05 vs OVCAR-3 cells treated with 5.0 μg·L-1 TGF-β; B: Chrysin significantly reduced the expression level of NF-κB(p65) in OVCAR-3 cells treated with TNF-α and TGF-β in a dose-dependent manner.*P<0.05 vs OVCAR-3 cells treated without chrysin.#P<0.05 vs OVCAR-3 cells treated with 5.0 μmol·L-1 chrysin. |
与乱序对照 siRNA转染细胞比较,NF-κB(p65) siRNA转染下调TGF-β和TNF-α联合处理诱导卵巢癌OVCAR-3细胞NF-κB(p65)蛋白表达(Fig 4A)和抑制球形成(Fig 4B)。同时,NF-κB(p65) siRNA转染协作白杨素抑制TNF-α处理合并TGF-β慢性暴露诱导卵巢癌OVCAR-3细胞自我更新和NF-κB(p65)蛋白表达水平增高作用。

|
| Fig 4 Inhibitory effects of chrysin enhanced by NF-κB (p65) siRNA A: NF-κB(p65) siRNA enhanced chrysin downregulating NF-κB(p65) expression in OVCAR-3 cells; B: NF-κB(p65) siRNA potentiated inhibitory effect of chrysin on the rate of tumor sphere formation of OVCAR-3 cells.*P<0.05 vs control siRNA transfected OVCAR-3 cells;#P<0.05 vs 5.0 μmol·L-1 chrysin treated control siRNA transfected OVCAR-3 cells |
致炎因子TGF-β和TNF-α诱导肿瘤细胞上皮间充质转化表型,从而赋予肿瘤干细胞功能和特性[4]。比较肿瘤球形成率大小是评价肿瘤细胞干细胞特性的一个重要指标,肿瘤球形成作用提高表示细胞的自我更新能力增强。本文采用TNF-α联合慢性暴露TGF-β方案处理卵巢癌OVCAR-3细胞,球形成率测定结果说明TGF-β(5.0 μg·L-1)联合慢性暴露TNF-α(10 μg·L-1)处理能有效地增强卵巢癌OVCAR-3细胞系细胞自我更新能力。结果显示,致炎因子促成OVCAR-3细胞系卵巢癌干样细胞表型。
卵巢癌是女性常见的生殖系统恶性肿瘤,手术治疗、放化疗是目前治疗卵巢癌的主要方法。目前,治疗卵巢癌的有效方案以铂类为基础的化疗方案为主,但是其不良反应大,影响患者治疗效果[13]。近年来,白杨素的抗肿瘤作用越来越受到人们关注,许多研究表明白杨素具有预防和治疗肿瘤作用[7-10]。本研究发现白杨素以剂量依赖方式抑制TNF-α联合慢性暴露TGF-β诱导OVCAR-3细胞系球形成并下调NF-κB(p65)蛋白表达,这些结果说明,白杨素具有抑制致炎因子诱导卵巢癌干样细胞自我更新作用。
NF-κB(p65)在细胞生长分化与凋亡、炎症反应以及肿瘤发生等生物学过程中具有重要作用,它一直是人们关注的药物作用靶点[14-16]。Li等[11]研究报道,TNF-α诱导TGF-β慢性暴露人乳腺上皮细胞和乳腺癌细胞Twist1表达需要NF-κB(p65),表明这个过程涉及激活经典NF-κB信号传导途径。本文结果也证实TNF-α联合慢性暴露TGF-β诱导上调OVCAR-3细胞NF-κB(p65)蛋白表达。为了探索NF-κB(p65)蛋白表达是否参与白杨素抑制致炎因子诱导卵巢癌OVCAR-3细胞系细胞自我更新作用,我们利用NF-κB(p65) siRNA转染技术初步探讨了白杨素逆转慢性暴露TGF-β联合TNF-α诱导卵巢癌OVCAR-3细胞系球形成的作用机制。结果显示,NF-κB(p65) siRNA转染协作白杨素抑制致炎因子诱导卵巢癌OVCAR-3细胞系细胞自我更新作用,提示联合其他相关药物可增强白杨素的抑制作用。这些结果为应用白杨素干预致炎因子诱导OVCAR-3卵巢癌干样细胞表型提供了证据,并阐释了抑制炎症与肿瘤联系的关键性转录因子NF-κB活性为白杨素的作用机制之一。
( 致谢: 本研究在湖南师范大学药物工程重点实验室完成,感谢所有给予帮助的老师和同学。 )
| [1] | Emons G, Kurzeder C, Schmalfeldt B, et al. Temsirolimus in women with platinum-refractory/resistant ovarian cancer or advanced/recurrent endometrial carcinoma[J]. Gynecol Oncol, 2016, 140 (3) : 450-6 doi:10.1016/j.ygyno.2015.12.025. |
| [2] | 于风胜, 李艺, 崔恒. 卵巢癌干细胞及卵巢癌治疗[J]. 中国实用妇科与产科杂志, 2014, 30 (1) : 14-7 . Yu F S, Li Y, Cui H. Ovarian cancer stem cells and treatment of ovarian cancer[J]. Chin J Pract Gynecol Obstet, 2014, 30 (1) : 14-7 . |
| [3] | Bar J K, Grelewski P, Lis-Nawara A, et al. The role of cancer stem cells in progressive growth and resistance of ovarian cancer: true or fiction[J]. Postep Hig Med Dosw, 2015, 69 (1077) : 86 . |
| [4] | Kong F, Zhu Y, Yuan H, et al. FOXM1 regulated by ERK pathway mediates TGF-beta 1-induced EMT in NSCLC[J]. Oncol Res, 2014, 22 (1) : 29-37 doi:10.3727/096504014X14078436004987. |
| [5] | Karin M, Greten F R. NF kappa B: Linking inflammation and immunity to cancer development and progression[J]. Nat Rev Immunol, 2005, 5 (10) : 749-59 doi:10.1038/nri1703. |
| [6] | Watabe T, Miyazono K. Roles of TGF-beta family signaling in stem cell renewal and differentiation[J]. Cell Res, 2009, 19 (1) : 103-15 doi:10.1038/cr.2008.323. |
| [7] | Ren K, Cao X, Liu Z, et al. 8-bromo-5-hydroxy-7-methoxychrysin targeting for inhibition of the properties of liver cancer stem cells by modulation of Twist signaling[J]. Int J Oncol, 2013, 43 (5) : 1719-29 . |
| [8] | Quan M, Xiao L, Liu Z, et al. 8-bromo-7-methoxychrysin inhibits properties of liver cancer stem cells via downregulation of beta-catenin[J]. World J Gastroenterol, 2013, 19 (43) : 7680-95 doi:10.3748/wjg.v19.i43.7680. |
| [9] | 周亭芳, 李高峰, 李朵, 等. 白杨素增强辐射诱导宫颈癌HeLa细胞系球形成细胞凋亡[J]. 湖南师范大学学报(医学版), 2015, 12 (3) : 1-3 . Zhou T F, Li G F, Li D, et al. Chrysin enhance radiation-induced apoptosis of sphere-forming cells from cervical cancer Hela cell line[J]. J Hunan Norm Univ(Med Sci), 2015, 12 (3) : 1-3 . |
| [10] | 曹晓正, 杨小红, 曹建国, 等. 8-溴-7-甲氧基白杨素逆转人宫颈癌SiHa细胞系球形成细胞上皮-间叶样表型转化[J]. 中国药理学通报, 2014, 30 (5) : 668-71 . Cao X Z, Yang X H, Cao J G, et al. 8-bromo-7-methoxychrysin reverses EMT of the sphere-forming cells derived from cervical cancer SiHa cell line[J]. Chin Pharmacol Bull, 2014, 30 (5) : 668-71 . |
| [11] | Li C, Xia W, Huo L, et al. Epithelial-mesenchymal transition induced by TNF-alpha requires NF-kappa B-mediated transcriptional upregulation of Twist1[J]. Cancer Res, 2012, 72 (5) : 1290-300 doi:10.1158/0008-5472.CAN-11-3123. |
| [12] | Qiu X, Wang Z, Li Y, et al. Characterization of sphere-forming cells with stem-like properties from the small cell lung cancer cell line H446[J]. Cancer Lett, 2012, 323 (2) : 161-70 doi:10.1016/j.canlet.2012.04.004. |
| [13] | 唐敏, 李鸿, 周国梅, 等. 大黄酸调控Rac1/LIMK1/cofilin信号通路抑制卵巢癌细胞运动与侵袭[J]. 中国药理学通报, 2016, 32 (3) : 366-72 . Tang M, Li H, Zhou G M, et al. Rhein inhibits the movement and invasion of human ovarian carcinoma cells through Rac1/LIMK1/cofilin signaling pathway[J]. Chin Pharmacol Bull, 2016, 32 (3) : 366-72 . |
| [14] | Arora R, Yates C, Gary B D, et al. Panepoxydone targets NF-κB and FOXM1 to inhibit proliferation, induce apoptosis and reverse epithelial to mesenchymal transition in breast cancer[J]. PLoS One, 2014, 9 (6) : 1-12 . |
| [15] | Dolcet X, Llobet D, Pallares J, et al. NF-κB in development and progression of human cancer[J]. Virchows Arch, 2005, 446 (5) : 475-82 doi:10.1007/s00428-005-1264-9. |
| [16] | Pateras I, Giaginis C, Tsigris C, et al. NF-kappa B signaling at the crossroads of inflammation and atherogenesis: searching for new therapeutic links[J]. Expert Opin Ther Tar, 2014, 18 (9) : 1089-101 doi:10.1517/14728222.2014.938051. |

