


2. 心肌电生理教育部重点实验室,四川 泸州 646000
2. Key Laboratory on Cardiac Electrophysiology of Education Ministry, Luzho Sichuan 646000,China
动脉硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD)是全球发病率和死亡率的主要原因,主要是由动脉粥样硬化导致。目前认为动脉粥样硬化是一种慢性炎症性疾病,包括内皮功能的紊乱、炎症细胞的募集、细胞因子产生以及血管壁的脂质沉积[1]。既往研究认为,动脉硬化与血脂紊乱有关,然而最近研究发现,血脂正常的自身免疫性疾病(如系统性红斑狼疮、类风湿关节炎、肠道炎症性疾病等)患者有严重的动脉粥样硬化,提示慢性炎症在动脉硬化过程中起重要作用[2-4]。
低密度脂蛋白受体(LDLr)是结合血浆来源LDL胆固醇和调节血浆胆固醇水平的主要受体,LDLr活性受细胞内胆固醇浓度的负反馈系统的严密调控[5]。该系统通过调控LDLr 介导的 LDL 摄入以及新生胆固醇合成,确保肝细胞和其他细胞内胆固醇水平稳定。因此,传统观念认为LDLr不参与细胞内胆固醇聚集以及泡沫细胞形成[6-7]。我们前期研究证实,炎症因子如脂多糖(LPS)可通过干扰巨噬细胞上LDLr负反馈调节,上调固醇调节元件结合蛋白-2(SREBP-2)及SREBP裂解激活蛋白(SCAP)的表达,天然LDL通过LDLr被巨噬细胞大量摄入,导致泡沫细胞形成。
雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)是哺乳动物细胞合成的一种丝氨酸/苏氨酸蛋白激酶。mTOR有2种细胞复合物形式,mTORC1和mTORC2,目前大多数研究都集中在mTORC1,雷帕霉素是其特异性抑制剂。近来研究发现,mTOR信号通路与SCAP/SREBP2复合物及胆固醇调控有密切联系。 但目前关于炎症应激下mTOR通路与细胞内胆固醇失稳态的关系尚不清楚。本研究探讨LPS诱导的炎症应激是否通过激活mTOR通路,增加SCAP/SREBP2表达,干扰SCAP/SREBP2负反馈调控,增加THP-1巨噬细胞对非修饰低密度脂蛋白胆固醇(LDL)摄取,导致泡沫细胞形成。
1 材料人单核细胞株(THP-1),由重庆医科大学脂质研究中心提供;细胞生长培养基RPMI 1640培养基、胎牛血清(FCS)购于Hyclone公司;低密度脂蛋白(LDL)购于广州奕源生物有限公司;青霉素、链霉素、小牛血清白蛋白(BSA)、佛波醇酯(PMA)、LPS、二甲基亚砜、四乙酸乙二胺(EDTA)、叔丁基对甲酚(BHT)、雷帕霉素(rapamycin)均购于Sigma;4%多聚甲醛、油红O、苏木精均购于北京索莱宝科技有限公司;总RNA提取试剂盒购于北京天根生化科技有限公司;逆转录试剂盒购于日本Toyobo公司;SYBR Green I PCR Mix购于日本TaKaRa公司;8联光学反应PCR管及光学盖子购于美国Bio-Rad公司;细胞蛋白提取试剂盒购自南京凯基生物技术公司;Bradford试剂购于北京百泰克生物科技有限公司;Anti-LDLr一抗、Anti-S6K1一抗、Anti-mTOR一抗购于美国ABI;鼠抗人Golgi一抗、羊抗兔Fluor(green)488 for SCAP 二抗、羊抗鼠Fluor(Red)594 for Golgi 二抗均购于Molecular Probes。
2 方法 2.1 细胞培养及分组THP-1细胞用含20%胎牛血清的RPMI 1640培养液培养,于37℃、5% CO2的细胞培养箱中培养,取对数期细胞进行实验。加佛波醇酯(160 μmol·L-1)于培养液,72 h后待悬浮细胞分化为贴壁生长的巨噬细胞后,用PBS清洗3次,换含抗氧化剂EDTA和BHT无血清培养基培养4 h,将细胞分为3组:① 对照组(5 mg·L-1 LDL);② 炎症刺激组(5 mg·L-1 LDL+200 μg·L-1 LPS);③ 炎症+雷帕霉素组(5 mg·L-1 LDL+200 μg·L-1 LPS+10 μg·L-1 Rapamycin)。以上各组细胞培养24 h后收获。
2.2 泡沫细胞鉴定待悬浮细胞分化为贴壁生长的巨噬细胞后,用PBS清洗3次,换含0.2% BSA无血清培养基培养4 h,用冷PBS清洗3次,4%多聚甲醛固定30 min,油红O染色液染色20 min,苏木精复染10 s,自来水冲洗5 min,显微镜下观察并照相。
2.3 总RNA提取和Real-timePCR 根据试剂盒操作说明提取THP-1巨噬细胞总RNA,反转录为cDNA;cDNA合成后,用SYBR GReen I PCR Master Mix进行荧光定量PCR反应,反应参数:50℃ 2 min,95℃ 5 min,然后40个循环(95℃ 20 s,55℃ 20 s,72℃ 45 s),72℃10 min 后终止。计算公式如下:实验组相对于对照组基因表达水平的倍数=-exp(△△CT),其中△△CT=实验组△CT-对照组△CT,△CT=靶基因CT值-β-actin CT值。引物序列:LDLr上游5′-GATAC CAAGGGCGTGAAGAG-3′,下游 5′-CACCAGCGAGTAGATGTCCA-3′;SREBP2上游5′-CCGCCTGTTCCGATGTACAC-3′,下游 5′-TGCACATTCAGCCAGGTTCA-3′;SCAP 上游 5′-TCTGACCGCAAACAAGGAG-3′,下游 5′-CCAGGGAAACACTGAGGACT-3′;mTOR上游 5′-GCCCTCACCTCACAAGACAT-3′,下游5′-GCTCTCTACCCAGCAGAAC-3′;β-actin 上游 5′-CCTGGCACCCACGCACAAT-3′,下游5′-GCCGATCCACACACGGAGTACT-3′。所有引物由上海生物工程技术有限公司设计。
2.4 Westernblot检测蛋白表达 收获细胞,用试剂盒提取蛋白后,定量总蛋白和胞核蛋白浓度,电泳,转膜,5%脱脂牛奶室温下封闭,用相应的一抗4℃孵育过夜,洗涤后换HRP标记二抗室温孵育1 h;最后ECL化学发光试剂A液、B液按1 ∶1混匀,均匀加至膜上,放入成像仪中采集图像,用Quantity One软件分析条带灰度值。
2.5 激光共聚焦扫描检测SCAP定位THP-1巨噬细胞经实验处理后培养于24孔板中,经PBS洗涤后,用5%福尔马林生理盐水室温下固定30 min;0.25% TritonX-100处理细胞15 min;1% BSA室温下封闭20 min;加入兔抗人SCAP 一抗(终浓度1 ∶100)和鼠抗人Golgi抗体(终浓度1 ∶100),200 μL每孔,4℃过夜;PBST洗涤后加入羊抗兔Fluor488 for SCAP 二抗(终浓度1 ∶100),室温下孵育1h;经PBST洗涤后,在激光共聚焦显微镜下观察并采集图片。
2.6 统计学分析数据用x±s表示。由SPSS 20.0统计软件处理,采用F检验比较组间差异。
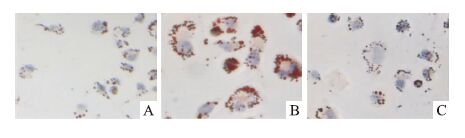
3 结果 3.1 不同干预条件对巨噬细胞内脂质沉积的影响油红O染色初步证实,与对照组比较,炎症刺激组可见明显的脂质沉积。加入雷帕霉素则抑制了细胞内脂质的沉积,见Fig 1。
|
| Fig 1 Morphological examination of macrophages with Oil Red O staining(×200) A:Control;B:LDL+LPS;C:LDL+LPS+Rapamycin |
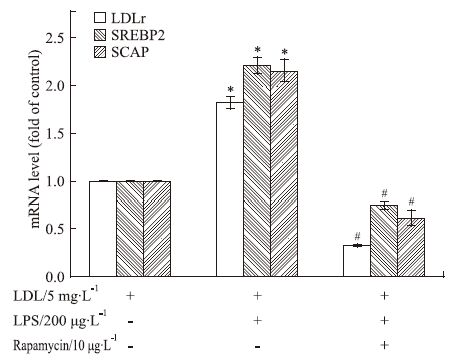
mRNA水平的影响 如Fig 2所示,与对照组比较,200 μg·L-1 LPS上调了LDLr、SREBP2和SCAP mRNA水平。加入10 μg·L-1 Rapamycin后,LDLr、SREBP2和SCAP mRNA水平被明显抑制。
|
| Fig 2 Effect of different conditions on LDLr, SREBP2 and SCAP mRNA levels in macrophages *P<0.05 vs control;#P<0.05 vs LPS alone |
mRNA水平的影响 200 μg·L-1 LPS上调了S6K1和mTOR mRNA水平。而加入10 μg·L-1 Rapamycin后,则可明显抑制S6K1和mTOR mRNA水平。见Fig 3。

|
| Fig 3 Effect of different conditions on S6K1 and mTOR mRNA levels in macrophages *P<0.05 vs control;#P<0.05 vs LPS alone |
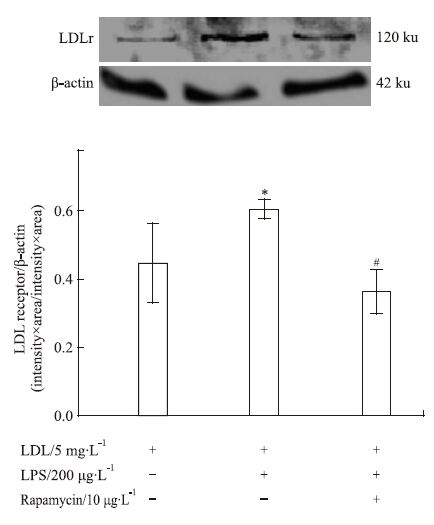
当有200 μg·L-1 LPS存在时,上调了LDLr蛋白表达。而加入10 μg·L-1 Rapamycin后,则可明显抑制LDLr蛋白表达。见Fig 4。
|
| Fig 4 Effect of different conditions on LDLr protein expression in macrophages *P<0.05 vs control;#P<0.05 vs LPS alone |
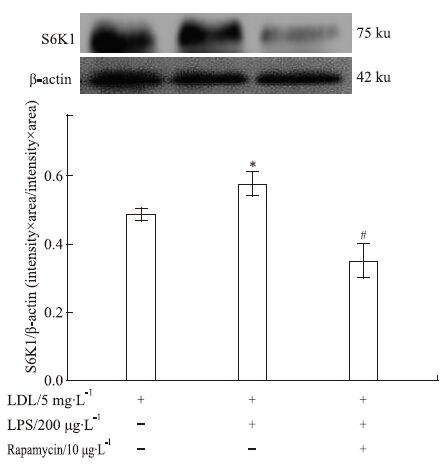
当有200 μg·L-1 LPS存在时,上调了S6K1蛋白表达。而加入10 μg·L-1 Rapamycin后,则可明显抑制S6K1蛋白表达。见Fig 5。
|
| Fig 5 Effect of different conditions on S6K1 protein expression in macrophages *P<0.05 vs control;#P<0.05 vs LPS alone |
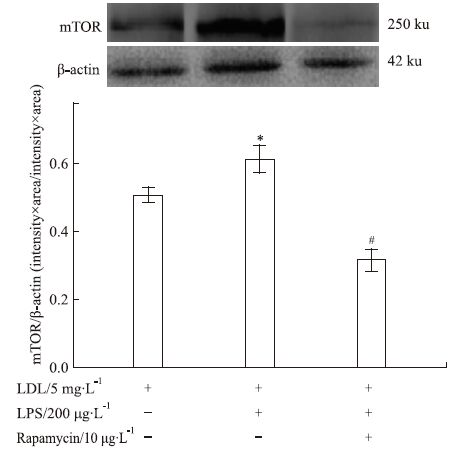
如Fig 6所示,当有200 μg·L-1 LPS存在时,上调了mTOR蛋白表达。而加入10 μg·L-1 Rapamycin后,则可明显抑制mTOR蛋白表达。
|
| Fig 6 Effect of different conditions on mTOR protein expression in macrophages *P<0.05 vs control;#P<0.05 vs LPS alone |
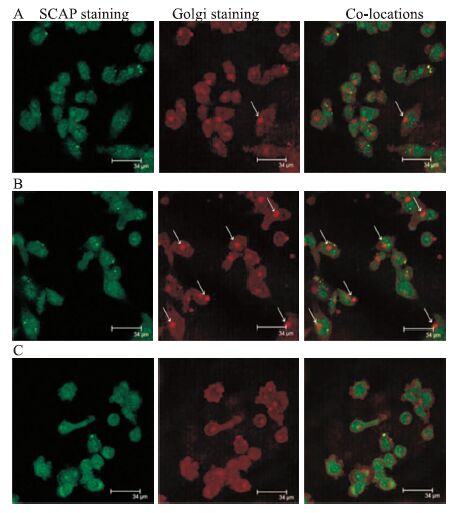
用无血清培养基培养巨噬细胞4 h后,分别加入5 mg·L-1 LDL、5 mg·L-1 LDL+200 μg·L-1 LPS、5 mg·L-1 LDL+200 μg·L-1 LPS+10 μg·L-1 Rapamycin处理24 h。用抗人的SCAP抗体和抗高尔基抗体双重染色,在激光共聚焦显微镜下观察(×1 000)。SCAP用绿色表示,高尔基体用红色表示,SCAP和高尔基体的共定位用黄色表示。结果显示,单独加入200 μg·L-1 LPS时,SCAP从内质网到高尔基体的转位异常增加;加入10 μg·L-1 Rapamycin后,明显抑制SCAP从内质网到高尔基体的转位,见Fig 7。
|
| Fig 7 Effect of different conditions on translocation of SCAP-SREBP2 complex from endoplasmic reticulum to the Golgi A: Control; B: LDL+LPS; C: LDL+LPS+Rapamycin |
mTOR是哺乳动物细胞合成的一种丝氨酸/苏氨酸蛋白激酶,有2种细胞复合物形式,mTORC1和mTORC2。目前大多数研究都集中在mTORC1,雷帕霉素是其特异性抑制剂。激活的mTOR 发挥两个方面的功能:一方面,磷酸化其下游区的效应子核糖体蛋白S6 激酶1(S6K1)和真核细胞翻译起始因子4E结合蛋白(4EBP1),从而启动翻译过程,促进细胞生长。第二,生理条件下,S6K1 和4EBP1 与真核细胞启动因子3(elF3)结合,处于无活性状态;在过度生长、炎症、应激等病理条件下,mTOR 与elF3 结合并磷酸化S6K1 和4EBP1,结果是S6K1 和4EBP1 活化,促进了翻译启动和细胞的生长[8]。因此,mTOR 在控制细胞生长及代谢方面起到中心作用。
LPS是一种常用炎症刺激物,通过作用于Toll样受体4(TLR-4)通路,进而激活转录因子-核因子κB(NF-κB),其最终生物学效应是肿瘤坏死因子-α(TNF-α)和白细胞介素-1β(IL-1β)合成分泌增加,导致炎症应激状态,故常用于细胞实验[9]。
近来研究发现,mTOR信号通路与SCAP/SREBP2复合物及胆固醇调控有密切联系[10]。研究发现,mTOR的上游调控蛋白之一,磷脂酰肌醇3激酶(PI3K)的特异性抑制剂LY294002可以明显抑制细胞内低胆固醇水平调控的SREBP2从内质网到高尔基体转位,使细胞内胆固醇持续处于低水平;同时,负性表达蛋白激酶B(DN-Akt)质粒转染的CHO细胞内胆固醇也是降低的,激光共聚焦也发现SCAP/SREBP2从内质网到高尔基体转位减少。Porstmann等[11-13]也发现mTOR特异性抑制剂雷帕霉素可以明显抑制SREBP2表达,导致细胞内胆固醇合成减少,细胞生长缓慢。
本实验发现,与对照组比较,LPS明显增加THP-1巨噬细胞组内脂质沉积,雷帕霉素则抑制了炎症组细胞内脂质的沉积(油红O染色证实)。Real-time PCR和Western blot检测发现,炎症LPS应激明显上调THP-1巨噬细胞LDLr mRNA水平和蛋白表达,促进巨噬细胞摄入胆固醇及细胞内胆固醇合成。进一步研究发现,炎症应激上调了细胞内胆固醇敏感期SCAP及其伴随蛋白SREBP2 mRNA水平,这2个蛋白是LDLr的上游调节基因,雷帕霉素抑制SCAP/SREBP2的表达,减少SCAP/SREBP2从内质网到高尔基体的转位,继而减少LDLr表达。我们检测mTOR和其下游调节因子S6K1的mRNA和蛋白表达,结果发现,炎症应激上调THP-1巨噬细胞mTOR和S6K1的mRNA和蛋白表达,提示mTOR信号通路被激活。雷帕霉素明显抑制mTOR和S6K1的mRNA和蛋白表达,继而减少SCAP/SREBP2/LDLr表达及SCAP/SREBP2转位,抑制细胞内脂质堆积,进一步证实炎症应激下THP-1巨噬细胞mTOR通路激活与细胞内脂质超载及泡沫细胞形成有关。
我们的实验数据提示,炎症应激可能是动脉粥样硬化的始动因子,在低血脂水平条件下,炎症应激同样可以促进脂质在巨噬细胞内聚积,导致巨噬细胞泡沫化。本实验给予细胞一个低水平的LDL浓度负荷,在炎症应激下却依然造成细胞内大量脂质聚集,这样或许能解释临床上有不少患者血脂正常甚至偏低,仍然有较高的动脉粥样硬化发生率,部分原因可能与炎症应激诱导脂质由血液向组织细胞分布有关[14]。
综上所述,在THP-1巨噬细胞,炎症应激通过激活mTOR通路,上调SCAP/SREBP2表达,致SCAP/SREBP2异常转位至高尔基体,上调 LDLr表达,导致细胞内胆固醇聚积,泡沫细胞形成,而雷帕霉素能够逆转炎症应激诱导mTOR通路激活,减少细胞内胆固醇沉积,提示炎症应激状态下mTOR可能是泡沫细胞形成的关键通路。
| [1] | Tuttolomondo A, Di Raimondo D, Pecoraro R, et al. Atherosclerosis as an inflammatory disease[J]. Curr Pharm Des, 2012, 18 (28) : 4266-88 doi:10.2174/138161212802481237. |
| [2] | Tanasescu C, Jurcut C, Caraiola S, et al. Endothelial dysfunction in inflammatory rheumatic diseases[J]. Rom J Intern Med, 2009, 47 (2) : 103-8 . |
| [3] | Libby P, Okamoto Y, Rocha V Z, Folco E. Inflammation in atherosclerosis: transition from theory to practice[J]. Circ J, 2010, 74 (2) : 213-20 doi:10.1253/circj.CJ-09-0706. |
| [4] | Wierda R J, Geutskens S B, Jukema J W, et al. Epigenetics in atherosclerosis and inflammation[J]. J Cell Mol Med, 2010, 14 (6A) : 1225-40 doi:10.1111/j.1582-4934.2010.01022.x. |
| [5] | Ruan X Z, Moorhead J F, Varghese Z. Lipid redistribution in renal dysfunction[J]. Kidney Int, 2008, 74 (4) : 407-9 doi:10.1038/ki.2008.226. |
| [6] | Ye Q, Chen Y, Lei H, et al. Inflammatory stress increases unmodified LDL uptake via LDL receptor: an alternative pathway for macrophage foam-cell fomation[J]. Inflamm Res, 2009, 58 (11) : 809-18 doi:10.1007/s00011-009-0052-4. |
| [7] | Ye Q, Lei H, Fan Z, et al. Difference in LDL receptor feedback regulation in macrophages and vascular smooth muscle cells: foam cell transformation under inflammatory stress[J]. Inflammation, 2014, 37 (2) : 555-65 doi:10.1007/s10753-013-9769-x. |
| [8] | Hayashi A A, Proud C G. The rapid activation of protein synthesis by growth hormone requires signaling through mTOR[J]. Am J Physiol Endoerinol Metab, 2007, 292 (6) : 1647-55 doi:10.1152/ajpendo.00674.2006. |
| [9] | 石翠格, 胡刚, 汪海. NF-κB在动脉粥样硬化中的始动作用[J]. 中国药理学通报, 2004, 20 (4) : 382-5 . Shi C G, Hu G, Wang H. Initialization effect of NF-κB on atherosclerosis[J]. Chin Pharmacol Bull, 2004, 20 (4) : 382-5 . |
| [10] | Ma K L, Liu J, Wang C X, et al. Activation of mTOR modulates SREBP-2 to induce foam cell formation through increased retinoblastoma protein phosphorylation[J]. Cardiovasc Res, 2013, 100 (3) : 450-60 doi:10.1093/cvr/cvt203. |
| [11] | Du X, Kristiana I, Wong J, Brown A J. Involvement of Akt in ER-to-Golgi transport of SCAP/SREBP: a link between a key cell proliferative pathway and membrane synthesis[J]. Mol Biol Cell, 2006, 17 (6) : 2735-45 doi:10.1091/mbc.E05-11-1094. |
| [12] | Porstmann T, Santos C R, Griffiths B, et al. SREBP activity is regulated by mTORC1 and contributes to Akt-dependent cell growth[J]. Cell Metab, 2008, 8 (3) : 224-36 doi:10.1016/j.cmet.2008.07.007. |
| [13] | Peterson T R, Sengupta S S, Harris T E, et al. mTOR complex 1 regulates lipin 1 localization to control the SREBP pathway[J]. Cell, 2011, 146 (3) : 408-20 . |
| [14] | Ruan X Z, Varghese Z, Moorhead J F. An update on the lipid nephrotoxicity hypothesis[J]. Nat Rev Nephrol, 2009, 5 (12) : 713-21 doi:10.1038/nrneph.2009.184. |

