


目前,脑卒中(stroke)已成为全球严重危害人类健康的重大疾病之一,其高致残率和高复发率特点为患者家庭和社会带来沉重的经济负担。缺血性脑卒中约占卒中发病率的70%,发病机制涉及能量代谢障碍、细胞钙离子超载、瀑布式自由基级联反应、炎性反应等环节。缺血性脑卒中的病理生理过程极其复杂,其中能量代谢障碍所引发的瀑布连锁反应,以及缺血后/再灌注损伤是导致脑组织损伤的主要原因。脑缺血/再灌注后半暗带区的神经元死亡与细胞凋亡有着密切的关系,如何有效干预缺血半暗带区受损神经元的凋亡是当前的重要课题。因此,研究引起细胞凋亡的信号转导机制可能为脑缺血疾病提供新的治疗前景。
Janus激酶-信号转导和转录激活子(Janus kinasesignal transducer and activator transcription,JAK/STAT)途径是新近发现的一条重要信号转导途径,由JAK蛋白家族和STAT蛋白家族组成。JAK/STAT通路在免疫应激、肿瘤发生以及视网膜疾病中发挥着重要的生物学效应。近年来的研究表明,许多细胞因子(IL2、IL4、IL6、IFN、CNTF等)、生长因子(EGF、PDGE、CSF等)可以通过JAK/STAT信号转导通路参与中枢神经系统的发育及神经细胞的生长、分化、凋亡等过程,并与脑卒中、脑肿瘤等中枢神经系统疾病的病理生理过程密切相关[1],但此信号通路在脑缺血后诱导神经细胞凋亡过程中的机制尚未十分清楚。现本文就JAK/STAT信号通路在缺血性脑卒中疾病中的研究进展进行综述。
1 JAK/STAT通路的结构基础 1.1 JAK激酶JAK是细胞质内一类非受体型酪氨酸蛋白激酶,溶解性强,分子量为120~130 ku,其mRNA转录范围长度为4.4~5.4 kb。迄今为止,已发现4个JAK家族成员,它们分别是JAK1、JAK2、TYK2以及JAK3。前3个成员广泛分布于各组织细胞中,而后者目前发现仅存在于骨髓及淋巴系统。JAK家族成员均含有7个高度保守的结构域(JAK homology domain,JH17),其中JH1和JH2具有催化功能。
1.2 STAT蛋白STAT是JAK的下游底物,其本质上是一类胞质蛋白,在外界信号分子刺激下可直接转入细胞核内与靶基因调控区的DNA结合,进而调节特定基因的转录与表达。STAT含有Src同源结构域2(Src homology 2,SH2)和Src同源结构域3(Src homology 3,SH3),以及可结合特定的含磷酸化酪氨酸的N末端氨基酸序列。目前在哺乳动物中已发现STAT的7个家族成员,分别是STAT1、STAT2、STAT3、STAT4、STAT5a、STAT5b、STAT6,分子量在84 ku~113 ku之间。STAT广泛存在于各种类型的组织和细胞中。人类的多种肿瘤均易导致STAT3的高度激活,诱导Bcl2、Bclx的过度表达,从而利于肿瘤细胞存活而加重病情。有研究报道,心肌缺血后诱导的STAT3异常激活,能够保护心肌细胞抵抗缺血性损伤。但脑缺血导致的STAT3异常激活的确切作用尚未明确。
2 JAK/STAT信号转导通路的活化过程与调控机制 2.1 JAK/STAT信号通路的活化过程JAK/STAT信号转导通路的活化始于细胞外的多种配体(IFN、LIF、EGF等)与膜上相应的受体结合,使与之偶联的JAK产生聚集而被磷酸化激活,活化后的JAK催化STAT上的酪氨酸残基磷酸化,磷酸化的酪氨酸残基与附近的氨基酸序列形成“停泊位点”(docking site)。此时,STAT通过特异SH2结构域结合到“停泊位点”后催化自身磷酸化反应而被激活。活化的STAT离开受体,互相结合形成同源或异源二聚体向核内移动,并与靶基因的启动子结合,直接激活靶基因表达,完成胞外信号分子介导的信号转导过程,从而表达相应的效应。STAT参与调节的基因范围很广:STAT1和STAT2介导IFN调节基因的表达;催乳素诱导靶基因的表达需要STAT5;IL4诱导的免疫球蛋白类型的转换需要STAT6;而研究最多的STAT3不仅参与IL19在人血管平滑肌细胞中的炎性反应调节[2],还在IL6诱导的急性反应期靶基因的表达中发挥重要作用。
2.2 JAK/STAT信号通路的负反馈调控机制JAK/STAT 通路的调控是在JAK 的激活、STAT 核内转运以及负反馈调节等多个方向上进行的。其中负反馈调节是最复杂,也是研究最深入的方向之一。
JAK/STAT信号通路依赖于自身的负反馈调节机制,使其整体处于动态平衡及精确调控中。目前对其具体的调控机制尚未十分清楚,但现在可以确定有3种不同类型的抑制蛋白与此通路的负反馈调节密切相关:细胞信号转导抑制蛋白(suppressor of cytokine signaling,SOCS);蛋白酪氨酸磷酸酶(PTPs),如SHP1/2 和CD45;STAT蛋白抑制因子(PIAS)。
2.2.1 SOCS蛋白家族已有确切研究证实,SOCS家族参与JAK/STAT信号转导通路的负反馈调控过程[3]。迄今为止,SOCS家族的8个成员为大家所知:SOCS1SOCS7以及CIS,其结构中都含有1个SH2结构域和1个C端SOCS盒。SOCS能与特异性细胞因子结合,通过JAK/STAT通路诱导转录SOCS mRNA,而其表达产物又可特异性的抑制细胞因子介导的JAK/STAT信号通路。目前研究发现,SOCS至少通过3种不同的途径对JAK/STAT通路进行这种负性调控:(1) 利用SH2结构域竞争性抑制JAK激酶与底物结合,从而阻断通路的信号传导;(2) SOCS通过与细胞因子受体结合使STAT的活化受阻;(3) 通过SOCS盒促进SOCS所结合的信号因子发生泛酸化降解。
促红细胞生成素(erythropoietin,EPO)及其受体(erythropoietin receptor,EPOR)是调节红系祖细胞增殖和分化的重要细胞因子。有研究发现,EPOEPOR可能通过JAK/STAT/BclxL通路对局灶性脑缺血大鼠提供神经保护作用[4]。有文献报道SOCS家族另一成员CIS可与EPOR的Y401结合而抑制EPO信号转导,而Y401正是EPOR与STAT5的结合位点之一。提示CIS可能通过与STAT5竞争性结合EPOR而达到调节信号转导的作用。
2.2.2 蛋白酪氨酸磷酸酶(PTPs)蛋白酪氨酸磷酸化是胞外信号分子信息传递的一个重要途径。在细胞内,酪氨酸磷酸化是一个可逆的动力学过程,蛋白酪氨酸激酶(PTKs)催化酪氨酸磷酸化,而PTPs催化去磷酸化过程。PTPs可分为3大类:特异性酪氨酸PTPs、双重特异性PTPs以及低分子量的PTPs。其中双重特异性PTPs又包括MAP 磷酸酶激酶(MKPs)、细胞周期调节因子CDC25 磷酸酶和肿瘤抑制因子PTEN等。CDC25 磷酸酶作为细胞周期调控中的核心因子,可以通过磷酸化激活周期蛋白依赖性蛋白激酶(CDK),进而实现对细胞周期的推进作用[5]。
CD45 又称为白细胞共同抗原,是一种单链跨膜糖蛋白,是PTPs家族成员。CD45广泛存在于造血细胞(T细胞、B细胞和巨噬细胞等)表面,能直接结合JAK,使JAK的酪氨酸残基去磷酸化而抑制其酶活性,从而对多种细胞因子信号转导起负调节作用。研究表明,CD45可以通过JAK/STAT信号转导通路,调控一些细胞因子的激活、分化和增殖[6]。有文献报道[7],IL6能刺激人骨髓瘤细胞系Sko007细胞中CD45 mRNA 和蛋白的表达明显增强,进一步研究证实这种生物学效应是由JAK/STAT 信号途径的活化介导。
SHP1和SHP2是均含2个SH2 区的PTPs,前者主要表达于造血系统中,通过其SH2结构域与EPOR第429位酪氨酸磷酸化的特异结合,从而表现EPO相应的效应。而Y429的缺失或者突变,使得EPOR不能结合SHP1,不仅对此种变异细胞表现出超高的敏感性,而且使JAK2的酪氨酸磷酸化水平长时间保持在较高范围。上述现象提示EPOR与SHP1结合后,通过其PTP活性使JAK2去磷酸化而失活,从而终止信号通路的转导[8]。不同于SHP1,SHP2已被证实参与多条转导通路的信号传递过程,如PI3K/AKT 通路、JAK/STAT通路、RAS/MARK 通路、JNK 通路、NFκB 通路等[9]。有研究发现[10],在IFNα诱导的JAK/STAT信号转导通路中,IFNα与其受体结合后激活JAK1 和TYK2,而SHP2可能是通过引起STAT1和STAT2的酪氨酸去磷酸化,下调JAK/STAT的活性来抑制IFNα的细胞毒性。
2.2.3 STAT蛋白抑制因子(PIAS)PIAS(protein inhibitor of activated STAT)蛋白家族成为近年来生物研究领域备受关注的热点。PIAS蛋白家族至少由5个成员组成:PIAS1、PIAS3、PIASxα、PIASxβ、PIASy,它们在结构上含有4个共同的结构域特征,包括1个N端SAP结构域、1个RING型锌链结构域、1个“PINIT” 结构域以及一段丝/苏氨酸富集序列。许多染色质连接蛋白中都存在SAP结构域,它主要参与序列或结构的DNA连接。
PIAS1、PIAS3分别与活化的STAT1和STAT3特异性结合,阻断STAT的转录与表达[11-12]。有研究发现,PIAS3可以通过抑制Akt的磷酸化,阻断PI3K/Akt信号通路的传导,从而发挥治疗肿瘤疾病的作用[13]。此外,PIASxα、PIASxβ能与STAT4相互作用,招募HDAC等抑制因子,形成转录抑制复合物,从而抑制STAT的活性[14]。
2.2.4 其他途径调节此外,还有其他途径的负调节机制,如:泛素蛋白酶体途径介导的蛋白降解、STATs的Ser去磷酸化以及天然STATs突变体等[15]。Smad 泛素化调节因子1(Smad ubiquitination regulation factor 1,Smurf l)是一种可以介导多种蛋白泛素化降解的HECT型泛素连接酶。Yuan等[16]研究发现,Smurf l可以介导STAT1发生K48位泛素化,并被26S蛋白酶体识别降解,且此过程不依赖STAT1的磷酸化。
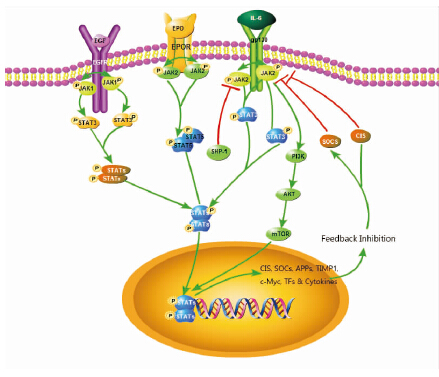
|
| Fig 1 Relevant signal molecule network diagram based on JAK/STAT pathway |
缺血后脑组织中JAK1[17]、JAK2、STAT1[17]、STAT3[18]阳性细胞表达均上调,出现脑水肿、梗死面积扩大、神经功能障碍等现象[19],研究发现,STAT1、STAT3的过度活化有促进神经元凋亡的作用,它能降低抗凋亡基因Bcl2、Bclx的表达。针刺对缺血性脑损伤有着多层次、多环节、多靶点的保护作用。有研究报道,电针治疗能明显改善脑缺血模型大鼠的神经功能,明显提高JAK1蛋白活性[20],提高STAT3、STAT5水平和STAT3 mRNA的表达,抑制STAT1基因表达[21],激活机体自我保护机制,达到有效抑制脑缺血后神经元凋亡的作用。
方舒东等[18]建立短暂性脑缺血大鼠模型,探讨大鼠短暂脑缺血/再灌注(I/R)后STAT3表达与神经元凋亡的关系。研究发现,STAT3蛋白高表达与神经元凋亡两者的时间段和部位基本一致。表现为全脑I/R后24h海马CA1区凋亡细胞数随着STAT3蛋白表达的增多而增多。从而推测STAT3的表达增强可能介导缺血性脑损伤的信号转导过程,并在脑缺血损伤神经元凋亡过程中扮演着重要角色。过氧化物酶体增殖物激活受体γ(PPARγ)是核激素受体家族成员之一,参与体内多种病理生理过程。研究发现[22],PPARγ激动剂能通过上调缺血/再灌注脑组织中PPARγ蛋白的表达,加强对缺血脑组织的保护作用 。进一步的实验证实,PPARγ激动剂能抑制缺血/再灌注大鼠再灌注区JAK2、STAT3的磷酸化,降低缺血/再灌注损伤大鼠的神经功能评分,减轻脑组织缺血/再灌注损伤[23]。推测PPARγ激动剂可能通过下调脑细胞内JAK2/STAT3信号通路来减轻脑缺血/再灌注后的损伤程度。李晋娜等[24]在探讨重组人促红细胞生成素(rhEPO)对慢性脑缺血大鼠的JAK/STAT信号通路的影响研究中发现,rhEPO能激活JAK2/STAT3信号转导通路,上调Bcl2和下调Bax的表达,达到减缓慢性脑缺血大鼠神经元凋亡的作用。刘荣[20]在研究中发现,脑缺血后使用电针治疗能提高脑皮质内JAK1的活性,减轻脑缺血损伤,参与修复受损组织。这种保护机制可能通过抑制炎性细胞因子介导的JAK2/STAT3信号通路来实现的。有研究证实[25],应用电针预处理可通过CB1(大麻素受体1)受体上调pSTAT3水平,从而促进脑缺血后超氧化物歧化酶2(SOD2)表达发挥脑保护作用。
目前尚未有研究报道STAT2蛋白参与脑缺血性损伤过程。从通路发现至今对缺血性脑卒中后有关JAK/STAT信号转导通路的干预与调节相关方面的研究报道较少,有待深入的实验研究以填补这一相关领域。
3.2 JAK/STAT信号通路在中药治疗缺血性脑卒中疾病中的研究进展缺血性脑卒中的危害性使得寻找其有效地预防治疗方法变得极其重要和迫切,中药因其多成分多靶点,在脑缺血/再灌注损伤的保护方面具有独到的优势。下面就目前研究较多的通路展开论述:
3.2.1 作用于JAK2/STAT3信号通路由16味中药制备而成的步长脑心通具有脑保护作用,通过抑制JAK2STAT3通路起到神经保护的作用。黎艳[26]灌胃脑缺血模型大鼠步长脑心通后发现,pJAK2、pSTAT3表达明显降低,脑梗死面积缩小,细胞凋亡减少。此结果显示,步长脑心通能通过抑制脑缺血大鼠脑组织的JAK2/STAT3信号通路,发挥脑神经保护作用。彭玲玲[27]采用相似的方法探讨怀牛膝对脑损伤大鼠脑组织pJAK2、pSTAT3蛋白表达的影响,发现怀牛膝的脑保护机制与上述相似。王凯华等[28]探讨补阳还五汤对JAK2/STAT3通路在缺血/再灌注脑损伤中的调控作用,发现给予AG490和补阳还五汤后,pJAK2、pSTAT3的表达水平均较模型组低,神经元凋亡数量也有所减少。上述结果提示补阳还五汤可能通过抑制JAK2/STAT3信号通路的激活发挥脑保护作用。
3.2.2 作用于JAK2/STAT5信号通路EPO作为一种神经递质,可以通过与相应受体结合引发一系列的信号转导,参与缺血后的脑保护。有研究显示,EPO可能通过与相应靶细胞表面EPOR结合成二聚体,磷酸化激活JAK2,使其自身磷酸化,继而引起下游信号转导,调节细胞凋亡。潘平康等[29]在研究中发现大鼠脑缺血后应用葛根素,能明显缩小梗死面积,降低EPO和STAT5表达水平,而此作用可能是通过EPORJAK2STAT5信号转导通路实现的。还有文献报道[30]葛根素能通过上调STAT3 mRNA的含量,下调NFκBp65 mRNA的表达,对脑缺血/再灌注产生抗炎保护作用。
电针能提高脑缺血皮质pSTAT5蛋白的表达,此现象与触发STAT5所诱导的相关细胞因子通路相关。梁超[31]发现,电针能促进EPO和EPO mRNA的表达,提高JAK2、STAT5磷酸化水平,从而改善脑缺血/再灌注后局部皮质病理形态变化,减轻缺血性脑损伤作用。
还有其他中药有效成分参与调控脑损伤疾病的病理过程,如姜黄素通过激活SHP2达到抑制JAK/STAT通路的作用,进而减轻脑小胶质细胞的炎症反应[32]。有研究发现[33],地黄单一活性成分梓醇可以上调脑缺血区EPO、EPOR、VEGF及pSTAT3的表达,加速缺血脑区的血管新生与重塑,推测梓醇调控血管新生可能与JAK2/STAT3信号通路相关。丹参水溶性成分——丹参多酚酸可能通过JAK2/STAT3信号通路,调节血管生长因子VEGF、Ang1、Ang2水平,以促进脑缺血后血管生成,改善神经功能障碍[34]。
综上所述,由于中药体系的复杂性,JAK/STAT通路虽作为单一信号转导通路,中药单方、复方或其有效成分可以通过干预JAK/STAT通路信号转导环节上的不同节点,上调或下调靶基因蛋白表达,发挥相应作用,最终达到减轻缺血性脑损伤的目的。目前对于JAK/STAT通路在缺血性脑卒中疾病中具体的调控机制尚未有定论,所以更需要我们进行深入研究,试图阐明清楚中药药效基础—即中药活性成分与JAK/STAT信号通路结合的位点之间的差异及其规律,为开发新一类有中医药特色的抗脑缺血疾病的新药提供研发方向。
4 结语与展望缺血性脑卒中是全球当前三大致死性疾病之一,其发病机制由多因素、多环节、多途径损伤的酶促级联反应调控,其中缺血后恢复脑血流,再灌注导致的缺血性损伤是该疾病发病严重的主要原因之一,因此研究如何防治脑缺血后/再灌注损伤成为当今医学界亟待解决的重要课题。JAK/STAT是人体重要的细胞内信号转导通路,它的缺陷和异常活化与多种疾病的发生发展及预后的关系正日益受到人们的关注,现已明确此通路的激活与脑缺血/再灌注损伤的病理生理过程密切相关[35]。有大量文献证实,JAKs、STATs的家族成员(包括JAK1、JAK2、STAT1、STAT3、STAT5等)在脑缺血疾病的发病过程中扮演着重要的角色。目前主要发现有3种不同蛋白(SOCS、PTPs、PIAS)参与JAK/STAT信号转导通路的负调控过程,机体通过对JAKs、STATs活化的持续时间和强度进行精准调节,使其整体维持在动态平衡中。据此,本文较系统地绘制了JAK/STAT途径相关信号因子在调控脑缺血/再灌注损伤的相互关系图,便于在整体上较全面地认识缺血性脑卒中疾病的病理过程。
如前所述,目前已有研究证实,多种中药或其有效成分可以通过调节JAK/STAT通路家族成员或上下游靶基因的表达,产生相应的生物学效应,进而减少脑缺血后神经元的凋亡数量,减轻缺血后脑组织损伤程度。但该治疗机制复杂,要阐明其具体机制需要我们进一步研究和深入探讨。同时,我们可以学习借鉴并研究国内外关于缺血性脑卒中损伤机制的最新研究成果,在以最新理念对脑缺血疾病损伤机制进行科学诠释的基础上,进一步开发中药宝库资源,从中药多靶点治疗脑卒中角度入手,从多方面阐释中药的抗缺血性脑卒中发病机制,为中药制剂治疗脑缺血疾病提供更确切的理论依据,为中药治疗卒中时代带来新的契机。
| [1] | Lai S Y, Johnson F M. Defining the role of the JAKSTAT pathway in head and neck and thoracic malignancies:implications for future therapeutic approaches[J]. Drug Resist Updat, 2010, 13 (3) : 67-78 doi:10.1016/j.drup.2010.04.001. |
| [2] | Gabunia K, Ellison S P, Singh H, et al. Interleukin19(IL19) induces heme oxygenase1 (HO1) expression and decreases reactive oxygen species in human vascular smooth muscle cells[J]. J Biol Chem, 2012, 287 (4) : 2477-84 doi:10.1074/jbc.M111.312470. |
| [3] | Bjorbaek C, Elmquist J K, ElHaschimi K, et al. Activation of SOCS3 messenger ribonucleic acid in the hypothalamus by ciliary neurotrophic factor[J]. Endocrinology, 1999, 140 (5) : 2035-43 . |
| [4] | Sola A, Rogido M, Lee B H, et al. Erythropoietin after focal cerebral ischemia activates the Janus kinasesignal transducer and activator of transcription signaling pathway and improves brain injury in postnatal day 7 rats[J]. Pediatr Res, 2005, 57 (4) : 481-7 doi:10.1203/01.PDR.0000155760.88664.06. |
| [5] | 孙松娴, 濮文渊, 张斌, 等. 细胞周期调控因子CDC25A及其抑制剂在肿瘤治疗中的研究进展[J]. 肿瘤, 2014, 34 (8) : 758-63 . Sun S X, Pu W Y, Zhang B, et al. Advances in research on the role of CDC25A in the treatment of tumor[J]. Tumor, 2014, 34 (8) : 758-63 . |
| [6] | Yamada T, Zhu D C, Saxon A, Zhang K. CD45 controls interleukin4mediated IgE class switch recombination in human B cells through its function as a Janus kinase phosphatase[J]. J Biol Chem, 2002, 277 (32) : 28830-5 doi:10.1074/jbc.M201781200. |
| [7] | 宋伦, 黎燕, 孙英勋, 等. IL6 诱导人骨髓瘤细胞表达CD45[J]. 中国免疫学杂志, 2001, 17 (6) : 309-13 . Song L, Li Y, Sun Y X, et al. Induction of CD45 expression in a myeloma cell line by IL6[J]. Chin J Immunol, 2001, 17 (6) : 309-13 . |
| [8] | 张纪岩. JAKSTATs信号转导通路的调控[J]. 国外医学免疫学分册, 2000, 23 (2) : 83-5 . Zhang J Y. Regulation of JAKSTATs signal transduction pathway[J]. Foreign Med Sci:Immunol, 2000, 23 (2) : 83-5 . |
| [9] | 蔡洪科, 邓甬川. 蛋白酪氨酸磷酸酶SHP2研究进展[J]. 浙江大学学报(医学版), 2012, 41 (5) : 581-5 . Cai H K, Deng Y C. Research progress of protein tyrosine phosphatase SHP2[J]. J Zhejiang Univ Med Sci, 2012, 41 (5) : 581-5 . |
| [10] | Du Z, Shen Y, Yang W, et al. Inhibition of IFNalpha signaling by a PKC and protein tyrosine phosphatase SHP2dependent pathway[J]. Proc Natl Acad Sci USA, 2005, 102 (29) : 10267-72 doi:10.1073/pnas.0408854102. |
| [11] | Chung C D, Liao J, Liu B, et al. Specific inhibition of Stat3 signal transduction by PIAS3[J]. Science, 1997, 278 (5344) : 1803-5 doi:10.1126/science.278.5344.1803. |
| [12] | O'Shea J J, Gadina M, Schreiber R D. Cytokine signaling in 2002:new surprises in the JAK/STAT pathway[J]. Cell, 2002, 109 (Suppl) : S121-31 . |
| [13] | Ogata Y, Osaki T, Naka T, et al. Overexpression of PIAS3 suppresses cell growth and restores the drug sensitivity of human lung cancer cells in association with PI3K/Akt inactivation[J]. Neoplasia, 2006, 8 (10) : 817-25 doi:10.1593/neo.06409. |
| [14] | Arora T, Liu B, He H. PIASx is a transcriptional corepressor of signal transducer and activator of transcription 4[J]. J Biol Chem, 2003, 278 (24) : 21327-30 doi:10.1074/jbc.C300119200. |
| [15] | 李积东, 吴洪福. JAKSTAT信号转导通路的负调节机制[J]. 青海医学院学报, 2005, 26 (2) : 134-7 . Li J D, Wu H F. Negative regulation mechanism of JAKSTAT signal transduction pathway[J]. J Qinghai Med Coll, 2005, 26 (2) : 134-7 . |
| [16] | Yuan C, Qi J N, Zhao X Y, Gao C J. Smurfl protein negatively regulates interferonγ signaling through promoting STATl protein ubiquitination and degradation[J]. J Biol Chem, 2012, 287 (21) : 17006-15 doi:10.1074/jbc.M112.341198. |
| [17] | 王莉安, 毕辉, 纪红蕊, 等. 蚓激酶对缺血/再灌注大鼠脑内JAKSTAT通路的作用[J]. 中国药学杂志, 2009, 44 (24) : 1862-65 . Wang L A, Bi H, Ji H R, et al. Effect of Lumbrokinase on JAKSTAT pathway in rat brain during cerebral ischemia and reperfusion[J]. Chin Pharm J, 2009, 44 (24) : 1862-65 . |
| [18] | 方舒东, 朱也森, 姜虹, 孙宇. 大鼠短暂性全脑缺血后STAT3表达与神经元凋亡的关系[J]. 上海交通大学学报(医学版), 2007, 27 (2) : 193-6 . Fang S D, Zhu Y S, Jiang H, Sun Y. Relationship between STAT3 expression and neuron apoptosis following transient global cerebral ischemia in rats[J]. J Shanghai Jiaotong Univ Med Sci, 2007, 27 (2) : 193-6 . |
| [19] | 钟华萍. 缺血后处理对大鼠局灶性脑缺血/再灌注后STAT3、Caspase3表达的影响[D]. 泸州:泸州医学院, 2012. |
| [20] | 刘荣. JAKs激酶在电针抗缺血性脑损伤中作用的研究[D]. 广州:广州中医药大学, 2012. Liu R. Study of Janus kinases in electroacupuncture effects on ameliorating cerebral ischemia[D]. Guangzhou: Guangzhou University of Chinese Medicine, 2012. |
| [21] | 于 涛. 脑缺血后脑内STAT系统调控及电针干预作用的研究[D]. 广州:广州中医药大学, 2009. Yu T. Study on regu1ation of STAT's signaltransduction system and the acupunctureintervention after cerebralischemia[D]. Guangzhou:Guangzhou University of Chinese Medicine, 2009. |
| [22] | Lee J, Reding M. Effector of thiazolidinediones on stroke recovery:a casematched controlled study[J]. Neurochem, 2006, 20 (8) : 2375-7 . |
| [23] | LiaoX M, SunJ, TangY G, 等. The influence of PPARγ agonists pioglitazone on focal cerebral ischemiareperfusion injury and JAK2/STAT3 signal transduction pathway[J]. Chin J Nerv Ment Dis, 2012, 38 (10) : 593-6 . |
| [24] | 李晋娜, 张金, 杨清洁, 郭军红. 慢性脑缺血大鼠rhEPO经鼻给药激活JAK2/STAT3通路及对Bcl2和Bax表达的影响[J]. 中国临床研究, 2015, 28 (6) : 693-701 . Li J N, Zhang J, Yang Q J, Guo J H. Activating JAK2/STAT3 pathway by rhEPO via intranasal administration and its impact on Bcl2 and Bax in rats with chronic cerebral ischemia[J]. Chin J Clin Res, 2015, 28 (6) : 693-701 . |
| [25] | 孙思斯. CB1 受体介导 STAT3 磷酸化上调 SOD2参与电针预处理脑保护的研究[D]. 西安:第四军医大学, 2014. Sun S S. SOD2 upregulation by electroacupuncture attenuates ischemic oxidative damage via cannabinoid CB1mediated STAT3 phosphorylation in stroke mice[D].Xi'an: The Fourth Military Medical University, 2014. |
| [26] | 黎艳. 步长脑心通对脑缺血/再灌注大鼠脑组织JAK2/STAT3信号通路的影响[J]. 黑龙江中医药, 2013, 1 : 37-9 . Li Y. Effects of Buchangnaoxintong on JAK2/STAT3 signaling pathway in cerebral ischemia reperfusion rats[J]. Heilongjiang J Tradit Chin Med, 2013, 1 : 37-9 . |
| [27] | 彭玲玲. 怀牛膝对颅脑损伤大鼠脑组织PJAK2、PSTAT3蛋白表达的影响[D]. 南宁:广西医科大学, 2012. Peng L L. The effect of radix achyranthis bidentatae on expression of the PJAK2 and PSTAT3 protein in the severe traumatic brain injury rats[D].Nanning: Guangxi Medical University, 2012. |
| [28] | 王凯华, 任丁, 黄龙坚. 补阳还五汤对大鼠脑缺血/再灌注后JAK2/STAT3的影响[J]. 陕西中医, 2013, 34 (8) : 1093-6 . Wang K H, Ren D, Huang L J. Effect of Buyanghuanwu decoction on JAK2/STAT3 after cerebral ischemia and reperfusion in rats[J]. Shaanxi J Tradit Chin Med, 2013, 34 (8) : 1093-6 . |
| [29] | 潘平康, 张超, 吴海琴, 等. 葛根素对大鼠脑缺血后海马中EPO和STAT5表达的影响[J]. 卒中与神经疾病, 2013, 20 (3) : 137-40 . Pan P K, Zhang C, Wu H Q, et al. Effects of puerarin on the expression of erythropoietin and STAT5 in the hippocampus of cerebral ischemia injuryed in rats[J]. Stroke Nerv Dis, 2013, 20 (3) : 137-40 . |
| [30] | 梅志刚, 王明智, 刘晓洁, 曾永保. 葛根素对大鼠脑缺血/再灌注损伤α7nAChR?NFкBp65及STAT3 mRNA表达的影响[J]. 中华中医药杂志, 2013, 28 (1) : 113-7 . Mei Z G, Wang M Z, Liu X J, Zeng Y B. Effect of puerarin on mRNA expression of α7nAChR,NFкBp65 and STAT3 in brain after cerebral ischemiareperfusion in rats[J]. Chin J Tradit Chin Med Pharm, 2013, 28 (1) : 113-7 . |
| [31] | 梁 超. 电针对脑缺血/再灌注大鼠脑皮质局部血流量和血管新生的影响研究[D]. 武汉:湖北中医药大学, 2014. Liang C. The study about effects of Electroacupuncture therapy on the regional cerebral blood flow and angiogenesis of the cerebral ischemia reperfusion rats cortex[D]. Wuhan: Hubei University of Chinese Medicine, 2014. |
| [32] | Kim H Y, Park E J, Joe E H, Jou I. Curcumin suppresses Janus kinaseSTAT inflammatory signaling through activation of Src homology 2 domaincontaining tyrosine phosphatase 2 in brain microglia[J]. J Immunol, 2003, 171 (11) : 6072-9 doi:10.4049/jimmunol.171.11.6072. |
| [33] | 王静欢, 邹利, 万东, 等. 梓醇多效性相关信号通路研究进展[J]. 中国药理学通报, 2015, 31 (9) : 1189-94 . Wang J H, Zou L, Wan D, et al. Review of Catalpo's pleiotropic signaling pathways[J]. Chin Pharmacol Bull, 2015, 31 (9) : 1189-94 . |
| [34] | 李耀汝. 注射用丹参多酚酸通过JAK2/STAT3信号通路促进脑缺血小鼠血管生成及改善行为功能[D]. 石家庄:河北医科大学, 2015. Li Y R. Salvianolic acids promotes angiogenesis and improves functional recovery after cerebral ischemia in mice through JAK2/STAT3 signaling pathway[D].Shijiazhuang: Hebei Medical University, 2015. |
| [35] | Choi J S, Kim S Y, Cha J H, et al. Upregulation of gp130 and STAT3 activation in the rat hippocampus following transient forebrain ischemia[J]. Glia, 2003, 41 (3) : 237-46 doi:10.1002/(ISSN)1098-1136. |

