


2. 复旦大学附属华山医院 中医科,上海 200040
2. Dept of Traditional Chinese Medicine,Huashan Hospital of Fudan University,Shanghai 200040,China
现代研究表明,肥胖作为一种低度炎症[1],可以促进以胰岛素抵抗为中心环节的多种代谢综合症,如高血糖、高血压、高血脂、2型糖尿病的发生发展。脂肪细胞中糖脂代谢失衡会导致脂肪组织中脂肪细胞增多及肿大,引发肥胖的发生与发展。三黄汤(sanhuang decoction,SHD)主要由黄芪、黄连、蒲黄等中药组成,依据国家自主知识产权的专利药物益气散聚方(公开号:CN 101530517A)的精简方(三黄方,医院协定处方)配制;该方具有推动气化、活血散瘀、清热祛湿、调脂消炎的功效;临床应用多年,用于治疗以糖脂异常、腹部肥胖、非酒精性脂肪肝等为主要症状的代谢综合症患者。前期,我们已报道了SHD(又名三黄口服液、益气汤)的制备方法,并对其进行了严格的质量控制研究,表明其主要化学成分为异喹啉类生物碱、绿原酸、黄酮类成分,另外含有少量的三萜皂苷类、倍半萜类化合物和其它有机酸类等[2-3]。本研究通过观察SHD对胰岛素抵抗3T3-L1脂肪细胞糖脂代谢的影响,以及对脂肪细胞糖转运过程起限速作用的GLUT-4表达的影响,探讨SHD改善脂肪细胞糖脂代谢的作用与机制,为临床应用提供理论支持。
1 材料 1.1 实验对象3T3-L1细胞株(购自中国科学院上海细胞典藏所)。
1.2 药品与试剂三黄汤(复旦大学附属华山医院制剂室制备,药材总含量4.20 g·mL-1,小檗碱、巴马汀、药根碱、绿原酸含量分别为8.39、1.74、0.76、1.96 g·L-1,患者口服量为1.20 g·kg-1·d-1;通常由医院制剂室统一煎制后发给患者,目前尚未成为正式院内制剂)由黄芪、黄连、蒲黄、泽泻、茵陈组成,药材全部购自上海虹桥中药饮片有限公司;马来酸罗格列酮(纯度>98%,郑州荔诺生物科技有限公司);小牛血清(Gibco,批号:1270008);优级胎牛血清(Gibco,批号:1300001);地塞米松(批号:123K11611)、胰岛素(Sigma,批号:096K16911)、3-异丁基-1-甲基黄嘌呤(Sigma,批号:BCBF4310 V)、油红O (Amresco,批号:2716B062);DMEM高糖培养基(Gibco,批号:1290007);KRP缓冲液(131.2×10-3 mol·L-1 NaCl、4.71×10-3 mol·L-1 KCl、2.47×10-3 mol·L-1 CaCl2、2.48×10-3 mol·L-1 Na3PO4、1.24×10-3 mol·L-1 MgSO4,10×10-3 mol·L-1 HEPES,pH7.4)、2-脱氧-[3H]-葡萄糖(武汉楷伦化学新材料有限公司);脱脂奶粉、硝酸纤维膜购自北京普利莱基因技术有限公司;葡萄糖临床检测试剂盒(上海荣盛生物技术有限公司,批号:20081013);甘油三酯试剂盒(南京建成生物工程研究所,批号:20130702),甘油含量测试盒(南京建成生物工程研究所,批号:E1002);游离脂肪酸测试盒(日本和光纯药工业株式会社,批号:KMM5430);TRIzol(Invitrogen,批号:5189701);反转录试剂盒(Fermentas,批号:00057250);SYBR Green PCR试剂盒(美国ABI公司,批号:0905051);引物由上海生工生物技术有限公司合成。考马斯亮蓝蛋白测定试剂盒(南京建成生物工程研究所,批号:20140521);蛋白Marker(Fermentas Life Science公司,批号:SM0671);兔抗大鼠β-actin一抗(美国SantaCruz公司,批号:0807);小鼠抗大鼠GLUT4抗体(R&D公司,批号:BKZ01);辣根过氧化物酶标记的山羊抗兔二抗(批号:ZB-2301)和辣根过氧化物酶标记的山羊抗小鼠二抗(批号:ZB-2305)、增强化学发光法(ECL)试剂盒(批号:GG98315)均为美国Pierce公司产品;丙烯酰胺(4.21 mol·L-1)-甲叉双丙烯酰胺(5.22×10-2 mol·L-1)、2×Sample Buffer、吐温20均购自北京鼎国生物技术有限责任公司。
1.3 仪器高速冷冻离心机(德国 Sigma公司,型号:2-16PK),二氧化碳培养箱(Thermo,型号:Heracell150I),倒置荧光显微镜(Nikon,型号:Ti-U),荧光定量PCR仪(ABI公司,型号:7500),酶标仪(BioTek,型号:SynergyHT),电泳仪(Tanon公司,EPS 300);转移脱色摇床(上海琪特分析仪器有限公司,型号:STS-8A);凝胶成像分析仪(GE公司,型号:LAS 3000)。
2 方法 2.1 构建3T3-L1脂肪细胞胰岛素抵抗模型与秦佑[4]报道方法类似,简言之,将3T3-L1细胞株,置于含10%小牛血清的高糖DMEM培养基中,37℃、饱和湿度、5% CO2培养箱内培养。待细胞融合2 d后(分化0 d),加含0.50×10-3 mol·L-1 3-异丁基-1-甲基黄嘌呤,1.01×10-6 mol·L-1地塞米松,1.72×10-4 mol·L-1 (1.0 mg·L-1)胰岛素,10%胎牛血清的DMEM高糖培养基培养72 h(分化3 d),换以含1.72×10-4 mol·L-1胰岛素的培养基再培养48 h(分化5 d),随后以10%胎牛血清的DMEM高糖培养基继续培养,每2 d 换培养液1次。
2.2 实验分组24孔板培养3T3-L1脂肪细胞,分化d 10进行分组。空白对照组(Con):10%胎牛血清的DMEM;三黄汤分为5个剂量组:相对生药量2.5、5、10、20、40 g·L-1;罗格列酮对照组(Ros):罗格列酮1.0×10-5 mol·L-1。每个试验药物重复6孔,各孔给予同等体积培养液培养,37 ℃温育24 h。
2.3 脂肪细胞染色鉴定采用油红O染色方法观察脂肪细胞分化情况[4]。3.33×10-3 mol·L-1甲醛室温下固定细胞1 h,PBS洗3次,应用浮片法油红O溶液室温染色2 h,用异丙醇洗去未着色的染料,然后用苏木精复染细胞核,明场镜下观察拍摄。
2.4 葡萄糖消耗与TG分解产物测定收集培养上清,应用葡萄糖氧化酶-过氧化物酶(GOD-POD)法测定残存的葡萄糖浓度,以未经培养的培养基中葡萄糖浓度与之相减得出葡萄糖消耗量,同时采用bicinchoninic acid(BCA)法测定总蛋白浓度,以mol·g-1·Pro校正结果;应用甘油激酶-甘油磷酸氧化酶-过氧化物酶法测定游离甘油的浓度;应用酯酰辅酶A合成酶-酯酰辅酶A氧化酶(ACS-ACOD)法测定NEFA浓度;各实验的具体步骤根据试剂说明书进行。
2.5 细胞内TG含量测定细胞刮刀收集脂肪细胞,37 ℃-液氮反复冻融3次裂解细胞,1 000 r·min-1离心5 min,应用甘油磷酸氧化酶-过氧化物酶(GPO-POD)法测定TG浓度,测定细胞蛋白浓度,以mol·mg-1·Pro校正细胞内TG含量。
2.6 葡萄糖转运实验将上述诱导好的3T3-L1细胞以KRP缓冲液洗3次,再以含有胰岛素(1.0×10-8 mol·L-1)的KRP缓冲液孵育30 min,加入含2-脱氧-[3H]-葡萄糖(1.85×104 Bq·mL-1)的KRP缓冲液孵育10 min,然后以预冷的含0.01 mol·L-1葡萄糖的PBS液快速洗涤3次终止反应,再加入1 mL NaOH(1.0×10-4 mol·L-1),2 h后取0.2 mL细胞裂解液于闪烁液中避光放置12 h,用液体闪烁计数器进行计数。另设一组细胞加入细胞松弛素B(1.0×10-5 mol·L-1)作为对照,所有数据减去该值,作为各组葡萄糖摄取率。
2.7 逆转录及实时定量PCR(real-timePCR)检测GLUT-4 mRNA的表达根据TRIzol说明书抽提细胞总RNA,紫外分光光度计测定浓度[5],由上海生工生物工程技术服务有限公司合成。取3 μg总RNA以Oligo(dT)18为引物,M-MuLV反转录酶反应总体积20 μL,其中2 μL cDNA样本进行PCR扩增。GLUT-4引物上游:5′-CCCCGCTGGAATGAGGTTTTTGAGGTGAT-3′,下游:5′-CAG ACAGGGGCCGAAGATTGGGAGACAGT-3′;β-actin引物上游:5′-GAGACCTTCAACACCCCAGCC-3′,下游:5′-AATGTCACGCACGATTTCCC-3′。PCR扩增条件:95℃预变性10 min,95℃ 25 s,55℃ 25 s,72℃ 50 s,共40个循环,72℃后延伸5 min。反应结束由7500软件分析结果,计算CT(每个反应管内的荧光信号到达设定的域值时所经历的循环数)值,为避免假阳性信号,使用熔解曲线来检查非特异性产物的构成。以β-actin基因为内标参照,使用比较法(△△CT)来计算基因的相对定量。
2.8 Westernblot检测GLUT-4蛋白的表达 与袁芳[6]报道方法类似,简要过程为:取15 μL样品经SDS聚丙烯酰胺凝胶电泳分离,转移到硝酸纤维素膜上,再用含脱脂奶粉和Tween20的TBST室温下封闭2 h后加入兔抗小鼠GLUT-4抗体(1 ∶1 000)和抗β-actin抗体(1 ∶1 000)孵育(一抗),4℃摇床上过夜,然后以吐温/PBS洗涤膜3次,每次10 min;加辣根过氧化物酶标记的羊抗兔IgG抗体(二抗)孵育膜,室温轻摇2 h,充分洗涤后用ECL显影曝光,洗片。扫描仪扫描电泳条带,用“MultiGauge”(version 3.1)软件进行光密度积分值分析,计算出GLUT-4与内参照β-actin的光密度积分值之比作为GLUT-4的相对含量值。
2.9 数据分析实验数据采用SAS 7.0统计软件分析,数据用x±s表示;两组间比较采用团体t检验,方差不齐时采用非参数统计方法中的两样本秩和检验(rank sum test)。
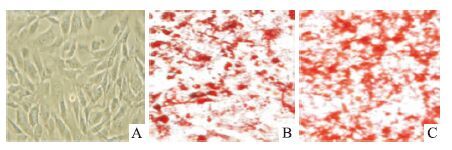
3 结果 3.1 脂肪细胞分化前后形态学变化3T3-L1前脂肪细胞为梭形,呈纤维母细胞的形态,细胞质内无脂滴。诱导分化后,细胞变大变圆,细胞质内逐渐出现脂滴,8~12 d后分化率85%以上。分化成熟的脂肪细胞,胞质内大量脂滴聚集于核周,脂滴可被油红O染成红色。见Fig 1。
|
| Fig 1 Morphological changes of 3T3-L1 adipocyte before and after differentiation(×200) A:3T3-L1 adipocyte before differentiation;B:3T3-L1 adipocyte before differentiation stained with oil O;C:3T3-L1 adipocyte after differentiation stained with oil O |
与Con比较,三黄汤各剂量组、罗格列酮对照组不同程度促进细胞葡萄糖摄取利用,培养上清葡萄糖消耗量较对照组均明显增加(P<0.01,除2.5 g·L-1组外),其中SHD各剂量组(由低到高)、Ros较对照组分别增加102%、120%、150%、166%、154%、215%;三黄汤降低细胞内TG积累(P<0.05或0.01),罗格列酮使细胞内TG积累增加(P<0.01);中高剂量的三黄汤增加细胞培养上清中甘油含量但降低游离脂肪酸的含量,作用明显(P<0.01);罗格列酮对培养上清中甘油和游离脂肪酸含量作用不明显(P>0.05)。结果见Tab 1。在实验条件下,20 g·L-1的三黄汤对胰岛素抵抗的3T3-L1细胞糖脂代谢的调节作用接近最大化。
| Group | Culture supernatant | Intracellular TG /mol·g-1 Pro | ||
| Glucose consumption/mol·g-1 Pro | Glycerol/10-3·mol·L-1 | NEFA/10-3·mol·L-1 | ||
| Con | 3.06±0.11 | 0.05±0.01 | 0.79±0.20 | 1.19±0.24 |
| SHD 2.5/g·L-1 | 3.12±0.26 | 0.07±0.02 | 0.75±0.18 | 0.93±0.17* |
| SHD 5/g·L-1 | 3.69±0.38** | 0.12±0.03** | 0.69±0.14** | 0.71±0.12** |
| SHD 10/g·L-1 | 4.58±0.42** | 0.17±0.03** | 0.63±0.14** | 0.66±0.12** |
| SHD 20/g·L-1 | 5.08±0.26** | 0.25±0.05** | 0.46±0.11** | 0.52±0.10** |
| SHD 40/g·L-1 | 4.71±0.46** | 0.18±0.04** | 0.60±0.10** | 0.62±0.05** |
| Ros | 6.60±0.42** | 0.06±0.01 | 0.85±0.22 | 1.65±0.36** |
| **P<0.01,*P<0.05 vs Con | ||||
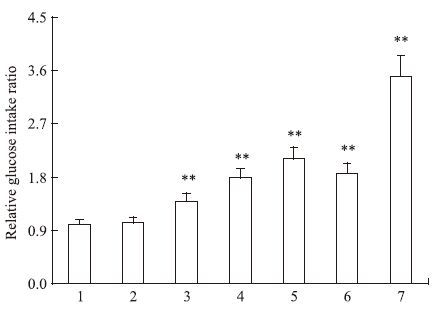
将Con组葡萄糖摄取率设为1,较正常细胞葡萄糖摄取率下降58.1%。干预12 h后,葡萄糖摄取率发生明显变化。由低到高三黄汤各剂量组、罗格列酮对照组不同程度促进胰岛素抵抗的3T3-L1脂肪细胞葡萄糖摄取率(P<0.01,除2.5 g·L-1三黄汤组外),它们较Con组分别增加2%、39%、78%、111%、86%、251%;2.5 g·L-1的三黄汤不能明显增加胰岛素抵抗的3T3-L1脂肪细胞葡萄糖摄取率(P>0.05),但有增加趋势。提示干预时间为12 h的条件下,20 g·L-1三黄汤对脂肪细胞葡萄糖摄取率的作用接近最大化,见Fig 2。
|
| Fig 2 Dose-effect of SHD on glucose intake ratio of insulin resistant 3T3-L1 adipocytes(x±s,n=6) 1:Con group;2:SHD 2.5 g·L-1 group;3:SHD 5 g·L-1 group;4:SHD 10 g·L-1 group;5:SHD 20 g·L-1 group;6:SHD 40 g·L-1 group;7:Ros group.**P<0.01 vs control group |
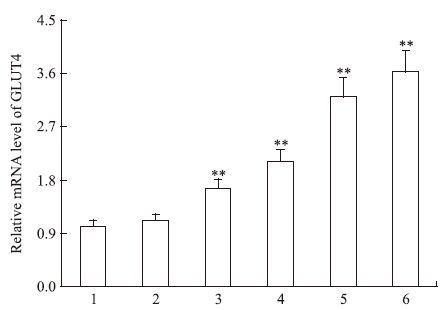
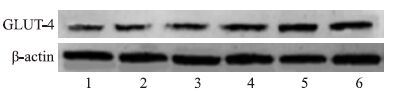
与Con组比较,三黄汤各剂量组及罗格列酮组均能不同程度升高脂肪细胞GLUT-4的mRNA和蛋白表达水平;其中中高剂量的三黄汤组、罗格列酮组与Con组相比较,对GLUT-4的mRNA表达水平的差异有统计学意义(P<0.01)。见Fig 3和Fig 4。
|
| Fig 3 Effect of SHD on expression of GLUT4 mRNA in 3T3-L1 adipocytes by real-time PCR 1:Con group;2:SHD 2.5 g·L-1 group;3:SHD 5 g·L-1 group;4:SHD 10 g·L-1 group;5:SHD 20 g·L-1 group;6:Ros group.**P<0.01 vs control group |
|
| Fig 4 Effect of SanHuang decoction on expression of GLUT4 protein in 3T3-L1 adipocytes by Western blot 1:Con group;2:SHD 2.5 g·L-1 group;3:SHD 5 g·L-1 group;4:SHD 10 g·L-1 group;5:SHD 20 g·L-1 group;6:Ros group |
从中医脏腑角度而言,代谢综合征的成因主要是脾气虚弱,加上多食肥甘,惰怠少动。肥者令人内热,甘者令人中满,从而伤及中焦气机,使中焦之气瘀滞,脾胃升降失常,枢机不得斡旋,脾气郁滞;脾主四肢肌肉,活动的减少,肌肉的怠惰,也会影响脾的健运。代谢综合征患者,脾的运化、散精功能出现障碍,精微物质进人体内,不能为机体所利用。脾不散精,物不归正化则为痰、为湿、为浊、为脂,临床出现高血糖、高血脂,伤及脉道,则还会引起高血压等一系列疾病[7]。“湿、浊、痰、瘀”之邪积存于腹下,则成腹型肥胖,积存于全身各处,则出现周身肥胖,痰浊结于中焦,郁而化热,出现痰热互结;痰浊日久,因痰致瘀,或因瘀致痰,则出现痰瘀互阻;痰浊壅塞,阻碍气机升降,使肝失疏泄,致气滞血瘀痰阻,脂浊流溢皮下,积于脉道,瘀久化热[8]。三黄汤以此立论,以益气散结、清热化痰为主,佐以祛湿降浊、化瘀调脂。
临床实践中,我们发现三黄汤对代谢综合征或2型糖尿病体形肥胖或超重、肚腹硕大者具有肯定的疗效,三黄汤还可明显降低代谢综合征人群胰岛素抵抗程度,并能改善炎症状态,减轻致心血管病的危险性[9]。3T3-L1脂肪细胞是体外研究胰岛素抵抗发病机制和降糖药物作用机制的重要细胞模型。本实验采用高浓度葡萄糖及高浓度胰岛素培养的脂肪细胞模型,能较好模仿胰岛素抵抗患者体内高糖高胰岛素血症的病理环境。以3T3-L1脂肪细胞为载体,给予不同剂量的三黄汤,并采用过氧化物酶体增殖物激活受体γ(PPARγ)激动剂-罗格列酮作为对照药物,实验发现,药物干预24 h,5个剂量的三黄汤与Ros均使葡萄糖消耗量分别增加到102%、120%、150%、166%、154%、215%,5个剂量的三黄汤较Ros组稍差。在多数情况下,葡萄糖转运都是细胞葡萄糖利用的限制步骤,而GLUT-4是负责脂肪细胞糖转运的主要蛋白;正常生理状态下,90%以上的GLUT-4分布于细胞内的囊泡中,受胰岛素刺激后,转位至细胞膜而促进细胞葡萄糖转运;刺激消失后,GLUT-4被细胞膜内吞而从细胞外膜运回细胞囊泡中[10]。三黄汤上调葡萄糖转运蛋白GLUT-4 的mRNA和蛋白的表达,与其重要组分茵陈中绿原酸以及黄连中小檗碱作用类似[11-12];本实验同时也验证了三黄汤与罗格列酮都能明显增加胰岛素抵抗的3T3-L1细胞对葡萄糖的转运率。
罗格列酮虽然增加胰岛素敏感性,但具有增加脂质积累、引起肥胖的不良反应,尽管其与三黄汤都可以通过上调葡萄糖转运蛋白GLUT-4的表达,增加脂肪细胞葡萄糖转用与消耗;但是与罗格列酮增加脂肪细胞胞内TG积累不同,三黄汤使胞内TG明显降低,与组方中高含量的生物碱成分特别是小檗碱抗脂肪细胞脂质生成的作用相似[13]。
胰岛素抵抗状态的脂肪细胞,其甘油三酯分解加快,FFA过度溢出,而高浓度的FFA又可引起和加重胰岛素抵抗,两者互为因果,相互影响[14]。罗格列酮作为噻唑烷二酮类衍生物胰岛素增敏剂的代表药物,可促进脂肪细胞的葡萄糖摄取,但对脂肪代谢作用并不明显。三黄汤不但改善脂肪细胞对葡萄糖的摄取,还可提高其储存脂肪能力,抑制外周游离脂肪酸的溢出,即三黄汤可以同时影响脂肪细胞的糖代谢与脂代谢来缓解胰岛素抵抗。但是,三黄汤这种作用的确切机制及能量的去处仍不明确,而且,药物在体内与体外的作用机制并不完全相同,会受到多种因素的影响,因此进一步研究其在体内的作用与影响因素将对临床应用带来更多的参考价值。
| [1] | Herder C, Schneitler S, Rathmann W, et al. Low-grade inflammation, obesity and insulin resistance in adolescents[J]. J Clin Endocr Metab, 2007, 92 (12) : 4569-74 . |
| [2] | 徐璐扬, 李中东, 刘庆丰, 等. HPLC测定三黄汤中4种成分含量[J]. 中国现代应用药学, 2011, 28 (12) : 1135-8 . Xu L Y, Li Z D, Liu Q F, et al. Determination of four components in sanhuang Decoction by HPLC[J]. Chin J Mod Appl Pharm, 2011, 28 (12) : 1135-8 . |
| [3] | Liu Q F, Shi X J, Li Z D, et al. Pharmacokinetic comparisons of berberine and palmatine in normal and metabolic syndrome rats[J]. J Ethnopharmacol, 2014, 151 (1) : 287-91 . |
| [4] | 秦佑, 杨瑞仪, 陈梅果, 等. 树豆酮酸A抑制3T3-L1细胞脂肪合成与分解的作用研究[J]. 中国药理学通报, 2016, 32 (2) : 189-93 . Qin Y, Yang R Y, Chen M G, et al. Inhibitory effect of cajanonic acid on lipogenesis and lipolysis in 3T3-L1 adipocyte[J]. Chin Pharmacol Bull, 2016, 32 (2) : 189-93 . |
| [5] | 张哲, 王超. KLF4在糖尿病小鼠心肌组织的表达及通心络胶囊干预作用研究[J]. 中国药理学通报, 2015, 31 (6) : 876-81 . Zhang Z, Wang C. Expression of KLF4 in diabetic mouse myocardium and the interventional effect of Tongxinluo capsule on diabetic cardiomyopathy[J]. Chin Pharmacol Bull, 2015, 31 (6) : 876-81 . |
| [6] | 袁芳, 李艳青, 滕旭, 等. 慢性间歇性低压低氧抑制线粒体途径介导的代谢综合征大鼠心肌组织细胞凋亡[J]. 中国药理学通报, 2015, 31 (8) : 1131-6 . Yuan F, Li Y Q, Teng X, et al. Chronic intermittent hypobaric hypoxia ameliorates myocardial apoptosis through inhibiting mitochondrial pathway in rats with metabolism syndrome[J]. Chin Pharmacol Bull, 2015, 31 (8) : 1131-6 . |
| [7] | 王文健. 代谢综合征的中西医结合防治[J]. 中西医结合学报, 2004, 2 (5) : 390-5 . Wang W J. Prevention and treatment of metabolie syndrome with integrated traditional Chinese and western medieine[J]. J Chin Integr Med, 2004, 2 (5) : 390-5 . |
| [8] | 刘喜明, 仝小林, 王朋倩. 试论“膏浊”致病论[J]. 世界中西医结合杂志, 2009, 4 (12) : 839-42 . Liu X M, Tong X L, Wang P Q. Argument on the point that“Gao Zuo” causes illness[J]. World J Integ Tradit West Med, 2009, 4 (12) : 839-42 . |
| [9] | 刘庆丰, 李中东, 施孝金, 钟明康. 三黄口服液治疗代谢综合征的疗效观察[J]. 中药药理与临床, 2012, 28 (4) : 104-6 . Liu Q F, Li Z D, Shi X J, Zhong M K. Clinical study of San-Huang Decoction in treating metabolic syndrome men[J]. Pharmacol Clin Chin Mat Med, 2012, 28 (4) : 104-6 . |
| [10] | Zheng D, MacLean P S, Pohnert S C, et al. Regulation of muscle GLUT-4 transcription by AMP-activated protein kinase[J]. J Appl Physiol, 2001, 91 (3) : 1073-83 . |
| [11] | 陈广, 陆付耳, 王增四, 等. 小檗碱改善2型糖尿病大鼠胰岛素抵抗与PI-3K、GLUT-4蛋白相关性的研究[J]. 中国药理学通报, 2008, 24 (8) : 1007-10 . Chen G, Lu F E, Wang Z S, et al. Correlation between the amelioration of insulin resistance and protein expression of PI-3K and GLUT4 in type2 diabetic rats treated with berberine[J]. Chin Pharmacol Bull, 2008, 24 (8) : 1007-10 . |
| [12] | 梁秀慈, 孟文, 钟英丽, 等. 绿原酸对高脂乳诱导小鼠胰岛素抵抗形成的影响[J]. 中国药理学通报, 2013, 29 (5) : 654-8 . Liang X C, Meng W, Zhong Y L, et al. Effects of chlorogenic acid on mouse insulin resistance development induced by high fat emulsion[J]. Chin Pharmacol Bull, 2013, 29 (5) : 654-8 . |
| [13] | Zhou J Y, Zhou S W. Berberine regulates peroxisome proliferator-activated receptors and positive transcription elongation factor b expression in diabetic adipocytes[J]. Eur J Pharmacol, 2010, 649 (1) : 390-7 . |
| [14] | 刘长锁, 申竹芳. 游离脂肪酸与胰岛素抵抗[J]. 中国药理学通报, 2005, 21 (2) : 145-9 . Liu C S, Shen Z F. Free fatty acids and insulin resistanc[J]. Chin Pharmacol Bull, 2005, 21 (2) : 145-9 . |
文章信息
-
文章历史
- 收稿日期: 2016-01-20
- 修订日期: 2016-03-10

