


2. 第四军医大学基础部生理学教研室,陕西 西安 710032
 ,
GU Xiao-ming2,
NAN Ying1,
ZHANG Jiang-ying2,
SUN Na1,
Zhu Juan-xia1,
ZHOU Jing-jun2
,
GU Xiao-ming2,
NAN Ying1,
ZHANG Jiang-ying2,
SUN Na1,
Zhu Juan-xia1,
ZHOU Jing-jun2

2. Dept of Physiology, The Fourth Military Medical University, Xi’an 710032, China
心肌缺血/再灌注损伤是急性心肌梗死溶栓治疗、冠状动脉成形术、心脏停跳手术过程中不可避免的伴随事件,可导致心肌顿抑、心肌梗死、心律失常,甚至因心衰致死。众所周知,钙超载是导致心脏缺血/再灌注过程产生不可逆损伤的一个重要原因,可引起心肌细胞结构损伤和功能障碍,但其具体机制仍不清楚[1]。
钙/钙调蛋白依赖性蛋白激酶Ⅱ(Ca2+/CaM dependent kinase Ⅱ,CaMKⅡ)是一种丝氨酸/苏氨酸蛋白激酶,主要表达于心脏,是心血管生理及病理变化过程中信号转导的重要组成部分,通过调节肌质网上的钙释放通道和钙泵,维持心肌细胞内钙稳态,并在心肌肥厚、心力衰竭、心律失常和扩张性心肌病的发生及发展中起重要作用[2-3]。本实验利用大鼠离体心脏钙反常现象(Ca2+ paradox),即短时间无钙液灌注,之后恢复有钙液灌注,可造成急性钙超载心肌损伤[4-6],观察了CaMKⅡ抑制剂KN-93对心肌损伤的影响,旨在初步明确CaMKⅡ在钙超载心肌损伤中的作用。
1 材料与方法 1.1 实验动物与试剂健康成年♂ SD大鼠32只,体质量250~300 g,购买于第四军医大学实验动物中心。CaMKⅡ抑制剂KN-93购于Calbiochem公司。2,3,5-氯化三苯基四氮唑(TTC)购于Sigma公司。乳酸脱氢酶(LDH)检测试剂盒购自Abnova公司。正常Krebs-Henseleit液(KH solution)成分及含量(mmol·L-1):NaCl 120,KCl 4.7,MgSO4 1.2,KH2PO4 1.2,CaCl2 1.25,NaHCO3 25,Glucose 11;无钙KH液:去除正常KH液中的CaCl2,其它成分保持不变,同时添加0.2 mmol·L-1 Na2EDTA。灌流前40 min用95% O2和5% CO2混合气体(V/V)向KH液中持续通气至实验结束,实验中KH液温度保持在37 ℃,pH维持在7.35~7.45。
1.2 方法 1.2.1 大鼠离体心脏灌流按实验室常规方法进行大鼠离体心脏灌流,基本过程为:大鼠腹腔内分别注射肝素500 U·kg-1及戊巴比妥钠(40 mg·kg-1),待麻醉后立即开胸摘取心脏置于4 ℃的正常KH液中,将主动脉根部固定于Langendorff灌流系统(Radnoti Glass Technology,USA)的管口,37 ℃正常KH液由主动脉口逆行灌注,灌注压维持在10.64 kPa(80 mmHg)。待心脏复跳后,于左心耳处剪一小口,将前端带有乳胶球囊的测压管经二尖瓣插入左心室,测压管的另一端经压力换能器(Model 100BP,Biopac System,USA)与计算机相连。调节球囊内的液体量使左心室舒张末压界于0.67~1.33 kPa(5~10 mmHg)之间,平衡灌流15 min,待心脏跳动稳定后标记为灌注开始,按照实验分组进行灌流。
1.2.2 实验分组如Fig 1所示,32只大鼠随机分成4组(n=8):① 正常对照组(Control):KH液灌注40 min;② 药物对照组(KN-93+control):用KH液灌注7 min,含KN-93的KH液灌注8 min,再用KH液灌注25 min;③ 钙反常组(Ca2+ paradox,CaP):KH液灌注8 min,无钙KH液灌注2 min,KH液灌注30 min;④ KN-93处理组(KN-93+CaP):KH液灌注7 min,含KN-93的KH液灌注1 min,无钙含KN-93的KH液灌注2 min,含KN-93的KH液灌注5 min,正常KH液灌注25min。

|
| Fig 1 Experimental protocol The time upon re-perfusion with KH solution containing 1.25 mmol·L-1 Ca2+ was set as 0. |
采用AcqKnowledge 3.8.1系统全程记录左心室内压(left ventricular pressure,LVP)、左室收缩峰压(left ventricular peak systolic pressure,LVPSP)及LVEDP的变化。左室发展压(LVDP)采用LVPSP-LVEDP计算获得,以LVDP和LVEDP反映左室功能变化。
1.2.4 LDH检测收集各组复钙开始后5 min内的冠脉流出液,按照Abnova公司提供的ELISA试剂盒说明,依次加入反应液,450 nm处检测吸光值。结果以实验组吸光值/对照组吸光值的比值来表示各组LDH的相对活性。
1.2.5 心肌梗死面积的测定实验结束后,快速取下心脏,置于-80 ℃冻存1 h;去除心房组织,沿心脏长轴自心尖向心底方向,连续切6片厚度为1 mm左右的环形切片,置于10 g·L-1 TTC溶液中,37 ℃下避光孵育10 min;4%多聚甲醛固定过夜;数码相机拍照,用OPTIMASv5.2软件双盲法分析心肌梗死面积。正常心肌组织呈现砖红色,坏死组织为白色。
心肌梗死面积百分比/%=(坏死区面积/总面积)×100%。
1.3 统计学分析数据用x±s表示,应用GraphPad Prism 5.0统计软件进行分析,组间差异比较采用单因素方差分析(One-way ANOVA),之后采用Turkey检验进行两两比较,以P<0.05表示差异有统计学意义。
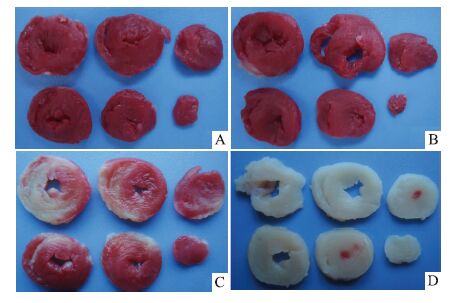
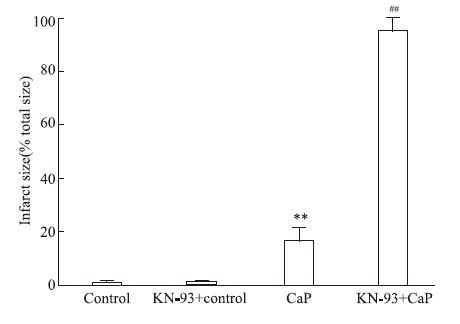
2 结果 2.1 各组大鼠心肌梗死面积比较TTC染色结果显示,对照组于心脏实验结束后未检测到心肌死亡(Fig 2A);药物对照组心脏接受KN-93(2.5 μmol·L-1)处理8 min,与正常对照组大鼠相比,心梗面积没有明显变化(P>0.05,Fig 2B,Fig 3);钙反常组心脏在用2 min无钙液、30 min正常KH液接替灌注后,心肌梗死面积明显增大,达(18±7.2)%(P<0.01,Fig 2C,Fig 3);KN-93处理心脏后可进一步增加梗死面积,变为(90±4.8)%(P<0.01,Fig 2D,Fig 3)。
|
| Fig 2 TTC staining of myocardial tissue slices in different groups A: Control; B: KN-93+control; C: CaP group; D: KN-93+CaP group. |
|
| Fig 3 The percentage of myocardial infarction **P<0.01 vs control;##P<0.01 vs CaP. |
如Tab 1所示,与正常对照组相比,KN-93(2.5 μmol·L-1)药物对照组大鼠心脏的冠脉流量没有明显变化(P<0.05);钙反常组在无钙KH液灌注末(0 min)、复钙液灌注的3 min、15 min、30 min时的冠脉流量减少(P<0.01);与钙反常组相比,KN-93处理组在无钙KH液灌注末(0 min)、复Ca2+灌注后3 min、15 min、30 min 的冠脉流量显著减少(P<0.01)。
| Group | Time/min | ||||
| -3 | 0 | 3 | 15 | 30 | |
| Control | 12.7±0.34 | 12.8±0.17 | 13.0±0.27 | 12.8±0.14 | 12.7±0.22 |
| KN-93+control | 12.3±0.64 | 12.4±0.50 | 12.6±0.51 | 12.5±0.47 | 12.4±0.47 |
| CaP | 12.2±0.60 | 9.2±0.54** | 9.3±0.52** | 9.3±0.53** | 9.3±0.51** |
| KN-93+CaP | 12.1±0.66 | 6.4±0.54## | 6.1±0.49## | 5.9±0.47## | 5.8±0.63## |
| **P<0.01 vs control;##P<0.01 vs CaP. | |||||
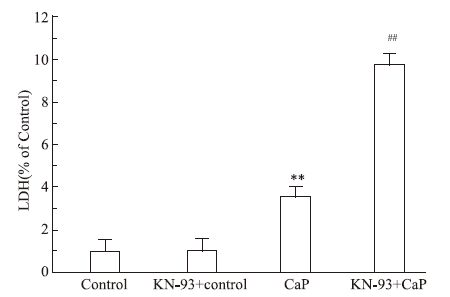
药物对照组大鼠心脏冠脉流出液中LDH含量与对照组相比较无明显差异(Fig 4);与对照组相比,钙反常组大鼠冠脉流出液中LDH含量升高(P<0.01,Fig 4);与钙反常组相比,KN-93处理组冠脉流出液中LDH含量明显增加(P<0.01,Fig 4)。
|
| Fig 4 The content of LDH in coronary effluent **P<0.01 vs control;##P<0.01 vs CaP. |
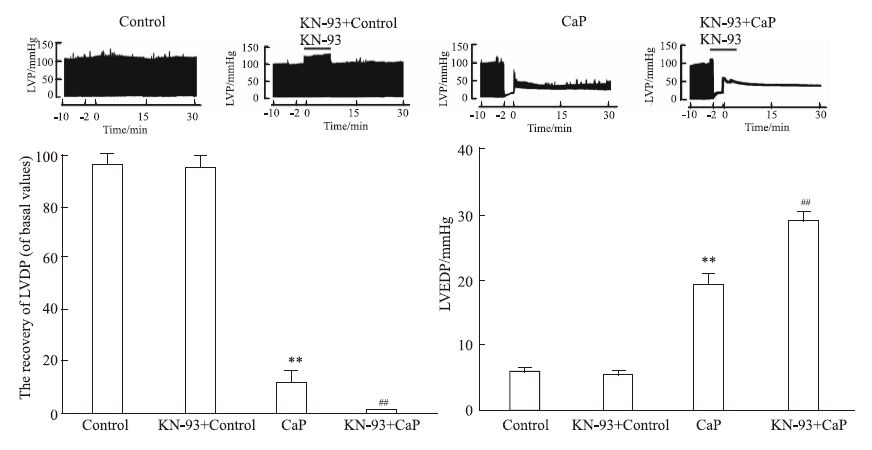
平衡灌注期,各组LVEDP、LVDP均无显著差异,对照组大鼠心脏正常KH液灌注40 min,心功能基本保持不变;用含KN-93(2.5 μmol·L-1)的KH液灌注8 min,与对照组相比,于实验结束时,心功能没有明显变化(P>0.05,Fig 5);钙反常组大鼠心脏接受2 min无钙液、30 min正常KH液接替灌注后,与正常对照组相比,LVEDP抬升,LVDP减小(P<0.01,Fig 5);KN-93干预钙反常大鼠心脏后,LVEDP升高更加明显,且LVDP消失(P<0.01,Fig 5)。
|
| Fig 5 KN-93 aggravates the heart function in calcium paradox The upper panel,the representative of left ventricular pressure (LVP) recording. The lower panel,group results on the recovery of LVDP and the LVEDP at the end of perfusion. 1 mmHg=0.133 kPa,**P<0.01 vs control;##P<0.01 vs CaP. |
心肌细胞缺血一段时间后会导致一定程度的损伤,然而,恢复血液供应后,缺血心肌的损伤不但没有改善,反而进一步加重,最终导致不可逆损伤,形成心肌缺血/再灌注损伤。目前,关于缺血/再灌注损伤的发病机制并不是十分清楚,而在心肌细胞缺血期的可逆性损伤转化为不可逆损伤的过程中,钙超载及其触发的复杂细胞信号转导过程起着重要作用[1]。本研究采用大鼠离体心脏急性钙超载模型,首次观察到CaMKⅡ抑制剂KN-93加重钙超载引起的心肌损伤,提示CaMKⅡ可能参与大鼠钙超载性心肌损伤,进一步完善了以往的研究。
CaMKⅡ参与胞内钙稳态的调节,调控胞内某些基因的表达以及细胞凋亡,是胞内生理活动和病理信号转导的关键蛋白之一。目前,关于CaMKⅡ的激活方式有Ca2+/CaM依赖激活、自身激活和氧化激活,研究比较清楚的是Ca2+/CaM依赖性的激活。Ca2+和CaM首先形成有活性的Ca2+/CaM复合体,进而结合CaMKⅡ调节域中的CaM识别区并激活CaMKⅡ,使CaMKⅡ单体构象发生改变[7]。有学者指出,CaMKⅡ是一种损伤分子,在离体灌注心脏的实验中45 min缺血后再灌注可激活CaMKⅡ,进而增加细胞凋亡/坏死,造成收缩功能障碍,且这种作用能被CaMKⅡ的抑制剂所拮抗[8-9];在心脏特异性敲除CaMKⅡ的小鼠,也观察到缺血/再灌注心肌梗死面积缩小,细胞凋亡减少,改善心功能[10]。然而有文献报道,CaMKⅡ是一种细胞保护分子,同样在离体灌注心脏的实验中,20 min缺血后再灌注可激活CaMKⅡ,减轻心肌顿抑,其作用可能与磷酸化肌浆网钙泵调节分子受磷蛋白(phospholamban)有关[11]。
KN-93是研究CaMKⅡ功能的重要工具药[12-13],本实验观察到: KN-93干预钙反常处理后,心脏梗死面积显著增大,冠脉流出液中LDH量明显增加,提示CaMKⅡ可能具有心肌保护作用,这与Said等[11]在心肌顿抑研究中的报道一致。然而,有文献报道,KN-93抑制钾通道,这一作用可不依赖CaMKⅡ[14]。因而,在离体心脏钙超载损伤中,KN-93对CaMKⅡ活性及其底物的影响有待进一步明确。
综上所述,我们观察到CaMKⅡ抑制剂KN-93能加重急性钙超载引起的心肌损伤,提示CaMKⅡ可能在这一过程中发挥重要作用。后续工作还需测定CaMKⅡ的活性,并探讨其分子机制,这将有助于阐明缺血/再灌注损伤机制,为心肌保护提供新思路。
| [1] | 孔令恒, 刘哲, 张建英, 等. 心肌缺血/再灌注—钙超载损伤的基础与临床研究[J]. 中国体外循环杂志, 2015, 13 (4) : 253-6 . Kong L H, LIU Z, Zhang J Y, et al. Myocardial ischemial/reperfusion experimental and clinical research of calcium overload injury[J]. Chin J Extracorpor Circ, 2015, 13 (4) : 253-6 . |
| [2] | 廖儒佳, 曹雯雯, 张伟. 蛋白磷酸酶1与Ca2+/钙调素依赖性蛋白激酶Ⅱ在心肌病中研究进展[J]. 中国药理学通报, 2012, 28 (12) : 1629-33 . Liao R J, Cao W W, Zhang W. Role of protein phosphatase 1 and Ca2+/calmodulin-dependent protein kinase Ⅱ in heart disease[J]. Chin Pharmacol Bull, 2012, 28 (12) : 1629-33 . |
| [3] | Zhang T, Maier L S, Dalton N D, et al. The deltaC isoform of CaMKⅡ is activated in cardiac hypertrophy and induces dilated cardiomyopathy and heart failure[J]. Circ Res, 2003, 92 (8) : 912-9 . |
| [4] | Piper H M. The calcium paradox revisited: an artefact of great heuristic value[J]. Cardiovasc Res, 2000, 45 (1) : 123-7 . |
| [5] | 刘英, 程翔, 廖玉华. 心肌钙反常模型细胞因子的表达及地尔硫卓的干预作用[J]. 中国药理学通报, 2010, 26 (3) : 309-11 . Liu Y, Cheng X, Liao Y H. Diltiazem inhibits cytokine expression in rat myocardium of calcium paradox model[J]. Chin Pharmacol Bull, 2010, 26 (3) : 309-11 . |
| [6] | Matsunaga M, Saotome M, Satoh H, et al. Different actions of cardioprotective agents on mitochondrial Ca2+ regulation in a Ca2+ paradox-induced Ca2+ overload[J]. Circ J, 2005, 69 (9) : 1132-40 . |
| [7] | Shifman J M, Choi M H, Mihalas S, et al. Ca2+/calmodulin-dependent protein kinase Ⅱ (CaMKⅡ) is activated by calmodulin with two bound calciums[J]. Proc Natl Acad Sci USA, 2006, 103 (38) : 13968-73 . |
| [8] | Vila-Petroff M, Salas M A, Said M, et al. CaMKⅡ inhibition protects against necrosis and apoptosis in irreversible ischemia-reperfusion injury[J]. Cardiovasc Res, 2007, 73 (4) : 689-98 . |
| [9] | Salas M A, Valverde C A, Sánchez G, et al. The signaling pathway of CaMKⅡ-mediated apoptosis and necrosis in the ischemia/reperfusion injury[J]. J Mol Cell Cardiol, 2010, 48 (6) : 1298-306 . |
| [10] | Ling H, Gray C B, Zambon A C, et al. Ca2+/Calmodulin-dependent protein kinase Ⅱ δ mediates myocardial ischemia/reperfusion injury through nuclear factor-κB[J]. Circ Res, 2013, 112 (6) : 935-44 . |
| [11] | Said M, Vittone L, Mundina-Weilenmann C, et al. Role of dual-site phospholamban phosphorylation in the stunned heart: insights from phospholamban site-specific mutants[J]. Am J Physiol Heart Circ Physiol, 2003, 285 (3) : H1198-205 . |
| [12] | Maier L S, Bers D M. Role of Ca2+/calmodulin-dependent protein kinase (CaMK) in excitation-contraction coupling in the heart[J]. Cardiovas Res, 2007, 73 (4) : 631-40 . |
| [13] | 王桂君, 姚玉胜, 王洪新, 等. Ca2+/CaMKⅡ信号通路在肿瘤坏死因子-α诱导心肌肥大中的作用[J]. 中国药理学通报, 2010, 26 (3) : 387-91 . Wang G J, Yao Y S, Wang H X, et al. Ca2+/calmodulin-dependent kinase Ⅱ are involved in tumor necrosis factor α-induced cardiomyocyte hypertrophy in rats[J]. Chin Pharmacol Bull, 2010, 26 (3) : 387-91 . |
| [14] | Anderson M E, Braun A P, Wu Y, et al. KN-93, an inhibitor of multifunctional Ca2+/calmodulin-dependent protein kinase, decreases early afterdepolarizations in rabbit heart[J]. J Pharmacol Exp Ther, 1998, 287 (3) : 996-1006 . |