


2. 药学院;
3. 生命科学院,安徽 合肥 230032
 ,
JIANG Yu-feng1,
WU Chao1,
MA Ying1,
CHEN Ning2,
TAO Li-fen-fang2,
ZHANG Yu-lu2,
ZHAO Xiang-long3,
YANG Yan1
,
JIANG Yu-feng1,
WU Chao1,
MA Ying1,
CHEN Ning2,
TAO Li-fen-fang2,
ZHANG Yu-lu2,
ZHAO Xiang-long3,
YANG Yan1

2. College of Pharmacy ;
3. School of Life Sciences, Anhui Medical University, Hefei 230032 China
目前常用的质粒转染技术主要有两种:瞬时转染、稳定转染[1]。稳定转染是将转染的外源性基因整合进入宿主细胞染色体中,实现长期稳定表达,应用较为广泛[2]。实现稳定转染常用的转染方法有磷酸钙法、电穿孔法、慢病毒载体基因转染法、脂质体介导基因转染法等。电穿孔法、磷酸钙法基因转染效率较低;慢病毒载体基因转染法转染率虽高,但存在的潜在危害性较大;脂质体转染法具有低细胞毒性,对多种类型的细胞都具有高转染效率等优点,是目前最常用的转染方法[3]。近年来研究发现,转化生长因子-β(transforming growth factor-beta,TGF-β)/Smad信号通路在肝细胞癌(hepatocellular carcinoma,HCC)的发生发展过程中的作用随阶段不同而异,在HCC早期,TGF-β1可抑制上皮细胞增殖、诱导细胞凋亡,对肿瘤起抑制作用,在HCC晚期则促进肿瘤浸润和转移,推动肿瘤进程,TGF-β信号的双重作用与Smad3的C末端和连接区磷酸化密切相关[4-5]。一方面,TGF-β通过活化I型TGF-β受体(TβRI)使Smad3C末端磷酸化形成pSmad3C,即TβRI/pSmad3C;另一方面,TGF-β可活化促丝裂原活化蛋白激酶(mitogen activated protein kinase,MAPK)通路,促进Smad3连接区磷酸化为pSmad3L,即MAPK/pSmad3L[5]。TβRI/pSmad3C介导的是肿瘤抑制信号,而MAPK/pSmad3L介导的是致有丝分裂和促进肿瘤发生信号[6]。提示,Smad3的不同位点磷酸化对肿瘤的发生发展起反向调控作用,降低Smad3L磷酸化水平、恢复或提高Smad3C磷酸化水平,可能阻断肝细胞向肝癌细胞转化或肝癌细胞向正常肝细胞转归。有关Smad3 WT、Smad3 EPSM及Smad3 3S-A 3种质粒稳定转染对于HepG2肝癌细胞的增殖、周期及凋亡等功能研究未见相关报道。本研究拟采用脂质体介导基因转染法,将携带Smad3不同位点磷酸化基因的质粒(Smad3 EPSM:Smad3连接区磷酸化位点突变,选择性磷酸化Smad3C;Smad3 3S-A:Smad3 C-末端磷酸化位点突变,选择性磷酸化Smad3L;以正常野生型基因Smad3 WT为对照)转入人肝癌HepG2细胞,建立稳转Smad3 WT-HepG2、Smad3 EPSM-HepG2及Smad3 3S-A-HepG2细胞模型,探讨稳转后不同目的基因的表达对肝癌HepG2细胞增殖、凋亡等功能的影响。
1 材料与方法 1.1 主要试剂与仪器DMEM培养基购自美国HyClone公司,新生胎牛血清购自杭州四季青生物工程材料有限公司,Recombinant Human TGF-β1购自Peprotech公司,Lipofectamine® LTX and Plus Reagent购自Invitrogen公司,G418、四甲基偶氮唑盐(MTT)购自美国Sigma公司产品,Western 及IP细胞裂解液和细胞周期检测试剂盒购自碧云天生物技术研究所,Annexin V-FITC细胞凋亡检测试剂盒购自贝博公司产品,质粒和兔抗pSmad3L抗体源于日本关西医科大学Matsuzaki博士惠赠,兔抗Smad3抗体购自Santa Cruz Biotechnology,兔抗pSmad3C抗体购自Cell Signaling Technology,YJ-1450型医用净化工作台购自北京冠鹏净化设备有限责任公司,Nap-co-6100 型CO2培养箱购自美国杜邦公司,各种规格移液器购自德国Eppendorf公司,多功能酶标仪购自荷兰雷勃公司,流式细胞仪购自美国Beckman公司。
1.2 细胞HepG2细胞株购于中国科学院上海细胞库。
1.3 稳转Smad3 WT、Smad3 EPSM及Smad3 3S-AHepG2细胞株的构建[7] 1.3.1 G418筛选浓度确定将2.5×108 cells·L-1的HepG2细胞接种于24孔细胞培养板,每孔加入500 μL含10%胎牛血清的DMEM培养,24 h后细胞达到80%~90%汇合率,分别加入100、200、300、400、500、600、700、800、900和1 000 mg·L-1浓度的G418培养液。培养7~14 d,细胞全部死亡的最低浓度即为筛选浓度(600 mg·L-1),维持浓度为筛选浓度一半(300 mg·L-1)。
1.3.2 细胞转染将对数生长期的HepG2细胞接种于6孔板内,过夜培养,当细胞密度为70%~80%时,进行转染。实验分为空白对照组、G418对照组、Smad3 WT转染组、Smad3 EPSM转染组、Smad3 3S-A转染组。取对数生长期的HepG2细胞,操作按脂质体转染试剂盒说明书进行。转染前1 d,接种待转染细胞于6孔板中,调整细胞数为每孔约5×108 cells·L-1×2 ml培养基(含10%胎牛血清,不含抗生素)中。待细胞达到80%~85%融合时转染:分别用250 μL opti-MEM培养基稀释4 μg Smad3 EPSM质粒、Smad3 3S-A质粒、Smad3 WT质粒;250 μL opti-MEM培养基稀4 μL lipofectamine®,并在室温下孵育5 min;将稀释了的质粒和稀释了的lipofectamine®混合,在室温下孵育20 min,促使二者复合物的形成,并在30 min内与HepG2细胞混合孵育;弃去原先6孔板中的培养液,用无血清的培养基冲洗待转染细胞两次,然后在5个孔中每孔分别加入高糖的DMEM(无血清)1.5 mL,再分别加入500 μL混合物,前后左右轻轻晃动培养板使混匀;5% CO2、37 ℃、饱和湿度的CO2细胞培养箱中孵育6 h后,将无血清培养基更换为含10%胎牛血清的DMEM(每孔2 ml)。
1.3.3 G418筛选稳定转染的细胞转染48 h后,细胞用含600 mg·L-1的G418和含10%胎牛血清的培养液筛选2周左右,直到空白对照组细胞完全死亡,然后用含300 mg·L-1的G418和含10%胎牛血清的培养液维持筛选并扩增培养,筛选成功的阳性细胞分别命名为Smad3 WT-HepG2细胞、Smad3 EPSM-HepG2细胞及Smad3 3S-A-HepG2细胞。
1.4 Western blot检测转染细胞株中Smad3、pSmad3C、pSmad3L蛋白水平实验分为转染Smad3 WT、Smad3 EPSM及Smad3 3S-A质粒的HepG2细胞,无(或有)TGF-β1(9 pmol·L-1,1 h)刺激的转染细胞组,和无(或有)TGF-β1(9 pmol·L-1,1 h)刺激的正常HepG2细胞组。分别收集对数生长期HepG2细胞(HepG2)、转染Smad3 WT质粒的HepG2细胞(Smad3 WT-HepG2)、转染Smad3 EPSM质粒的HepG2细胞(Smad3 EPSM-HepG2)、转染Smad3 3S-A质粒的HepG2细胞(Smad3 3S-A-HepG2),调整细胞密度至2.5×108 cells·L-1,种瓶(25 cm2培养瓶,4 mL),待细胞单层铺展面积达80%~90%,更换为无血清DMEM培养基,继续培养24 h,在培养结束前1 h,于相应细胞组加9 pmol·L-1 TGF-β1共培养。培养结束后,提取细胞总蛋白,Western blot检测pSmad3C、pSmad3L、Smad3蛋白水平,以GAPDH为内参[8]。
1.5 MTT比色法检测转染Smad3 WT、Smad3 EPSM及Smad3 3S-A质粒对HepG2细胞增殖的影响收集对数生长期HepG2、Smad3 WT-HepG2、Smad3 EPSM-HepG2、Smad3 3S-A-HepG2细胞,调整细胞密度至1.0×104 cells·L-1接种于96孔培养板,每孔200 μL。实验分为HepG2组、HepG2+TGF-β1(9 pmol·L-1)组、Smad3 WT-HepG2组、Smad3 WT-HepG2+TGF-β1(9 pmol·L-1)组、Smad3 EPSM-HepG2组、Smad3 EPSM-HepG2+TGF-β1(9 pmol·L-1)组、Smad3 3S-A-HepG2组、Smad3 3S-A-HepG2+TGF-β1(9 pmol·L-1)组,每组设3个复孔。待细胞单层铺展面积达80%时,更换无血清培养基,继续培养12 h后,于相应组别加9 pmol·L-1 TGF-β1共培养16 h,每孔加MTT(5 g·L-1)20 μL,继续培养4 h,弃孔内上清液,每孔加二甲基亚砜(DMSO)150 μL,水平摇床上震荡10 min后,置酶标仪上检测各孔吸光度值(A570nm)[9]。实验重复3次。
1.6 流式细胞术(flow cytometry,FCM)检测转染Smad3 WT、Smad3 EPSM及Smad3 3S-A质粒对HepG2细胞周期的影响取对数生长期的HepG2、Smad3 WT-HepG2、Smad3 EPSM-HepG2及Smad3 3S-A-HepG2细胞,调整细胞密度至1.0×108 cells·L-1接种于6孔培养板,继续培养至细胞单层铺展面积达90%时,更换为无血清培养基培养过夜,加9 pmol·L-1 TGF-β1共培养16 h,弃上清液,加PBS洗涤、胰酶消化,收集各组细胞液至EP管中,离心(1 000×g,5 min;下同)沉淀细胞,加预冷的PBS重悬细胞,离心,弃上清,加预冷的70%乙醇固定(4 ℃,过夜)。次日,离心,弃上清,加预冷的PBS洗涤,离心,弃上清,加300 μL预冷的PBS重悬细胞后,加入RNaseA溶液20 μL,轻轻震荡混匀,37 ℃水浴30 min,再加入400 μL碘化丙碇(propidium iodide,PI)染液,混匀后4 ℃避光孵育1 h,上流式细胞仪检测细胞周期分布,Multicycles软件分析结果。
1.7 FCM检测转染Smad3 WT、Smad3 EPSM及Smad3 3S-A质粒对HepG2细胞周期及凋亡的影响细胞分组及处理同“1.7”,培养结束后收集细胞,采用Annexin V-FITC试剂盒检测细胞凋亡率,实验操作严格按照试剂盒说明书执行。Cell Questt软件分析实验。
1.8 统计学分析定量资料采用x±s表示,数据统计分析采用SPSS11.0软件处理,两组间比较采用Student’s t-test,多组均数间的两两比较采用One-Way ANOVA。
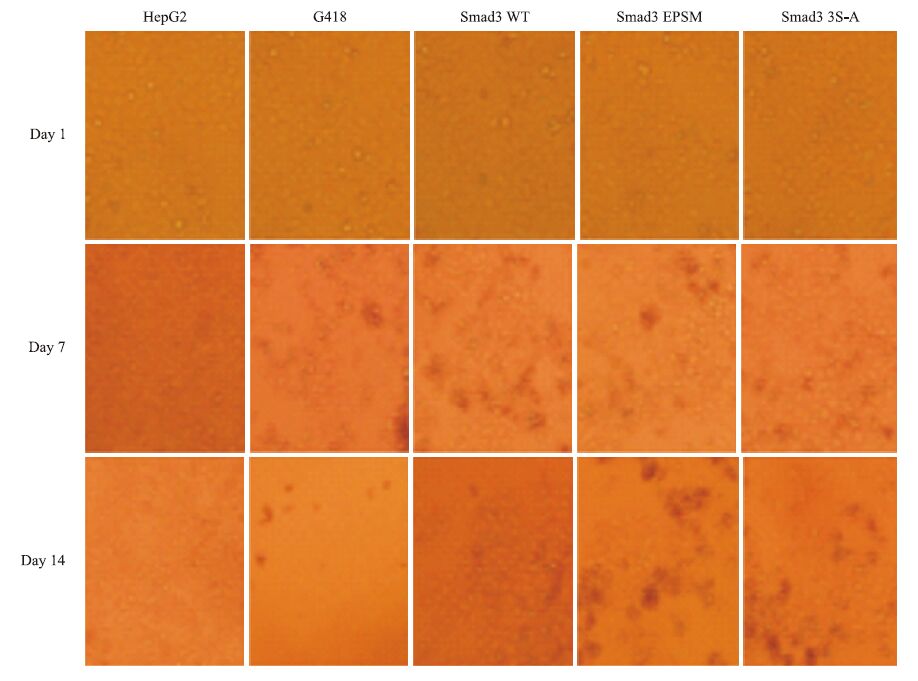
2 结果 2.1 动态观察各组细胞筛选情况及形态学特征筛选d 1 HepG2细胞呈典型梭形,各组细胞形态基本一致。筛选d 7 G418对照组及转染3种质粒的HepG2细胞组因抗生素G418长期高压筛选作用,细胞有一定死亡。筛选d 14 G418对照组细胞最终全部死亡,而转染Smad3 WT、Smad3 EPSM及Smad3 3S-A质粒组细胞仍有大部分存活(Fig 1)。
|
| Fig 1 Inverted microscope observing screening solution of each cell results and morphological feature (×200) |
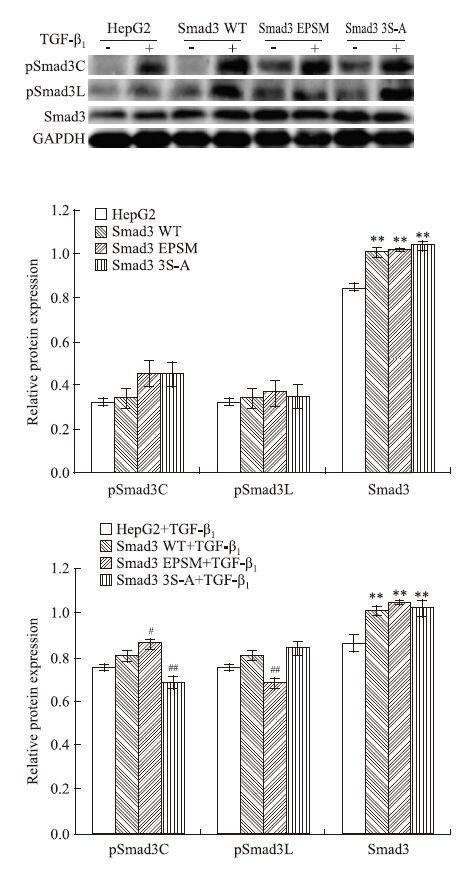
Western blot检测结果显示,与正常HepG2细胞相比,稳定转染3种不同质粒(Smad3 WT、Smad3 EPSM、Smad3 3S-A)组Smad3蛋白的表达量明显增多,TGF-β1刺激后,转染Smad3 WT质粒组细胞pSmad3C/L蛋白水平明显上调;转染Smad3 EPSM质粒组细胞pSmad3C蛋白水平上调明显,而pSmad3L蛋白表达较正常HepG2细胞差异无显著性;转染Smad3 3S-A质粒组细胞pSmad3L蛋白水平明显增加,pSmad3C蛋白水平较正常HepG2细胞微有上调(Fig 2)。上述结果表明,Smad3 WT-HepG2、Smad3 EPSM-HepG2及Smad3 3S-A-HepG2稳转细胞株构建成功,外源性TGF-β1刺激是实现3种质粒稳转HepG2细胞选择性高表达相应目的蛋白的必要条件。
|
| Fig 2 The target gene expression level of transfecting Smad3 WT,Smad3 EPSM and Smad3 3S-A plasmids **P<0.01 vs HepG2 or HepG2+TGF-β1;#P<0.05,##P<0.01 vs Smad3 WT+TGF-β1. |
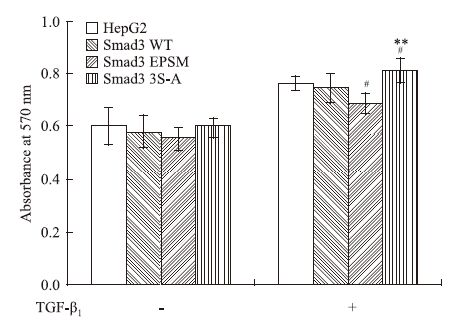
MTT结果显示,转染3种质粒后对HepG2细胞的增殖影响较小,无统计学差异,9 pmol·L-1 TGF-β1刺激16 h后,对正常HepG2细胞,转染Smad3 WT、Smad3 EPSM及Smad3 3S-A质粒的HepG2细胞的细胞增殖均有一定的促进作用(Fig 3);转染Smad3 EPSM质粒的HepG2细胞,较未转染、转染Smad3 WT或Smad3 3S-A质粒的HepG2细胞对TGF-β1诱导的细胞增殖反应减弱,差异有显著性,转染Smad3 3S-A质粒的HepG2细胞,较未转染或转染Smad3 WT质粒组细胞,对TGF-β1诱导的细胞增殖反应略有增强(Fig 3)。提示选择性上调pSmad3C蛋白水平能够抑制HepG2细胞增殖,而上调pSmad3L蛋白水平,可能促进HepG2细胞的恶性增殖。
|
| Fig 3 Effects of transfecting Smad3 WT, Smad3 EPSM and Smad3 3S-A plasmids on cell proliferation in different groups stimulated by TGF-β1 **P<0.01 vs Smad3 EPSM+TGF-β1;#P<0.05 vs Smad3WT+TGF-β1. |
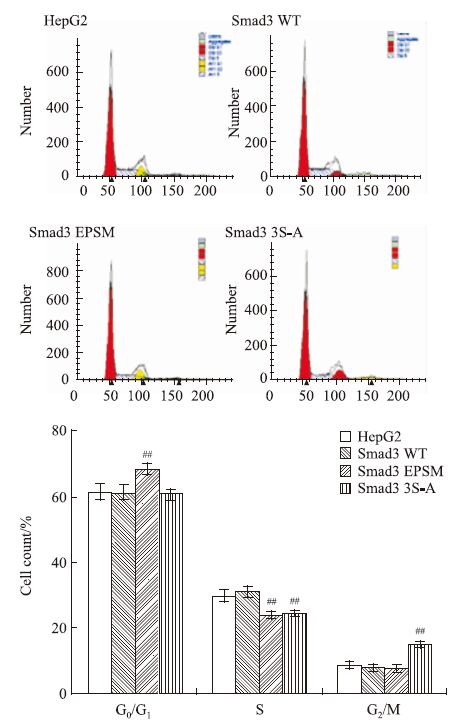
结果显示,TGF-β1刺激下,转染Smad3 WT质粒的HepG2细胞较正常HepG2细胞周期分布差异无显著性;转染Smad3 EPSM质粒的HepG2细胞,较正常HepG2或转染Smad3 WT质粒的HepG2细胞,表现出明显的G1期阻滞,进入S期细胞数明显减少;转染Smad3 3S-A质粒的HepG2细胞,较正常HepG2或转染Smad3 WT质粒的HepG2细胞,S期细胞数明显减少,而G2/M期细胞数增多(Fig 4)。提示,选择性上调pSmad3C蛋白水平,诱导HepG2细胞G1期阻滞;选择性上调pSmad3L蛋白水平,促进HepG2细胞由S期进入G2/M期,推动细胞周期进程。
|
| Fig 4 Effects of transfecting Smad3 WT,Smad3 EPSM and Smad3 3S-A plasmids on cell cycle distribution of HepG2 cells induce by TGF-β1(x±s,n=3) ##P<0.01 vs Smad3 WT |
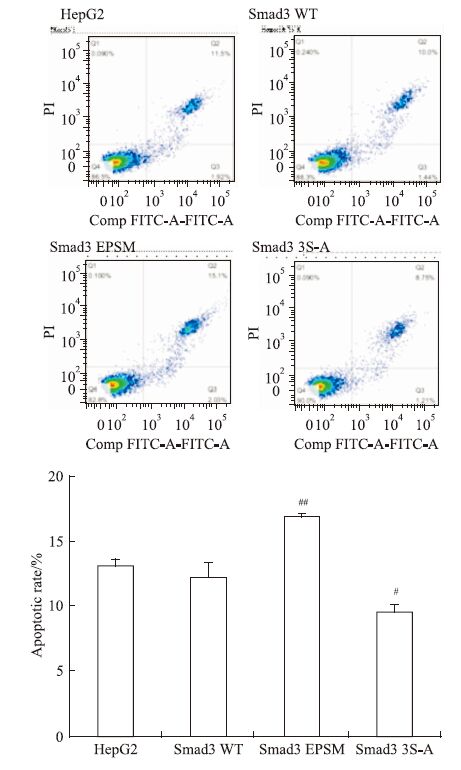
FCM检测结果显示,TGF-β1刺激下,转染Smad3 WT质粒组较正常HepG2细胞组,细胞凋亡率差异无显著性;转染Smad3 EPSM质粒组,较转染Smad3 WT质粒组,细胞凋亡率明显升高(P<0.01);转染Smad3 3S-A质粒组,较转染Smad3 WT质粒组,细胞凋亡率明显降低(P<0.05,Fig 5)。提示,选择性上调pSmad3C蛋白水平,促进HepG2细胞凋亡,而选择性上调pSmad3L蛋白水平抑制HepG2细胞凋亡。
|
| Fig 5 Effects of transfecting Smad3 WT,Smad3 EPSM and Smad3 3S-A plasmids on apoptotic rate of HepG2 cells induce by TGF-β1 (x±s,n=3) #P<0.05,##P<0.01 vs Smad3 WT |
TGF-β是一类对于细胞生长、增殖、分化、凋亡等生命活动均具有调节作用的多功能细胞因子[10]。TGF-β首先结合靶细胞膜上的TGF-β受体,受体活化,进而磷酸化胞质中的Smad蛋白,磷酸化的Smad蛋白异位入核,调控靶基因的转录,最终影响靶细胞的生物学功能[11]。目前研究表明,Smad3是参与TGF-β信号胞内提取和转化的关键节点,依赖TβRI活化的Smad3 C-末端(即pSmad3C),介导的是肿瘤抑制信号;依赖丝裂原活化蛋白激酶(MAPK)活化的Smad3连接区(即pSmad3L),介导的是致有丝分裂或促肿瘤发生信号[12]。临床研究发现,最终发展成为HCC的慢性乙肝及慢性丙肝患者肝组织中pSmad3L大量表达,而pSmad3C则表达有限;反之,pSmad3C大量表达,而pSmad3L表达有限的慢性乙肝及丙肝患者则不发展为HCC[13]。提示,在HCC发生发展过程中,pSmad3L发挥着类似癌基因的作用,而pSmad3C扮演着抑癌基因的作用。
随着分子生物学技术的发展与革新,基因水平的干预或基因治疗,已逐渐成为人类防病治病的应对策略。脂质体转染、慢病毒转染技术的逐步成熟,帮助人类实现外源基因导入宿主细胞转录翻译,产生功能蛋白而调控靶细胞生物学功能的设想。本实验中,采用脂质体转染法将携带正常Smad3基因的质粒Smad3 WT、连接区磷酸化位点突变的Smad3基因的质粒Smad3 EPSM、C-末端磷酸化位点突变的Smad3基因的质粒Smad3 3S-A导入人肝癌细胞株HepG2,倒置显微镜动态观察筛选过程,结果显示,筛选d 14转染组细胞仍有部分存活,而未转染组几乎全部死亡,因为转入细胞的质粒中含有抗性基因neo,其携带的氨基糖苷磷酸转移酶可以将G418转变为无毒形式,而未转染组不含抗性基因neo,推测可能获得稳转细胞株。Western blot法对筛选结果作进一步验证,结果显示,TGF-β1刺激下,转染相应质粒的HepG2细胞选择性高表达相应质粒携带的目的基因蛋白,提示,已成功获得Smad3 WT、Smad3 EPSM及Smad3 3S-A稳转HepG2细胞株。
随后,初步探究了转染Smad3 WT、Smad3 EPSM及Smad3 3S-A质粒后HepG2细胞的功能学。结果显示,单纯转染3种质粒后对HepG2细胞功能几乎没有影响;与转染野生型质粒经TGF-β1刺激后相比,当Smad3C末端磷酸化位点突变,经TGF-β1刺激仅pSmad3L蛋白表达,能明显抑制HepG2细胞增殖、诱导HepG2细胞G1期阻滞和促进HepG2细胞凋亡,当Smad3链接区末端磷酸化位点突变,经TGF-β1刺激仅表达pSmad3C蛋白,对HepG2细胞增殖略有促进作用、诱导HepG2细胞由S期向G2/M期转变,并抑制HepG2细胞凋亡。提示,转染3种质粒本身对细胞本身影响较小,选择性上调HepG2细胞中pSmad3C、pSmad3L蛋白水平,可影响HepG2细胞的增殖,推测选择性增加pSmad3C蛋白水平可能通过诱导细胞周期阻滞和促进细胞凋亡,从而抑制肝癌细胞的增殖,发挥抗癌作用;选择性上调HepG2细胞中pSmad3L蛋白水平,可能通过促进细胞周期进程和抑制细胞凋亡,从而促进肝癌细胞的恶性增殖,发挥促癌作用。
本研究证实了在HepG2细胞中选择性调控pSmad3C/L蛋白水平或含量比值,能够改善癌细胞的恶性程度,可能促进癌细胞向正常细胞转归。而研究中建立的Smad3 WT、Smad3 EPSM及Smad3 3S-A稳转HepG2细胞株,为下一步本课题组在细胞和分子水平研究能够经由pSmad3C/pSmad3L调控的药物奠定基础。
| [1] | 刘家云, 李庆霞, 黄红艳, 等. 瞬时转染和稳定转染对RNAi抑制乙型肝炎病毒S基因表达的影响[J]. 第四军医大学学报, 2005, 26 (11) : 961-4 . Liu J Y, Li Q X, Huang H Y, et al. Effect of transient and stable transfection on inhibition of hepatitis B virus S gene expression by RNA interference[J]. J Fouth Mil Med Univ, 2005, 26 (11) : 961-4 . |
| [2] | 张富东, 高丽辉, 冯国华, 等. hSGLTs-CHO-K1稳定转染细胞株的建立及芒果苷对SGLTs转运蛋白表达的影响[J]. 中国药理学通报, 2013, 29 (4) : 553-6 . Zhang F D, Gao L H, Feng G H, et al. Establishment of CHO-K1 cell lines stably expressing hSGLTs structure protein and effect of mangiferin on expression of SGLTs[J]. Chin Pharmacol Bull, 2013, 29 (4) : 553-6 . |
| [3] | 王月丽, 魏继楼, 程红蕾, 等. 外源基因转染细胞技术的研究进展[J]. 现代生物医学进展, 2014, 14 (7) : 1382-4 . Wang Y L, Wei J L, Cheng H L, et al. Advances in technology of heterologous genes thansfecting cells[J]. Progr Mod Biomed, 2014, 14 (7) : 1382-4 . |
| [4] | Pardali K, Moustakas A. Actions of TGF-β as tumor suppressor and pro-metastatic factor in human cancer[J]. Biochim Biophys Acta, 2007, 1775 (1) : 21-62 . |
| [5] | Sekimoto G, Matsuzaki K, Yoshida K, et al. Reversible Smad-dependent signaling between tumor suppression and oncogenesis[J]. Cancer Res, 2007, 67 (11) : 5090-6 . |
| [6] | Yoshida K, Murata M, Yamaguchi T, Matsuzaki K. TGF-beta/Smad signaling during hepatic fibro-carcinogenesis(review)[J]. Int J Oncol, 2014, 45 (4) : 1363-71 . |
| [7] | 刘春亮, 冯惠枝, 刘燕, 等. IDO基因稳定转染HepG2细胞系的建立[J]. 医学研究杂志, 2012, 41 (2) : 68-70 . Liu C L, Feng H Z, Liu Y, et al. Construction of a HepG2 cell line with IDO gene steady transfection[J]. J Med Res, 2012, 41 (2) : 68-70 . |
| [8] | Liu X, Yang Y, Zhang X, et al. Compound astragalus and salvia miltiorrhiza extract inhibits cell invasion by modulating transforming growth factor-beta/Smad in HepG2 cell[J]. J Gastroenterol Hepatol, 2010, 25 (2) : 420-6 . |
| [9] | 王玉美, 梁佳玉, 杨雁. 3种MAPK抑制因子对HepG2细胞中Smad2/3磷酸化的影响[J]. 安徽医科大学学报, 2006, 41 (6) : 648-50 . Wang Y M, Liang J Y, Yang Y. The effect of three MAPK inhibitors on Smad2/3 phosphorylation[J]. Acta Univ Med Anhui, 2006, 41 (6) : 648-50 . |
| [10] | Mehra A, Wrana J. TGF-beta and the Smad signal transduction pathway[J]. Biochem Cell Biol, 2002, 80 (5) : 605-22 . |
| [11] | Shi Y, Massagué J. Mechanisms of TGF-β signaling from cell membrane to the nucleus[J]. Cell, 2003, 113 (6) : 685-700 . |
| [12] | Nagata H, Hatano E, Tada M, et al. Inhibition of c-Jun NH2-terminal kinase switches Smad3 signaling from oncogenesis to tumor-suppression in rat hepatocellular carcinoma[J]. Hepatology, 2009, 49 (6) : 1944-53 . |
| [13] | Murata M, Matsuzaki K, Yoshida K, et al. Hepatitis B virus X protein shifts human hepatic transforming growth factor(TGF)-beta signaling from tumor suppression to oncogenesis in early chronic hepatitis B[J]. Hepatology, 2009, 49 (4) : 1203-17 . |