


2.安徽医科大学附属省立医院 病理科,安徽 合肥 230001
2.Dept of Pathology,Anhui Provincial Hospital Affiliated to Anhui Medical University,Hefei 230001,China
在慢性高糖状态非酶糖基化终末产物(advanced glyclation end-products ,AGEs)形成增加,并且AGEs多肽在糖尿病患者的肾脏中清除受到影响,导致体内AGEs水平的进一步升高,AGEs在肾脏局部组织的积聚可通过多种直接和间接的机制导致肾脏损伤[1],在糖尿病肾病的发生中发挥重要的作用。二甲双胍(metformin ,MET)作为治疗2型糖尿病的一线首选药物,除降糖作用,尚可预防和延缓糖尿病肾病的发生和发展[2]。本研究通过观察二甲双胍对2型糖尿病大鼠肾组织AGEs的表达及经尿排泄的影响,初步探讨其对肾脏保护作用及其机制。
1 材料与方法 1.1 材料 1.1.1 主要仪器设备DFM-96型10管放射免疫计数仪,购于安徽合肥众成机电公司;DS-5型糖化血红蛋白检测仪,购于英国DREW公司;胰岛素放射免疫试剂盒,购于北京原子高科公司;ABI 7500型扩增仪,购于美国Bio-Rad公司;NDl000紫外/分光光度仪,购于美国Nano-Drop公司;DG-3022A型酶联免疫检测仪,购于江苏南京国营华东电子管厂。
1.1.2 实验动物健康清洁级♂ SD大鼠42只,2月龄,体质量180~200 g,购自安徽医科大学实验动物中心(scxk皖2011~002)。在饲养期间,12 h交替照明,室温 (19±1)℃,相对湿度48%,大鼠自由进食进水。
1.1.3 药物与试剂白蛋白放射免疫试剂盒,购于天津市协和公司;链脲佐菌素(streptozotocin,STZ),美国Sigma公司;二甲双胍,购于上海施贵宝公司;格列本脲(glyburide,GLY),天津太平洋公司;尿素氮、肌酐试剂盒,南京建成科技公司;AGEs免疫组化试剂盒,购于武汉博士德生物工程有限公司;胰岛素放射免疫试剂盒,购于北京原子高科公司;尿AGEs ELISA试剂盒,购于上海艾来萨生物科技公司;PCR试剂盒及引物、TRIzol均购于大连TaKaRa公司。
1.2 方法 1.2.1 2型糖尿病模型大鼠的制备健康清洁级♂ SD大鼠42只,随机分成两组:模型组(DM组,n=33),给予高脂饮食(常规饲料加10%猪油、2%胆固醇);正常对照组(NC组,n=9),普通饲料喂养。高脂饮食1个月后,测血浆胰岛素水平(fasting insulin,FINS) 和空腹血糖(fasting peripheral blood glucose,FBG),并且计算胰岛素抵抗指数(homeostasis model assessment-insulin resistance,HOMA-Ir)[HOMA-Ir=(FBG×FINS)/22.5]。给予STZ 30 mg·kg-1(溶解于现配制的0.1 mmol·L-1枸橼酸缓冲液中,pH=4.4) 腹腔内一次性注射。正常对照组大鼠注射等量枸橼酸缓冲液。1周后测随机血糖,血糖≥16.7 mmol·L-1,且伴胰岛素抵抗者为T2DM大鼠成模标准。
1.2.2 动物给药及分组方法29只SD大鼠造模成功,将大鼠随机分为3组:糖尿病组(T2DM组,n=11,后期死亡1只);二甲双胍治疗组(300 mg·kg-1·d-1,MET组,n=9);格列本脲组(5 mg·kg-1·d-1,GLY组,n=9)。NC组及T2DM组给予等量的生理盐水。于每日清晨灌胃给药1次,高脂饲料,共8周。
1.2.3 标本收集干预治疗后8周末,对代谢笼12 h尿液进行收集,并准确计量,留取5 mL混匀后的尿液,置于-40℃冰箱待测尿肌酐(urine creatinine,Ucr)、尿白蛋白(urinary albumin,UAlb)和尿AGEs。收集尿标本后,用10%的水合氯醛对各组大鼠进行腹腔注射麻醉,麻醉后行腹主动脉插管采血法收集血标本,测FBG、FINS、糖化血红蛋白(hemoglobin A1c,HbA1c)及血尿素氮(blood urea nitrogen,BUN)。最后取双侧肾组织用生理盐水反复灌洗除去包膜,右侧肾组织放于液氮保存,用于日后做Real-time PCR;左肾制成石蜡切片,留日后观察大鼠肾组织的病理变化。
1.3 检测指标及方法 1.3.1 免疫组化测肾组织AGEs的表达载玻片防脱片处理,石蜡切片脱蜡水化,微波抗原修复,灭活内源性酶,滴加封闭液,滴加经稀释的一抗(兔IgG 1 ∶200),4 ℃过夜,PBS洗,再滴加聚合HRP标记抗兔IgG(SV-0002)二抗,室温孵育30 min。DAB显色,苏木精轻度复染,脱水,透明,封片,观察。于400倍镜下进行拍照,且每张切片取3个视野。用全自动图像分析系统(Image pro plus 6.0)对每张图片中阳性反应部位的累积光密度(integral optegral density,IOD)进行测定,从而得到每张切片中AGEs阳性物质的相对含量,用AGEsIOD表示。
1.3.2 生化指标的检测尿AGEs采用ELISA法,尿白蛋白采用放射免疫分析法,血尿素氮采用尿酶法,尿肌酐采用苦味酸比色法。尿AGEs和尿白蛋白排泄分别用尿AGEs肌酐比[urinary AGEs/urine creatinine,UGCR(pg·g-1)]和尿白蛋白肌酐比[urinary albumin/urine creatinine,UACR(mg·g-1)],以排除由尿液稀释造成的影响。
1.3.3 Real-time PCR测肾组织RAGE mRNA的表达肾组织的RNA采用TRIzol法提取;取2μg的总RNA进行逆转录获得cDNA;cDNA产物进行Real-time PCR。RAGE引物序列上游引物:5′-CAGGGTCACAGAAACCGG-3′,下游引物: 5′-ATTCAGCTCTGCACGTTCCT-3′;β-actin引物序列上游引物:5′-GCCTTAGCCTGGACCCATAG-3′,下游引物:5′-GACCACCAATCCACACAGA-3′。使用ABI7500型扩增仪,采用20 μL反应体系荧光染料法:95℃预变性30 s;95℃变性5 s;60℃退火34 s;72℃延伸1 min的热循环40次;95℃ 15 s、60℃ 1 min与95℃ 15 s循环1次。目的和内参片段分别同批扩增,每组均设置3个复孔,运用ΔΔCt法分析Ct值,2-ΔΔCt表示目的基因mRNA表达拷贝数和β-actin拷贝数的比值。
1.3.4 电镜处理透射电镜下,取1 mm3大小的肾皮质;用2.5%戊二醛固定,制成超薄切片;将超薄切片置于高倍镜下(×10 000)采集10个视野,并随机观察和测量8处肾小球基底膜的厚度(glomerular basement membrane thickness,GBMT)并取平均值。
1.4 统计学处理所有数据均应用SPSS 22.0软件进行分析,用x±s表示。多组间比较运用方差分析,方差齐性者用单因素方差分析(One-Way ANOVA)进行两两比较,用SNK检验;方差不齐者采用Dunnett′s T3检验。
2 结果 2.1 各组大鼠一般生化指标比较8周末,各组糖尿病大鼠的血BG、HbA1c、FINS及BUN水平均明显比NC组高,且差异有统计学意义(P<0.05);与T2DM组相比,MET组和GLY组上述指标明显下降(P<0.05),但MET组与GLY组之间BG、HbA1c值差异没有统计学意义(P>0.05);而两组之间的BUN水平差异有统计学意义(P<0.05)。见Tab1。
| Group | n | BG/mmol·L-1 | HbA1c/% | BUN/mmol·L-1 | FINS/mU· L-1 | UACR/mg·g-1 | UGCR/pg·g-1 |
| NC | 9 | 4.45±1.07 | 4.13±0.89 | 6.91±2.52 | 17.53±3.42 | 0.25±0.66 | 44.16±7.44 |
| T2DM | 10 | 15.6±1.56* | 12.41±0.61* | 18.95±0.98* | 28.16±4.98* | 2.86±0.10* | 188.63±13.89* |
| MET | 9 | 11.75±0.98*△ | 8.78±0.32*△ | 11.30±2.02*△ | 22.08±2.61*△ | 1.80±0.08*△ | 63.50±10.05*△ |
| GLY | 9 | 11.78±1.43*△ | 8.85±1.07*△ | 14.03±2.55*△# | 22.89±0.15*△ | 2.37±0.12*△# | 83.16±9.13*△# |
| *P<0.05 vs NC;△P<0.05 vs T2DM;#P<0.05 vs MET | |||||||
与NC组相比,各组糖尿病大鼠UGCR和UACR明显升高,且差异有统计学意义(P<0.05);与T2DM组相比,MET组和GLY组UGCR及UACR值明显降低(P<0.05);与GLY组相比,MET组UGCR和UACR明显降低,差异有统计学意义(P<0.05)。见Tab1。
2.3 各组大鼠肾组织AGEs蛋白表达的变化与NC组比较,其余各组肾组织AGEsIOD水平均明显升高,且差异有统计学意义(P<0.05);与T2DM组相比,MET组及GLY组肾组织AGEsIOD水平明显降低,且MET较GLY组下降水平更明显,各组之间差异有统计学意义(P<0.05)。见Fig1和Tab2。

|
| Fig.1 Immunohistochemical staining for AGEs(×400) A: NC;B: T2DM;C: GLY;D: MET |
| Group | n | GBMT/nm | AGEsIOD | RAGEmRNA |
| NC | 9 | 106.00±10.23 | 11.90±2.37 | 1.00±0.18 |
| T2DM | 10 | 266.58±21.68* | 116.26±19.99* | 26.65±0.63* |
| MET | 9 | 150.98±17.25*△ | 37.14±14.03*△ | 1.67±0.66*△ |
| GLY | 9 | 203.67±23.32*△# | 54.39±11.45*△# | 1.96±0.03*△# |
| *P<0.05 vs NC;△P<0.05 vs T2DM;#P<0.05 vs MET | ||||
mRNA表达的变化 与NC组相比,T2DM组肾组织RAGE mRNA表达明显升高(P<0.05);与T2DM组相比,MET及GLY干预组肾组织RAGE mRNA表达明显降低,且MET组肾组织RAGE mRNA表达量明显低于GLY组(P<0.05)。见Tab2。
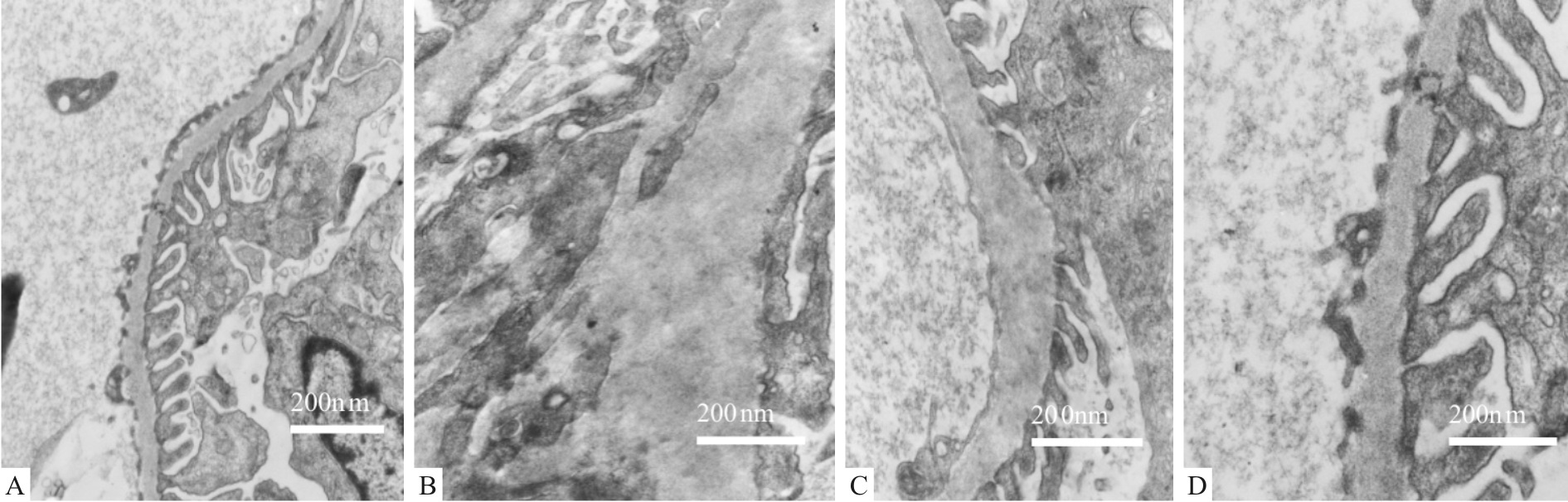
2.5 各组大鼠GBMT的变化与NC组比较,T2DM组GBMT明显增厚,差异有统计学意义(P<0.05);MET组、GLY组GBMT较T2DM组明显减低(P<0.05);GLY组与MET组比较,MET组GBMT改善更明显,差异有统计学意义(P<0.05)。见Fig2和Tab2。
|
| Fig.2 Histopathological changes of renal tissue under electron microscopy among four groups(×10 000) A: NC;B: T2DM;C: GLY;D: MET |
AGEs是持续高血糖状态下非酶糖基化反应形成的终末产物,近年来研究认为AGEs在肾脏局部堆积可通过多种直接和间接的途径参与糖尿病肾病(DN)的发生和发展[2]。在糖尿病患者的肾脏中AGEs的大量聚集,刺激系膜细胞表面的AGEs受体,使层黏连蛋白及其它肾小球系膜结构蛋白明显增加,最终致系膜区扩张,肾小球基膜增厚,加速肾小球硬化[1]。本研究结果显示,糖尿病大鼠肾组织AGEs蛋白和RAGE mRNA表达明显增强,尿AGEs排泄明显增加,提示糖尿病大鼠肾组织AGEs聚集增加,并诱导RAGE的表达,参与DN的发生。
二甲双胍作为治疗2型糖尿病的首选抗糖尿病药物[3],乔进等[4]的动物实验结果显示,二甲双胍可使大鼠血清AGEs含量明显下降。Ishibashi等[5]研究显示,二甲双胍可有效抑制肾小管细胞AGEs形成及其诱导的RAGE表达,进而减轻其损伤。李友元等[6]报道二甲双胍可降低肾脏组织RAGE mRNA的过度表达,抑制AGEs的结合位点及肾组织蛋白的非酶糖基化作用,从而阻断AGEs与其受体作用所介导的一系列信号通路[7]。本动物实验结果显示:经二甲双胍和格列本脲干预8周后,二甲双胍干预组及格列本脲组GBMT及UACR均低于2型糖尿病模型组,MET组低于格列本脲组,但2组血糖和HbA1c水平无明显差异,提示二甲双胍在相似降血糖的情况下,其肾脏保护作用优于格列本脲。进一步观察显示二甲双胍组糖尿病大鼠尿AGEs排泄明显减少,肾组织AGEs蛋白表达和RAGE mRNA表达明显降低,且其降低程度优于格列本脲组,提示二甲双胍具有降糖之外减少2型糖尿病大鼠肾脏AGEs的形成和抑制RAGE mRNA表达的作用,进而减轻肾脏损害。二甲双胍降低糖尿病肾组织AGEs表达的机制尚不明确,有研究者发现二甲双胍抑制肾脏组织AGEs的形成可能与其减轻氧化应激有关[8],而氧化应激是DN发病的中心环节[2]。近期庞若宇等[9]研究指出AGEs可以诱导细胞凋亡,而二甲双胍可以起到抗凋亡作用,其机制可能通过激活腺苷酸活化蛋白激酶(AMPK),抑制NF-κB的激活及活性氧族的生成有关。有研究报道二甲双胍可以通过激活AMPK并抑制AGEs和NADPH氧化酶的生成,使体外培养的足细胞中活性氧自由基含量降低,发挥肾脏保护作用[10, 11]。
本实验初步研究结果显示,二甲双胍可抑制糖尿病大鼠肾脏组织蛋白非酶糖基化产物反应,降低AGEs生成和肾组织RAGE mRNA表达,该作用可能与其肾脏保护部分有关,具体机制还有待进一步研究。
| [1] | 林 虹,朱鹏立.晚期糖基化终末产物及其受体在原发性高血压中的作用机制[J].国际老年医学杂志,2010,31(4):165-70. Lin H,Zhu P L. Pathophysiologic mechanisms of advanced glycation end products and their receptors in primary hypertension[J].Int J Geriatr,2010,31(4):165-70. |
| [2] | Zhou X,Wang B,Zhu L,et al.A novel improved therapy strategy for diabetic nephropathy: Targeting AGEs[J].Organogenesis,2012,8(1):18-21. |
| [3] | Viollet B,Guigas B,Sanz G N,et al.Cellular and molecular mechanisms of metformin:an overview[J].Clin Sci(Lond),2012,122(6): 253-70. |
| [4] | 乔 进,窦志华,吴 锋.灵芝多糖联合二甲双胍对2型糖尿病大鼠心肌AGEs及CTGF的影响及其机制[J].中国药理学通报,2014,30(4):536-41. Qiao J ,Dou Z H,Wu F.Effect of combination of ganoderma lucidum polysaccharide and metformin on AGEs and CTGF of cardiac muscle in type 2 diabetic rats and the mechanism[J].Chin Pharmacol Bull,2014,30(4):536-41. |
| [5] | Ishibashi Y,Matsui T,Takeuchi M,et al.Beneficial effects of metformin and irbesartan on advanced glycation end products(AGEs)-RAGE-induced proximal tubular cell injury[J].Pharmacol Res,2012,65(3):297-302. |
| [6] | 李友元,邓洪波,王 蓉,等.糖尿病鼠肾脏组织损伤机制及二甲双胍的保护作用[J].医学临床研究,2005,22(5):641-6. Li Y Y,Deng H B,Wang R,et al.The mechanism of kidney tissue damage and protective effect of metformin in diabetic mouse[J].J Clin Res,2005,22(5):641-6. |
| [7] | Ishibashi Y,Matsui T,Takeuchi M,et al.Metformin inhibits advanced glycation end products(AGEs)-induced growth and VEGF expression in MCF-7 breast cancer cells by suppressing AGEs receptor expression via AMP-activated protein kinase[J].Horm Metab Res,2013,45(5):387-90. |
| [8] | Wu D,Wen W,Qi C L,et al.Ameliorative effect of berberine on renal damage in rats with diabetes induced by high-fat diet and streptozotocin[J].Phytomedicine,2012,19(8-9): 712-8. |
| [9] | 庞若宇,关美萍,郑宗基,等. 二甲双胍对糖基化终末产物诱导的成纤维细胞凋亡及相关蛋白caspase-3、Bax及Bcl-2表达的影响[J].南方医科大学学报,2015,35(6):898-902. Pang R Y,Guan M P,Zheng Z J,Xue Y M.Effects of metformin on apoptosis induced by advanced glycation end-products and expressions of caspase-3,Bax and Bcl-2 in human dermal fibroblasts in vitro[J].J South Med Univ,2015,35(6):898-902. |
| [10] | Tzeng T F,Liou S S,Chang C J,et al.The ethanol extract of Zingiber zerumbet attenuates streptozotocin-induced diabetic nephropathy in rats[J].Evid Based Complement Alternat Med,2013,2013: 340645. |
| [11] | Piwkowska A,Rogacka D,Jankowski M,et al.Metformin induces suppression of NAD(P)H oxidase activity in podocytes[J].Biochem Biophys Res Commun,2010,393(2):268-73. |

