


抑郁症(depression)是一种表现为抑郁心境低落的综合征,以心境低落、思维迟缓、认知功能损害、意志活动减退和躯体症状为主要特征,严重后果的患者可能引起自杀。目前,关于抑郁症的发病机制存在着很多假说,如单胺神经递质及其受体学说、下丘脑-垂体-肾上腺(PHA)轴功能失调学说、神经营养因子学说等。但没有一种学说能完全解释抑郁症的发病机制,发病机制的不清,导致诊断不明确,误诊和漏诊率较高,对抑郁症的治疗也存在药效延迟、部分抑郁患者疗效不佳、复发率高等现象。因此,我们必须更好地了解抑郁症的发生和进展机制,从而能够有效地对抑郁症进行彻底治疗。研究发现,抑郁患者会出现记忆下降、学习能力降低等情况,而海马与学习记忆有着密切关系。因此,研究海马组织对于研究抑郁症的发病机制有着重大的意义[1]。前期的实验结果及参考文献,引出本文蛋白质组学研究。
抑郁症的发生和进展过程包含了细胞内多种信号通路的协同改变,研究这些机制的有效办法就是从整体角度思考这些复杂的变化。蛋白质组学通过对整体蛋白质的大规模分析,研究生物学过程相关蛋白质的表达和功能的改变[2]。同位素标记相对和绝对定量(isobaric tags for relative and absolute quantification,ITRAQ)联合液相色谱串联质谱(LC-MS/MS)是近年来开发的一种新的蛋白质组学定量技术,可同时对多达8种样品进行定量研究,并且与传统蛋白质组学研究相比较,ITRAQ技术中运用的定性和定量方法重复性更好,特别适用于低峰度蛋白质的研究,而且能够通过同位素标记的方法,准确把握差异表达蛋白的动态变化,能够更好地对蛋白质含量进行定量测定[3]。
1 材料与方法 1.1 实验动物清洁级♂SD大鼠20只,体质量180~220 g,从重庆医科大学实验动物中心购买,合格证书编号SCXK(渝)2012-0001。实验室环境为25℃,给予所有大鼠正常饮食、饮水,实验室内黑暗与光照交替出现,黑暗12 h,光照12 h,所有大鼠饲养1周以适应环境。
1.2 试剂与仪器H2O(HPLC级别)(美国Sigma公司),ITRAQ 标记试剂盒(美国Applied Biosystems公司),BCA试剂盒(中国碧云天公司),胰酶(美国Sigma公司),Cocktail蛋白酶抑制剂(美国罗氏公司),全蛋白提取试剂盒(上海生工),蛋白裂解液(中国碧云天公司),尿素(美国Sigma公司),Anti-GABA Transporter(ab431),聚偏氟乙烯膜(PVDF)0.45 μm(Merck Millipore,IPVH00010),SDS-PAGE 蛋白上样缓冲液(5×)(碧云天生物技术研究所,P0015),鲁米诺化学发光液底物100 mL(Merck Millipore,WBLUC0100),TBST缓冲液(北京鼎国昌盛生物技术有限责任公司),电泳/电转仪(Bio-Rad公司,041BR88778)。旷场实验行为测试仪、强迫游泳行为测试仪、高架十字迷宫(重庆医科大学药理实验室制)。低温冰箱(-20℃)(德国西门子),Aallegra台式高速冷冻离心机(美国Beckman Coulter公司),超低温冰箱(-80℃)(美国Thermo Fisher),高效液相色谱仪(岛津半制备型HPLC系统),RVT4104低温冷冻干燥器(美国Thermo Fisher),SpeedVac真空离心器(美国Applied Biosystems公司),MALDI/TOF/TOF5800蛋白分析仪及配套软件Mascot软件(美国Applied Biosystems公司)。
1.3 方法 1.3.1 慢性温和不可预见性应激大鼠模型♂SD大鼠20只,先进行旷场实验评分,采用随机区组设计,按旷场实验结果将其分为正常组和模型组,每组10只。正常组正常饲养,模型组孤立喂养并接受21 d各种不同温和刺激,包括禁水24 h、禁食24 h、4℃冰水游泳5 min、昼夜颠倒、热刺激(45℃,5 min)、湿垫料、异味刺激、45°鼠笼倾斜24 h,每天随机选择1种刺激,相同刺激不得重复出现,同种刺激不能超过3次。造模完成后,即d 22时,进行旷场实验、强迫游泳实验、高架十字迷宫等行为学实验,以判断造模是否成功。模型成功后,大鼠断颈处死,冰台上迅速分离出海马组织,液氮速冻,-80℃冰箱保存。
1.3.2 海马组织蛋白质的提取① Lysis buffer中加入5 μL磷酸酶抑制剂、1 μL蛋白酶抑制剂和10 μL PMSF混匀。② 冰上预冷玻璃匀浆器,2支lysis buffer。③ 取冻存的大鼠海马组织,每组3只,PBS清洗,按组放入玻璃匀浆器,分别加预冷的lysis buffer,手动研磨,至均质匀浆。④ 加入TCA-冰丙酮,-20℃沉淀2 h后,3 000×g,4 ℃,离心30 min,弃上清液,取沉淀。再加入丙酮,-20 ℃沉淀30 min,4 ℃,离心30 min,反复操作,至沉淀变为白色。-80℃冻存。
1.3.3 ITRAQ标记① 蛋白溶解,定量:取冻存的2组样品,各加入40 mL裂解液和20 mL变性剂,震荡混悬溶解,离心去除沉淀。用Bradford法进行蛋白定量,调整溶液的蛋白浓度,使每组蛋白样品量为40 μg,体积20 μL。② 还原,封闭:按试剂盒提供方案进行还原、封闭。③ 酶解:向各组蛋白溶液中加入1 μg胰酶,37℃温育16 h。④ 标记:各试管标记试剂中加入50 μL异丙醇,混匀,分别加入各管样品中,室温反应1 h,之后各加入3倍体积水,使标记试剂分解。真空冷冻干燥。⑤ 除盐:将相关buffer和标记试剂的盐除去。
1.3.4 肽段的分离和鉴定① 第一维强阳离子柱(SCX)分离:流动相A液:10 mmol·L-1 KH2PO4,25% CAN,pH=2.6;B 液:10 mmol·L-1 KH2PO4,350 mmol·L-1 KCl和25% ACN,pH=2.6。80 μL A液中溶解冻干样品,上样。将紫外检测波长设置为214 nm/280 nm,然后将流速设置为200 μL·min-1。线性梯度洗脱:5~40 min,5%~25% B;40~45 min,25%~80% B;45~50 min,80% B;50~60 min,0%B。根据峰形和时间共收取20个梯度,真空离心浓缩后,每馏分用50 μL反相液相色谱的A 相溶解,进样量20 μL。② 第二维反相液相色谱:流动相A液包含:5%(体积分数)乙腈和0.1%甲酸溶液。流动相B液包含:95%乙腈和0.1%甲酸溶液。RPLC柱线性梯度洗脱:0~5 min,上样;5~70 min,5%~35% B;70~75 min,35%~80% B;75~80 min,80% B;80~81 min,80%~5% B;90 min停止。③ 质谱鉴定:喷雾针直接连接于反相色谱柱末端作为喷雾接口,喷雾电压2.2 kV。MS扫描范围:400~1 800 m/z,一个谱图选择4个最强母离子进行串级扫描,MS/MS扫描范围100~2 000 m/z。
1.3.5 生物信息学鉴定利用Protein.pilot3.0软件检索质谱分析所得数据,差异蛋白筛选标准设定为:① 肽段≥3,② 模型组与正常组大鼠海马组织蛋白分子质量比≥2.0或≤0.5,③ P<0.05。运用Uniport软件分析各蛋白生物学过程及分子功能,运用DAVID软件从生物过程、细胞成分、分子功能注释对蛋白进行分类,选择KEGG数据库对蛋白所涉及的通路进行分类和富集分析。
1.3.6 Western blot验证通过文献检索,选择了差异蛋白Sodium-and chloride-dependent GABA transporter 3进行Western blot验证。按照碧云天SDS-PAGE凝胶试剂盒提供配方制备凝胶;选取冻存大鼠海马组织,每组3只,提取蛋白并定量,调整每管蛋白浓度至均值,加入含2-巯基乙醇和溴酚蓝的2×蛋白上样缓冲液,100℃孵育10 min,冷却到室温后,将变性蛋白样品直接上样到SDS-PAGE胶加样孔内;蛋白上样后电压设置在100 V,时间设定为90~120 min,当溴酚蓝到达胶的底端处附近即可停止电泳;然后经过转膜,封闭,一抗孵育,二抗孵育,按1 ∶1加入AB显影液,室温放置5 min后,吸尽膜上水分,将膜放入暗盒,曝光5 min,在Bio-Rad 的化学发光成像仪上显影,然后分析灰度值,再计算灰度系数比。
2 结果 2.1 行为学实验结果根据前期的研究结果显示[4],21 d造模后,在旷场实验中,模型组大鼠水平运动和垂直运动次数较正常组减少。在强迫游泳实验中,模型组大鼠禁止不动时间较正常组增加。在高架十字迷宫实验,模型组大鼠进入开臂的次数及停留时间百分率明显缩短,进入高架十字迷宫总次数明显减少。说明CUMS致大鼠出现抑郁行为。
2.2 ITRAQ实验结果根据设定的Protein.pilot3.0软件,共鉴定到5 109个蛋白,其中差异蛋白33个,模型组较正常组表达上调的蛋白8个,下调的蛋白25个。Uniport数据库分析各个蛋白生物学过程及分子功能,见Tab1。
| 编号 | 蛋白名称 | 表达情况 | 生物学过程 | 分子功能 |
| O88763 | Phosphatidylinositol 3-kinase catalytic subunit type 3 | 高表达 | 细胞自噬,细胞周期,细胞分裂 | 激酶,转移酶 |
| P31647 | Sodium-and chloride-dependent GABA transporter 3 | 高表达 | 脑发育,神经递质的运输,离子的同向转运 | 钠离子的同向转运活动,神经递质的绑定 |
| P09215 | Protein kinase C delta type | 高表达 | 激酶,丝氨酸/苏氨酸蛋白激酶,转移酶 | 细胞凋亡,细胞周期 |
| P42123 | L-lactate dehydrogenase B chain | 高表达 | 碳水化合物、乳酸、NAD代谢过程 | 氧化还原 |
| P63182 | Cerebellin-1 | 高表达 | 小脑颗粒细胞的分化,积极调节突触组装 | |
| P13221 | Aspartate aminotransferase | 高表达 | 氨基酸的生物合成 | 氨基转移酶 |
| P60203 | Myelin proteolipid protein | 高表达 | 星形胶质细胞的发育,中枢神经系统髓鞘的形成,炎症反映,黑质体的发育,轴突发育,胶质细胞分化,长链脂肪酸生物合成过程 | 髓鞘的结构成分,结构分子活性 |
| Q5BJY9 | Keratin,type I cytoskeletal 18 | 高表达 | 结构分子活性 | |
| Q6P6R2 | Dihydrolipoyl dehydrogenase | 低表达 | 2-氧戊二酸盐的代谢过程,乙酰辅酶A从丙酮酸的生物合成过程 | 氧化还原酶类 |
| P11507 | Sarcoplasmic/endoplasmic reticulum calcium ATPase 2 | 低表达 | 钙离子的运输,离子转运 | 水解酶类 |
| P17764 | Acetyl-CoA acetyltransferase | 低表达 | 肝脏、近曲小管、脂肪组织的发育,脑发育,激素应答,饥饿应答 | 酰基转移酶 |
| P06399-2 | Isoform 2 of Fibrinogen alpha chain | 低表达 | 免疫,血液凝固 | |
| P49621 | Diacylglycerol kinase beta | 低表达 | 细胞内信号传递 | 三磷酸腺苷的结核,二酰基甘油激酶的活性 |
| Q920L2 | Succinate dehydrogenase[ubiquinone] flavoprotein subunit | 低表达 | 电子传递,三羧酸循环 | 氧化还原酶类 |
| Q5XI78 | 2-oxoglutarate dehydrogenase | 低表达 | 糖酵解 | 氧化还原酶类 |
| P21707 | Synaptotagmin-1 | 低表达 | 检测钙离子,监管钙离子的胞外分泌,调节神经突触的传递 | 网格蛋白的绑定,载体活性,突触融合蛋白的绑定 |
| P48768 | Sodium/calcium exchanger 2 | 低表达 | 反向转运,离子转运,钙离子、钠离子的运输 | 钙、钠逆向转运活动 |
| P52873 | Pyruvate carboxylase | 低表达 | 葡萄糖异生作用,脂类的生物合成及代谢 | 合成酶类 |
| P63039 | 60 ku heat shock protein | 低表达 | 检测错误折叠的蛋白,负调节神经元凋亡,积极调节炎症反映,等 | 分子伴侣 |
| P49432 | Pyruvate dehydrogenase E1 component subunit beta | 低表达 | 碳水化合物的代谢,葡萄糖的代谢,三羧酸循环 | 氧化还原酶类 |
| Q5YLM1 | Sn1-specific diacylglycerol lipase alpha | 低表达 | 脂类的代谢 | 水解酶类 |
| P62944 | AP-2 complex subunit beta | 低表达 | 内吞作用,蛋白质的转运 | 蛋白质的转运活动,网格蛋白的绑定 |
| P21571 | ATP synthase-coupling factor 6 | 低表达 | 离子转运 | 氢离子的跨膜转运活动 |
| Q09073 | ADP/ATP translocase 2 | 低表达 | 染色体分离,负调节线粒体外膜透化作用参与凋亡信号通路,积极调节细胞增值,跨膜转运 | 转运活动 |
| P55067 | Neurocan core protein | 低表达 | 细胞粘附,中枢神经系统发育,骨骼系统开发 | 糖结合,细胞外基质的结构组成 |
| Q9ER34 | Aconitate hydratase | 低表达 | 三羧酸循环 | 裂解酶 |
| P08461 | Dihydrolipoyllysine-residue acetyltransferase component of pyruvate dehydrogenase complex | 低表达 | 碳水化合物的代谢,葡萄糖代谢,三羧酸循环 | 酰基转移酶,转移酶 |
| Q505J9 | ATPase family AAA domain-containing protein 1 | 低表达 | 学习,记忆,代谢过程,负调节突触传递 | 水解酶类 |
| Q5HZW3 | Aspartate beta-hydroxylase domain-containing protein 2 | 低表达 | 金属离子的结合,氧化还原酶类 | |
| Q63564 | Synaptic vesicle glycoprotein 2B | 低表达 | 神经递质的摄取 | 跨膜运输活动 |
| Q9R1Z0-2 | Isoform 2 of voltage-dependent anion-selective channel protein 3 | 低表达 | 电压门控通道的活性 | 核苷酸连接区,孔蛋白活性 |
| P63012 | Ras-related protein Rab-3A | 低表达 | 胞外分泌,蛋白质的转运,转运 | ATP酶催化剂的活性 |
| P63100-2 | Isoform 2 of calcineurin subunit B type 1 | 低表达 | 蛋白质的脱磷酸作用 | 蛋白磷酸酶的活性 |
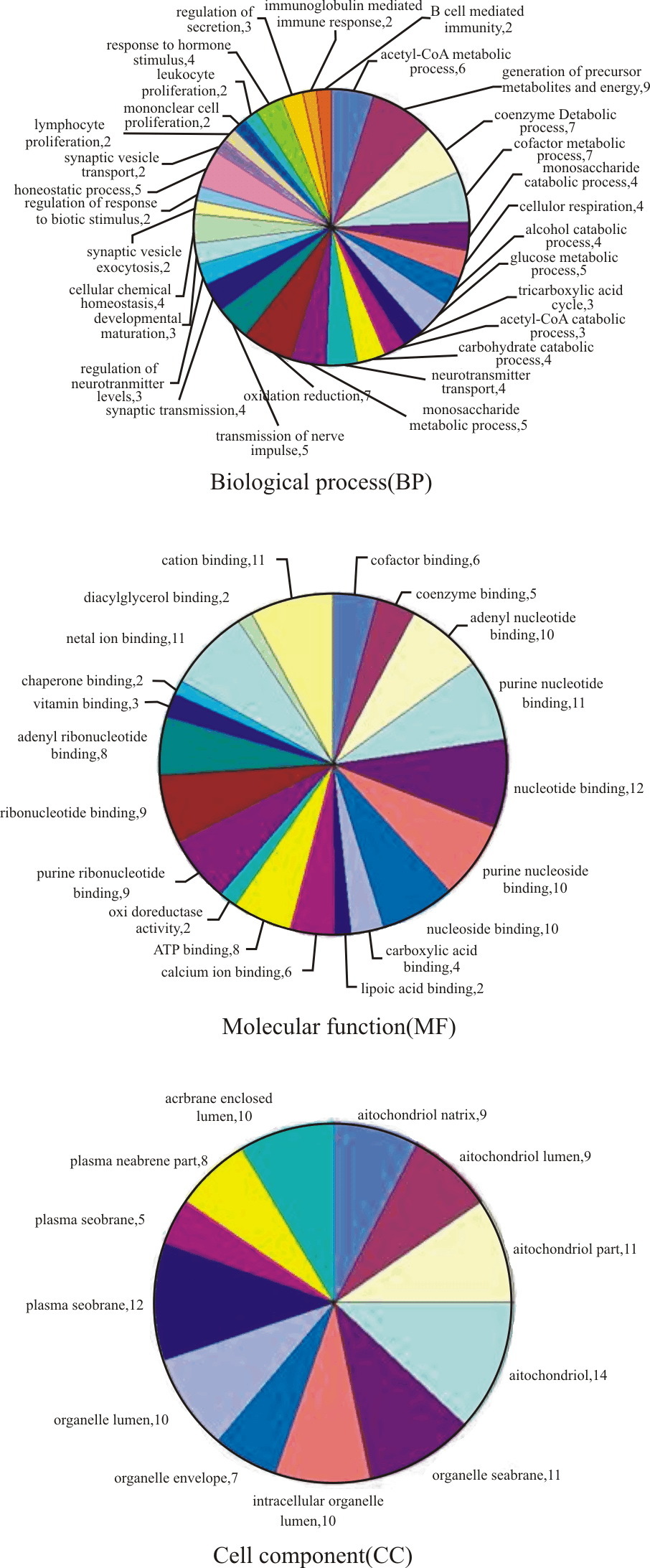
通过DAVID富集分析系统对本实验获得的33种差异蛋白进行GO分析和pathway分析。对差异蛋白进行GO分析,研究这些蛋白的功能,BP分析发现差异表达蛋白大多参与物质的代谢、能量的产生、机体免疫及神经冲动的传导。MF分析揭示这些蛋白大多数与体内分子的结合与捆绑相关,CC分析得出差异蛋白主要分布在细胞膜和线粒体上(Fig1)。通过KEGG PATHWAY发现,共有23个蛋白,参与了7个生物代谢通路,有7个蛋白参与了柠檬酸循环,6个蛋白参与了丙酮酸代谢,4个蛋白参与了糖酵解和糖异生,5个蛋白参与了钙信号途径,5个蛋白参与了亨廷顿舞蹈症,4个蛋白参与了帕金森病,4个蛋白参与了阿尔茨海默病。
|
| Fig.1 Rat hippocampus proteome classified according to GO annotations |
ITRAQ实验结果显示,蛋白Sodium-and chloride-dependent GABA transporter 3在CUMS大鼠海马组织中表达上调3.05倍。Western blot实验结果表明,相对于正常大鼠海马组织蛋白,Sodium-and chloride-dependent GABA transporter 3在CUMS大鼠海马组织中明显高表达。见Fig2。

|
| Fig.2 P31647 expression in rat hippocampus revealed by Western blot analysis |
抑郁症是临床常见的精神障碍性疾病,发病率逐年增加。目前药物治疗是抑郁症的主要治疗手段,但经过药物治疗的患者存在着复发率高,治疗不彻底的现象。因此研究抑郁症的发病机制,寻找更有效的药物,是国内外一个重要的研究方向。ITRAQ技术作为一种新的蛋白质组学研究方法,在蛋白质定量方面显出无可比拟的优越性,运用该技术寻找和发现CUMS大鼠海马组织区别于正常生理状态下的疾病特异表达蛋白,有利于疾病发病机制的阐明及寻找生物标志物。Chung等[5]运用ITRAQ联合LC-MS/MS技术寻找出了人类肺腺癌潜在的生物标志物AGR2。
本实验运用慢性不可预见性温和应激建立大鼠抑郁模型,该模型是一种经典的动物抑郁模型,被国内外实验室广泛使用,能模拟出人类抑郁的核心症状,与人类抑郁发病机制较为接近[6]。行为学结果显示:旷场实验中,模型组大鼠水平运动和垂直运动次数较正常组减少。强迫游泳实验中,模型组大鼠禁止不动时间较正常组增加。高架十字迷宫实验,模型组大鼠进入开臂的次数及停留时间百分率明显缩短,进入高架十字迷宫总次数明显减少。说明CUMS致大鼠出现抑郁行为。
本实验运用ITRAQ技术结合2D LC-MS/MS分析CUMS大鼠与健康大鼠的海马组织差异表达蛋白质。共鉴定出5 109个蛋白,差异蛋白33个,其中8个蛋白表达上调,25个蛋白表达下调。GO分析发现参与神经冲动传导的蛋白共6个,其中表达上调的是Myelin proteolipid protein;表达下调的有Synaptic vesicle glycoprotein 2B、Neurocan core protein、Synaptotagmin-1、Ras-related protein Rab-3A、Isoform 2 of voltage-dependent anion-selective channel protein 3。参与神经递质运输的蛋白有4个,其中表达上调的蛋白是Sodium-and chloride-dependent GABA transporter 3;表达下调的蛋白有Synaptic vesicle glycoprotein 2B、Synaptotagmin-1、Ras-related protein Rab-3A。参与突触传导的蛋白是Synaptic vesicle glycoprotein 2B、Neurocan core protein、Synaptotagmin-1、Ras-related protein Rab-3A、Isoform 2 of voltage-dependent anion-selective channel protein 3,都表达下调并且也参与了细胞间信号的传导。参与调节神经递质水平的蛋白共有3个,都表达下调,蛋白包括Synaptic vesicle glycoprotein 2B、Synaptotagmin-1、Ras-related protein Rab-3A。本实验发现蛋白Neurocan core protein、Isoform 2 of voltage-dependent anion-selective channel protein 3参与了3种生物学过程,Synaptic vesicle glycoprotein 2B、Synaptotagmin-1、Ras-related protein Rab-3A参与了5种生物学过程。并且蛋白Synaptic vesicle glycoprotein 2B、Neurocan core protein、Synaptotagmin-1、Ras-related protein Rab-3A、Isoform 2 of voltage-dependent anion-selective channel protein 3分别在CUMS大鼠海马组织表达是正常大鼠的19%、35%、44%、13%、13%。这些蛋白表达的降低与抑郁症的发生、发展有着密切的关联。Abumaria等[7]的研究中也发现抑郁样症状的大鼠synaptic vesicle glycoprotein 2b蛋白会减少。Dimatelis等[8]通过ITRAQ联合MALDI-MS/MS实验发现,与突触可塑性相关的Neurocan core protein参与调节大鼠母婴分离所带来的焦虑及抑郁症状。Baker等[9]也证实,Synaptotagmin-1与人类运动的控制及认知的发展密切相关。
KEGG PATHWAY分析发现,CUMS大鼠海马组织与三羧酸循环相关的7个蛋白Dihydrolipoyl dehydrogenase、Succinate dehydrogenase[ubiquinone] flavoprotein subunit、2-oxoglutarate dehydrogenase、Pyruvate carboxylase、Pyruvate dehydrogenase E1 component subunit beta、 Aconitate hydratase、Dihydrolipoyllysine-residue acetyltransferase component of pyruvate dehydrogenase complex均是低表达,这些蛋白的表达下调主要影响三羧酸循环的正常进行,在能量供给方面发挥着负面作用,与抑郁症的发生发展密切相关。与Kaibara等[10]的研究结果相符。参与了钙信号通路的5个蛋白Sarcoplasmic/endoplasmic reticulum calcium ATPase 2、Sodium/calcium exchanger 2、ADP/ATP translocase 2、Isoform 2 of voltage-dependent anion-selective channel protein 3、Isoform 2 of calcineurin subunit B type 1,均是低表达。Gavio等[11]的研究显示,突触前膜钙通道和钙流入的减少会导致突触稳态的自我调节功能减弱,继而影响到学习记忆睡眠质量的降低。随之可能带来精神方面的负面影响,引起抑郁。本实验发现蛋白ADP/ATP translocase 2、Succinate dehydrogenase[ubiquinone] flavoprotein subunit、ATP synthase-coupling factor 6、Isoform 2 of voltage-dependent anion-selective channel protein 3、AP-2 complex subunit beta参与了亨廷顿舞蹈症,蛋白ADP/ATP translocase 2、Succinate dehydrogenase[ubiquinone] flavoprotein subunit、ATP synthase-coupling factor 6、Isoform 2 of voltage-dependent anion-selective channel protein 3参与了帕金森病,而蛋白Sarcoplasmic/endoplasmic reticulum calcium ATPase 2、 Isoform 2 of calcineurin subunit B type 1、 Succinate dehydrogenase[ubiquinone] flavoprotein subunit、 ATP synthase-coupling factor 6参与了阿尔茨海默病。这3种疾病都是由于神经变性疾病引起的大脑退化性疾病,并且当病情发展到一定程度都会引起抑郁症状的发生[12]。本实验发现参与这3种疾病代谢通路的蛋白表达均降低,并且蛋白ADP/ATP translocase 2、Isoform 2 of voltage-dependent anion-selective channel protein 3参与2种疾病的代谢通路,而蛋白Succinate dehydrogenase[ubiquinone] flavoprotein subunit、ATP synthase-coupling factor 6甚至参与了3种代谢通路。这些参与2种,甚至3种的蛋白质会不会是引起神经退行性病变的关键蛋白,从而引导其他蛋白进入相应的代谢通路,值得我们进一步研究,从而寻找抗抑郁药物的靶蛋白,并以此为基础研发新型的抗抑郁药物。
(致谢:本项目是在重庆医科大学完成。感谢重庆医科大学为本实验提供的仪器设备的支持,及技术上的帮助。感谢实验过程中给予过无私帮助的老师及同学们。)
| [1] | Spiegel D,Giese-Davis J,Taylor C B,et al. Stress sensitivity in metastatic breast cancer: analysis of hypothalamic-pituitary-adrenal axis function[J]. Psychoneuroendocrinology,2006,31(10): 1231-44. |
| [2] | Zhu G,Yan W,He H,et al. Inhibition of proliferation,invasion,and migration of prostate cancer cells by downregulating elongation factor-1 expression[J]. Mol Med,2009,15(8): 363-70. |
| [3] | 李 敏,姜 鹏,王淑萍,等. 蛋白质组学在中药研究中的应用[J]. 药学实践杂志,2013,31(4): 76-82. Li M,Jiang P,Wang S P,et al. Proteomics in study of traditional Chinese medicine[J]. J Pharm Pract,2013,31(4): 76-82. |
| [4] | 曹莉莎,叶 云,王继生,等. 尼美舒利对慢性应激大鼠抑郁行为的影响[J]. 中国医院药学杂志,2014,34(11): 890-5. Cao L S,Ye Y,Wang J S,et al. Effect of nimesulide on chronic unpredictable mild stress-induced depressive behavior in rats[J]. Chin Hosp Pharm J,2014,34(11): 890-5. |
| [5] | Chung K,Nishiyama N,Wanibuchi H,et al. AGR2 as a potential biomarker of human lung adenocarcinoma[J]. Osaka City Med J,2012,58(1): 13-24. |
| [6] | 罗 文,马庆阳,杨俊卿,等. 美洛昔康对慢性应激大鼠抑郁行为的影响[J]. 中国药理学通报,2012,28(1): 123-7. Luo W,Ma Q Y,Yang J Q,et al. Effect of Meloxicam on CUMS-induced depressive behavior in rats[J]. Chin Pharmacol Bull,2012,28(1): 123-7. |
| [7] | Abumaria N,Rygula R,Hiemke C,et al. Effect of chronic citalopram on serotonin-related and stress-regulated genes in the dorsal raphe nucleus of the rat[J]. Eur Neuropsychopharmacol, 2007,17(6-7): 417-29. |
| [8] | Dimatelis J J,Hendricks S,Hsieh J,et al. Exercise partly reverses the effect of maternal separation on hippocampal proteins in 6-hydroxydopamine-lesioned rat brain[J]. Exp Physiol,2013,98(1): 233-44. |
| [9] | Baker K,Gordon S L,Grozeva D,et al. Identification of a human synaptotagmin-1 mutation that perturbs synaptic vesicle cycling[J]. J Clin Invest,2015,125(4): 1670-8. |
| [10] | Kaibara T,Sutherland G,Colbourne F,et al. Hypothermia: depression of tricarboxylic acid cycle flux and evidence for pentose phosphate shunt upregulation[J]. J Neurosurg, 1999,90(2): 339-47. |
| [11] | Gavio M A,Ford K J,Archila S,et al. Homeostatic synaptic depression is achieved through a regulated decrease in presynaptic calcium channel abundance[J]. Elife,2015,4: 05473. |
| [12] | Marttinen M,Kurkinen K M,Soininen H,et al. Synaptic dysfunction and septin protein family members in neurodegenerative diseases[J]. Mol Neurodegener,2015,10(1):13024-39. |

