


近年来研究表明,白花丹的主要活性成分白花丹醌(plumbagin)具有明显的抗肝纤维化作用[1, 2, 3],其抗肿瘤也被临床实践所验证,是一种很有潜力且十分具有应用前景的抗肿瘤天然药物,对人乳腺癌细胞侵袭和迁移有较好的抑制作用[4],能够诱导人肺癌细胞发生凋亡和自噬作用[5]。白花丹醌对人肝癌细胞HepG2的增殖有抑制作用[6],但其抗肝癌的具体机制未明,目前报道很少。本实验以人肝癌细胞株(HepG2)为研究对象,采用MTT法检测白花丹醌对HepG2细胞增殖的影响,Transwell细胞体外侵袭实验观察HepG2细胞的侵袭能力,应用流式细胞仪Annexin V/PI双染法检测细胞凋亡的情况,免疫组化检测白花丹醌对HepG2细胞凋亡相关蛋白Bax、Bcl-2表达的影响,探讨白花丹醌抗肝癌的可能机制。
1 材料与仪器 1.1 细胞株人肝癌细胞HepG2,购自南京凯基生物科技发展有限公司。
1.2 药物与试剂白花丹醌(批号:SLBG3436V)购自Sigma公司,用二甲基亚砜(DMSO)溶解,制备成0.1 mol·L-1的白花丹醌溶液,置于4 ℃避光保存,用时稀释成不同浓度的工作液,DMSO在各组工作液的总浓度均低于0.1%;高糖DMEM培养基购自Hyclone公司,新生牛血清购自四季青公司;MTT试剂盒,购自Vazyme公司;鼠抗人Bax、Bcl-2单克隆抗体、SP试剂盒、DAB显色试剂盒均购自Santa Cruz 公司;Annexin V/PI细胞凋亡检测试剂盒,购自美国BD公司。
1.3 主要仪器细胞培养箱(Sanyo MCO-18AIC,日本);高速离心机(Thermo Fisher Sorvall ST 16R,美国);酶标仪(Epoch Biotek,美国);电热恒温培养箱(DNP-9162,中国);光学显微镜(Olympus BX53,日本);倒置生物显微镜(Leica DM2500,德国);流式细胞仪(BD LSRFortessa,美国)。
2 方法 2.1 细胞培养人肝癌细胞HepG2,在37 ℃、5% CO2饱和湿度条件下,于10%新生牛血清的高糖DMEM培养液中培养,观察细胞生长情况,每2~3 d传代1次,取对数生长期的细胞用于实验。
2.2 MTT细胞增殖抑制实验取对数生长期的人肝癌细胞HepG2细胞进行细胞计数,调整细胞浓度为4×107·L-1,以每孔100 μL接种于96孔培养板中,设置空白孔(无细胞)、对照孔(培养基不加药,有细胞)、实验孔(不同浓度的白花丹醌干预),每组设定5个复孔。细胞常规培养24 h后完全贴壁,去除孔中培养液,分别加入1、2、4、8 μmol·L-1 的白花丹醌工作液。干预24、48 h后,每孔加入10 μL MTT (5 g·L-1),孵育4 h,小心吸弃上清,每孔加入100 μL DMSO,微型混合器上水平震荡5 min后于酶标仪上测定570 nm处的OD值。按下列公式计算不同浓度白花丹醌对HepG2细胞的增殖抑制率:抑制率(IR)/%=(1-实验组OD值/对照组OD值)×100%。根据不同浓度的白花丹醌对细胞增殖的能力,选择最佳作用时间(后续实验以此作为时间条件)。
2.3 Transwell体外侵袭实验观察细胞的侵袭能力冰上将融化后的BD Matrigel用冰高糖DMEM稀释4倍,混匀,往预冷的Transwell板上室加稀释后的Matrigel,每孔50 μL,均匀铺平,并置于细胞培养箱中孵育3~4 h。消化已用无血清高糖DMEM饥饿20 h的HepG2细胞,并细胞计数,调整细胞浓度为4×108·L-1,离心弃上清液后,分别用100 μL 0.1% BSA的培养液配制的不同浓度的白花丹醌重悬细胞,加入Matrigel已成胶的Transwell上室中,下室加入600 μL 10%新生牛血清培养液,每组设3个复孔,置于培养箱中孵育。20 h后,取出Transwell板,移去培养液,PBS清洗Transwell小室2次,4%多聚甲醛固定20 min,无水甲醛透化20 min,0.1%结晶紫染色15 min,每步均用PBS清洗2次,用棉签轻轻拭去没有侵袭的细胞及基质胶,封片,倒置显微镜下随机取5个视野观察、拍照并细胞计数。
2.4 流式细胞术Annexin V/PI双染法检测细胞凋亡情况各白花丹醌用药组细胞严格按照凋亡检测试剂盒说明书进行操作。药物与细胞共孵育48 h后,细胞消化成单个细胞悬液,离心后完全培养基清洗细胞2次,进行Annexin V、PI联合标记,加入5 μL Annexin V,20 μL PI,混匀,以3 000 r·min-1离心5 min,洗涤后,加入500 μL完全培养基重悬细胞,随即用流式细胞仪检测细胞凋亡率。
2.5 免疫细胞化学检测Bax、Bcl-2蛋白水平采用免疫组化SP法,将对数生长期的HepG2细胞接种于放有盖玻片的6孔板中,24 h待细胞贴壁生长后,白花丹醌分组干预。药物与细胞共孵育48 h后,取出盖玻片置于载玻片上,用4%多聚甲醛固定,3% H2O2消除内源性过氧化氢酶,正常血清封闭后分别加入鼠抗人Bax、Bcl-2单克隆抗体,4℃孵育过夜,随后加入生物素二抗工作液及辣根酶标记链霉卵白素工作液,经DAB显示,脱水、封片,光学显微镜下观察。以PBS代替一抗作为阴性对照。检测方法严格按照试剂盒说明书进行操作。Bax、Bcl-2表达阳性的细胞,光学显微镜下可观察到细胞的胞质内呈现特异性棕褐色,阳性表达率/%=(500个细胞内阳性细胞数/500个细胞数)×100%。
2.6 统计学处理实验数据采用SPSS 17.0统计软件进行分析,组间比较采用单因素方差分析,各均数两两比较采用q检验。
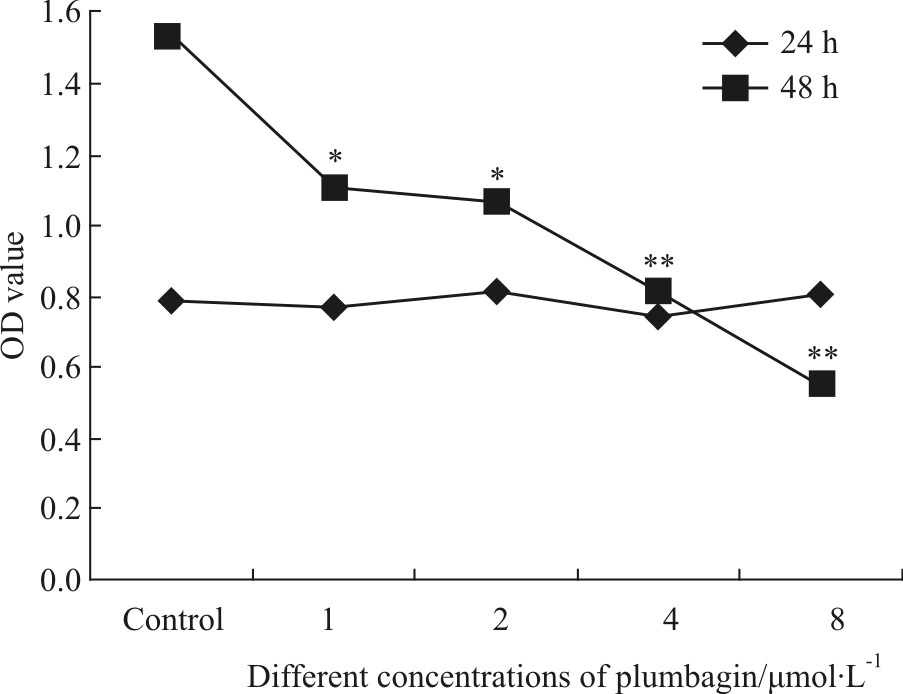
3 结果 3.1 白花丹醌对HepG2细胞增殖的影响采用不同浓度白花丹醌干预不同时间(24、48 h)后,MTT分析(Fig1)发现,各浓度白花丹醌干预24 h对HepG2细胞的增殖无明显抑制作用(P>0.05),而干预48 h,白花丹醌呈剂量依赖性抑制HepG2细胞的增殖,以8 μmol·L-1浓度最为明显,与对照组比较差异最具明显(P<0.01),后续实验采用48 h干预时间。
|
| Fig.1 Effect of plumbagin on proliferation of HepG2 cells(x±s,n=5) *P<0.05,**P<0.01 vs control group |
Transwell侵袭实验显示,白花丹醌干预HepG2细胞后,细胞侵袭能力明显减弱,白花丹醌4,8 μmol·L-1尤其明显(P<0.01,Fig2,Tab1)。

|
| Fig.2 The microscopic images of invasion amount of HepG2 cells at different concentrations of plumbagin(×200) A:Control group;B:Plumbagin 1 μmol·L-1 group;C:Plumbagin 2 μmol·L-1 group;D:Plumbagin 4 μmol·L-1 group;E:Plumbagin 8 μmol·L-1 group |
| Group | Invasion amount | Invasion rate/% |
| Control | 194.00±6.000 | / |
| Plumbagin 1 μmol·L-1 | 180.00±8.185* | 92.78 |
| Plumbagin 2 μmol·L-1 | 175.00±5.000* | 90.21 |
| Plumbagin 4 μmol·L-1 | 81.00±4.583** | 41.75 |
| Plumbagin 8 μmol·L-1 | 45.67±2.517** | 23.19 |
| *P<0.05,**P<0.01 vs control group | ||
V/PI双染法检测细胞凋亡 与对照组比较,白花丹醌4、8 μmol·L-1 组凋亡最为明显,差异均具有显著性(P<0.01,Fig3,Tab2)。

|
| Fig.3 Annexin V-FITC show HepG2 apoptosis case at different concentrations of plumbagin A:Control group;B:Plumbagin 1 μmol·L-1 group;C:Plumbagin 2 μmol·L-1 group;D:Plumbagin 4 μmol·L-1 group;E:Plumbagin 8 μmol·L-1 group |
| Group | Apoptosis rate/% |
| Control | 21.200±1.054 |
| Plumbagin 1 μmol·L-1 | 23.800±0.625 |
| Plumbagin 2 μmol·L-1 | 28.067±0.950 |
| Plumbagin 4 μmol·L-1 | 45.067±4.910** |
| Plumbagin 8 μmol·L-1 | 49.367±4.884 ** |
| **P<0.01 vs control group | |
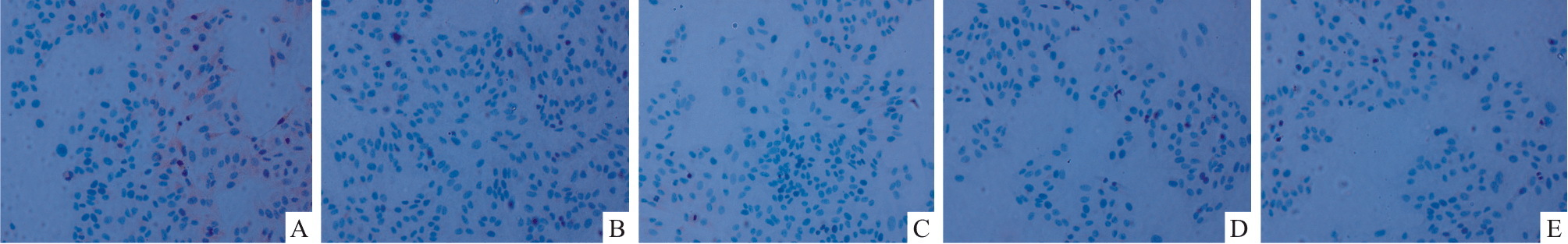
不同浓度的白花丹醌作用48 h后,HepG2细胞内均出现不同程度的棕褐色颗粒物,随着浓度增加,促凋亡基因Bax蛋白表达明显上调,抗凋亡基因Bcl-2表达明显降低,即能明显下调Bcl-2/Bax蛋白的比值,与对照组比较差异均有显著性(P<0.01,Fig4,Fig5,Tab3)。

|
| Fig.4 Effect of plumbagin on expression of Bax protein in HepG2 cells(×200) A:Control group;B:Plumbagin 1 μmol·L-1 group;C:Plumbagin 2 μmol·L-1 group;D:Plumbagin 4 μmol·L-1 group;E:Plumbagin 8 μmol·L-1 group |
|
| Fig.5 Effect of plumbagin on expression of Bcl-2 protein in HepG2 cells(×200) A:Control group;B:Plumbagin 1 μmol·L-1 group;C:Plumbagin 2 μmol·L-1 group;D:Plumbagin 4 μmol·L-1 group;E:Plumbagin 8 μmol·L-1 group |
| Group | Bax protein expression rate/% | Bcl-2 protein expression rate/% |
| Control | 35.800±1.311 | 49.733±2.120 |
| Plumbagin 1 μmol·L-1 | 44.400±1.442 | 37.133±1.514* |
| Plumbagin 2 μmol·L-1 | 54.067±1.747* | 30.800±1.200* |
| Plumbagin 4 μmol·L-1 | 67.933±1.747** | 21.500±1.323** |
| Plumbagin 8 μmol·L-1 | 94.533±1.405** | 11.867±0.808** |
| *P<0.05,**P<0.01 vs control group | ||
肝细胞癌是临床常见的恶性肿瘤之一,肿瘤细胞的转移和侵袭是恶性肿瘤的基本特征,尤其在肿瘤发展的最后阶段,控制转移是决定患者预后的关键因素。肿瘤细胞的运动性在侵袭转移中的作用已被众多实验所证实,迁移运动能力与侵袭之间的关系呈正相关。如何阻断肿瘤细胞的侵袭和转移是目前肿瘤治疗研究的热点之一。已有研究表明,某些中草药具有抑制肿瘤侵袭和迁移的作用。白花丹醌是白花丹的主要活性成分,是从植物白花丹中提取的一种小分子萘醌化合物,具有广泛的药理活性,包括抗菌消炎、抗生殖、抗凝、抗动脉粥样硬化、强心、抗肝纤维化、抗癌等作用[7, 8],其抗癌活性引起了广泛的关注,研究显示,白花丹醌对白血病、骨肉瘤、乳腺癌等有明显的杀伤和抑制作用[9, 10, 11]。本研究以MTT法检测白花丹醌对HepG2细胞增殖的影响,发现随着药物浓度的增加,其抑制作用增强,并呈剂量-效应关系。Matrigel包被的小室实验是模拟人体内基质环境来研究肿瘤细胞的侵袭能力的实验,本实验观察到,与对照组相比,白花丹醌4、8 μmol·L-1干预组可以明显降低HepG2细胞穿透人工基底膜的细胞数量,说明白花丹醌具有明显抑制HepG2细胞侵袭能力。
细胞凋亡是指为维持内环境稳定,由基因控制细胞自主有序的死亡,这一过程受多种促凋亡和抗凋亡的蛋白调节,其中Bcl-2家族蛋白担任着重要的角色,Bcl-2家族成员主要定位在核膜、细胞器膜上,与膜结合是其发挥生物功效的保障[12]。Bax和Bcl-2通过形成同源二聚体或异源二聚体,来改变线粒体外膜各种通道的开放程度,从而调节细胞凋亡。当Bax形成同源二聚体是诱导细胞凋亡,特别是大于80%时,且在适当信号诱导下,细胞凋亡作用增大;Bax和Bcl-2形成异源二聚体时则抑制细胞凋亡,因而认为Bcl-2/Bax比率是启动细胞凋亡的“分子开关”,其数值越低说明凋亡趋势越明显[13]。本实验研究发现,白花丹醌能诱导HepG2细胞发生凋亡,白花丹醌作用HepG2细胞48 h,4、8 μmol·L-1组细胞凋亡率均明显高于对照组。并且使HepG2细胞Bax蛋白水平上调,下调Bcl-2蛋白水平,即Bcl-2/Bax比值下降,并存在剂量依赖性,这可能是白花丹醌诱导肝癌细胞凋亡的分子机制之一。
综上所述,白花丹醌能够抑制HepG2细胞增殖,促进HepG2细胞凋亡,抑制HepG2细胞的侵袭,说明白花丹醌具有抗肝癌的作用。白花丹醌调控肝癌细胞的侵袭及凋亡的具体分子机制,有待进一步研究,为白花丹醌临床治疗肝癌提供实验依据。
(致谢:本文全部实验均在广西中医药大学科学实验中心完成,特此致谢!)
| [1] | 刘雪梅,韦燕飞,彭 岳,等.白花丹醌对瘦素诱导人肝星状细胞增殖与α-SMA 表达的影响[J].中国药理学通报,2010,26(9): 1154-7. Liu X M,Wei Y F,Peng Y,et al. Effects of plumbagozeylanica(plumbago) on expression of α-SMA in human hepatic stellate cells activated by leptin[J]. Chin Pharmacol Bull,2010,26(9): 1154-7. |
| [2] | 韦燕飞,钟振国,黄仁彬,等.白花丹醌对人肝星状细胞凋亡及相关蛋白表达的影响[J].世界华人消化杂志,2011,19(4): 349-54. Wei Y F,Zhong Z G,Huang R B,et al. Effects of plumbagin on apoptosis and expression of apoptosis-related proteins in human hepatic stellate cells[J]. World Chin J Dig,2011,19(4): 349-54. |
| [3] | 刘雪梅,赵铁建,彭 岳,等.白花丹醌对人肝星状细胞肿瘤坏死因子-α、血小板衍化生长因子BB表达的影响[J].中药材,2013,36(4): 594-7. Liu X M,Zhao T J,Peng Y,et al. Effects of plumbagin on expression of TNF-α and PDGF-BB in human hepatic stellate cells activated by leptin[J]. J Chin Med Mat,2013,36(4): 594-7. |
| [4] | Yan W,Tu B,Liu Y Y,et al. Suppressive effect of plumbagin on invasion and migration of breast cancer cells via the inhibition of STAT3 signaling and down-regulation of inflammatory cytokine expressions[J].Bone Res,2013,1(4): 362-70. |
| [5] | Li Y C,He S M,He Z X,et al. Plumbagin induces apoptotic and autophagic cell death through inhibition of the PI3K/Akt/mTOR pathway in human non-small cell lung cancer cells[J]. Cancer Lett,2014,344(2): 239-59. |
| [6] | 张吉仲,万 谦,刘 圆.白花丹醌对人肝癌细胞HepG2、SMMC-7721增殖及其Bax / Bcl-2、Cyclin D1 mRNA 表达的影响[J].中国药理学通报,2012,28(12): 1729-32. Zhang J Z,Wan Q,Liu Y. The influence of plumbagin on proliferation of the human hepatoma carcinoma cells HepG2,SMMC-7721 and mRNA expression of Bax/Bcl-2,Cyclin D1[J]. Chin Pharmacol Bull,2012,28(12): 1729-32. |
| [7] | Aziz H,Dreckschmidt E,Verma K. Plumbagin,a medicinal plant-derived naphthoquinone,is a novel inhibitor of the growth and invasion of hormone refractory prostate cancer[J]. Cancer Res,2008,68(21): 9024-32. |
| [8] | Son T G,Camandola S,Arumugam T V,et al. Plumbagin,a novel Nrf2/ARE activator,protects against cerebral ischemia[J]. J Neurochem,2010,112(5):1316-26. |
| [9] | Gaascht F,Teiten M H,Cerella C,et al. Plumbagin modulates leukemia cell redox status[J]. Molecules,2014,19(7):10011-32. |
| [10] | Yan C H,Li F,Ma Y C. Plumbagin shows anticancer activity in human osteosarcoma(MG-63) cells via the inhibition of S-phase checkpoints a down-regulation of c-myc[J]. Int J Clin Exp Med,2015,8(8):14432-9. |
| [11] | Saqar S,Esau L,Moosa B,et al. Cytotoxicity and apoptosis induced by a plumbagin derivative in estrogen positive MCF-7 breast cancer cells[J]. Anticancer Agents Med Chem,2014,14(1): 170-80. |
| [12] | Yin X M. Signal transduction mediated by Bid,a pro-death Bcl-2 family proteins,connects the death receptor and mitochondria apoptosis pathways[J]. Cell Res,2000,10(3): 161-7. |
| [13] | Zhang Z G,Zou J,Huang Y,et al. Kinetin inhibits proliferation of hepatic stellate cells by interrupting cell cycle and induces apoptosis by down-regulating ratio of Bcl-2/Bax[J].J Huazhong Univ Sci Technol Med Sci,2015,35(5): 672-8. |

