


2. 安徽医科大学药学院,安徽 合肥 230032;
3. 安徽医科大学第二附属医院妇产科,安徽 合肥 230601
2. School of Pharmacy, Anhui Medical University,Hefei 230032,China;
3. Dept of Gynaecology and Obstetrics,the Second Affiliated Hospital of Anhui Medical University,Hefei 230601,China
是肝纤维化发生发展的中心环节,抑制HSC活化增殖是防治肝纤维化的重要措施之一[1]。研究证实[2, 3],抑制瞬时感受器电位M7,可抑制人胚肺成纤维细胞株(MRC-5)、大鼠肝星状细胞株(HSC-T6)活化增殖,促进其凋亡。提示离子通道蛋白可影响HSC增殖活化,可能在肝纤维化进程中发挥作用。HSC 细胞膜上的离子通道成为调控HSC增殖与凋亡的新靶点。
瞬时受体电位通道(transient receptor potential channels,TRP channels)是位于细胞膜上的一类重要的阳离子通道,TRPV为TRP家族中的一个亚家族,TRPV广泛存在于人体各种组织中,如心脏、肝、脾、肾、大脑、子宫等,参与人体的生理功能和病理变化。瞬时感受器电位离子通道香草素受体亚家族4(transient receptor potential vanilloid receptor 4,TRPV4)属TRPV家族成员,TRPV4不仅参与炎症和神经性疼痛的痛觉调控,还能感知热知觉,并且可调节细胞的生长死亡等生理作用,具有重要的临床和药理学研究价值[4]。TRPV4在肝纤维化中的作用及可能的作用机制还不明确。本研究通过在体、离体观察TRPV4在肝纤维化组织及活化的HSC中的表达变化,通过阻断、沉默TRPV4,观察其对HSC活化增殖的影响,及对蛋白激酶B(protein kinase B,Akt/PKB)蛋白表达的影响,探讨其可能的作用机制。
1 材料 1.1 实验动物♂ Spague-Dawlay(SD)大鼠,体质量180~220 g,由安徽医科大学动物中心提供。动物自由饮食,饮用自来水,喂养标准颗粒饲料,室温(18~26) ℃,常规饲养观察1周后使用。
1.2 细胞株HSC-T6细胞株购于上海中科院细胞库。以DMEM高糖培养基(内含10%胎牛血清、100 kU·L-1青霉素、100 mg·L-1链霉素),在37℃含5% CO2恒温培养箱孵育。实验取对数生长期细胞。
1.3 试剂CCl4,汕头西陇化工厂,临用前用花生油1 ∶1稀释;钌红(ruthenium red,Ru),Sigma公司产品;重组人转化生长因子(recombinant human TGF-β1),PeproTech公司产品;透明质酸(HA)、层黏连蛋白(LN)、Ⅳ型胶原(CⅣ),北京北方生物技术研究所;羟脯氨酸(Hyp),南京建成生物工程研究所;MTT(3,4,5-dimethylthiazo-2-yl-2,5- diphenyltetrazolium bromide)粉,美国Sigma公司,用PBS配制成5 g·L-1,过滤除菌,4 ℃避光保存;TRIzol Reagent试剂,Invitrogen Life Technology公司;Reverse Transcription System逆转录试剂盒、PCR试剂盒,Fermentas公司产品;抗TRPV4抗体,美国Abcam公司产品;抗β-actin抗体、抗Akt抗体,Santa Cruz 公司产品;抗α-SMA抗体,博士德公司产品;辣根过氧化酶(HRP)标记的兔抗小鼠IgG、HRP标记的山羊抗兔IgG,北京中杉金桥生物技术公司产品。
2 方法 2.1 大鼠肝纤维化模型的建立大鼠适应性饲养1周后,随机分为正常组、模型组,每组10 只。CCl4(分析纯)与花生油1 ∶1配制成植物油溶液,模型组于大鼠背部皮下注射含50% CCl4的花生油1 mL·kg-1,每周2次,连续12周。正常组注射花生油1 mL·kg-1。12周末,大鼠禁食8 h处死,取血及肝脏组织,检测HA、LN、CⅣ、Hyp、病理及α-SMA、Akt、TRPV4蛋白表达情况。
2.2 纤维化指标检测按试剂盒说明书要求规范操作,测定血清HA、LN、CⅣ含量以及肝组织匀浆Hyp含量。
2.3 病理学检测取肝左叶相同部位的肝脏组织,大小为 5 mm×5 mm,置于4%多聚甲醛中固定24 h。样品经梯度乙醇脱水和二甲苯透明后,用石蜡包埋,制备5 μm连续切片后,HE、Masson 染色切片,光镜下观察肝脏组织形态学变化情况。
2.4 MTT法检测细胞增殖0.25%胰蛋白酶消化对数生长期的HSC-T6 细胞,接种于96 孔板中,每孔1× 104个细胞,培养液体积为200 μL,培养细胞密度至80%~90%进行实验。实验组加入1 μmol·L-1的Ru,对照组加入等体积的DMEM,每组设5个平行孔,37℃、5% CO2培养箱中培养24 h。培养结束前4 h,每孔加入20 μL浓度为5 g·L-1的 MTT,吸去上清液,加入DMSO,每孔200 μL,混匀10 min后,酶标仪570 nm处测定各孔吸光度A值。对照组细胞存活率为100%,其余各组按:存活率/%=[(各实验组吸光度值-本底吸光度值)/(对照组吸光度-本底吸光度值)]×100%,实验重复3次。
2.5 TRPV4siRNA的转染靶向目的基因TRPV4的序列设计正义链:5′-CCGUGUCCUUCUACAUCAATT-3′,反义链:5′-UUGAUGUAGAAGGACACGGTT-3′;阴性对照组正义链:5′-UUCUCCGAACGUGUCACGUTT-3′,反义链:5′-ACGUGACACGUUCGGAGAATT-3′。应用BLAST 检索GenBank表达序列标签(EST)数据库,确定siRNA序列唯一性,上海吉玛制药有限公司合成。实验分正常组、模型组、对照组和TRPV4-siRNA 转染组。细胞传代至6 孔培养板,培养液体积为2 mL,每孔2×105个细胞,模型组加入20 μL浓度为1 mg·L-1的TGF-β1,使其终浓度为10 μg·L-1,对照组转染scrambled-RNAi并加入相同量的TGF-β1,转染组转染TRPV4-siRNA并加入相同量的TGF-β1。以Opti-MEM 和脂质体转染,脂质体与siRNA量均为5 μL,siRNA 终浓度为100 pmol·L-1,置于 37℃、5% CO2培养箱转染6 h后,正常组加入完全培养基,其余每组加入含TGF-β1的完全培养基,继续培养48 h,收获细胞,实验重复3次。
2.6 Western blot提取组织、细胞总蛋白,进行12% SDS-PAGE电泳,0.45 μm PVDF膜转移,一抗4 ℃孵育过夜,再与辣根过氧化物酶偶联二抗室温孵育1 h,ECL 显色。成像结果应用Image J 软件分析,通过分析α-SMA、TRPV4、p-Akt、Akt、β-actin的灰度值,计算各蛋白的含量变化是否具有统计学意义,实验重复3次。
2.7 统计学处理采用SPSS 13.0 软件进行统计分析,数据以x±s表示。两组间比较采用t检验,多组间比较采用单因素方差分析。
3 结果 3.1 大鼠肝纤维化模型建立以CCl4诱导大鼠肝纤维化,观察血清HA、LN、CⅣ及肝组织匀浆中Hyp表达变化,结果发现(Tab1、Tab2),与正常组相比,模型组血清HA、LN、CⅣ明显增加(P<0.01),肝组织匀浆中Hyp亦明显增加(P<0.01)。 HE 染色显示(Fig1),正常组大鼠肝细胞完整,肝组织无异常纤维增生;模型组可见肝小叶结构破坏,成纤维细胞出现,假小叶形成,肝组织中有明显炎性细胞浸润。Masson 染色结果显示,正常大鼠肝细胞完整,无纤维组织增生;模型组大鼠有较多的成纤维细胞出现,纤维结缔组织增生,肝索排列紊乱并伴有假小叶形成。提示大鼠肝纤维化模型建立成功。
| Group | HA/μg·L-1 | LN/μg·L-1 | CⅣ/μg·L-1 |
| Normal | 53.63±14.23 | 107.52±21.12 | 51.42±12.42 |
| Model | 326.48±71.36** | 153.84±34.26** | 106.43±24.16** |
| **P<0.01 vs normal group | |||
| Group | Hyp/μg·g-1 |
| Normal | 121±18.34 |
| Model | 376±34.21** |
| **P<0.01 vs normal | |

|
| Fig.1 Pathological observation of experimental rat liver sections stained with hematoxylin and eosin(HE) staining and Masson staining(×200) |
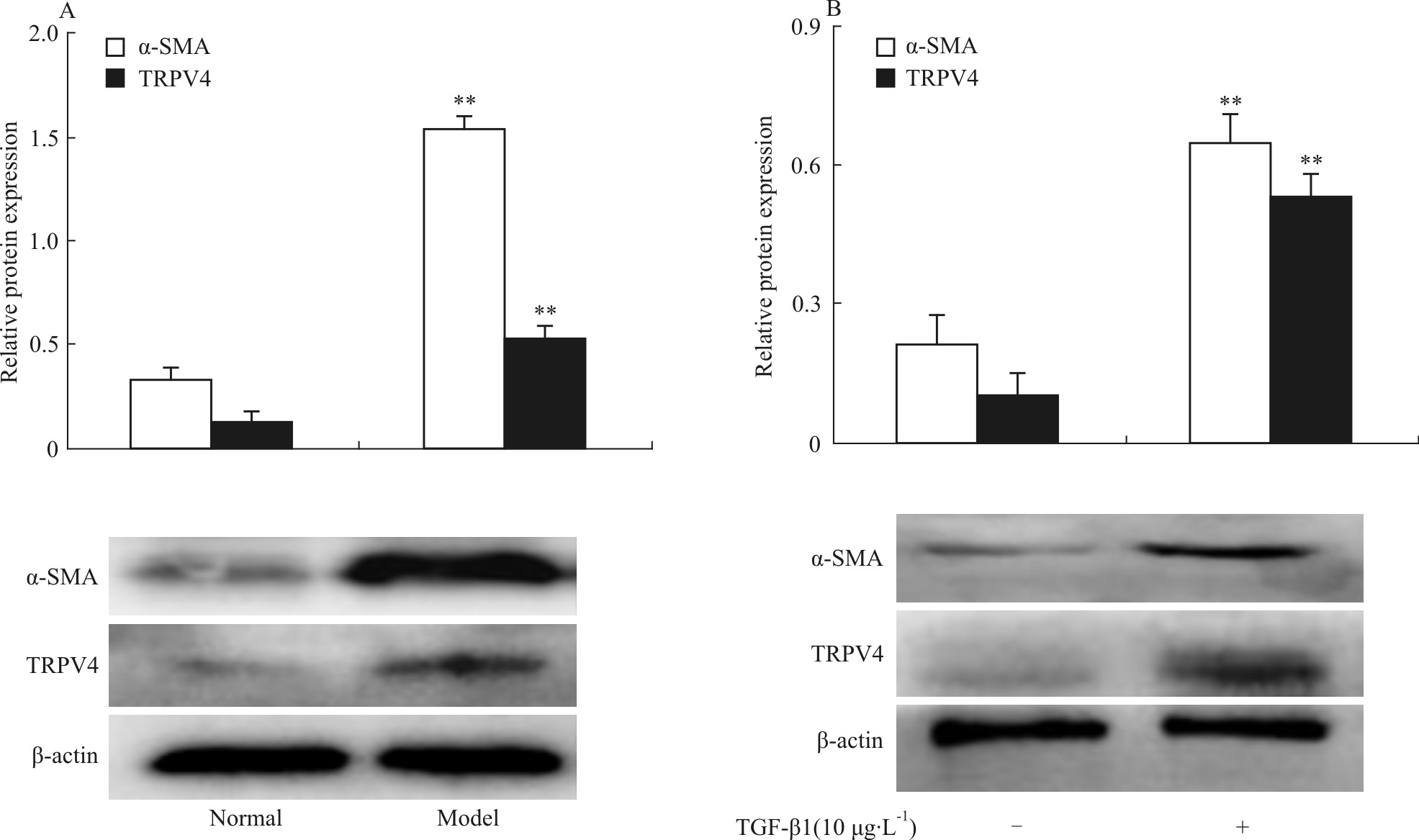
进一步观察TRPV4的表达变化。Western blot 检测发现(Fig2A),与正常组相比,模型组大鼠肝组织α-SMA、TRPV4蛋白表达明显增加(P<0.01)。进一步以TGF-β1(10 μg·L-1)刺激HSC-T6细胞株,亦发现TGF-β1可明显促进α-SMA、TRPV4蛋白表达(Fig2B)。提示肝纤维化HSC活化增殖过程中,TRPV4表达增高。
|
| Fig.2 Up-regulation of TRPV4 and α-SMA in CCl4-treated rats and TGF-β1-treated HSC-T6 cells A:Whole-cell extracts were isolated from the liver tissues of CCl4-treated rats or vehicle-treated group,and subjected to immunoblot for TRPV4,α-SMA and β-actin. Representative images of three independent experiments are shown. **P<0.01 vs vehicle control;B:Whole-cell extracts were isolated from TGF-β1-treated HSC-T6 cells,and subjected to Western blot analysis with TRPV4,α-SMA and β-actin antibodies. Representative blots of three independent experiments are shown. **P<0.01 vs non-treated cells. |
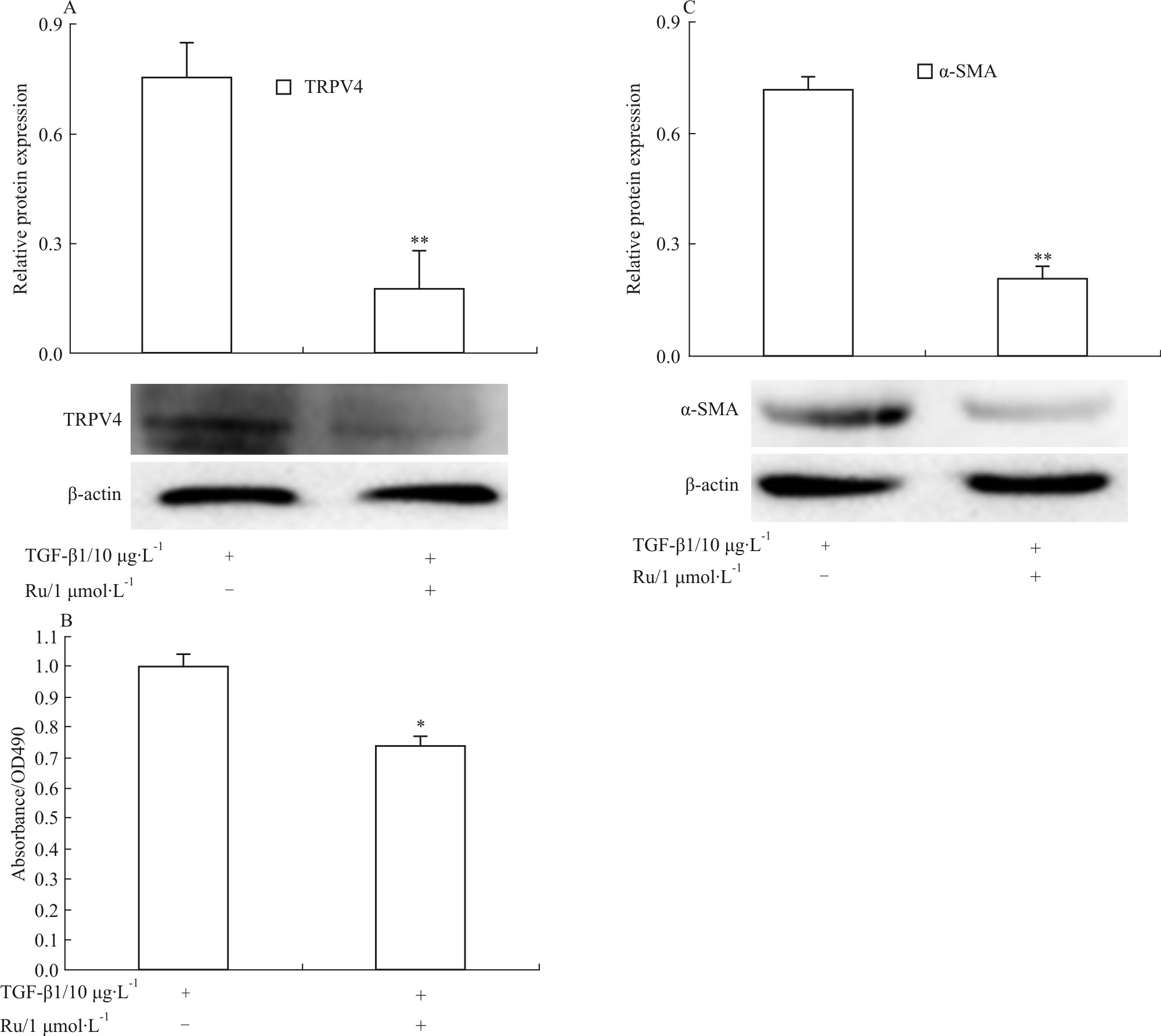
为观察TRPV4对HSC活化增殖的影响,应用TRPV4非特异性抑制剂钌红(Ru 1 μmol·L-1) 作用于TGF-β1刺激的HSC-T6细胞,24 h后,Western blot结果发现(Fig3A),与TGF-β1(10 μg·L-1)刺激的
|
| Fig.3 Ru prevented the proliferation and activation of HSC-T6 cells in vitro A:Whole-cell protein extracts were made from HSC-T6 cells treated with or without TGF-β1 and Ru,and subjected to Western blot analysis of TRPV4. Representative images of three independent experiments are shown;B:HSC-T6 cells were seeded in triplicate on day 0 and incubated in DMEM containing 10% fetal bovine serum or same media supplemented with Ru for further 24 h. Proliferation was measured by adding 5 g·L-1 MTT reagent per well and incubating it for 4 h; C:Whole-cell protein extracts were made from HSC-T6 cells treated with or without TGF-β1 and Ru,and subjected to Western blot analysis of α-SMA. Representative images of three independent experiments are shown. *P<0.05,**P<0.01 vs TGF-β1-treated cells. |
HSC-T6细胞比较,经钌红处理后,TRPV4蛋白水平明显下调,差异有统计学意义。MTT及Western blot结果亦发现,与TGF-β1(10 μg·L-1)刺激的HSC-T6细胞比较,钌红可明显抑制TGF-β1(10 μg·L-1)刺激的HSC-T6细胞株增殖及α-SMA的蛋白表达。提示TRPV4可能参与肝纤维化HSC活化增殖的过程(Fig3B、3C)。
3.4 沉默TRPV4抑制HSC活化增殖为了进一步研究TRPV4对HSC活化增殖的影响,应用TRPV4-siRNA特异性沉默TRPV4。转染特异性TRPV4-siRNA 48 h后,Western blot结果发现,与阴性对照组相比,转染组TRPV4蛋白表达明显降低(P<0.01),差异有统计学意义(Fig4A)。MTT及Western blot实验结果显示,与阴性对照组相比,转染组HSC-T6细胞的增殖明显受到抑制,α-SMA蛋白水平明显下调,差异有统计学意义(Fig4B、4C)。提示TRPV4参与肝纤维化HSC活化增殖的过程。

|
| Fig.4 TRPV4-siRNA inhibited HSC-T6 proliferation and α-SMA expression A:Whole-cell protein extracts were made from HSC-T6 cells treated with or without TGF-β1 and TRPV4 siRNA,and subjected to Western blot analysis of TRPV4. Representative images of three independent experiments are shown;B:HSC-T6 cells were seeded in triplicate on day 0 and incubated in DMEM containing 10% fetal bovine serum or same media supplemented with TRPV4 siRNA for further 24 h. Proliferation was measured by adding 5 g·L-1 MTT reagent per well and incubating it for 4 h; C:Whole-cell protein extracts were made from HSC-T6 cells treated with or without TGF-β1 and TRPV4 siRNA,and subjected to Western blot analysis of α-SMA. Representative images of three independent experiments are shown. *P<0.05,**P<0.01 vs non-treated cells; #P<0.05,##P<0.01 vs scrambled siRNA -treated cells. |
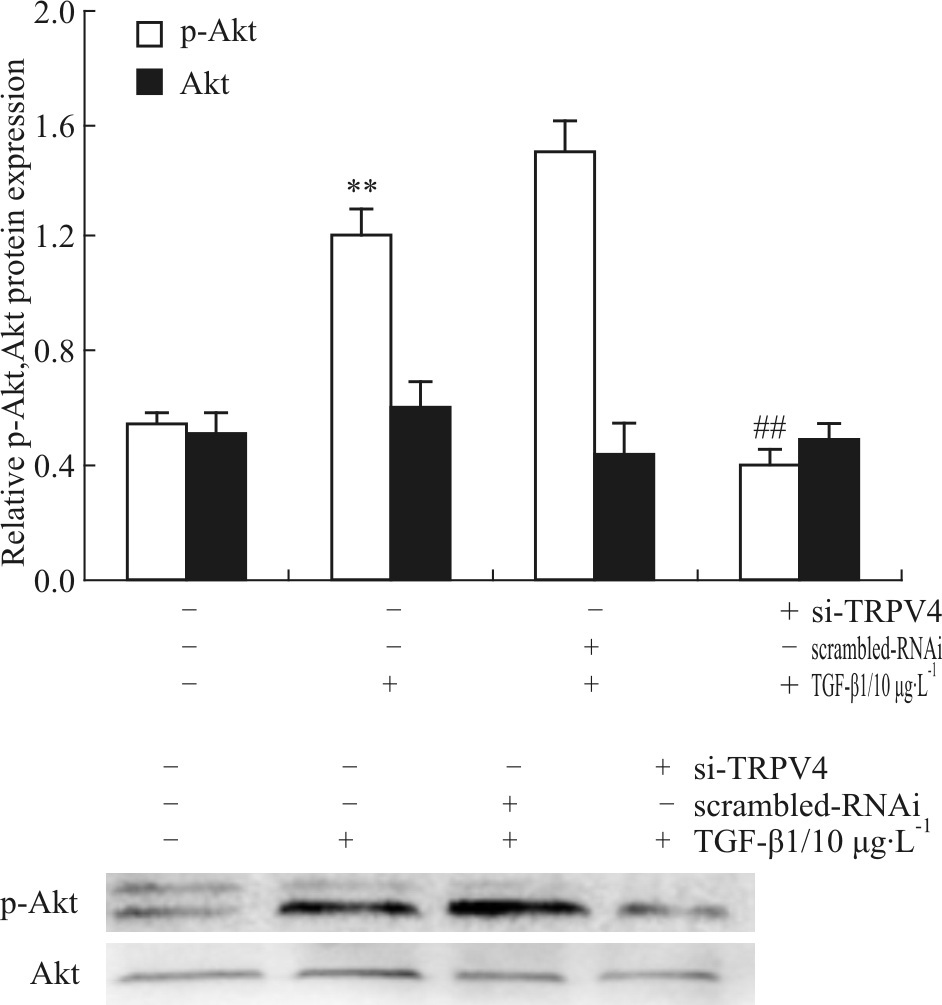
研究证实,Akt通路在肝纤维化过程中发挥着重要的作用[5, 6]。如Fig5所示,应用TRPV4-siRNA特异沉默TRPV4,可明显抑制p-Akt的表达,与对照组相比差异有统计学意义(P<0.01)。此结果提示TRPV4可抑制p-Akt的蛋白表达。
4 讨论肝纤维化是慢性肝病共有的病理过程,其持续发展可形成肝硬化、甚至肝细胞癌。深入研究肝纤维化发病机制,可能为慢性肝病的防治提供新的思路。HSC的活化、增殖,平滑肌肌动蛋白(α-SMA)表达增加,合成和分泌ECM增多是肝纤维化发生、发展的中心环节[7]。因此,抑制HSC活化、增殖和细胞外基质的形成是治疗肝纤维化的重要策略之一。TGF-β1作为TGF-β超家族中的重要成员之一,是致肝纤维化发生发展主要的细胞因子之一[8]。本实验研究亦发现,以浓度为10 μg·L-1的TGF-β1刺激HSC-T6细胞株,α-SMA表达明显升高;同时,MTT实验显示,TGF-β1刺激HSC-T6细胞株能明显促进HSC-T6细胞的增殖。
Di Sario等[9]报道,选择性的Na/H+泵(NHE)抑制剂cariporide可明显抑制在体及离体状态下 PDGF 诱导的大鼠 HSC 增殖。实验室前期研究发现,抑制瞬时受体电位 M7 通道(transient receptor potential melastatin 7,TRPM7)可抑制MRC5、HSC-T6细胞株活化增殖,促进其凋亡,上述研究提示,离子通道功能的改变影响细胞的增殖、凋亡等生理功能[2, 3, 10, 11, 12]。瞬时受体电位通道是位于细胞膜上的一类重要的阳离子通道,TRPV为TRP家族中的一个亚家族。研究发现,TRPV家族成员TRPV4不仅参与炎症和神经性疼痛的痛觉调控,感知热知觉,并且可调节细胞的生长、死亡等生理作用,具有重要的临床和药理学研究价值。但TRPV4在肝纤维化中的作用还不明确。我们研究发现,CCl4诱导大鼠肝纤维化模型中,大鼠肝纤维化组织中TRPV4表达明显升高。进一步以HSC-T6为研究对象,以转化生长因子-β1(TGF-β1)诱导其活化,结果亦证实,HSC中存在TRPV4的表达,并且活化的HSC中,TRPV4表达明显升高。应用TRPV4阻断剂钌红作用于HSC-T6,实验发现,钌红可明显抑制TGF-β1诱导的HSC-T6增殖,并且HSC活化的特异标志物α-SMA的蛋白表达亦明显降低。提示TRPV4可能参与了HSC活化增殖。进一步应用TRPV4-siRNA特异性沉默TRPV4,结果发现,特异性沉默TRPV4可明显抑制TGF-β1诱导的HSC-T6增殖与α-SMA的表达。上述的实验表明,TRPV4蛋白具有调控HSC活化增殖的功能。
|
| Fig.5 TRPV4-siRNA decreased p-Akt expression Whole-cell protein extracts were made from HSC-T6 cells treated with or without TGF-β1 and TRPV4 siRNA,and subjected to Western blot analysis of Akt and p-Akt. Representative images of three independent experiments are shown. **P<0.01 vs non-treated cells; ##P<0.01 vs scrambled siRNA -treated cells. |
文献及实验室前期研究发现,Akt信号通路在维持细胞存活、增殖过程中具有关键性作用[5, 6, 13],可调控HSC活化增殖。前期实验发现,TRP家族成员,TRPM7可以通过Akt通路抑制HSC增殖、促进其凋亡。作为TRP家族成员TRPV4是否调控Akt信号通路,还未见文献报道。本实验研究发现,TGF-β1诱导的HSC-T6中p-Akt表达明显升高,TRPV4-siRNA特异沉默TRPV4可明显降低p-Akt的蛋白表达,表明TRPV4调控p-Akt的蛋白表达。
综上所述,TRPV4作为阳离子通道蛋白,在HSC活化增殖过程中具有重要作用,阻断其表达可抑制HSC活化增殖。并且阻断TRPV4可抑制p-Akt蛋白表达。本实验为研究离子通道蛋白在肝纤维化中的作用提供了实验参考。
| [1] | Pellicoro A,Ramachandran P,Iredale J P,et al. Liver fibrosis and repair: immune regulation of wound healing in a solid organ[J]. Nat Rev Immunol,2014,14(3): 181-94. |
| [2] | Fang L,Zhan S,Huang C,et al. TRPM7 channel regulates PDGF-BB-induced proliferation of hepatic stellate cells via PI3K and ERK pathways[J]. Toxicol Appl Pharmacol,2013,272(3): 713-25. |
| [3] | Liu H,Li J,Huang Y,et al. Inhibition of transient receptor potential melastain 7 channel increases HSCs apoptosis induced by TRAIL[J].Life Sci,2012,90(15-16): 612-8. |
| [4] | Fernandes J,Lorenzo I M,Andrade Y N,et al. Valverde IP3 sensitizes TRPV4 channel to the mechano-and osmotransducing messenger 5′-6′-epoxyeicosatrienoic acid[J]. J Gen Physiol,2008,131(5): i2. |
| [5] | 黄 成,李 俊,马陶陶.PI3K/Akt 信号通路与肝纤维化[J].中国药理学通报,2011,27(8):1037-41. Huang C,Li J,Ma T T.PI3K/Akt signaling pathway and liver fibrosis[J].Chin Pharmacol Bull,2011,27(8):1037-41. |
| [6] | Bian E B,Huang C,Ma T T,et al. DNMT1-mediated PTEN hypermethylation confers hepatic stellate cell activation and liver fibrogenesis in rats[J]. Toxicol Appl Pharmacol,2012,264(1):13-22. |
| [7] | Puche J E,Saiman Y,Friedman S L. Hepatic stellate cells and liver fibrosis[J]. Compr Physiol, 2013,3(4): 1473-92. |
| [8] | Zhang L,Liu C,Meng X M,et al. Smad2 protects against TGF-beta1/Smad3-mediated collagen synthesis in human hepatic stellate cells during hepatic fibrosis[J]. Mol Cell Biochem,2015,400(1-2): 17-28. |
| [9] | Di Sario A,Bendia E,Taffetani S,et al. Benedetti selective Na+/H+ exchange inhibition by cariporide reduces liver fibrosis in the rat[J]. Hepatology,2003,37(2): 256-66. |
| [10] | Yu M,Huang C,Huang Y,et al. Inhibition of TRPM7 channels prevents proliferation and differentiation of human lung fibroblasts[J]. Inflamm Res,2013,62(11): 961-70. |
| [11] | Li X,Wang X,Wang Y,et al. Inhibition of transient receptor potential melastatin 7(TRPM7) channel induces RA FLSs apoptosis through endoplasmic reticulum(ER) stress[J]. Clin Rheumatol,2014,33(11): 1565-74. |
| [12] | Wu B M,Wang X H,Zhao B,et al. Electrophysiology properties of voltage-gated potassium channels in rat peritoneal macrophages[J]. Int J Clin Exp Med,2013,6(3):166-73. |
| [13] | Zhang H,Zhao B,Huang C,et al. Melittin restores PTEN expression by down-regulating HDAC2 in human hepatocelluar carcinoma HepG2 cells[J]. PLoS One,2014,9(5): e95520. |

