


2.广州医科大学药学院,广东 广州 511436
2.School of Pharmaceutical Sciences, Guangzhou Medical University, Guangzhou 511436, China
Hedgehog信号家族在早期胚胎的发育及分化,特别是中胚层的分化中具有极为重要的作用[1],并且参与细胞及组织的生理与病理的发育过程[2]。在对果蝇的基因突变进行筛查的时候,Nusslein-Vollhard和Wieschaus于1980年发现了Hedgehog基因及Patched基因。经典的Hedgehog抑制剂cyclopamine的发现,以及研究发现类固醇生物碱信号通路激活的作用方式是通过阻断Smo受体的功能来实现的,也使得近年来Hedgehog信号通路的研究成为一股新的热潮。Hedgehog家族有3个分支:Shh、Ihh、Dhh,其中,Ihh表达于内脏及软骨细胞[3, 4],Dhh表达于间质细胞[5],而Shh广泛表达于很多发育过程中,是最具典型特征的一个分支[6]。因此,我们选择Shh分支作为研究切入点。Shh信号通路在很多器官可以促进血管再生发挥组织修复作用[7, 8],在成人的心血管系统里,Shh主要参与动脉血管的形成并且促进血管再生[9]。Shh的膜受体蛋白Ptch-1/Smo已经被认知,Ptch是Hedgehog的结合蛋白,Smo是调控蛋白,在Shh信号通路未被激活的时候,Ptch抑制Smo的表达。两者起着拮抗共生的作用,这种拮抗共生的现象被称为刺猬现象,英文Hedgehog syndrome,在蛋白通路里也是少有的拮抗共生的通路,于是沿用了“刺猬”这个名词,取名为“刺猬通路”[10]。研究表明,Shh可以激活内在的细胞内通路, 与经典的心肌缺血/再灌(IR)保护作用相关[11],但与心肌梗死的关系尚未明确。
研究表明,Shh能够促进血管再生,改善血流灌注,这些表现在肌肉组织Shh及上调的下游基因十分明显,同时伴有Ang-1及VEGF等促进血管生成的表达。Shh的信号转导主要涉及几种重要的信号分子:① Shh在消化道、神经系统等组织是以分泌型蛋白的存在起作用;② 有跨膜区结构的跨膜蛋白受体patched(Ptch-1);③ Smoothened(Smo)在信号传导的通路中十分重要;④ Gli-1的锌指结构可调节促进血管生长的目的基因。信号转导途径一般为:Shh下调时,Smo和Ptch-1结合,Gli-1被抑制;Shh上调时,Ptch-1与Shh结合,Smo被激活并且呈游离状态,Gli-1成为激活因子,参与转录DNA结合诱导目的基因。Ptch-1、Gli-1的表达说明了Sonic Hedgehog信号通路的活性程度。本研究旨在通过缺血缺氧模型,观察Hedgehog信号通路在激活情况下,对心脏组织及细胞的保护作用。
1 材料与方法 1.1 左前降支心肌梗死模型的建立SPF级♀ SD大鼠200~250 g 24只(中山大学动物实验中心),分为正常组(6只)、心肌梗死组(6只)、心肌梗死+Shh激动剂组(6)、心肌梗死+Shh拮抗剂组(6只)。
10%多聚甲醛(0.3 mL/100 g)腹腔注射麻醉,气管插管,接呼吸机(DW-3000B,安徽淮华),呼吸频率90次/分钟,潮气量8~10 mL, 呼吸比为1 ∶1。剔除胸部毛发及消毒后,在左侧胸部第3、4肋间钝性分离组织,感到突破感后迅速放入开胸器,在左心耳及肺动脉圆锥中1/3进针,用6-0棉线行外科结扎,见心室前壁跳动减缓,1 min之后会见到左室前壁苍白,部分出现室性心律失常,无需特别处理,关胸,成半卧位侧卧放于37 ℃热毯上。
1.2 超声心动图测定LAD结扎术大鼠14d后行超声心动图。经乙醚吸入麻醉,卧位固定,取胸骨旁短轴为切面,M型超声记录左室收缩末内径、左室舒张末内径、左室短轴缩短分数、左室收缩期前壁及后壁厚度、左室舒张期前壁及后壁厚度。左室射血分数(EF)<50%来确认心肌梗死模型是否成功。
1.3 心肌组织的病理形态学常规HE及Masson染色后,可见心肌组织在显微镜下呈现区域性变性变化,病变区肌纤维排列紊乱,细胞核固缩破裂,肌丝断裂溶解,有炎性细胞浸润,存活的心肌细胞呈岛样分布,周围可见纤维组织生成,坏死的心肌被纤维组织替代。
1.4 H9C2细胞培养及缺血缺氧模型的构建H9C2细胞(广东省人民医院医学研究中心),37 ℃温浴,铺6孔板上,10% FBS+DMEM,细胞生长至融合80%时,注入30% H2O2 30 μL·mL-1培养基。12 h后,观察到培养基颜色为黄色清亮液体,并且,相比对照组,失去一半细胞,细胞壁边缘不规整,并用CCK-8试剂盒加以确认,免疫荧光染色,取10个视野,数细胞核数目,取平均值,可见细胞核较正常组减少40%~50%。
1.5 缺血缺氧的H9C2的Hedgehog信号在缺血缺氧的H9C2细胞中分别加入Shh激动剂(Purmorphamine,No.S3042 Selleck)和抑制剂(Cyclopamine,No.s1146 Selleck),作用24 h,免疫荧光及Western blot 观察Hedgehog通路的(Shh、Gli-1、Smo、Ptch-1)的表达。
1.6 Western blot检测组织研磨至看不见颗粒,6孔板中细胞用细胞刮刀进行冰上刮取,并加入RIPA+蛋白酶抑制剂,置于EP管中,12 000 r·min-1 4℃离心,15 min,取上清液,BCA法测定蛋白浓度,加入loading buffer制备蛋白样品,加热10 min,立即上样配好的胶上,80 V电泳90 min,300 mA电转60 min转膜。分别敷育一抗(Shh、Ptch、Smo、Gli-1)(Gli-1,ab151796 Abcam;Sonic Hedgehog,NBP1-47966 NOVUS;Ptch,NB100-91923 NOVUS;Smoothened,ab113438 Abcam)4℃过夜,TBXT洗膜3次,每次10 min,孵育二抗(Anti-rabbit IgG,ab9721 Abcam;或者Anti-mouse IgG ab6728 Abcam ),TBXT洗膜。ECL法曝光,将A液及B液1 ∶1比例混匀,自动曝光仪曝光。
1.7 免疫荧光检测组织和处理后细胞,阴干,组织用多聚赖氨酸包被,加入4% PFA 30 min,PBS+1% BSA洗后加入5% BSA封闭120 min,依次加入一抗孵育4℃过夜,二抗孵育60 min,DAPI 10 min,封片。在荧光显微镜下观察心梗区组织及H9C2细胞的荧光表达,取10个视野,取平均值。试剂同上。
1.8 统计学方法采用SPSS 20.0软件进行统计学分析。采用单因素方差分析(One-way ANOVA)考虑到每组6个样本为小样本,故采用one-way ANOVA比较总体,两两比较采用未假定方差齐性的Dunnett′s T3检验。
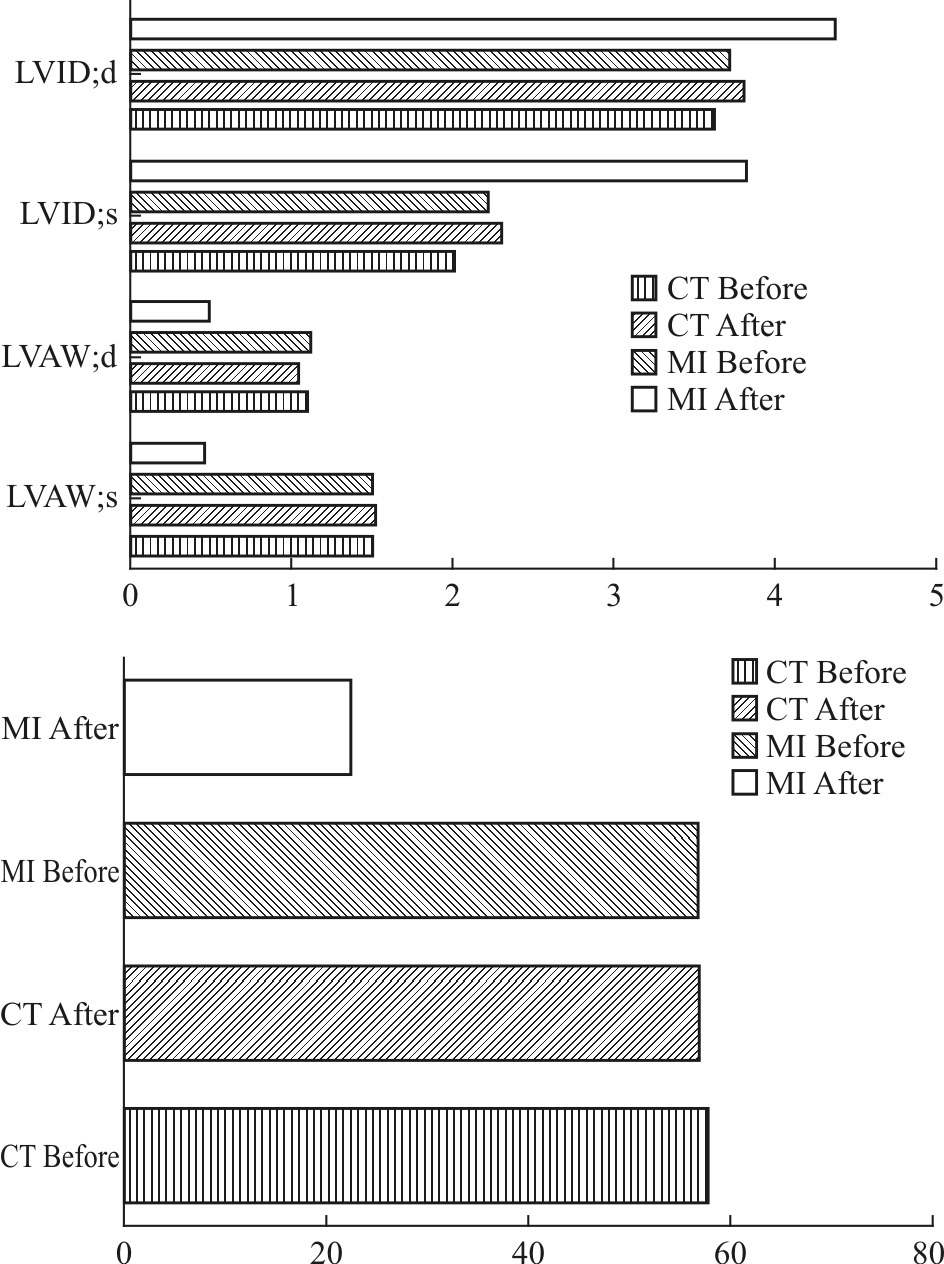
2 结果 2.1 心肌梗死超声图及指标超声心动结果提示,结扎左前降支4周后,LVID和LVAW出现明显下降,而对照组无明显变化。同时,EF结果提示结扎左前降支后出现明显下调,与对照组比较差异明显(Fig1、Fig2)。

|
| Fig.1 Echocardiogram of myocardial infarction |
|
| Fig.2 Changes in myocardial index in normal myocardium(CT) and myocardial infarction (MI) before and after modeling |
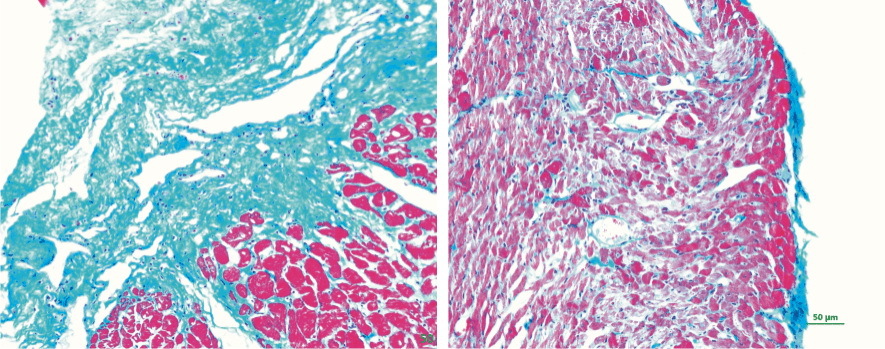
采用HE和Masson染色提示,实验组结扎左前降支后,病变区肌纤维排列紊乱,细胞核固缩破裂,肌丝断裂溶解,有炎性细胞浸润,存活的心肌细胞呈岛样分布,周围可见纤维组织生成,坏死的心肌被纤维组织替代。而对照组心肌细胞分布均匀,肌纤维排列整齐,无明显炎症浸润(Fig3、Fig4)。

|
| Fig.3 HE staning of normal hearts (left) and hearts with myocardial infarction (right) |
|
| Fig.4 Masson staining of normal hearts (left) and hearts with myocardial infarction (right) |
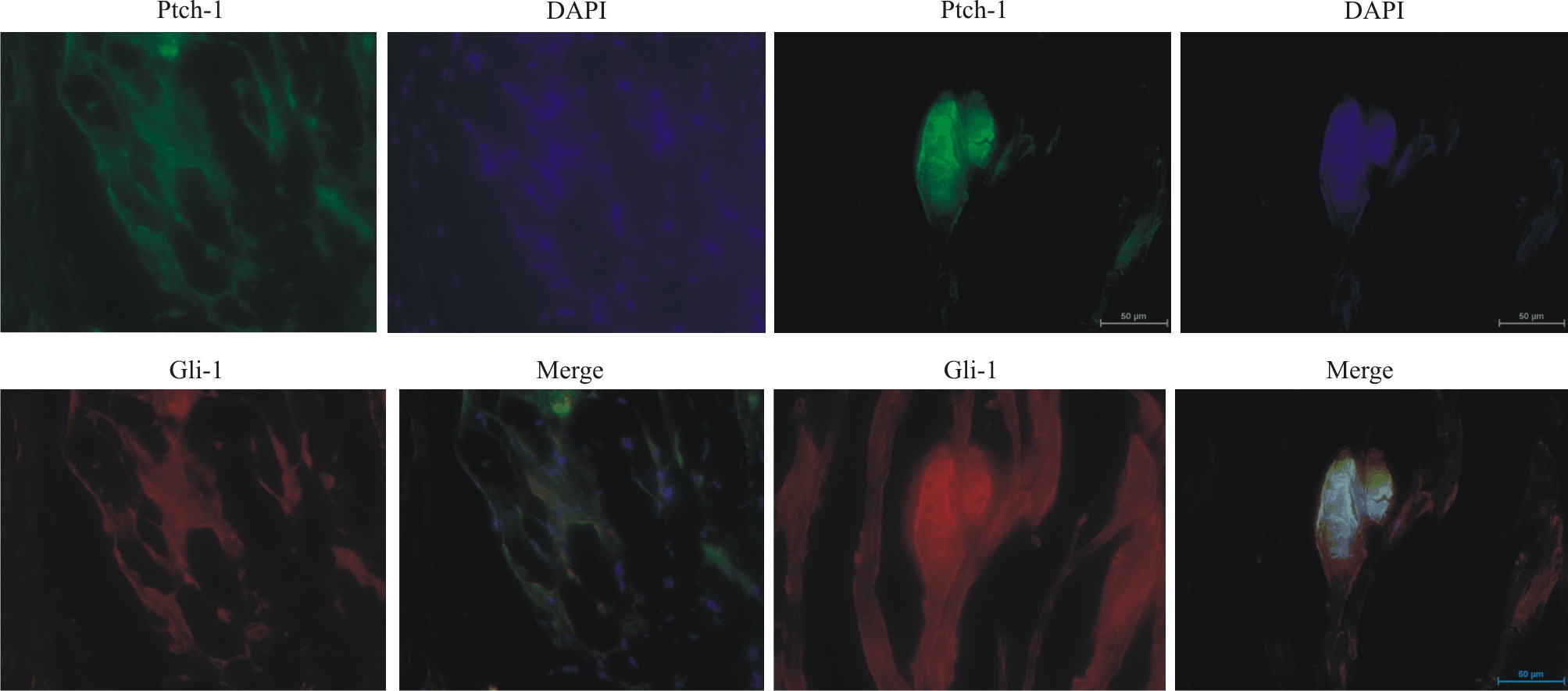
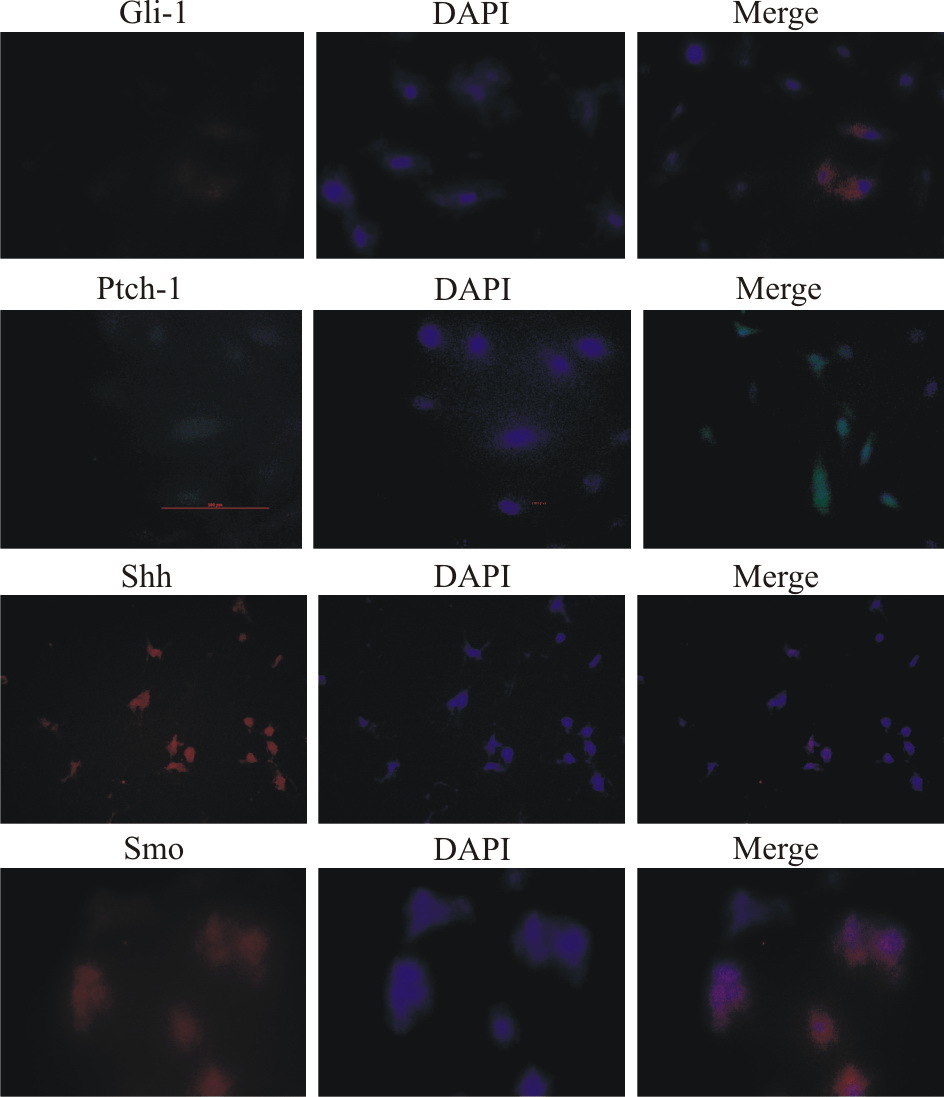
免疫荧光检测提示,Ptch-1和Gli-1在正常心脏及心肌梗死中均有表达。H9C2在Shh激动剂和H2O2作用下,Hedgehog信号增强;而在Shh抑制剂和H2O2作用下,Hedgehog信号减弱(Fig5、Fig6、Fig7、Fig8)。
|
| Fig.5 Protein expression of Gli-1, Ptch-1 in normal myocardia (left) and myocardial infarction (right) tissues |

|
| Fig.6 Hedegehog pathway of cyclopamine+H2O2+H9C2 |
|
| Fig.7 Hedgehog pathway of purmorphamine+H2O2+H9C2 |
|
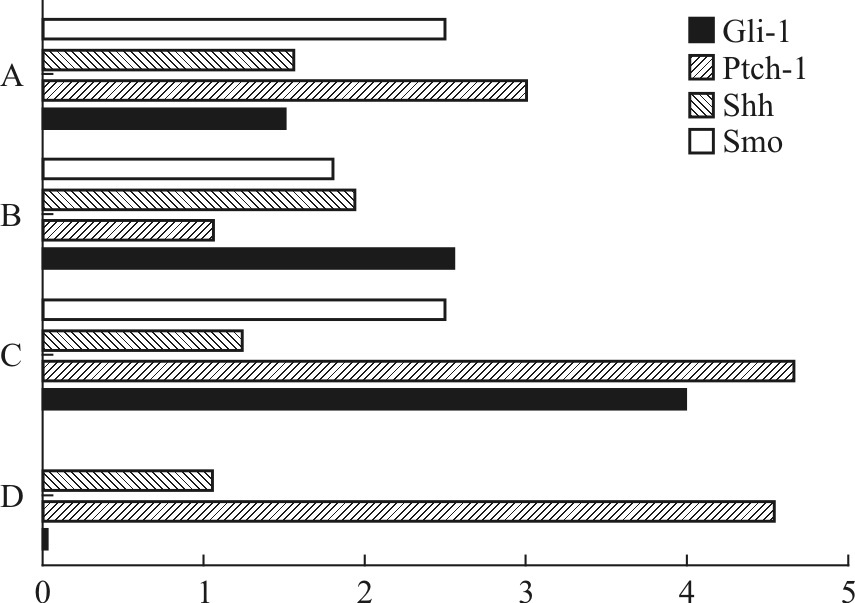
| Fig.8 Immunofluorescence of Shh pathway expressions of H2O2 induced H9C2 cells A:H2O2+H9C2+Purmorphamine;B:H2O2+H9C2+Cyclopamine;C:H2O2+H9C2;D:Control |
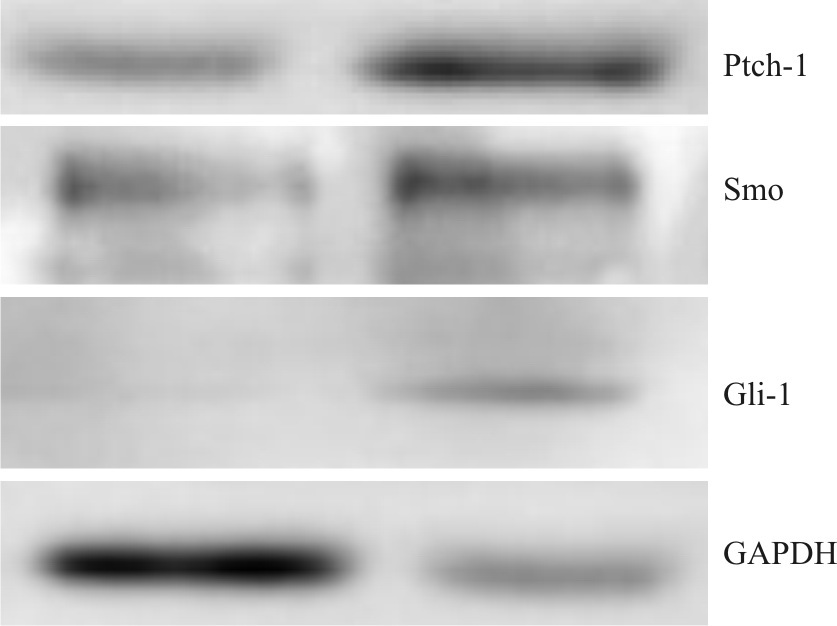
Gli-1、Shh在正常心脏及H9C2不表达,Ptch-1、Smo在正常及心肌梗死组均有表达,未处理H9C2的Ptch-1、Smo均表达,抑制剂处理的缺血缺氧H9C2的Gli-1、Shh表达低于同期PBS组H9C2,激动剂处理的缺血缺氧H9C2的Gli-1、Shh表达高于同期PBS组H9C2。显示Shh通路能够对缺血缺氧性损伤起着保护作用(Fig8、Fig9)。
|
| Fig.9 Westeren blot result of normal myocardium (left) and myocardial infarction (right) tissues |
研究表明,成年心脏组织存在Hedgehog信号通路,心肌梗死后的Shh通路能够保护心肌损伤及细胞损伤,这也说明了Shh通路在人胚胎发育和心肌生成中的重要作用。同时,我们研究也证明,在缺血缺氧的条件下,组织层面及细胞层面均显示该通路的激活,给予激动剂的作用下,该通路表达更为明显,减少了纤维化的发生和凋亡的作用,说明激活该通路在心肌梗死后的表达可以逆转心肌纤维化并且促进心肌组织新生。最近有报道,骨骼肌组织梗死之后也会发现明显的Shh mRNA和蛋白的上调[12, 13, 14]。
本研究的Western blot 和免疫荧光检测结果,说明了Ptch-1、Gli-1、Smo及Shh之间的相互作用关系符合经典的Hedgehog通路。在成年大鼠心脏组织,Shh、Ptch、Smo、Gli-1均不表达,在心梗组才发现表达,说明心脏的自我修复功能在正常情况下处于关闭状态,只有一定程度的刺激才被激活。在细胞层面上,哈佛的干细胞研究人员报道了肾脏的Sonic hedgehog 信号通路的激活,并且说明与干细胞再生的相关能力起着十分关键的作用[15]。本研究表明,细胞水平的正常组Gli-1、Shh、Ptch-1、Smo不表达,经过H2O2的诱导刺激作用,Gli-1、Shh、Ptch-1、Smo开始表达,与整体动物实验结果一致,说明在氧化应激的条件下该信号通路被激活,且具有促进心肌细胞的损伤修复作用。
有研究发现,Ptch-1既是Hedgehog的膜受体,又是Hedgehog的转录目的蛋白,所以它的表达既说明了Hedgehog信号的反应性,又说明了Hedgehog通路的激活[15]。当Smo功能发生获得性的改变,或者Ptch对其解除链接作用的时候,会引发整个Hedgehog信号通路的活化,这在本研究结果也表现明显。我们推测,如果在病损的心脏组织中抑制Smo信号通路的活化,可能是心脏组织治疗的一种新的思路。Gli-1 的上调能够调节目的基因的转录,并且最终导致Hedgehog通路对该细胞或是组织的修复作用。通过我们的实验,Gli-1在正常的心脏组织、正常的H9C2是不表达的,而心肌梗死组织及H2O2诱导的H9C2细胞中表达,提示氧化应激是Gli-1表达激活的一个重要诱发因素。
综上所述,Sonic Hedgehog信号通路不仅在胚胎的生长发育中起着至关重要的作用,而且在氧化应激条件下起着重要的维持稳态作用。有关该信号通路在心肌损伤与修复的作用地位以及潜在的治疗靶点,有待进一步深入研究。
(致谢:感谢广东省人民医院的林秋雄主任、单志新主任的点滴提醒,感谢李晓红、潘宇、孟锦秀、麦丽萍老师的指导,感谢肖静、杨翔宇的帮助。)
| [1] | Assmus B, Iwasaki M, Schachinger V, et al. Acute myocardial infarction activates progenitor cells and increases Wnt signalling in the bone marrow[J]. Eur Heart J, 2012, 33(15):1911-9. |
| [2] | Parmacek M S, Epstein J A. An epigenetic roadmap for cardiomyocyte differentiation[J]. Circ Res, 2013, 112(6):881-3. |
| [3] | Alrefai M T, Murali D, Paul A, et al. Cardiac tissue engineering and regeneration using cell-based therapy[J]. Stem Cells Cloning, 2015, 14(8):81-101. |
| [4] | Rassaf T, Totzeck M, Hendgen-Cotta U B, et al. Circulating nitrite contributes to cardioprotection by remote ischemic preconditioning[J]. Circ Res, 2014, 114(10):1601-10. |
| [5] | Bambakidis N C. Erratum: Improvement of neurological recovery and stimulation of neural progenitor cell proliferation by intrathecal administration of Sonic hedgehog[J]. J Neurosurg, 2013, 118(2):488. |
| [6] | Kawamura M, Miyagawa S, Miki K, et al. Feasibility, safety, and therapeutic efficacy of human induced pluripotent stem cell-derived cardiomyocyte sheets in a porcine ischemic cardiomyopathy model[J]. Circulation, 2012, 126(11 Suppl 1):S29-37. |
| [7] | Stoller M, de Marchi S F, Seiler C. Function of natural internal mammary-to-coronary artery bypasses and its effect on myocardial ischemia[J]. Circulation, 2014, 129(25):2645-52. |
| [8] | Singh B, Koyano-Nakagawa N, Donaldson A, et al. Hedgehog signaling during appendage development and regeneration[J]. Genes, 2015, 6(2):417-35. |
| [9] | Vukusic K, Jonsson M, Brantsing C, et al. High density sphere culture of adult cardiac cells increases the levels of cardiac and progenitor markers and shows signs of vasculogenesis[J]. Biol Med Res Int, 2013, 2013:1-11. |
| [10] | Xiao Q, Hou N, Wang Y P, et al. Impaired sonic hedgehog pathway contributes to cardiac dysfunction in type 1 diabetic mice with myocardial infarction[J]. Cardiovasc Res, 2012, 95(4):507-16. |
| [11] | 李峰杰, 李贻奎.心肌梗死动物模型研究进展[J]. 中国药理学通报, 2013, 29(1):5-10. Li F J, Li Y K. Research progress on animal myocardial infarction model[J]. Chin Pharmacol Bull, 2013, 29(1):5-10. |
| [12] | Huang J, Parmacek M S. Modulation of smooth muscle cell phenotype: the other side of the story[J]. Circ Res, 2012, 111(6):659-61. |
| [13] | Sreejit P, Verma R S. Natural ECM as biomaterial for scaffold based cardiac regeneration using adult bone marrow derived stem cells[J]. Stem Cell Rev Rep, 2013, 9(2):158-71. |
| [14] | Araszkiewicz A, Grygier M, Pyda M, et al. Postconditioning reduces enzymatic infarct size and improves microvascular reperfusion in patients with ST-segment elevation myocardial infarction[J]. Cardiology, 2014, 129(4):250-7. |
| [15] | Pan J Y, Zhou S H. The hedgehog signaling pathway, a new therapeutic target for treatment of ischemic heart disease[J]. Pharmazie, 2012, 67(6):475-81. |

