


2. 烟台大学生命科学学院,线粒体与健康衰老研究中心,山东 烟台 264005;
3. 兰州大学生命科学学院,甘肃 兰州 730000;
4. 中国科学院西北高原生物研究所,青海 西宁 810001
 , SI Ying-ying2, WANG Zhan-yang1, MI Xiang-quan3, LYU Huan-huan4, XU Bo2, LI Gang4, LI Ji2, HE Jie2, WANG Zhen-hua2
, SI Ying-ying2, WANG Zhan-yang1, MI Xiang-quan3, LYU Huan-huan4, XU Bo2, LI Gang4, LI Ji2, HE Jie2, WANG Zhen-hua2

2. Center of Mitochondrion and Healthy Aging, College of Life Sciences, Yantai University, Yantai Shandong 264005, China;
3. School of Life Sciences, Lanzhou University, Lanzhou 730000, China;
4.Northwest Institute of Plateau Biology, Chinese Academy of Sciences, Xining 810001, China
阿尔茨海默病(AD)是一种常见的中枢神经系统退行性疾病,其病理特征主要表现为淀粉样蛋白(β-amyloid, Aβ)沉积形成的老年斑、tau蛋白过度磷酸化导致的神经纤维缠结(neurofibrillary tangles, NFTs)以及神经元丢失和突触损伤。其中,NFTs主要由过度磷酸化的tau蛋白聚集形成配对螺旋状细丝(paired helical filament, PHF)组成[1],而tau蛋白在维持神经突触微管稳定(尤其是轴突)方面具有重要的作用。体外研究表明:tau蛋白的磷酸化程度直接影响神经元生长与成熟过程中微管的稳定性,一般新生体含有丰富的磷酸化tau,而随着神经元的成熟,主要通过下调蛋白激酶和上调磷酸酯酶从而降低tau的磷酸化水平[2];体内研究证明:tau主要通过调节脯氨酸依赖性的蛋白激酶,从而调节tau蛋白的磷酸化水平,例如细胞周期素依赖性激酶(CDK)、促分裂原激活蛋白激酶(MAPK)和糖原合成激酶(GSK-3β)[3, 4],目前开发多种激酶抑制剂,主要以降低tau蛋白磷酸化水平作为治疗AD的新药开发的新途径。
LiCl是发现的第一类tau蛋白激酶GSK-3β特异性抑制剂[5]。体内研究表明,LiCl可通过下调GSK-3β的表达,上调抗凋亡因子Bcl-2、神经营养因子,从而降低Aβ毒性和tau蛋白的磷酸化程度,因此具有神经保护作用;同时,LiCl能和镁竞争性与GSK-3β结合,亦可降低GSK-3β的活性[6, 7]。体外研究表明,LiCl可阻止过表达突变tau蛋白和GSK-3β转基因小鼠的tau蛋白的高度磷酸化,减少不溶性tau蛋白的形成[8, 9, 10]。
本研究以全反式维甲酸(ATRA)诱导SK-N-SH神经母细胞瘤再分化的成熟神经元为研究对象,考察了冈田酸(OA)致神经元突触萎缩和tau蛋白Ser-262位点磷酸化的作用,进一步观察了LiCl对OA神经毒性的保护作用,旨在为AD新药评价提供一个新的体外模型。
1 材料与方法 1.1 材料与试剂SK-N-SH细胞购自中国典型培养物保藏中心(CCTCC);DMEM培养基、胎牛血清(fetal bovine serum, FBS),美国Gibco公司;胰蛋白酶、Giemsa、LiCl、OA、ATRA均为Sigma产品;磺基罗丹明B,上海晶纯生化科技股份有限公司;兔抗synaptophysin、兔抗p-tau(Ser-262)、鼠抗tau5抗体,均购自Santa Cruz Biotechnology公司;辣根过氧化物酶标记抗体(二抗)及荧光剂,Santa Cruz Biotechology公司。
1.2 仪器与设备SpectraMax Paradigm型多功能酶标仪,美国美谷分子仪器有限公司;电泳仪,美国Bio-Rad公司;HC-3018R型高速冷冻离心机,安徽中科中佳科学仪器有限公司;倒置显微镜及照相系统,麦克奥迪实业集团有限公司;凝胶图像分析扫描仪,上海Tanon科技有限公司。
1.3 细胞培养及分组SK-N-SH细胞生长在含10%胎牛血清、100 kU·L-1青霉素和100 mg·L-1链霉素的DMEM培养基中,置于37℃、5% CO2饱合湿度的培养箱中培养传代。
LiCl储备液:用DMEM培养基溶解LiCl,配成浓度为1 mol·L-1的贮存液,-20℃保存备用。使用前以含1% FBS的DMEM培养液稀释,使LiCl的终浓度为0.1、1、10 mmol·L-1。
1.4 冈田酸复制分化SK-N-SH神经元损伤SK-N-SH细胞的诱导分化部分参考文献[11]已在本实验的前期研究中完成,并确定采用10 μmol·L-1ATRA可诱导SK-N-SH细胞分化为成熟的神经元细胞。将分化SK-N-SH细胞以1.5×107·L-1的密度接种于96孔板中,用10 μmol·L-1 ATRA诱导分化后,分别加入不同浓度OA,建立OA细胞损伤模型,继续培养48 h,通过Giemsa染色观察不同浓度的OA对SK-N-SH细胞的损伤情况,并采用Western blot检测p-tau262、tau5的蛋白表达。
1.5 SRB法测定LiCl对SK-N-SH分化成熟神经元活性的影响取ATRA诱导分化的SK-N-SH细胞,经不同浓度LiCl处理后,取出培养板,每孔加入50 μL 4℃预冷的三氯乙酸(TCA)溶液(30%, W/V)固定细胞,TCA的终浓度为10%,然后在4℃冰箱中放置1 h。各孔用去离子水洗涤5 遍,自然晾干后,每孔加入100 μL 0.4%的SRB溶液(1% 的乙酸配制),静置染色30 min后,倒掉染液,用1%乙酸洗涤5遍,去除未结合的染料,空气中干燥后用100 μL Tris碱液(10 mmol·L-1, pH=10.5)溶解,在微孔板振荡器上振荡20 min,多功能酶标仪在540 nm波长下测量各孔的吸光值。按下式计算药物对细胞增殖的抑制率:
抑制率/%=(对照组OD值-给药组OD值)/对照组OD值×100%
1.6 Giemsa染色观察SK-N-SH细胞形态变化取ATRA诱导分化的SK-N-SH细胞,接种于含盖玻片的6孔培养板中,待细胞贴附到盖玻片后,吸去培养液,分别加入不同浓度LiCl培养后,取出盖玻片,PBS洗涤2次,甲醇固定10 min,PBS洗涤2次,滴加Giemsa染液显色5 min,自然晾干,二甲苯透明,甘油封片;于显微镜下观察并拍照。光镜下观察细胞核呈紫红色或蓝紫色,细胞质呈粉红色。
1.7 Western blot检测synaptophysin、tau蛋白磷酸化水平取ATRA诱导分化的SK-N-SH细胞,经不同浓度LiCl及40 nmol·L-1 OA处理后。弃去培养基,用预冷PBS洗2遍,加入RIPA细胞裂解液,冰上裂解30 min,用细胞刮刀收集细胞,12 000×g离心30 min。取上清液,BCA法测定裂解液中的蛋白浓度。再加入4倍变性液,水浴锅中100℃、5 min煮沸。在12% SDS-PAGE胶进行电泳,将蛋白质转移到硝酸纤维素膜上,分别用synaptophysin抗体、抗磷酸化tau抗体(Ser262位点)和抗总tau蛋白抗体(tau5)与硝酸纤维素膜4℃孵育过夜,用TBST漂洗3次,与辣根过氧化物酶标记二抗(1 ∶5 000)室温孵育2 h,再用TBST漂洗3次后,用Tanon 5500凝胶成像系统拍照,并分析蛋白产物条带的相对光密度值。
1.8 统计学分析实验数据用±s表示,用SPSS 22.0统计学分析软件进行数据统计分析。以t检验进行组间统计学差异比较。
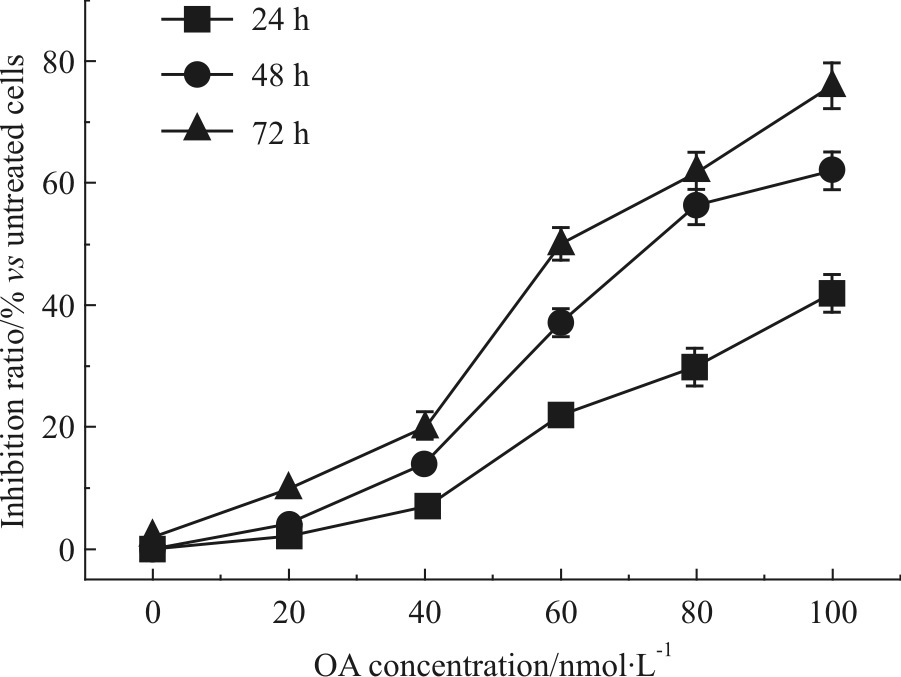
2 结果 2.1 OA对SK-N-SH细胞分化成熟神经元的毒性作用不同浓度OA处理经ATRA诱导分化的SK-N-SH细胞24、48、72 h,结果发现,40 nmol·L-1 OA处理48 h即表现出对SK-N-SH细胞增殖的抑制作用,随着OA浓度的增加,细胞的抑制作用明显增强,呈浓度依赖性(Fig1)。通过Giemsa染色观察发现,正常组(成熟的神经元细胞)铺展良好、轴突较长,且轴突长度为胞体长度3.3倍;而40 nmol·L-1 OA处理48 h的细胞贴壁不良,轴突长度仅为胞体的0.24倍,甚至出现轴突消失、胞体变圆,提示40 nmol·L-1 OA可引起成熟的神经元细胞突触的损伤(Fig2)。
|
| Fig.1 Effects of OA on proliferation of differentiated SK-N-SH neuroblastoma cells(n=3) |

|
| Fig.2 Morphological transformation induced by OA in differentiated SK-N-SH neuroblastoma cells(×200) Up:Observed after Giemsa stainning;Down: The measure of axon length.**P<0.01 vs control |
不同浓度LiCl处理诱导成熟的SK-N-SH细胞24、48、72 h,用SRB法检测LiCl的细胞毒性。如Fig3所示, 随着LiCl浓度的增加,可浓度依赖性地抑制细胞的增殖,随着LiCl作用时间的延长,可时间依赖性地抑制细胞的增殖,0.01 mmol·L-1 LiCl几乎无毒性,100 mmol·L-1 LiCl可明显抑制细胞的增殖。因此,本实验选0.1、1、10 mmol·L-1为LiCl的低、中、高浓度进行深入的研究。

|
| Fig.3 Effects of LiCl on proliferation of differentiated SK-N-SH neuroblastoma cells(n=3) |
诱导成熟的SK-N-SH细胞与终浓度0.1、1、10 mmol·L-1的LiCl孵育24 h,然后用40 nmol·L-1 OA处理48 h,最后采用Giemsa染色并显微镜下拍照观察。结果如Fig4和Fig5所示, 与模型组(40 nmol·L-1 OA处理)比较,10 mmol·L-1的LiCl预处理组的细胞铺展良好、轴突粗壮较长,细胞突触萎缩被明显抑制,细胞基本恢复正常形态(P﹤0.01)。同时采用Western blot方法分析LiCl对OA致SK-N-SH分化成熟神经元synaptophysin表达的影响,结果如Fig6所示,40 nmol·L-1OA处理组synaptophysin蛋白表达明显下降,与正常组相比差异有统计学意义(P﹤0.01);不同浓度的LiCl(0.1、1、10 mmol·L-1)预处理12 h后,synaptophysin蛋白水平均能升高,尤其当LiCl浓度为10 mmol·L-1时,synaptophysin的表达升高最明显,与模型组相比差异具有统计学意义(P﹤0.01)。综合形态学和蛋白表达表明LiCl对OA诱导的SK-N-SH细胞分化神经元损伤有一定的保护作用。

|
| Fig.4 Effects of LiCl on cell damage induced by okadaic acid in differentiated SK-N-SH neuroblastoma cells(×200) A:Control;B:OA 40 nmol·L-1;C:LiCl 0.1 mmol·L-1;D:LiCl 1 mmol·L-1;E:LiCl 10 mmol·L-1 |

|
| Fig.5 Effects of LiCl on synaptic damage induced by okadaic acid in differentiated SK-N-SH neuroblastoma cells **P<0.01 vs OA;##P<0.01 vs control |

|
| Fig.6 Effect of LiCl on synaptophysin protein induced by okadaic acid in differentiated SK-N-SH neuroblastoma cells(n=3) **P<0.01 vs OA;##P<0.01 vs control |
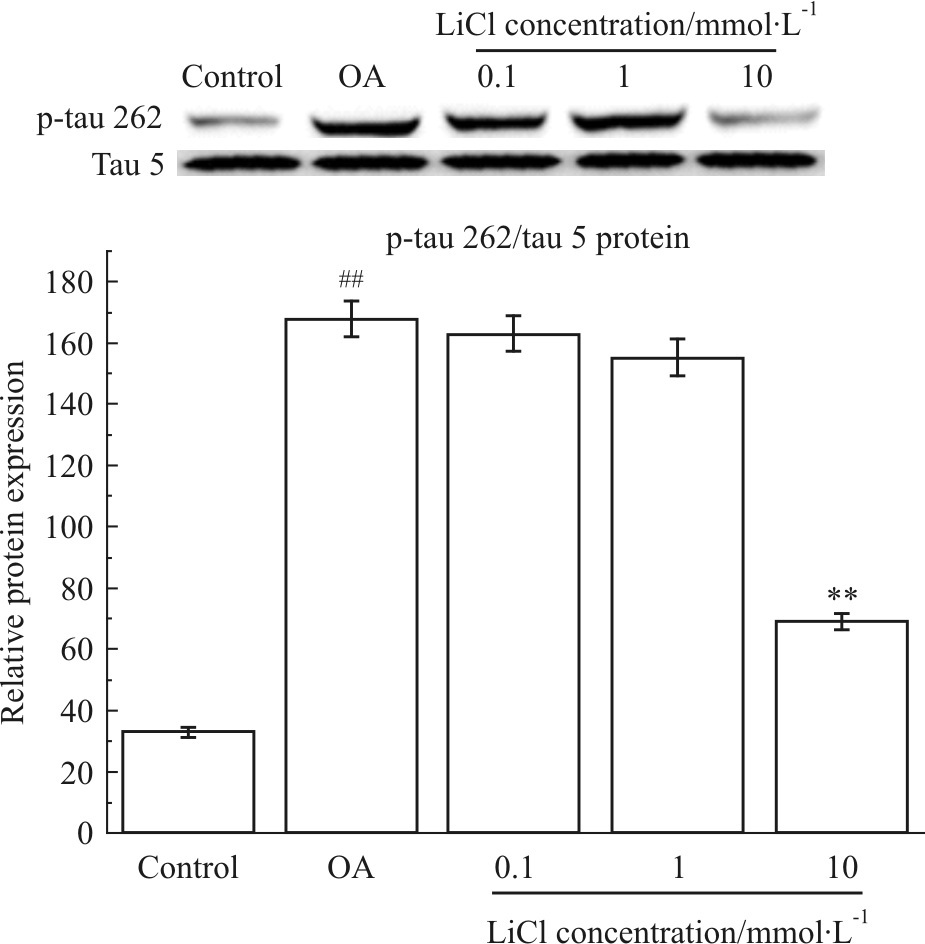
进一步采用Western blot方法检测LiCl对OA诱导的SK-N-SH分化成熟神经元p-tau/tau蛋白表达的影响。结果如Fig7所示, 40 nmol·L-1 OA处理组tau蛋白Ser-262磷酸化表达明显升高,而总的tau蛋白基本不变,与正常组相比差异有统计学意义(P<0.01);不同浓度的LiCl(0.1、1、10 mmol·L-1)预处理12 h后,tau蛋白Ser-262磷酸化水平均能降低,但当LiCl浓度为10 mmol·L-1时,p-tau262/tau5表达明显降低,与模型组相比差异具有统计学意义(P﹤0.01)。表明LiCl对OA诱导的SK-N-SH细胞分化神经元tau蛋白异常磷酸化有一定的保护作用。
|
| Fig.7 Effect of LiCl on phosphorylation of tau protein induced by okadaic acid in differentiated SK-N-SH neuroblastoma cells(n=3) **P<0.01 vs OA;##P<0.01 vs control |
阿尔茨海默病是一种最常见的神经退行性疾病,其主要的病理学改变是由p-tau组成的神经元纤维缠结,而tau蛋白的磷酸化状态受蛋白激酶和蛋白磷酯酶共同调节,当激酶活性升高,酯酶活性下降时,tau蛋白即会过度磷酸化,高度磷酸化的tau蛋白与微管分离,丧失了促进微管组装的生物活性,并隔离微管装配的正常tau蛋白,从而使微管解聚,出现轴突转运障碍,导致突触的萎缩。目前研究发现,GSK-3β是调控tau蛋白磷酸化中一种重要的蛋白激酶,而LiCl是GSK-3β蛋白激酶抑制剂,它可以阻止GSK-3β的促磷酸化作用,进而抑制tau蛋白的过磷酸化和突触萎缩,这为AD临床治疗提供新的思路[12]。
诱导分化是指恶性肿瘤在体内外分化诱导剂存在下,重新向正常方向分化的现象。本实验室前期的研究以高度恶性未分化的神经元性肿瘤细胞(SK-N-SH细胞)为研究对象,以ATRA为诱导分化剂,发现10 μmol·L-1 ATRA可诱导SK-N-SH细胞分化为成熟的神经元。分化后的神经元细胞向正常的神经元转变,形态上突触明显变长、synaptophysin蛋白表达明显升高,同时出现许多成熟神经元的生化和功能特性,因此能更好地用于AD中神经元突触萎缩模型的制备[11]。
冈田酸是一种海洋生物的提取物,可通过抑制蛋白磷酸酯酶PP1和PP2A的活性,从而使tau蛋白高度磷酸化[13]。有研究表明,OA可导致tau蛋白Ser199/202、Ser404、Ser396等位点的磷酸化,而本实验主要针对tau蛋白Ser-262位点的磷酸化进行考察。实验中选用40 nmol·L-1 OA建立AD细胞模型,结果表明,成熟的神经细胞与40 nmol·L-1 OA共同孵育后,细胞的轴突明显变短甚至消失,胞体变圆;进一步从Western blot的结果可得,用 40 nmol·L-1 OA处理成熟的神经细胞,tau蛋白Ser-262位点磷酸化水平明显升高(P﹤0.01),这与国内外的文献报导一致,由此提示,本实验使用OA诱导的AD细胞模型是可靠且有效的。同时tau蛋白的磷酸化受蛋白激酶和蛋白磷酸酶的动态调节,其中最主要的是蛋白磷酸酯酶PP2A和蛋白激酶GSK-3β。体内研究发现,在AD患者脑内GSK-3β与过度磷酸化的tau蛋白共定位、且胞质内GSK-3β含量较正常人明显升高;体外研究显示,GSK-3β不仅调控神经细胞的tau蛋白过度磷酸化,且对记忆的损害也起重要作用[14]。因此,通过抑制GSK-3β的活性,从而减轻tau蛋白磷酸化水平可能是一种防治AD的有效的手段。
在早期的临床研究中,LiCl作为精神稳定性药物广泛用于治疗双相感情障碍性疾病。近年来的研究发现LiCl不仅可以增加神经前祖细胞的增殖和分化,同时可减轻中度AD患者的认知功能障碍,对退行性疾病有一定的治疗作用。LiCl作为GSK-3β的抑制剂,体内的研究表明,LiCl能够明显抑制大鼠脑内tau蛋白Ser-199、Ser-396位点的磷酸化水平,改善tau蛋白的病变,减轻记忆功能的障碍。然而,针对神经元突触损伤的保护作用和缓解tau蛋白Ser-262位点磷酸化的研究少见报道。同时由于tau蛋白Ser-262位点是最早磷酸化的位点,它的磷酸化将会启动其他位点的磷酸化;且Ser-262位点位于微管的结合区域,其磷酸化可导致神经元细胞突触蛋白表达下降和树突的损伤[15]。所以本实验以LiCl为研究对象,探讨其对冈田酸诱导拟AD病模型中神经元突触损伤和tau蛋白Ser-262异常磷酸化的保护作用。结果发现,LiCl能够改善OA所致神经元突触的损伤,并伴随着synaptophysin表达升高、tau蛋白Ser-262位点异常磷酸化水平的降低。亦有研究表明,tau蛋白的异常磷酸化与活性氧密切相关,因此我们推测LiCl可能通过清除胞内活性氧从而降低tau蛋白的磷酸化,但其具体的机制有待于进一步研究[16]。
综上所述,OA能诱导成熟神经细胞突触萎缩及tau蛋白Ser-262位点磷酸化水平升高,而LiCl可改善OA所致神经细胞突触的损伤,并上调synaptophysin的表达、下调tau蛋白Ser-262的磷酸化水平,这为LiCl在AD方面的治疗提供了一定的理论依据和实践基础。
| [1] |
Whittington R A, Bretteville A, Dickler M F, et al. Anesthesia and tau pathology[J]. |
| [2] |
Noble W, Planel E, Zehr C, et al. Inhibition of glycogen synthase kinase-3 by lithium correlates with reduced tauopathy and degeneration |
| [3] |
Kramer T, Schmidt B, Lo Monte F. Small-molecule inhibitors of GSK-3: structural insights and their application to Alzheimer′s disease models[J]. |
| [4] |
Wang J Z, Grundke-Iqbal I, Iqbal K. Kinases and phosphatases and tau sites involved in Alzheimer neurofibrillary degeneration[J]. |
| [5] |
Rametti A, Esclaire F, Yardin C, et al. Lithium down-regulates tau in cultured cortical neurons: a possible mechanism of neuroprotection[J]. |
| [6] |
Mangialasche F, Solomon A, Winblad B, et al. Alzheimer′s disease: clinical trials and drug development[J]. |
| [7] |
Brunden K R, Ballatore C, Crowe A, et al. Tau-directed drug discovery for Alzheimer′s disease and related tauopathies: a focus on tau assembly inhibitors[J]. |
| [8] |
Liu H C, Leu S J, Chuang D M. Roles of glycogen synthase kinase-3 in Alzheimer′s disease: from pathology to treatment target[J]. |
| [9] |
Riadh N, Allagui M S, Bourogaa E, et al. Neuroprotective and neurotrophic effects of long term lithium treatment in mouse brain[J]. |
| [10] |
刘 超, 闵 苏, 魏 珂, 等.2, 6-二异丙基苯酚、人参皂苷Rg-1和氯化锂逆转电休克后嗅球切除抑郁大鼠学习记忆障碍[J].中国药理学通报, 2012, 28(8):1125-30. Liu C, Min S, Wei K, et al. 2, 6-Diisopropylphenol, ginsenoside Rg-1 and lithium protects against the impairment of learning-memory induced by electroconvulsive shock in depressed rats[J]. |
| [11] |
Fontan-Gabas L, Oliemuller E, Martinez-Irujo J J, et al. All-trans-retinoic acid inhibits collapsin response mediator protein-2 transcriptional activity during SK-N-SH neuroblastoma cell differentiation[J]. |
| [12] |
李 静, 王 涛, 沈玉君, 等.MANF对神经细胞中tau蛋白过度磷酸化的抑制作用[J].中国药理学通报, 2012, 28(8):1111-5. Li J, Wang T, Shen Y J, et al. MANF inhibits tau hyperphosphorylation in cultured neuronal cell[J]. |
| [13] |
Kamat P K, Tota S, Rai S, et al. Okadaic acid induced neurotoxicity leads to central cholinergic dysfunction in rats[J]. |
| [14] |
Mandelkow E M, Mandelkow E. Biochemistry and cell biology of tau protein in neurofibrillary degeneration[J]. |
| [15] |
Tom E D, Katrien P, Koen D W, et al. Derailed intraneuronal signalling drives pathpgenesis in sporadic and familial Alzheimer′s disease[J]. |