


2. the Affiliated Hospital,
3. Basic Medical College,
4.4. School of Stomatology,Qingdao University,Qingdao Shandong 266000,China)
左卡尼汀是一种广泛存在于机体组织内的氨基酸衍生物,是哺乳动物能量代谢必需的体内天然物质,主要分布在哺乳动物的骨骼肌以及心肌中。人体可以通过膳食补充左卡尼汀,肉类、禽类、鱼类以及乳制品都富含左卡尼汀,而蔬菜和谷物中左卡尼汀的含量较少[1]。左卡尼汀主要功能是促进机体脂类代谢,在能量生成的过程中起着至关重要的作用,它可以协助活化的脂肪酸进入线粒体基质进行β氧化产生能量,并进一步辅助中间产物输出线粒体,以防止中间产物的聚集[2]。近期研究表明,左卡尼汀除了参与能量代谢,还可以调控细胞的程序性死亡。Fan等[3]报道:左卡尼汀可以选择性诱导肝癌细胞凋亡而对正常肝细胞没有任何不良影响。截止目前,对左卡尼汀诱导癌细胞凋亡的机制,尚无深入研究。
多形性成胶质细胞瘤(GBM)被世界卫生组织分类为四级星形细胞瘤,占所有星形细胞瘤的50%,是一种极为普遍且极具侵袭性的恶性胶质瘤[4]。其治疗措施包括手术、放疗、化疗等,但由于GBM的基因多样性以及其复杂的分子病理,GBM患者会不同程度的对治疗产生抵抗[5, 6, 7]。因此,目前治疗恶性胶质瘤成为肿瘤领域的重大挑战之一。近期已有研究发现:针对特异性分子信号通路的靶向药物对恶性胶质瘤特别有效,可能成为胶质瘤治疗的新热点。目前,肿瘤坏死因子相关凋亡诱导配体(tumor necrosis factor-related apoptosis inducing ligand ,TRAIL)已经被认为是最具有潜力的治疗GBM药物靶点[8]。本研究中,探讨了左卡尼汀作为TRAIL的敏化剂,增强TRAIL对GBM细胞诱导凋亡的效果,并对其敏化作用的机制进行了研究,旨在为临床GBM的治疗提供新的有效手段。
1 材料与方法 1.1 试剂与仪器人恶性胶质瘤细胞株U87购自American Type Culture Collection 公司。 左卡尼汀、胎牛血清、青霉素、链霉素购自Sigma公司,DMEM培养基购自Invitrogen公司,所有抗体均购于Santa Cruz Biotechnology,流式凋亡试剂盒购于BD Pharmingen公司,caspase-3活性测定试剂盒购于Keygen公司,Nuclear Extraction试剂盒购于Active Motif。酶标仪为Tecan公司产品(型号Infinite M1000),流式细胞仪为BD Biosciences公司产品(型号FACSCanto),PCR仪为Thermofisher公司产品(型号GeneAmp 9700)。
1.2 细胞培养U87培养于含有10% 胎牛血清、1×105 U·L-1 青霉素和100 mg·L-1链霉素双抗的高糖DMEM 完全培养液中,置于37℃、5% CO2的细胞培养箱中培养。根据细胞培养情况,3~4 d 传代1次,取对数生长期、健康的细胞进行实验。
1.3 CCK-8法测定细胞存活率 将细胞接种于96孔板中,相应药物处理后,向每孔加入10 μL CCK-8溶液后将96孔板放入细胞培养箱孵育3 h。用酶标仪检测450 nm处各孔的吸光度,计算各组细胞存活率。
1.4 AnnexinV-FITC/PI检测细胞凋亡 将细胞接种至6孔板中,相应药物处理后,用胰酶消化、离心、收集细胞沉淀,PBS重悬细胞并计数。取3×105个细胞,加入100 μL结合液,重悬细胞,再加入5 μL Annexin V-FITC,混匀后加入5 μL碘化丙啶(propidium iodide,PI),置于室温避光孵育15 min,用流式细胞仪检测细胞凋亡情况。
1.5 Westernblot检测蛋白表达 收集细胞,预冷的裂解液(含1% NP 40、0.5%脱氧胆酸钠、0.1% SDS、蛋白酶抑制剂cocktail,pH 6.8)每组100 μL冰上裂解10 min,12 000 r·min-1 4℃离心20 min收集上清液,BCA蛋白定量试剂盒测定蛋白含量。上样10 μL,10%聚丙烯酰胺凝胶电泳,4℃低温条件下转膜,NC膜以5%脱脂奶粉封闭液室温封闭2h。将对应的特异性一抗按1 ∶200、β-actin按1 ∶1 000稀释后,4℃孵育过夜。洗膜3次,加入辣根过氧化酶结合的二抗,37℃孵育1 h,洗膜3次,加入DAB显色。图像经Quantity One凝胶成像分析系统进行分析。
1.6 NF-κB活性测试以Nuclear Extraction试剂盒(Active Motif)进行细胞核内成分提取。细胞用PBS清洗,离心收集细胞,取细胞沉淀备用。每20 μL细胞沉淀加入200 μL核蛋白抽提试剂A(含PMSF),混匀冰浴10~15 min,然后加入核蛋白抽提试剂B 10 μL,混匀后冰浴1 min,离心吸取上清即为核蛋白。NF-κB活性利用ELISA 试剂盒按步骤进行检测,用酶标仪在450 nm波长处测量OD值。
1.7 Caspase-3活性检测 Caspase-3活性利用试剂盒测定(Keygen Biotech,Nanjing,China)。细胞以PBS缓冲液重悬,冰上孵育60 min,10 000×g离心1 min。收集上清与特异性酶底物在37℃下温育4 h,利用分光光度计检测450 nm处吸光度。
1.8 细胞转染将3条靶向p65/NF-κB基因的特异性siRNA转入细胞,筛选出对p65/NF-κB表达抑制最有效的一条。转染前取对数生长期细胞,用含10%胎牛血清的DMEM/High Glucose培养液悬浮后,以2×105个/孔的密度接种于6孔板中。Lipofectamine 2000用Opti-MEM预混后,静置5 min,加入Opti-MEM稀释后的p65/NF-κB siRNA和control-siRNA并混匀,室温静置20 min。p65/NF-κB siRNA序列为5′-GATGAAGACTTCTCCTCCATTGCGGACAT-3′(shRNA),control-siRNA序列为5′-TGACCACCCTGACCTACGGCGTGCAGTGC-3′,将混合物按分组加入含胶质瘤细胞的6孔板中,置于37℃、5% CO2的细胞培养箱中培养,48 h后收集细胞进行试验。
1.9 定量PCR测试于转染后48 h收获细胞,每孔加0.5 mL TRIzol,按照TRIzol试剂说明书进行操作。测定紫外分光光度计260 nm/280 nm波长处的吸光度值,计算浓度,2%琼脂糖电泳检测总RNA的完整性。逆转录条件参照AMV酶说明书进行,PCR扩增应用ABI PRISM 7000 Sequence Detection系统(Applied Biosystems)进行检测。引物序列如下 (sense) 5′-CGGACTATAGAGTGCTGATGG-3′ 以及 (antisense) 5′-GATTATCAGGCAGATTCCTAG-3′。GADPH用作内参来定量PCR产物。
1.10 统计学分析数据以 ±s表示,单个实验重复至少3次,Graphpad Prism 5.01软件处理数据,SNK统计学软件进行组间统计。
±s表示,单个实验重复至少3次,Graphpad Prism 5.01软件处理数据,SNK统计学软件进行组间统计。
首先检测TRAIL以及左卡尼汀对细胞存活率的影响。如Fig1A所示,当TRAIL浓度为100 μg·L-1处理细胞48 h,可以明显降低细胞存活率(P<0.05)。左卡尼汀对细胞存活率的影响如Fig1B所示,左卡尼汀对细胞存活率的抑制呈现浓度依赖,与对照组相比较,20 mmol·L-1左卡尼汀处理48 h可以将细胞的存活率降低至(62.1±5.2)%。基于以上的结果,以50 μg·L-1 TRAIL与10 mmol·L-1左卡尼汀组合进行后续实验。如Fig1C所示,50 μg·L-1 TRAIL与10 mmol·L-1左卡尼汀联合处理细胞48 h,细胞的存活率降至(49.2±4.9)%。

|
| Fig.1 Effect of L-carnitine or/and TRAIL on cell viability Cells were treated with indicated concentration of L-carnitine,TRAIL,or both for 48 h.*P<0.05 vs DMSO; #P<0.05 vs TRAIL |
利用流式细胞仪,对左卡尼汀与TRAIL联合诱导凋亡的效果进行检测。如Fig2A所示,当TRAIL浓度为50 μg·L-1,不能够在细胞中引起明显的凋亡(P0.05)。但是当50 μg·L-1 TRAIL与10 mmol·L-1左卡尼汀联合给药时,左卡尼汀可以明显增强细胞对TRAIL诱导凋亡作用的敏感度,两者联用可以在细胞中引起明显的凋亡(P<0.05)。细胞的凋亡与caspase-3和PARP的活化紧密相关,因此,检测了两者联用对caspase-3以及PARP活化状态的影响。如Fig2B所示,TRAIL与左卡尼汀联用导致活化caspase-3和PARP的表达明显升高。caspase-3的活化也进一步的被酶活性检测结果所证实,如Fig2C所示。

|
| Fig.2 Combinatory treatment with L-carnitine plus TRAIL induced apoptosis mediated via caspase-dependent pathway Cells were treated with indicated concentration of L-carnitine,TRAIL,or both for 48 h.*P<0.05 vs DMSO;#P<0.05 vs TRAIL |
U87细胞的凋亡与c-FLIP的水平密切相关[10, 16],本研究检测了左卡尼汀是否通过调节c-FLIP水平提高U87细胞对TRAIL的敏感度。如Fig3A所示,50 μg·L-1 TRAIL并未引起细胞内c-FLIP水平的明显变化(P>0.05),而10 mmol·L-1左卡尼汀也只是将细胞内的c-FLIP水平 稍微下调(P>0.05)。但是当两者联用,细胞中的c-FLIP水平呈现出明显的下降(P<0.05)。为了进一步证实以上结果,利用RT-PCR检测了c-FLIP的mRNA表达水平。如Fig3B所示,TRAIL与左卡尼汀联合,明显抑制c-FLIP的mRNA表达,表明左卡尼汀增强TRAIL诱导凋亡效果伴随c-FLIP水平的下调。

|
| Fig.3 Effects of TRAIL and L-carnitine on c-FLIP expression in U87 cells Cells were treated with indicated concentration of L-carnitine,TRAIL,or both for 48 h.*P<0.05 vs DMSO |
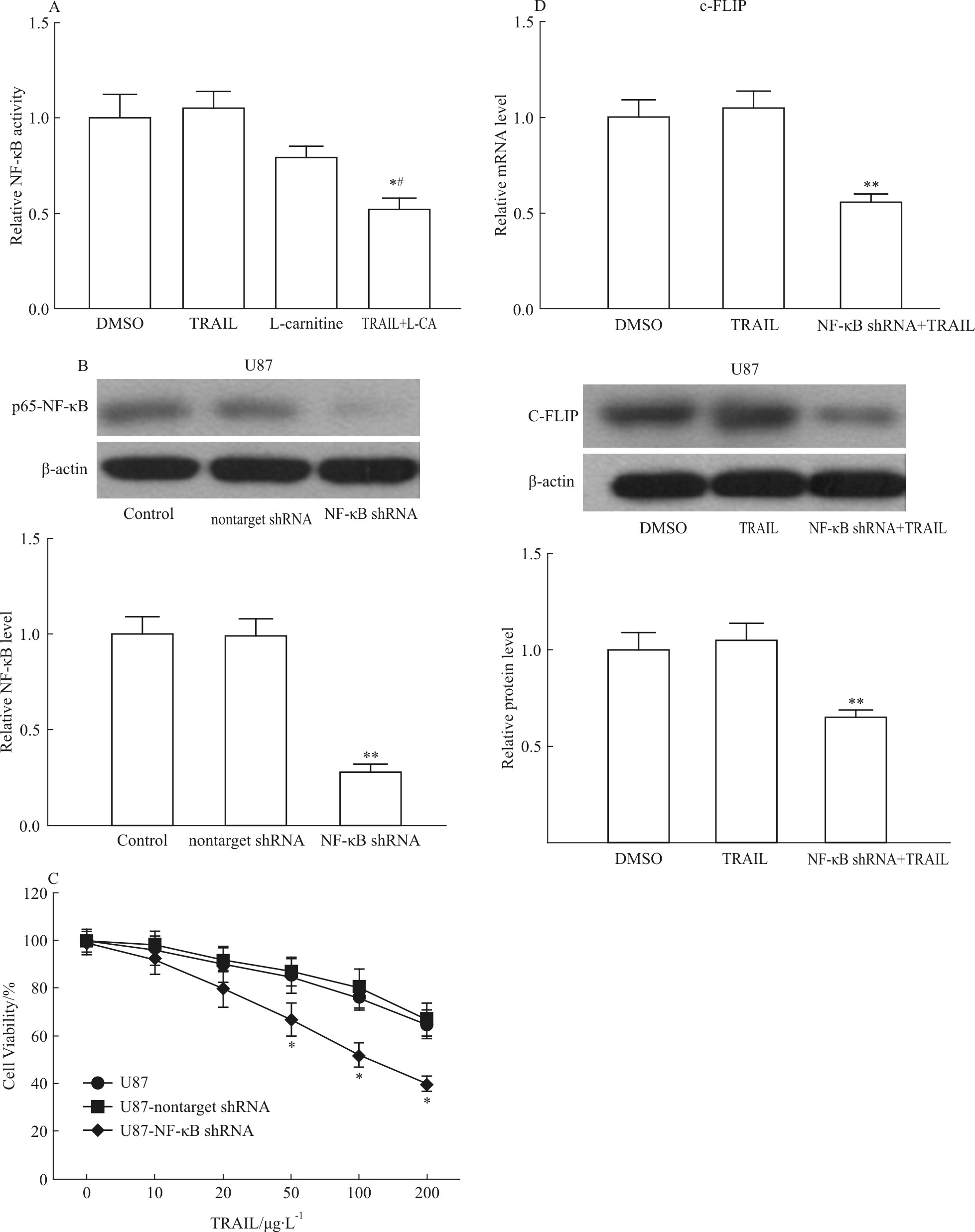
NF-κB对于细胞内c-FLIP水平起到关键的调节作用[10],本研究检测了TRAIL、左卡尼汀以及两者联用对NF-κB信号通路的影响。如Fig4A所示,ELISA的检测结果表明,100 μg·L-1 TRAIL可以将NF-κB的核内转运比例稍稍上调,而左卡尼汀可以稍微下调p65亚基的核内转运。但是当二者联用时,与对照组相比,NF-κB的活化显示出明显抑制(P<0.05),提示左卡尼汀对于TRAIL诱导凋亡的敏化作用与NF-κB通路活化受阻有密切关系。
2.4 沉默p65/NF-κB基因诱导U87细胞的神经毒性为了更直观的显示NF-κB信号通路抑制对于TRAIL诱导细胞凋亡的敏化作用,以shRNA沉默了p65/NF-κB基因。转染48 h以后,对p65/NF-κB基因沉默的效果利用免疫印迹进行验证,如Fig4B所示,siRNA转染可以明显抑制p65/NF-κB的表达。 MTT实验结果表明,沉默p65/NF-κB基因可以明显增强TRAIL对于U87细胞存活率的抑制(Fig4C)。同时,RT-PCR和Western blot结果也表明,p65/NF-κB基因沉默明显降低了U87细胞内c-FLIP mRNA以及蛋白的表达(Fig4D)。以上结果显示,抑制NF-κB信号通路的活化可以在U87细胞中增强TRAIL诱导的凋亡,这种敏化效果与c-FLIP蛋白的下调有关。
|
| Fig.4 L-carnitine -potentiated TRAIL-induced apoptosis partially dependent on activation of NF-κB Cells were treated with L-carnitine,TRAIL,or both for 48 h in GBM cells transfected with nontarget shRNA or NF-κB specific shRNA.*P<0.05,**P<0.01 vs DMSO;#P<0.05 vs TRAIL |
多形性成胶质细胞瘤(GBM)是成人患者中最常见的脑部肿瘤,具有高侵袭性、高死亡率的特点,中位存活期只有14.6月[9]。由于分子病理异相性,GBM的治疗相较于其他肿瘤尤其困难。为了改善预后,提高生存率,针对凋亡以及存活通路的一系列药物已经被用于治疗GBM,包括针对表皮生长因子的erlotinib与gefitinib,针对Akt通路的perifosine,针对mTOR靶点的temsirolimus,以及针对Bcl-2的gossypol。已有临床前研究表明,人类TRAIL能在活体动物模型中抑制胶质瘤生长[10],提示TRAIL具有应用于临床治疗的巨大潜力。但是,大部分胶质瘤细胞对TRAIL呈现出耐受,极大的限制了TRAIL的临床应用。近10年来,一系列研究结果显示,将TRAIL与其他抗癌药物相结合,可以有效克服TRAIL耐受,提高治疗效果。Saito等[11]发现将Temozolomide与TRAIL相结合可以明显延长荷瘤小鼠的存活期。Lee等[12]也证实了一些天然产物可以与TRAIL联用,提高胶质瘤细胞对TRAIL的敏感度。本项研究中,我们对左卡尼汀与TRAIL的协同作用进行了研究,并对其相关机制进行了探讨。
TRAIL通过与死亡受体DR4/TRAIL-R1以及DR5/TRAIL-R2相结合,引致DISC形成,从而激活caspase-8,诱导细胞凋亡。从DISC发出的凋亡信号可以被细胞内FLICE抑制蛋白(c-FLIP)所抑制。c-FLIP属于death effector domain(DED)家族,是具有催化活性的没有caspase-8/-10的同系物,并且已经被发现在多种肿瘤中呈现高表达,被认为是凋亡的抑制因子之一[13]。3种c-FLIP片段变体已经被鉴定为细胞内蛋白,包括55 ku的长型 c-FLIP(L)、26 ku的短型c-FLIP(S)以及24 ku的c-FLIP(R)。当处于高表达状态,所有3种c-FLIP都被认为可以作为抗凋亡蛋白,并且与caspase-8/-10竞争,参与DISC的富集[9]。相反的,在生理条件下,c-FLIP呈现低表达,c-FLIP可以促进caspase-8的活化以及死亡受体介导的凋亡[9]。Kang等的研究表明,利用siRNA敲除c-FLIP可以增强TRAIL诱导的凋亡。以上研究都提示:对于TRAIL诱导的凋亡,c-FLIP起到至关重要的作用。与此前研究结果相吻合,我们的研究结果也发现,左卡尼汀对于TRAIL诱导凋亡的敏化效果与c-FLIP下调有密切关系。
已有研究显示[14]:NF-κB信号通路参与调节不依赖生长因子的细胞增殖,抑制凋亡、无限复制、组织的侵袭以及转移,与肿瘤的发生发展紧密相关。 NF-κB信号通路在神经胶质瘤的发展中也起着重要作用,其活性增加与不良预后呈正性相关。另外,NF-κB信号通路活化与转录水平上的c-FLIP上调也呈正性相关。因此,抑制NF-κB信号通路已成为治疗神经胶质瘤的方案之一。Jane等[15]发现Bortezomib与TRAIL联用,可以对神经胶质瘤的生长产生协同抑制,其机制与抑制NF-κB信号通路活化有关。本研究也发现左卡尼汀可以有效地抑制U87细胞中NF-κB信号通路活化,且NF-κB信号通路抑制是左卡尼汀敏化TRAIL诱导凋亡的主要机制。
综上所述,本研究表明左卡尼汀可以在神经胶质瘤细胞中增强TRAIL诱导的凋亡,其机制与抑制NF-κB信号通路及其下游c-FLIP表达有关。此结果为将左卡尼汀应用于神经胶质瘤临床治疗提供了理论依据。
(致谢:感谢青岛大学国家实验教学中心人体机能实验室全体人员的帮助。)
| [1] | Shimada K,Sakuma Y,Wakamatsu J,et al. Species and muscle differences in L-carnitine levels in skeletal muscles based on a new simple assay[J]. Meat Sci,2004,68(3):357-62. |
| [2] | Jogl G,Hsiao Y S,Tong L. Structure and function of carnitine acyltransferases[J]. Ann N Y Acad Sci,2004,1033: 17-29. |
| [3] | Fan J P,Kim H S,Han G D. Induction of apoptosis by L-carnitine through regulation of two main pathways in Hepa1c1c 7 cells[J]. Amino Acids,2009,36(2):365-72. |
| [4] | Ohgaki H,Kleihues P. Population-based studies on incidence,survival rates,and genetic alterations in astrocytic and oligodendroglial gliomas[J]. J Neuropathol Exp Neurol,2005,64(6):479-89. |
| [5] |
余永强,陈 骏,钱银锋,等. 立体定向建立大鼠C6脑胶质瘤模型Yu Y Q,Chen J,Qian Y F,et al. Establishment of rat C6 glioma models with stereotaxis[J]. |
| [6] | Park D M,Rich J N. Biology of glioma cancer stem cells[J]. Mol Cells,2009,28(1):7-12. |
| [7] | Stupp R,Mason W P,van den Bent M J,et al. Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma[J]. N Engl J Med,2005,352(10):987-96. |
| [8] | Ashkenazi A,Pai R C,Fong S,et al. Safety and antitumor activity of recombinant soluble Apo2 ligand[J]. J Clin Invest,1999,104(2):155-62. |
| [9] | Schleich K,Warnken U,Fricker N,et al. Stoichiometry of the CD95 death-inducing signaling complex: experimental and modeling evidence for a death effector domain chain model[J]. Mol Cell,2012,47(2):306-19. |
| [10] | Roth W,Isenmann S,Naumann U,et al. Locoregional Apo2L/TRAIL eradicates intracranial human malignant glioma xenografts in athymic mice in the absence of neurotoxicity[J]. Biochem Biophys Res Commun,1999,265(2):479-83. |
| [11] | Saito R,Bringas J R,Panner A,et al. Convection-enhanced delivery of tumor necrosis factor-related apoptosis-inducing ligand with systemic administration of temozolomide prolongs survival in an intracranial glioblastoma xenograft model[J]. Cancer Res,2004,64(19):6858-62. |
| [12] | Lee D H,Kim D W,Jung C H,et al. Gingerol sensitizes TRAIL-induced apoptotic cell death of glioblastoma cells[J]. Toxicol Appl Pharmacol,2014,279(3):253-65. |
| [13] | Tian F,Lu J J,Wang L,et al. Expression of c-FLIP in malignant melanoma,and its relationship with the clinicopathological features of the disease[J]. Clin Exp Dermatol,2012,37(3):259-65. |
| [14] | Nogueira L,Ruiz-Ontaon P,Vazquez-Barquero A,et al. The NF-κB pathway: a therapeutic target in glioblastoma[J]. Oncotarget,2011,2(8):646-53. |
| [15] | Jane E P,Premkumar D R,Pollack I F. Bortezomib sensitizes malignant human glioma cells to TRAIL,mediated by inhibition of the NF-{kappa}B signaling pathway[J].Mol Cancer Ther,2011,10(1):198-208. |
| [16] | 陈立立,陈忠明,王冠林,等. 以细胞存亡调控蛋白c-FLIP为靶点的癌症治疗研究Chen L L,Chen Z M,Wang G L,et al. Studies on cell death and survival regulatory protein c-FLIP as a target for cancer treatment[J].中国药理学通报2014,30(11): 1496-502., |

