


失眠被定义为入睡或维持睡眠困难[1],是现代生活常见的睡眠障碍性疾病,它既可以是一种原发性疾病,也可能是其他疾病的一种临床症状,严重影响人们的生活质量,同时也会产生各种躯体障碍和精神疾病。缺乏睡眠可能会导致白天嗜睡、记忆损伤、焦虑、抑郁等症状[2]。目前,临床应用的镇静催眠药物有:① 苯二氮卓类;② 非苯二氮卓类;③ 褪黑素受体激动剂;④ orexin受体拮抗剂[3]。
药物治疗失眠被推荐用于短期治疗,因为长期服用镇静催眠药物会引起诸多不良反应,例如睡眠结构的破坏、药物成瘾和耐受。理想的镇静催眠药物应具备快速诱导睡眠,对睡眠结构无影响,无次日残留作用,不影响记忆功能,无呼吸抑制作用,长期使用无依赖或戒断症状等特点[4]。而现有的镇静催眠药物显然不能完全满足临床需求,因此寻找新型镇静催眠药物具有重要意义。
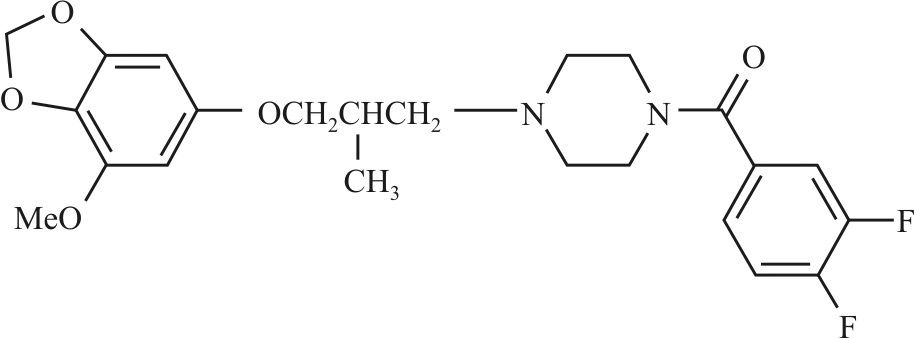
本实验室与药化室张纯贞研究员课题组合作,从一系列哌嗪类化合物中筛选出化合物H057(Fig1),其结构新颖,且具有较强的镇静催眠活性。本文旨在对化合物H057的镇静催眠活性进行药效学评价及机制的初步研究。
|
| Fig.1 Chemical structure of H057 |
♂ ICR小鼠,体质量18~22 g,清洁级,购自北京维通利华实验动物技术有限公司,许可证编号:SCXK(京)2012-0001。分笼饲养(8只/笼),室温保持在25℃,湿度40%~70%,自由进食和饮水,照明时间8 ∶00~20 ∶00。实验前动物适应环境至少3 d。
1.1.2 药品与试剂化合物H057(分子质量:448) 由本所胡伟教授合成,其结构(3,4-difluorophenyl)(4-(3-((7-methoxybenzo[d][1, 3]dioxol-5-yl)-2-methylpropyl)piperazin-1-yl)methanone。H057为白色粉末,水溶性差,易溶于有机溶剂。地西泮购自北京益民药业有限公司。戊巴比妥钠为Fluka产品。H057及地西泮用1%的Tween 80浸润并研磨后,溶于生理盐水中配制成相应浓度。戊巴比妥钠用生理盐水配制成相应浓度。用生理盐水(含1% Tween 80)作为溶剂对照。实验给药途径均为腹腔注射,阳性对照地西泮的给药剂量为5 mg·kg-1,戊巴比妥钠诱导小鼠翻正反射消失的阈下剂量为25 mg·kg-1,阈上剂量为40 mg·kg-1。γ-氨基丁酸(γ-aminobutyric acid,GABA)、邻苯二甲醛(o-phthalaldehyde,OPA)、去甲肾上腺素(norepinephrine,NE)和5-羟色胺(serotonin,5-HT)均为Sigma产品;β-巯基乙醇(β-mercaptoethanol,BME)购自Amresco公司;甲醇为色谱纯,购自北京化工厂;玻璃离子水门汀购自上海荣祥齿科材料有限公司;30%过氧化氢(批号:20130917)购自国药集团化学试剂有限公司;其余试剂均为国产分析纯,购自北京化学试剂公司。
1.1.3 溶液配制 1.1.3.1 衍生化试剂称取27 mg OPA溶于1 mL甲醇中,配制成27 g·L-1邻苯二甲醛溶液,4℃避光保存;四硼酸钠用双蒸水配制成0.1 mol·L-1,调pH为10.4,避光室温保存;β-巯基乙醇用甲醇稀释20倍,4℃避光保存。取1.5 mL的四硼酸钠溶液加入50 μL OPA溶液和5 μL β-巯基乙醇,即配成衍生化试剂(每次现用现配)。
1.1.3.2 人工脑脊液配方氯化钠(NaCl 125 mmol·L-1),氯化钾(KCl 2.5 mmol·L-1),碳酸氢钠(NaHCO3 26 mmol·L-1),磷酸二氢钾(KH2PO4 0.3 mmol·L-1),葡萄糖(Glucose 10 mmol·L-1),氯化钙 (CaCl2 2.4 mmol·L-1),硫酸镁(MgSO4 1.3 mmol·L-1)和磷酸二氢钠(NaH2PO4 0.8 mmol·L-1)(pH 7.2~7.4)[5]。
1.1.4 仪器鼠博士自发活动实验系统(RD1413,上海移数信息科技有限公司),BehaviorSys2.2.0软件。脑立体定位仪(68002,深圳市瑞沃德生命科技有限公司);高速颅骨钻头(STRNG90,韩国Seashin);微透析套管(839024,瑞典CMA公司);微透析针(8010434,CMA 12 MD,4 mm; O.D. 0.5 mm;Cut-off: 2000Dlton,瑞典CMA公司);微量注射泵(圣诺SN-50F6);高效液相色谱泵(LC-10A,日本岛津公司);电化学检测器(LC-4C,美国BAS公司),色谱柱(Diamonsil(R)C18,150 mm×4.6 mm,5 μm,北京迪马科技有限公司),工作站(JS-3070,大连江申)。
1.2 方法 1.2.1 开场实验(OFT)[6 , 7]开场实验在一个放有不透明的方形自主活动箱(50 cm×50 cm×40 cm)的暗室中进行,自主活动箱正上方有摄像头记录小鼠在箱中的活动。♂ ICR小鼠随机分为5组,分别为溶剂对照组、地西泮(5 mg·kg-1)组和H057(1、5、25 mg·kg-1)组。腹腔注射(i.p.)溶剂对照、地西泮或H057,15 min后将小鼠放入单个自主活动箱内,摄像机记录5 min内小鼠的活动路程,并用BehaviorSys2.2.0软件进行自动分析。
1.2.2 协同阈下剂量戊巴比妥钠诱导睡眠实验[8 ]♂ ICR小鼠随机分为5组,分别为溶剂对照组、地西泮组(5 mg·kg-1)和H057(1、3、5 mg·kg-1)组。腹腔注射溶剂对照、地西泮或H057,20 min后各组腹腔注射阈下剂量戊巴比妥钠(25 mg·kg-1),观察15 min内各组入睡的动物数。
1.2.3 翻正反射消失实验(LORR)[9 ]♂ ICR小鼠随机分为5组,分别为溶剂对照组、戊巴比妥钠组(40 mg·kg-1,i.p.)和H057组(40、50、60 mg·kg-1,i.p.)。以翻正反射消失超过1 min为入睡指标,从注射药物到翻正反射消失记为睡眠潜伏期,从翻正反射消失至翻正反射消失恢复记为睡眠维持时间。记录小鼠翻正反射消失时间和翻正反射恢复时间,并计算其入睡潜伏期和睡眠时间。
1.2.4 利用微透析测定大鼠大脑皮层细胞外液GABA和单胺神经递质的含量[10 ] 1.2.4.1 微透析手术SD大鼠用4%的水合氯醛麻醉,将其固定于脑立体定位仪,电动剃毛器刮掉颅骨上方毛发,剪开头皮,3% H2O2腐蚀头皮,暴露出前囟,定位前囟,记下前囟坐标。参照大鼠脑立体定位图谱[11],确定SD大鼠前额叶皮层坐标为(bregma AP+2.8 mm,ML+0.7 mm,DV 1 mm),根据此坐标确定打孔位置,用电动钻头进行打孔,至脑膜暴露,用细针将脑膜小心挑破(切勿扎破血管),将套管埋入相应深度,用玻璃离子水门汀对套管进行固定。手术完毕,待恢复1 d后测定。
1.2.4.2微透析取样和处理大鼠清醒状态下,将套管小心拔出,插入CMA 4 mm探针,微灌注泵灌注透析用人工脑脊液,用0.2 μm微孔滤膜过滤。透析时保持灌流液温度37.0~38.0℃,灌流速度为1 μL·min-1。微透析探针置入2 h后收集透析液,待透析液中基础值稳定后,腹腔注射生理盐水或H057(25 mg·kg-1)。对于GABA含量测定,给药后每10 min收集1管透析液,将收集的透析液与衍生化试剂以1 ∶2的比例冰上反应2 min后,用高效液相色谱电化学法(HPLC-EC)进行检测;对于单胺神经递质的测定,给药后每1 h收集1管透析液(透析管中预先加入10 μL 0.1 mol·L-1 HClO4以防止收集液中递质的氧化),收集的透析液用高效液相进行检测。
1.2.5 HPLC分析检测条件检测电压0.6 V;增益为2 nA;灵敏度1 ng;泵流速1.2 mL·min-1。
1.2.6 统计学处理实验数据以 ±s表示,用SPSS 19.0软件进行统计学分析。自主活动采用单因素方差分析(one-way ANOVA);结果显示组间差异有显著性时进行Dunnett检验,比较各剂量组与对照组的差异。小鼠睡眠发生率实验采用卡方检验进行统计学分析。脑内GABA含量用Student's t-test进行分析。
±s表示,用SPSS 19.0软件进行统计学分析。自主活动采用单因素方差分析(one-way ANOVA);结果显示组间差异有显著性时进行Dunnett检验,比较各剂量组与对照组的差异。小鼠睡眠发生率实验采用卡方检验进行统计学分析。脑内GABA含量用Student's t-test进行分析。
开场实验用于筛选具有镇静作用的药物,一般具有明显中枢抑制作用的药物可明显降低小鼠的自主活动[12]。如Fig2所示,小鼠分别腹腔注射生理盐水、地西泮(5 mg·kg-1)和H057(1、5、25 mg·kg-1),15 min后测定小鼠自主活动。结果显示,H057(5、25 mg·kg-1)能明显抑制小鼠自主活动,两剂量组的抑制率分别为25%和66%,与溶剂对照组相比差异有显著性(Dunnett′s test,P<0.05和P<0.01)。结果表明,H057具有明显的镇静作用。

|
Fig.2
Effect of H057 on spontaneous locomotor activity in mice( ±s,n=8)
*P<0.05,**P<0.01 vs vehicle group ±s,n=8)
*P<0.05,**P<0.01 vs vehicle group
|
如Tab1所示,与溶剂对照组相比,H057能明显增强阈下剂量戊巴比妥钠诱导小鼠睡眠的作用,3、5 mg·kg-1组小鼠的入睡率分别增加为62.5%和87.5%,在统计学上差异均具有显著性(P<0.01)。
| Group | Dose/mg·kg-1 | Sleep onset/% |
| Vehicle | - | 0 |
| Diazepam | 5 | 100** |
| H057 | 1 | 0 |
| 3 | 62.5** | |
| 5 | 87.5** | |
| **P<0.01 vs vehicle | ||
以翻正反射消失时间超过1 min为入睡指标,如Tab2所示,与溶剂对照组相比,腹腔注射H057(60 mg·kg-1)能引起小鼠100%入睡(P<0.01)。Tab3所示为各组小鼠的睡眠潜伏期和睡眠时间。
| Group | Dose/mg·kg-1 | Sleep onset/% |
| Vehicle | - | 0 |
| Sodium pentobarbital | 40 | 100** |
| H057 | 40 | 20 |
| 50 | 87.5** | |
| 60 | 100** | |
| **P<0.01 vs vehicle | ||
 ±s,n=8)
±s,n=8)
| Group | Dose /mg·kg-1 | Latency/min | Sleeping time/min |
| Vehicle | - | - | - |
| Sodium pentobarbital | 40 | 6±1.2 | 59±7 |
| H057 | 60 | 24±4 | 96±8 |
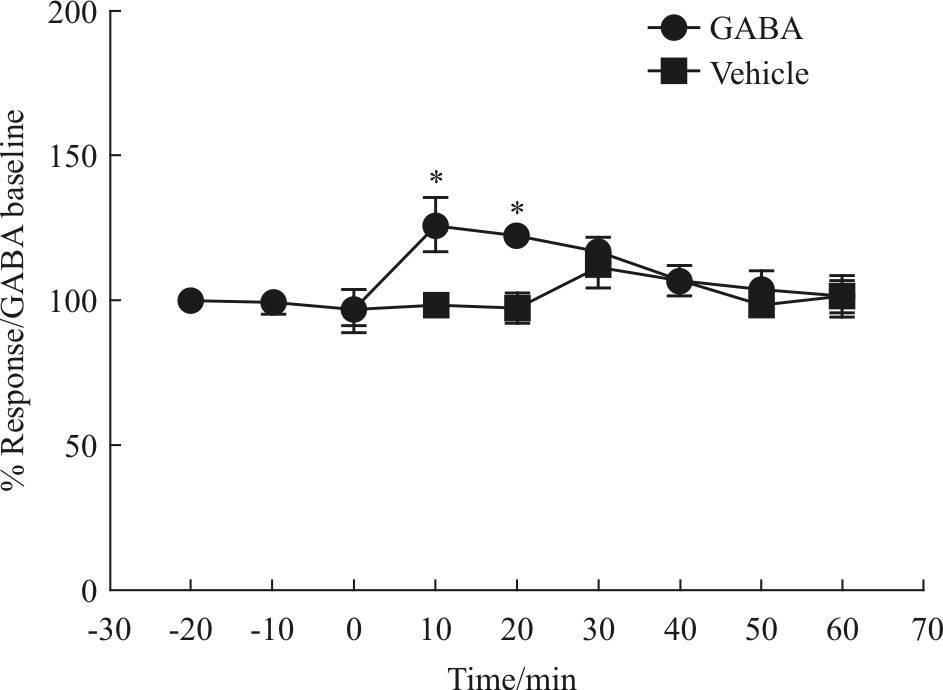
微透析实验中,探针插入核团平衡2 h后,腹腔注射H057(25 mg·kg-1)。10 min内细胞外液GABA含量开始明显升高,且达到峰值,给药30 min后,GABA含量逐渐降至基础水平(Fig3)。
|
Fig.3
Effect of H057 on cerebral cortex extracellular GABA level in rats( ±s,n=8)
Before rats were injected with H057,three consecutive dialysates were collected. The average of three values was defined as the basal level (as one hundred percent)and the subsequent dialysate samples were expressed as percentages of the level.*P<0.05 vs basal level ±s,n=8)
Before rats were injected with H057,three consecutive dialysates were collected. The average of three values was defined as the basal level (as one hundred percent)and the subsequent dialysate samples were expressed as percentages of the level.*P<0.05 vs basal level
|
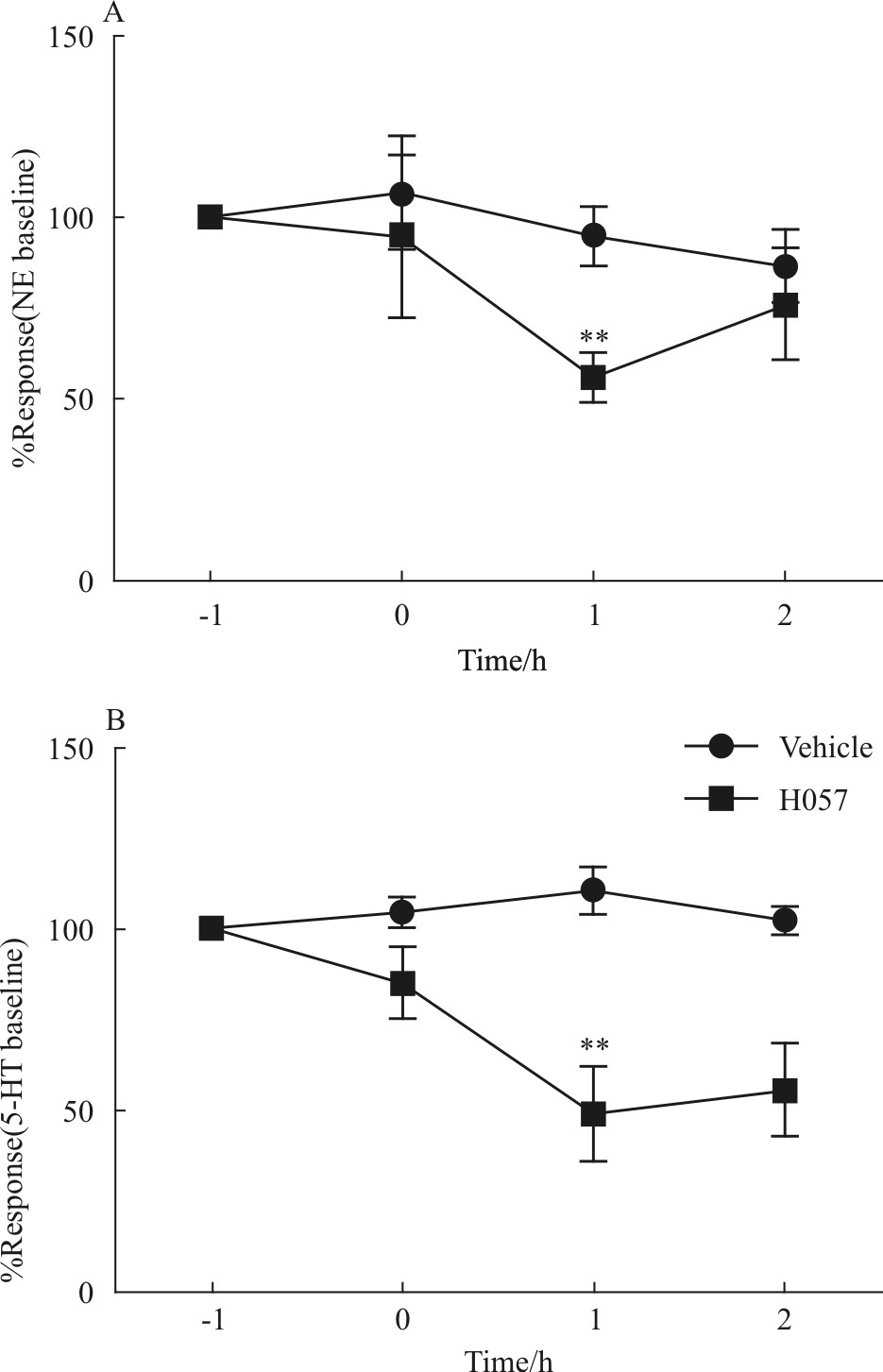
微透析实验表明,腹腔注射H057(25 mg·kg-1)后1 h,大鼠大脑皮层细胞外液5-HT和NE含量均明显降低,分别降低38%和50%(Fig4)。给药2 h后NE的含量基本恢复至基础水平,而5-HT含量仍未恢复。
|
Fig.4
Effects of H057 on contents of NE(A) and 5-HT(B) in extracellular fluid in cerebral cortex in rats( ±s,n=8)
**P<0.01 vs vehicle group ±s,n=8)
**P<0.01 vs vehicle group
|
小鼠开场实验是药理学研究中常用的方法之一,在评价药物对中枢神经系统影响方面有重要的意义。动物的自主活动情况反映其中枢神经系统的功能状态,兴奋时自主活动数增加,抑制时活动次数减少。本实验结果表明,腹腔注射H057(5、25 mg·kg-1)能明显抑制小鼠自主活动。协同阈下剂量戊巴比妥钠实验常用于镇静催眠化合物的初步筛选[13]。在该实验中我们发现,H057能明显增加阈下剂量戊巴比妥钠诱导小鼠的入睡率。小鼠翻正反射消失超过1 min可作为小鼠睡眠的行为学标志[14]。ICR小鼠腹腔注射H057(≥60 mg·kg-1)可直接诱导小鼠100%翻正反射消失。
GABA是大脑中主要的抑制性神经递质,脑中不同部位的GABA神经元共同起到了促进睡眠的作用。GABA可使觉醒转化为睡眠[15]。目前临床上主要的镇静催眠药物,如苯二氮卓类的地西泮和非苯二氮卓类的唑吡坦均以GABA受体作为靶点。因此,首先我们探索了化合物H057对GABA系统的影响。实验室前期研究结果已经证明化合物H057与GABAA受体无相互作用。因此,我们探究H057对GABA含量的影响。我们利用微透析技术,测定大鼠大脑皮层细胞外液GABA含量。脑微透析技术是一种在体脑化学采样技术,其原理是脑细胞外液中可溶性小分子可通过一种半透膜管的微小孔径顺浓度梯度扩散,是监测脑细胞外液中小分子物质的一种重要手段[16]。微透析实验结果显示,H057能明显升高大鼠大脑皮层细胞外液GABA水平,这一结果与H057使动物镇静催眠的药效学一致。
单胺能神经系统是促觉醒系统中非常重要的一个分支,它主要包括腹侧导水管周围灰质(vPAG)多巴胺神经元,背侧和正中脊核(DR)5-HT能神经元和蓝斑核(LC)去甲肾上腺素能神经元。这些神经元共同组成了促觉醒系统的一条激活途径,激活大脑皮层,发挥促觉醒的作用。本研究利用微透析技术测定了化合物H057对大鼠大脑皮层细胞外液单胺神经递质含量的影响。结果发现,化合物H057能够明显降低5-HT和NE的水平。
GABA能神经系统和单胺能神经系统之间有密切的投射,两者相互抑制,共同维持睡眠和觉醒的平衡状态。对于H057具体是如何升高GABA含量,降低5-HT和NE含量来发挥镇静催眠作用需要进一步的探索。
| [1] | Wafford K A,Ebert B. Emerging anti-insomnia drugs: tackling sleeplessness and the quality of wake time[J]. Nat Rev Drug Discov,2008,7(6): 530-40. |
| [2] | Roth T,Drake C. Evolution of insomnia: current status and future direction[J]. Sleep Med,2004,5(Suppl 1): S23-30. |
| [3] | Sun H,Kennedy W P,Wilbraham D,et al. Effects of suvorexant,an orexin receptor antagonist,on sleep parameters as measured by polysomnography in healthy men[J]. Sleep,2013,36(2): 259-67. |
| [4] | Roehrs T,Roth T. Insomnia pharmacotherapy[J]. Neurotherapeutics,2012,9(4): 728-38. |
| [5] | Shi Y,Dong J W,Tang L N,et al. N(6)-(3-methoxyl-4-hydroxybenzyl) adenine riboside induces sedative and hypnotic effects via GAD enzyme activation in mice[J]. Pharmacol Biochem Behav,2014,126: 146-51. |
| [6] | 李 伟,张建军. 腺苷类似物WS090501的镇静、催眠和抗惊厥作用[J]. 药学学报,2011,46(6):742-6. Li W,Zhang J J. Sedative,hypnotic and anticonvulsive effects of an adenosine analogue WS090501[J]. Acta Pharm Sin,2011,46(6): 742-6. |
| [7] | 赵施施 ,张科学 ,包素红,等. 丙泊酚对幼小鼠自主活动和学习记忆行为的影响[J] .中国药理学通报,2013,29(2):198-201. Zhao S S,Zhang K X,Bao S H,et al. Effects of propofol on spontaneous motor activity and learning behaviors in juvenile mice[J]. Chin Pharmacol Bull,2013,29(2):198-201. |
| [8] | 邹宗尧,王燕枝,胡慭然,等. 黄连生物碱促小鼠睡眠实验研究[J]. 中国药理学通报,2014,30(12):1752-6. Zou Z Y,Wang Y Z,Hu Y R,et al. Study of Rhizoma Coptidis alkaloids on promoting sleep in mice[J]. Chin Pharmacol Bull,2014,30(12):1752-6. |
| [9] | Tabatabai S A,Rezaee Zavareh E,Reyhanfard H,et al. Evaluation of anxiolytic,sedative-hypnotic and amnesic effects of novel 2-phenoxy phenyl-1,3,4-oxadizole derivatives using experimental models[J]. Iran J Pharm Res,2015,14(Suppl): 51-7. |
| [10] | Bredewold R,Schiavo J K,van der Hart M,et al. Dynamic changes in extracellular release of GABA and glutamate in the lateral septum during social play behavior in juvenile rats: implications for sex-specific regulation of social play behavior[J]. Neuroscience,2015,307: 117-27. |
| [11] | Paxinos G,Watson C. The rat brain in stereotaxic coordinates[M]. 7th ed. Elsevier: Academic Press,2007. |
| [12] | 谢 云,唐月月,魏晶晶,等. 地西泮对焦虑、抑郁小鼠体重、痛阈和自主活动的影响[J]. 中国药理学通报,2010,16(11):1529-30. Xie Y,Tang Y Y,Wei J J,et al. The effect of diazepam on the weight,pain threshold and independent activity of anxious mice and depressive mice[J]. Chin Pharmacol Bull,2010,16(11): 1529-30. |
| [13] | 吴军凯,霍金海,都晓伟. 黑水缬草挥发油对中枢神经系统药理作用的研究[J]. 中药材,2007,30(8):977-80. Wu J K,Huo J H,Du X W. Pharmacological effects of volatile oil of Valeriana amurensis on CNS[J]. J Chin Med Mater,2007,30(8): 977-80. |
| [14] | Harvey M,Sleigh J,Voss L,et al. Determination of hypnotic potency in rats of the novel ketamine ester analogue SN 35210[J]. Pharmacology,2015,96(5-6): 226-32. |
| [15] | Manns I D,Lee M G,Modirrousta M,et al. Alpha 2 adrenergic receptors on GABAergic,putative sleep-promoting basal forebrain neurons[J]. Eur J Neurosci,2003,18(3): 723-7. |
| [16] | Anderzhanova E,Wotjak C T. Brain microdialysis and its applications in experimental neurochemistry[J]. Cell Tissue Res,2013,354(1):27-39. |

