


杜冠华(1956-),男,博士,研究员,博士生导师,研究方向:药理学、药物筛选,通讯作者,Tel/Fax:010-63165184,E-mail:dugh@imm.ac.cn
糖尿病周围神经病变(diabetic peripheral neuropathy,DPN)是指在排除其他原因的情况下,糖尿病患者出现周围神经功能(感觉和运动)障碍相关的症状和(或)体征,如温度觉或痛觉异常、神经传导功能下降等。糖尿病是导致外周神经病变的首要因素,大约一半以上的糖尿病病人最终会发展成DPN。在2型糖尿病患者,高达10%~20%的病人在诊断为糖尿病时即存在糖尿病神经病变[1]。2型糖尿病DPN的发病机制尚未完全清楚,现已知它是多种因素综合作用的结果。除高糖外,还存在胰岛素抵抗、血脂紊乱、炎症等多种因素参与。本文着重对导致2型糖尿病周围神经病变的机制进行探讨。
1 高糖应激参与的外周神经损伤机制神经细胞能量的获得主要依赖葡萄糖,高血糖引起的代谢紊乱直接影响神经细胞的代谢,而血糖控制有助于糖尿病神经病变控制。研究表明,波动的血糖水平对糖尿病神经病变进展的影响更大。强化的血糖控制可以使1型糖尿病患者获益,而2型糖尿病则效果有限[2]。高血糖引起的外周神经损伤主要通过如下途径发挥作用。
1.1 多元醇通路激活长期高血糖时,葡萄糖的旁路代谢——多元醇通路激活。多元醇通路有两个关键酶,醛糖还原酶(aldose reductase,AR)和山梨醇脱氢酶,葡萄糖经前者催化生成山梨醇,山梨醇再经山梨醇脱氢酶催化生成果糖。神经组织内不含果糖激酶,不能利用果糖,从而造成山梨醇和果糖的大量堆积,在胞内形成很高的渗透压,导致神经细胞肿胀、变性甚至坏死[3]。在葡萄糖被醛糖还原酶还原为山梨醇的反应中,大量消耗了还原型辅酶Ⅱ(NADPH)。NADPH 是谷胱甘肽还原酶催化氧化型谷胱甘肽(GSSG)转化为谷胱甘肽(glutathione,GSH)的辅酶,导致GSSG 向GSH的转化受限。GSH的降低限制了GSH过氧化物酶将过氧化氢还原为水,使氧化应激增加。高血糖还可导致Na+/K+泵的功能异常,导致轴突外Na+的堆积,Na+跨膜运输下降,轴突结构和功能受损[4]。
肌醇是合成细胞膜脂质—聚磷酸肌醇磷脂的主要成分,具有模拟胰岛素的特性,可以降低餐后血糖。肌醇代谢异常与胰岛素抵抗和糖尿病微血管并发症相关。肌醇可以用来预防和治疗糖尿病神经病变[5]。葡萄糖与肌醇的空间结构相似,高血糖时,细胞外大量的葡萄糖可竞争性抑制神经组织摄取肌醇,细胞内大量多元醇的聚积也干扰肌醇的正常代谢,致使神经细胞内肌醇减少甚至耗竭,从而影响神经功能。
1.2 晚期糖基化终产物导致外周神经损伤持续高血糖的环境下,蛋白质、脂质或核酸等大分子物质在没有酶参与的条件下,自发地与葡萄糖或其他还原单糖反应,生成稳定的共价化合物,该反应过程称非酶糖基化反应,所形成的不可逆聚合物称晚期糖基化终末产物(advanced glycation endoproducts,AGEs)。沉积于神经组织的AGEs修饰细胞骨架蛋白、髓鞘蛋白及基质蛋白等,从而破坏神经结构[6]。
细胞外脂肪和蛋白AGEs结合到细胞表面的受体,特别是AGE受体(RAGE),启动炎症级联反应,改变外周神经的功能和结构,导致神经病变。2型糖尿病病人的皮肤活检标本发现RAGE的表达水平在DPN病人中升高[7]。AGEs与RAGE结合,可破坏髓鞘的完整性,影响神经组织的微管蛋白。微管系统结构和功能的改变可引起神经分泌障碍、轴索神经传导缺陷以及轴索的萎缩,使胞内基质蛋白对周围神经纤维的营养作用受到损害,神经的再生和修复受阻[8]。另外,AGEs可修饰血浆蛋白产生配体,与位于巨噬细胞、平滑肌细胞、血管内皮细胞及雪旺细胞上的RAGE结合。AGEs 与RAGE 结合可以诱导细胞内活性氧簇(ROS)明显增多,从而造成氧化应激损伤。乙二醛酶则可通过干预AGEs的生成,对糖尿病神经病变具有保护作用。AGEs与其受体结合可迅速活化NAD(P)H 氧化酶,后者是高糖诱导ROS产生的主要致病因素[9]。
1.3 硝化应激的细胞毒作用硝化应激在DPN早期即发挥重要作用,有可能成为药物干预的靶点。当ROS生成过多时,过量产生的超氧阴离子与NO通过非酶促化学反应形成细胞毒性更强的ONOO-,后者与蛋白和脂质反应,导致DPN的发生。超氧阴离子还可通过促进诱生型NO氧合酶(iNOS)的表达,增加NO的产生。研究表明,STZ诱导的敲除iNOS基因的糖尿病小鼠模型神经病变较对照组轻,而nNOS敲除小鼠糖尿病神经病变加重[10]。硝基酪氨酸可作为一种DPN进展的生物标记物[11]。
1.4 外周神经组织内质网应激内质网应激在糖尿病及糖尿病前期病变引起的外周神经病变中均发挥作用。在糖尿病长期慢性应激的情况下,可出现大量未折叠蛋白,进而导致内质网应激的发生。内质网应激可导致合成的蛋白质异常折叠,引起代谢、转录调节和基因表达受损,并最终出现细胞凋亡,是细胞损伤的重要机制。在糖尿病动物的坐骨神经和脊髓中,内质网应激导致的非折叠蛋白质反应增加,给予糖尿病动物化学分子伴侣(三甲胺氧化物),可减轻内质网应激、外周神经功能障碍和表皮内神经纤维丢失,但对血糖水平无影响[12]。内质网应激可导致感觉神经的钙稳态失衡。
1.5 高糖导致线粒体功能障碍线粒体功能障碍导致的氧化应激在DPN的发生、发展中起着重要作用。高糖能降低线粒体内膜电位及呼吸链活性。糖尿病动物背根神经节(dorsal root ganglion,DRG)细胞中线粒体呼吸功能降低程度与线粒体氧化磷酸化、三羧酸循环及抗氧化活性降低程度一致。高血糖时,过于旺盛的代谢可通过两种途径损伤神经元,一是氧供应充足情况下,过多的代谢物进入线粒体,电子传递链过度活跃,导致活性氧产生过多,进而抑制线粒体关键成分的活性,导致线粒体功能异常。二是在氧供应有限的情况下,过多的丙酮酸流入乳酸途径。一旦乳酸堆积并且NAD+耗竭,糖酵解将被抑制,神经元的功能会受损[13, 14]。在糖尿病患者中,神经元线粒体表型会发生变化,从而引起能量供应障碍和神经纤维缺失。高糖也可导致AMPK/PGC-1α信号途径激活,从而改变线粒体的功能、分裂和增殖,使神经功能障碍[15]。
2 血脂紊乱对外周神经损伤的影响 2.1 血脂紊乱加重外周神经功能的损伤2型糖尿病重要的特征之一是患者存在血脂紊乱。血脂异常通常包括血浆中甘油三酯和LDL胆固醇水平升高,同时还存在HDL胆固醇水平的下降。血脂异常参与了糖尿病神经病变的发生发展。单独的高脂血症即可导致外周神经功能障碍[16, 17]。影响脂肪代谢的左旋肉碱也在糖尿病并发症中发挥作用[18]。在高血糖合并高脂的情况下,雪旺细胞可出现内质网应激,并伴随钙稳态失衡。脂质与ROS或过氧化物反应形成的脂质过氧化物具有细胞毒性并消耗GSH。然而,仅仅为高葡萄糖暴露而没有脂毒性存在时,则不影响细胞的活性或内质网钙水平。降血脂药物非诺贝特可降低糖尿病患者的截肢发生率。结合一部分糖尿病神经病变患者给予强化葡萄糖控制治疗,未见明显的神经功能改善,提示脂质代谢异常在糖尿病神经病变中发挥重要作用。
2.2 氧化低密度脂蛋白启动氧化应激和炎症反应低密度脂蛋白(low-density lipoprotein,LDL)是一种复合物,氧化后的低密度脂蛋白(ox-LDL)含脂肪酸氧化产物、脂质氧化产物、蛋白氧化产物等,使LDL的生物学特性发生改变。在糖尿病中,血浆中的脂蛋白位于一个氧化的环境,血浆ox-LDL水平明显升高,ox-LDL水平可间接反映糖尿病患者外周神经病变程度。小鼠给予高脂饮食可以增加ox-LDL和全身及神经系统氧化应激,产生神经传导速度改变及感觉神经障碍,该改变出现早于葡萄糖耐量受损。外周感觉神经元与血管内皮细胞一样,可以表达ox-LDL的受体,包括氧化型LDL受体1(LOX-1)和Toll受体4(TLR4)。TLR4与TLR6组成异二聚体,启动下游反应。TLR4敲除后,可降低LOX-1的表达和自噬,提示LOX-1和TLR4存在正相关[19]。神经元表达的RAGE也可结合糖化LDL。这些受体内化ox-LDL和糖基化LDL,释放具有损伤作用的甘油三酯和游离脂肪酸(free fatty acids,FFA),启动炎症信号途径,导致NADPH氧化酶激活,并耗竭NADPH产生超氧自由基。氧化应激还可通过p38 MAPK信号途径增加ox-LDL和RAGE产生 ,对损伤产生正反馈。
2.3 游离脂肪酸的神经细胞毒作用游离脂肪酸被认为是导致糖尿病神经病变的主要因素之一。FFA的增加也参与胰岛素抵抗和β细胞功能障碍,并共同促进了糖尿病神经病变的发生。FFA以甘油三酯的形式贮存在脂肪细胞中,是禁食情况下的主要能量来源。脂肪分解代谢活跃状态下,FFA大量入血,产生高FFA血症。FFA与胰岛素抵抗有密切关系,可以抑制葡萄糖氧化,抑制胰岛素的信号传导,使GLUT-4转位下降,导致葡萄糖运输降低。FFA可损伤血管内皮,导致糖尿病并发症的发生。血液循环中长链脂肪酸(LCFAs)水平增多的情况下,线粒体对LCFAs的摄取增加,导致不完全的β氧化。LCFAs也可使线粒体生成ATP解偶联。长链酰基辅酶A合成酶1(Acsl1)可纠正这种改变。体外实验发现,在PC-12细胞中,高浓度的FFA可通过p38-MAPK途径诱导P2X7的表达和IL-6的释放[20]。在原代培养的雪旺细胞中,Acsl1过表达可防止长链脂肪酸诱导的氧化应激的线粒体功能障碍[21]。除了直接对外周神经系统的损伤作用,FFA可以通过促进炎性因子的释放,导致外周神经的损伤。
2.4 脂类介质对外周神经功能的影响脂类介质(lipid mediators)也在糖尿病神经病变中发挥重要作用。去氧鞘脂是具有神经毒性的鞘脂,经由丝氨酸棕榈转移酶形成。循环中如果1-去氧鞘脂的水平升高,会导致感觉和运动神经功能障碍。2型糖尿病患者去氧鞘脂的水平升高,给予非诺贝特(fenofibrate)可降低1-去氧鞘脂的水平,改善糖尿病神经病变。而同样能降低TG水平,但对1-去氧鞘脂无降低作用的烟酸则无改善作用。补充L-丝氨酸可以降低1-去氧鞘脂的水平。L-丝氨酸对血糖、体重和食物摄入均无影响,在STZ大鼠中,补充L-丝氨酸可以预防糖尿病神经病变的发生发展[22]。
2.5 氧化型胆固醇氧化型胆固醇(oxysterols)是胆固醇的中间或终氧化型衍生物。与胆固醇相比,氧化型胆固醇可以更快通过细胞膜和血脑屏障,同时作为胆固醇的一种运输形式,也参与胆固醇的周转,是胆固醇诱导代谢作用的生理介质。氧化型胆固醇在多种生理过程中发挥作用,包括胆固醇动态平衡、动脉粥样硬化、鞘脂类代谢、凋亡等。氧化型胆固醇可以在脑内堆积,导致神经退行性病变,也可通过线粒体介导的细胞死亡通路,损伤PC-12细胞导致神经毒性[13, 14]。
3 代谢性炎症引起神经病变慢性低度炎症是引起2型糖尿病的因素之一。糖尿病患者血液循环中的炎性标记物升高水平可以用于预测糖尿病并发症的发生和进展。
糖尿病神经病变循环血液中,前炎性细胞因子增多,其中包括炎症细胞因子、黏附分子和趋化因子,如TNF-α、白介素(IL)-1、IL-6、IL-8、单核细胞趋化因子蛋白-1和C-反应蛋白。循环和局部产生的内皮黏附分子,血管细胞黏附分子-1(ICAM-1)和E-选择素,也呈增加趋势[23]。有研究提示血小板特异性黏附分子、P-选择素、sICAM-1水平在糖尿病神经病变患者中明显升高,这些炎性标志物与神经传导速度受损和振动觉阈值检测结果呈相关性[24]。
TNF-α是一种强力的参与糖尿病神经病变前炎症因子。TNF-α基因敲除的糖尿病小鼠无神经病变表现。英夫利昔是可溶性TNF-α 相结合的单克隆抗体,TNF-α+/+小鼠单次给予英夫利昔单抗可抑制血浆中的TNF-α增多,同时可改善动物外周神经的电生理和生化指标等的缺陷[25]。动物实验显示,抑制相关的信号通路IkappaB,可抑制糖尿病神经病变的进展。
应用非甾体抗炎药如环氧合酶-2(COX-2)抑制剂或高剂量阿司匹林,也对糖尿病神经病变病人具有较好的治疗效果。COX-2抑制剂在啮齿类动物也可见对糖尿病神经病变具有保护作用。但是并非所有的研究均提示应用抗炎药对糖尿病并发症具有好的效果。
4 胰岛素抵抗导致外周神经功能障碍胰岛素抵抗是2型糖尿病区别于1型糖尿病的特征之一。1型糖尿病动物给予胰岛素可缓解疼痛,并且逆转感觉和运动神经传导速度的降低,提示胰岛素对神经元的直接营养作用。胰岛素受体和胰岛素受体底物广泛地表达在外周神经元的胞体和轴突。高胰岛素血症时,神经元可出现胰岛素抵抗,影响神经细胞功能,影响下游信号PI3K/Akt,p70S6K 和 GSK3β信号传导,从而导致神经元损伤和功能障碍。在ob/ob 2型糖尿病小鼠模型中,DRG神经元的胰岛素刺激Akt磷酸化和神经轴突的生长均受抑制[26]。长期慢性的胰岛素信号途径异常,影响PI3K/Akt途径调节线粒体代谢和氧化磷酸化能力,从而对神经元线粒体的功能产生影响,导致氧化应激,影响线粒体的生成[27]。
5 神经滋养血管病变促进外周神经损伤糖尿病中血管因长期高糖刺激,造成动脉粥样硬化、管腔狭窄,致使远端末梢循环供血不足,神经滋养血管(vasa nervorum)出现低灌注。组织形态学显示,糖尿病患者周围神经滋养血管的管壁基底膜增厚,发生透明变性,内皮细胞肿胀和增生,管腔狭窄,导致血管阻力增加,造成神经低灌注和神经内膜缺氧,进而发生神经变性坏死。
糖尿病神经病变的进展传统上被认为是血管异常,如毛细血管基底膜增厚和内皮细胞异常增生,从而导致缺氧。应用血管紧张素酶抑制剂和α1受体拮抗剂可增加神经的传导速度,增加神经血流。糖尿病神经病变作为微血管并发症最近存在争议,一些研究者认为,神经血管病变是神经元和神经胶质细胞损伤的继发性结果。一些研究提示糖尿病神经病变选择性靶向感觉和自主神经元,而非运动神经元,后者仅有少量的血管参与[9]。
6 其他因素雪旺细胞和轴突之间存在节区,该区的密度稍大,且胰岛素受体、葡萄糖转运体、钠钾通道和线粒体分布更为集中,对糖尿病神经病变影响较大[28]。神经元轴突的长短也很重要,长的神经纤维传导速度下降较早,这也是刺痛感和感觉缺失最早出现在足部,然后逐渐上升到其他部位的原因。
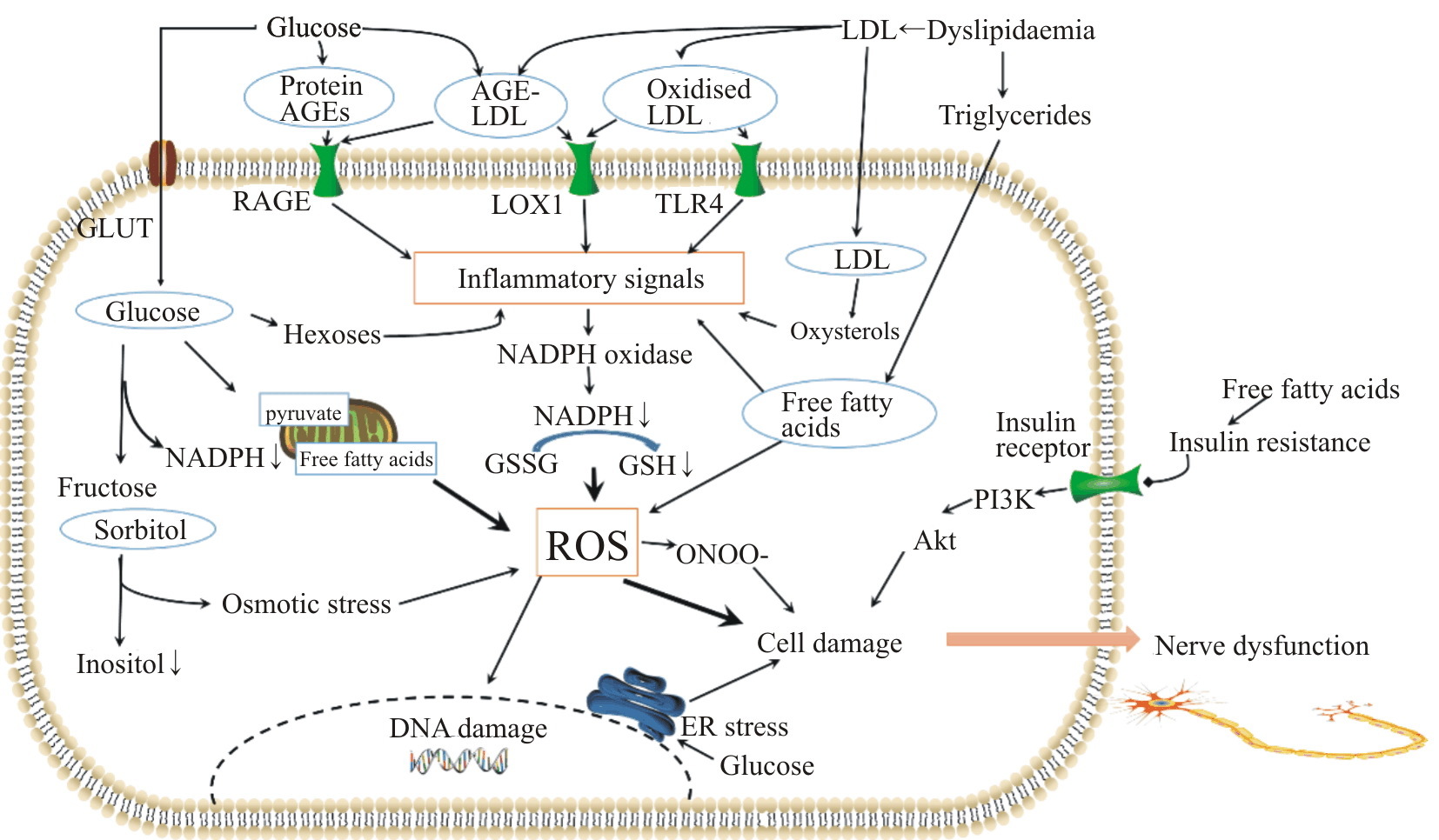
|
| Fig.1 Hyperglycemia,hyperlipidemia and insulin resistance activate multiple injury mechanisms in neurons |
另外,神经元、神经纤维功能的维持有赖于各种神经营养因子的作用,如神经生长因子(NGF)、脑源性神经营养因子(BDNF)及神经营养因子-3(NT-3),缺乏会影响神经正常生理功能或损伤后的修复再生,进而引起不同程度的神经病变[29]。
7 结语综上所述,2型糖尿病DPN 的发病涉及复杂而相互关联的发病机制(Fig 1)。高血糖导致外周神经损伤的机制包括:糖基化修饰蛋白质和脂质直接损伤神经细胞,并通过AGEs受体引起炎性信号通路激活,进一步加重损伤;激活多元醇信号通路,引起高渗性损伤和氧化应激;过于旺盛的代谢导致线粒体产生氧自由基增多、硝基化反应、内质网应激等。血脂紊乱的影响包括生成的氧化和糖基化LDL、FFA、脂类介质、氧化型胆固醇等引起的直接氧化应激损伤,和炎症等信号通路激活导致的间接损伤作用。另外代谢性炎症、胰岛素抵抗、神经滋养血管病变、神经营养因子、外周神经的解剖学特点均参与其中。
从既往的动物及临床实验来看,以任一发病机制为目标的治疗方案都难以取得理想的效果。而以减轻氧化应激损伤、降低炎性反应、改善线粒体的生物学功能及纠正生长因子缺乏的综合治疗将是治疗DPN 的长期原则。目前已经进入2期临床试验的药物主要靶向促进血管血流、诱导神经再生、降血糖、控制氧化应激和炎症反应。还有一些研究提示中药具有良好的效果[30]。因此,疾病的治疗需要从多靶点、多方位进行综合治疗。
| [1] | Charles M,Ejskjaer N,Witte D R,et al. Prevalence of neuropathy and peripheral arterial disease and the impact of treatment in people with screen-detected type 2 diabetes: the ADDITION-Denmark study[J]. Diabetes Care,2011,34(10): 2244-9. |
| [2] | Callaghan B C,Little A A,Feldman E L,Hughes R A. Enhanced glucose control for preventing and treating diabetic neuropathy[J]. Cochrane Database Syst Rev,2012,6: CD007543. |
| [3] | Miranda-Massari J R,Gonzalez M J,Jimenez F J,et al. Metabolic correction in the management of diabetic peripheral neuropathy: improving clinical results beyond symptom control[J]. Curr Clin Pharmacol,2011,6(4): 260-73. |
| [4] | Kiernan M C. Emergence of a predictive clinical biomarker for diabetic neuropathy[J]. Diabetes,2012,61(6): 1346-7. |
| [5] | Croze M L,Soulage C O. Potential role and therapeutic interests of myo-inositol in metabolic diseases[J]. Biochimie,2013,95(10): 1811-27. |
| [6] | 杨秀颖,杜冠华. 糖基化终末产物及相关药物研究进展[J]. 中国药理学通报,2011,27(9): 1185-8. |
| [6] | Yang X Y,Du G H.Advanced glycosylation end products and related drug development[J]. Chin Pharmacol Bull,2011,27(9):1185-8. |
| [7] | Park S Y,Kim Y A,Hong Y H,et al. Up-regulation of the receptor for advanced glycation end products in the skin biopsy specimens of patients with severe diabetic neuropathy[J]. J Clin Neurol,2014,10(4): 334-41. |
| [8] | Chowdhury S K,Dobrowsky R T,Fernyhough P.Nutrient excess and altered mitochondrial proteome and function contribute to neurodegeneration in diabetes[J].Mitochondrion,2011,11(6):845-54. |
| [9] | Forbes J M,Cooper M E. Mechanisms of diabetic complications[J]. Physiol Rev,2013,93(1): 137-88. |
| [10] | Vareniuk I,Pacher P,Pavlov I A,et al. Peripheral neuropathy in mice with neuronal nitric oxide synthase gene deficiency[J]. Int J Mol Med,2009,23(5): 571-80. |
| [11] | Edwards J F,Casellini C M,Parson H K,et al. Role of peroxynitrite in the development of diabetic peripheral neuropathy[J]. Diabetes Care,2015,38(7): e100-1. |
| [12] | Lupachyk S,Watcho P,Stavniichuk R,et al. Endoplasmic reticulum stress plays a key role in the pathogenesis of diabetic peripheral neuropathy[J]. Diabetes,2013,62(3): 944-52. |
| [13] | Vincent A M,Callaghan B C,Smith A L,Feldman E L. Diabetic neuropathy: cellular mechanisms as therapeutic targets[J]. Nat Rev Neurol, 2011,7(10): 573-83. |
| [14] | O'Brien P D,Hinder L M,Sakowski S A,Feldman E L. ER stress in diabetic peripheral neuropathy: A new therapeutic target[J]. Antioxid Redox Signal,2014,21(4): 621-33. |
| [15] | Chowdhury S K,Smith D R,Fernyhough P. The role of aberrant mitochondrial bioenergetics in diabetic neuropathy[J]. Neurobiol Dis, 2013,51: 56-65. |
| [16] | Obrosova I G,Ilnytska O,Lyzogubov V V,et al. High-fat diet induced neuropathy of pre-diabetes and obesity: effects of “healthy” diet and aldose reductase inhibition[J]. Diabetes,2007,56(10): 2598-608. |
| [17] | Vincent A M,Hayes J M,McLean L L,et al. Dyslipidemia-induced neuropathy in mice: the role of ox-LDL/LOX-1[J]. Diabetes,2009,58(10): 2376-85. |
| [18] | 曹 玉,李 萍,徐毅君,等. 糖尿病及其并发症患者血浆中左卡尼汀及其酰化物的含量分析研究[J]. 中国药理学通报,2014,30(7): 952-5. |
| [18] | Cao Y,Li P,Xu Y J,et al.Content of L-carnitine and its acylates in plasma of patients with diabetes and diabetes complications[J]. Chin Pharmacol Bull,2014,30(7):952-5. |
| [19] | Ding Z,Liu S,Wang X,et al. Lectin-like ox-LDL receptor-1 (LOX-1)-Toll-like receptor 4 (TLR4) interaction and autophagy in CATH.a differentiated cells exposed to angiotensin Ⅱ[J]. Mol Neurobiol,2015,51(2): 623-32. |
| [20] | Xu H,Wu B,Jiang F,et al. High fatty acids modulate P2X(7) expression and IL-6 release via the p38 MAPK pathway in PC12 cells[J]. Brain Res Bull,2013,94: 63-70. |
| [21] | Hinder L M,Figueroa-Romero C,Pacut C,et al. Long-chain acyl coenzyme A synthetase 1 overexpression in primary cultured Schwann cells prevents long chain fatty acid-induced oxidative stress and mitochondrial dysfunction[J]. Antioxid Redox Signal,2014,21(4): 588-600. |
| [22] | Othman A,Benghozi R,Alecu I,et al. Fenofibrate lowers atypical sphingolipids in plasma of dyslipidemic patients: a novel approach for treating diabetic neuropathy[J]. J Clin Lipidol,2015,9(4): 568-75. |
| [23] | Bluher M,Unger R,Rassoul F,et al. Relation between glycaemic control,hyperinsulinaemia and plasma concentrations of soluble adhesion molecules in patients with impaired glucose tolerance or type Ⅱ diabetes[J]. Diabetologia,2002,45(2): 210-6. |
| [24] | Doupis J,Lyons T E,Wu S,et al. Microvascular reactivity and inflammatory cytokines in painful and painless peripheral diabetic neuropathy[J]. J Clin Endocrinol Metab,2009,94(6): 2157-63. |
| [25] | Yamakawa I,Kojima H,Terashima T,et al. Inactivation of TNF-alpha ameliorates diabetic neuropathy in mice[J]. Am J Physiol Endocrinol Metab, 2011,301(5): E844-52. |
| [26] | Grote C W,Morris J K,Ryals J M,et al. Insulin receptor substrate 2 expression and involvement in neuronal insulin resistance in diabetic neuropathy[J]. Exp Diabetes Res,2011,2011: 212571. |
| [27] | Kim B,Feldman E L. Insulin resistance in the nervous system[J]. Trends Endocrinol Metab,2012,23(3): 133-41. |
| [28] | Zenker J,Ziegler D,Chrast R. Novel pathogenic pathways in diabetic neuropathy[J]. Trends Neurosci,2013,36(8): 439-49. |
| [29] | Tan W,Rouen S,Barkus K M,et al. Nerve growth factor blocks the glucose-induced down-regulation of caveolin-1 expression in Schwann cells via p75 neurotrophin receptor signaling[J]. J Biol Chem,2003,278(25): 23151-62. |
| [30] | 王 超,张会欣,邢邯英,等. 通心络胶囊抑制p38 MAPK磷酸化抑制糖尿病周围神经病变小鼠氧化应激[J]. 中国药理学通报,2015,31(5): 726-30. |
| [30] | Wang C,Zhang H X,Xing H Y,et al.Tongxinluo capsule inhibits oxidative stress in diabetic peripheral neuropathy mice by inhibiting the activity of p-p38 MAPK[J]. Chin Pharmacol Bull,2015,31(5):726-30. |
