


2. 南阳理工学院张仲景国医学院, 河南 南阳 473004
2. Zhangzhongjing Chinese Medicine College, Nanyang Institute of Technology, Henan 473004, China
成年中枢神经再生(neurogenesis)是指哺乳动物成年后中枢神经系统内以神经干细胞(neural stem cells,NSCs)为基础借助适宜环境产生成年新生神经细胞的过程[1]。海马齿状回(dental gyrus,DG)的颗粒细胞下层(subgranular cell zone,SGZ)是成年神经再生的最主要脑区之一。近年来大量的研究提示,抑郁症可能与成年海马神经再生下调引起海马结构可塑性的改变有关[2]。因此,抑制或者逆转海马萎缩,诱导海马成体干细胞增殖分化,促进DG区的神经再生,已经成为抗抑郁研究的一个热点。
我们前期的研究证实,中药复方加味四逆散(Jiaweisinisan,JWSNS)具有确切的抗抑郁效应[3, 4],本研究将通过观察JWSNS对应激性抑郁症大鼠海马DG区神经再生以及脑源性神经营养因子(brain -derived neurotrophic factor,BDNF)和N-甲基-D-天冬氨酸受体(N-methyl-D-aspartate receptor,NMDAR)1(NR1)表达的影响,进一步探讨JWSNS抗抑郁的作用机制。
1 材料与方法 1.1 慢性应激性抑郁症模型采用慢性不可预计轻度应激(chronic unpredictable mild stress,CUMS)动物模型[5]并加以改进:接受应激处理的大鼠单独放在一间房间内,在21 d内随机接受不同类型的应激刺激。应激原包括:限制空间1 h、45°斜笼7 h、湿笼17 h(200 g铺料倒100 mL水,使垫料湿透)、新入侵者(两笼并笼)23 h、持续光照36 h、空瓶1 h、禁食禁水23 h。造模前:所有大鼠单笼饲养1周适应环境。d 1:接受双瓶训练,一瓶是1%(W/V)的蔗糖水(放置在鼠笼的左侧),一瓶是纯水(放置在鼠笼的右侧),训练48 h(d 1 9 :30至d 3 9 :30);d 3: 9 :30开始禁食禁水23 h,至d 4 8 :30;进行1 h糖水消耗实验。根据糖水消耗实验结果和体重情况进行分组。造模期:每天8 :30灌胃,模型组与正常组分房饲养,单笼饲养。d 1 9 :30~10 :30限制空间1 h。d 2,20 :30,至d 3,8 :30持续光照36 h。d 3,9 :30~ 16 :30 45°斜笼7 h。d 4,9 :30,至d 5,8 :30,两笼并笼,新入侵者23 h。d 5,9 :30,开始禁水3 h,12 :30~13 :30空瓶1 h,15 :30,至d 6,8 :30湿笼17 h。d 6,16 :00至d 7 15 :00开始禁食禁水23 h。d 8 8 :30至d 9 20 :30持续光照36 h。d 10 9 :30至d 11 8 :30两笼并笼,新入侵者23 h。d 11 9 :30开始禁水3 h,12 :30~13 :30空瓶1 h;15 :30~16 :30限制空间1 h。d 12 9 :30~16 :30 45°斜笼7 h;16 :30至d 13 9 :30湿笼17 h。d13 9 :30至d 14 8 :30开始禁食禁水23 h。d 14 15 :30~16 :30限制空间1 h。d 15 9 :30至d 16 8 :30两笼并笼,新入侵者23 h。d 16 8 :30至d 17 20 :30持续光照36 h。d 18 9 :30开始禁水3 h,12 :30~13 :30空瓶1 h,15 :30至d 19 8 :30湿笼17 h。d 20 9 :30~16 :30 45°斜笼7 h。16 :00至d 21:15 :00开始禁食禁水23 h。d 21 15 :00~16 :00开始糖水消耗实验(包括测体重)。
1.2 动物及分组给药SPF级Wistar大鼠,♂性,体质量180~220 g,南方医科大学实验动物中心提供,实验动物合格证号:0039901。大鼠单笼饲养,自由摄食饮水,在光暗周期为12h,温度为(23±2)℃的安静环境适应并训练共计2周后,根据糖水消耗实验结果和体重情况进行分组。分为4组:正常组(Control,不施加任何刺激)、模型组(Model)、 JWSNS组(JWSNS,每天早上8 :30灌胃中药复方JWSNS,每次2 mL,相当于临床成人用药剂量的2倍)和盐酸氟西汀组(fluoxetine hydrochloride,每天早上8 :30灌胃1mL·(100 g)-1,相当于临床成人用药剂量的1倍)。正常组及模型组每次灌胃等量蒸馏水。其中正常组大鼠与其余各组大鼠分房饲养。
1.3 主要药品、试剂及仪器JWSNS由柴胡、白芍、枳壳、枸杞子、干地黄等组成。药材由本校第一附属医院药房提供,经药剂科鉴定均为纯正药材。将中药制成粗粉,按比例取以上中药粗粉加8倍量水浸泡30 min,沸腾后文火加热30 min汁;第2煎直接加6倍量水煎煮,沸腾后文火加热30 min取汁。合并两次所得药液,4层纱布过滤,待稍冷却后用旋转蒸发仪浓缩药液至含生药1.69×103 g·L-1药液常温冷却后,置4 ℃冰箱内保存备用。盐酸氟西汀胶囊由Patheon France生产,礼来苏州制药有限公司提供,规格:20 mg/粒,产品批号:8147A,用生理盐水将胶囊内粉末配制成0.18 g·L-1混悬液,4℃冰箱内保存备用。5-溴-2-脱氧脲苷(5-BrdU):购自Sigma公司,批号:20080126。4%多聚甲醛购自国药集团化学试剂有限公司,批号:F20080103。中性树胶购自国药集团化学试剂有限公司,批号:20080513。DEPC购自AMRESCO公司,批号:080210。Triton X-100购自AMRESCO公司,批号:080723。驴血清购自广州蕊特生物科技有限公司,批号:080816。兔来源BrdU抗体购自北京博奥森公司,批号:bs-0917R。Alexa Fluor® 488 donkey anti-rabbit IgG购自MP(invitrogen)公司,批号:439378。Mouse Anti-NeuN购自Millipore公司,批号:LV1519148。Alexa Fluor® 594 donkey anti-mouse IgG购自MP(Invitrogen)公司,批号:56568A。BDNF原位杂交试剂盒、DAB染色试剂盒、原位杂交专用PBS均购自武汉博士德生物工程有限公司。Rabbit polyclonal to BDNF购自Abcam公司,批号76313。Rabbit polyclonal to NMDAR1 a/b/c/d购自Abcam公司,批号:73676。主要仪器:旋转蒸发仪(LABORATA4000,德国Heidolph公司);冰冻切片机(CM 1850型,德国Leica公司);超纯水器(Nexpower 1000,韩国Human coporation公司);pH计(59000-20,美国COLE-PARMER公司);光学显微镜及摄像系统(1X 71,日本OLYMPUS公司);图像分析软件Image-Pro Plus 6.0(Media-Cybornetics,美国)。
1.4 糖水消耗实验所有大鼠在完成1周的单笼饲养适应后,接受1周的双瓶训练,每日清晨添加糖水或纯水。之后所有大鼠禁食禁水23 h,进行1 h糖水消耗实验,测量基础糖水偏爱度和基础体重。经过禁食禁水23 h后,在整个实验进程的d 21 15 :00~16 :00再次进行糖水消耗实验,测量造模后糖水偏爱度和体重。糖水偏爱度/%=造模后糖水偏爱度/基础糖水偏爱度×100%。
1.5 大鼠海马DG区NeuN、BrdU表达检测距离实验取材前3 d(每天固定同一时间)连续使用BrdU腹腔注射(每次用量:50 mg·kg-1,临用时用灭菌生理盐水配制成浓度为10 g·L-1水溶液)。制备冰冻切片:3.5%水合氯醛[35 mg·(100 g)-1,即1 mL·(100 g)-1]腹腔注射麻醉大鼠,经升主动脉灌注生理盐水10 min后换用4%多聚甲醛液(pH 7.14)灌注30 min,断头取脑。脑组织放入4%多聚甲醛,4℃环境下后固定4 h。取出后用PBS表面冲洗2次,再浸入30%的蔗糖PBS溶液中脱水过夜。组织块下沉后取出,ORC包埋冷冻后使用冷冻切片机在距离前囱3.14~4.52 mm的范围内连续冠状切片,片厚20 μm。把切片加载至多聚赖氨酸处理过的载玻片,室温干燥后放入-20℃冰箱保存。免疫组化荧光标记程序:将盛载标本的切片盒从-20℃转置4℃平衡30 min,再转置室温平衡30 min。抗原修复:用耐高温塑料盒盛600 mL柠檬酸盐缓冲液放入高压锅,不加压力阀,加热至液体沸腾,将切片放入沸腾的缓冲液中,加压力阀,继续加热3 min至喷气。冷却至室温取出,用蒸馏水洗5 min,PBS/0.1% Triton洗5 min×3次。冰上用1 mol·L-1 HCl孵育10 min,打开待标记组织细胞的DNA结构。用2 mol·L-1 HCl在室温下孵育10 min,然后转入37℃湿盒内孵育20 min。用0.1 mol·L-1硼酸缓冲液在室温下处理12 min,PBS洗5 min。用5%驴血清(PBS/0.1% Triton、1 mol·L-1甘氨酸稀释)室温下封闭60 min。小心吸去样品周围液体,用混合一抗工作液(PBS/0.1% Triton稀释。NeuN稀释比例1 :200;BrdU稀释比例1 :350)4℃孵育过夜。PBS洗5 min×3次。用混合二抗工作液(PBS/0.1% Triton稀释,稀释比例均为1 :400),室温下避光孵育2 h。PBS洗(避光)5 min×3次。用50%甘油碳酸盐缓冲液封片,避光放置30 min,荧光显微镜下观察拍照。图像的采集和分析:用Image-Pro Plus图像分析软件对图像进行采集和分析。采集过程中在同一视野下分别切换Olympus 1X71显微镜的WB、WG激发滤光片激发样品中的荧光标记物Alexa Fluor® 488、Alexa Fluor® 594,对采集到的图像分组(同一视野下的2张片为一组)以16位灰度图形模式进行保存。分析时用Image-Pro Plus软件载入所保存的图片,按照软件使用指南用颜色通道工具对同组的2张图片进行重叠,将所有照片反相(Invert Image)后在DG区创建AOI,分别计算AOI区域BrdU和NeuN的平均光密度,间接进行平均荧光强度的分析。
1.6 大鼠海马DG区BDNF表达检测制备冰冻切片的步骤同上,然后将切片盒从-20℃转置4℃平衡30 min,再转置室温平衡30 min。免疫组织化学荧光标记程序,一抗工作液:BDNF用PBS/0.25% Triton稀释,稀释比例1 :150。其余步骤同上。原位杂交DAB染色程序:将切片盒从-20℃转置4℃平衡30 min,再转置室温平衡30 min。灭活内源性过氧化物酶:室温下用0.6% H2O2处理30 min,蒸馏水洗涤3次。消化:室温下切片上滴加3%柠檬酸新鲜稀释的胃蛋白酶(1 mL 3%柠檬酸加2滴浓缩型胃蛋白酶,混匀)消化2 min,原位杂交用PBS洗5 min×3次,蒸馏水洗1次。后固定:室温下用1%多聚甲醛/0.1 mol·L-1 PBS(pH 7.2~7.6,含有0.1% DEPC)固定10 min,蒸馏水洗涤3次。预杂交:每张切片加20 μL预杂交液连同湿盒放入40℃恒温箱2 h,吸取多余液体。杂交:每张切片20 μL杂交液,放入38℃恒温箱杂交过夜。杂交后洗涤:揭掉盖切片,37℃水温2×SSC洗涤5 min×2次;37℃ 0.5×SSC洗涤15 min×1次;37℃ 0.2×SSC洗涤15 min×2次。封闭:滴加封闭液放入37℃恒温箱30 min,甩去多余液体。滴加生物素化鼠抗地高辛放入37℃恒温箱60 min,原位杂交用PBS洗5 min×4次。滴加SABC放入37℃恒温箱20 min,原位杂交用PBS洗5 min×3次。滴加生物素化过氧化物酶放入37℃恒温箱20 min,原位杂交用PBS洗5 min×4次。DAB显色:使用DAB显色试剂盒(1 ml蒸馏水加显色剂A、B、C各一滴,混匀)显色20~30 min,充分水洗。封片观察:酒精脱水,二甲苯透明,中性树胶封片,显微镜观察。图像的采集和分析:步骤同上。
1.7 大鼠海马DG区NR1免疫组织化学荧光标记检测制备冰冻切片步骤同上,将切片盒从-20℃转置4℃平衡30 min,再转置室温平衡30 min。免疫组织化学荧光标记程序,一抗工作液:NMDA R1用PBS/0.25% Triton稀释,稀释比例1 :50。其余步骤同上。图像的采集和分析:步骤同上。
1.8 统计学处理实验结果以x± s 表示,采用SPSS 15.0统计软件进行t检验、方差分析。
2 结果 2.1 各组大鼠糖水偏爱度的变化与正常组比较,模型组大鼠糖水偏爱度明显下降(P <0.01)。与模型组比较,JWSNS组和Fluoxetine hydrochloride组大鼠糖水偏爱度没有下降(P <0.01,Tab 1)。
| Group | Sucrose preference/% |
| Control | 0.95±0.03 |
| Model | 0.78±0.05** |
| JWSNS | 0.93±0.03△△ |
| Fluoxetine hydrochloride | 0.92±0.03△△ |
| **P<0.01 vs control;△△P<0.01 vs model | |
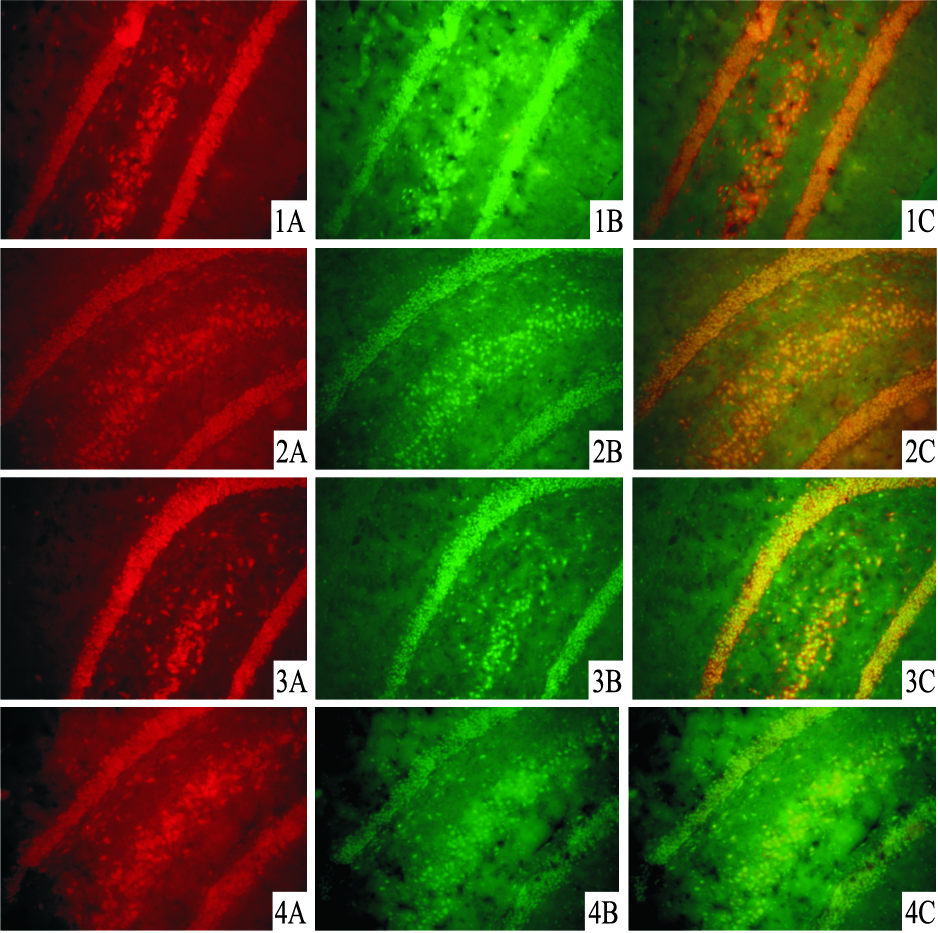
海马部位的CA3区和DG区为NeuN阳性标记的集中区,BrdU阳性标记的细胞散在海马各处,以CA3区和DG区最为集中。模型组、JWSNS组以及Fluoxetine hydrochloride组BrdU标记的平均荧光强度值均低于正常组(P<0.01),JWSNS组和Fluoxetine hydrochloride组的平均荧光强度值高于模型组(P<0.01)。
模型组和西药组的NeuN标记平均荧光强度值明显低于正常组(P<0.01)。JWSNS组平均荧光强度值明显高于模型组(P<0.05)和Fluoxetine hydrochloride组(P<0.01)。
BrdU-NeuN联合标记平均荧光强度值的比较结果表明,模型组高于正常组(P<0.01)。BrdU-NeuN联合标记平均荧光强度值与BrdU标记平均荧光强度值比值的比较结果表明,模型组、JWSNS组以及Fluoxetine hydrochloride组均明显高于正常组(P<0.01)。JWSNS组明显低于模型组(P<0.01)和Fluoxetine hydrochloride组(P<0.05,Tab 2,Fig 1)。
| Group | Mean fluorescence intensity(BrdU tag)(A) | Mean fluorescence intensity(NeuN tag)(B) | Mean fluorescence intensity (BrdU-NeuN combined tag)(C) | (C)/ (A) |
| Control | 0.433±0.074 | 0.497±0.052 | 0.451±0.129 | 0.876±0.247 |
| Model | 0.287±0.077** | 0.359±0.086** | 0.597±0.086** | 1.507±0.075** |
| JWSNS | 0.388±0.094△△ | 0.460±0.080△## | 0.470±0.066 | 1.207±0.107**△△ |
| Fluoxetine hydrochloride | 0.383±0.101△△ | 0.329±0.149** | 0.521±0.089 | 1.397±0.190** |
| **P<0.01 vs control;△P<0.05,△△P<0.01 vs model;##P<0.01 vs Fluoxetine hydrochloride | ||||
|
| Fig 1 Immunofluorescence tag of expression of NeuN A line:nerve cells tagged by NeuN;B line:proliferated cells tagged by BrdU;C line:A and B. The 1 st row:Control;The 2 nd row:Model;The 3 rd row:JWSNS;The 4 th row:Fluoxetine hydrochloride |
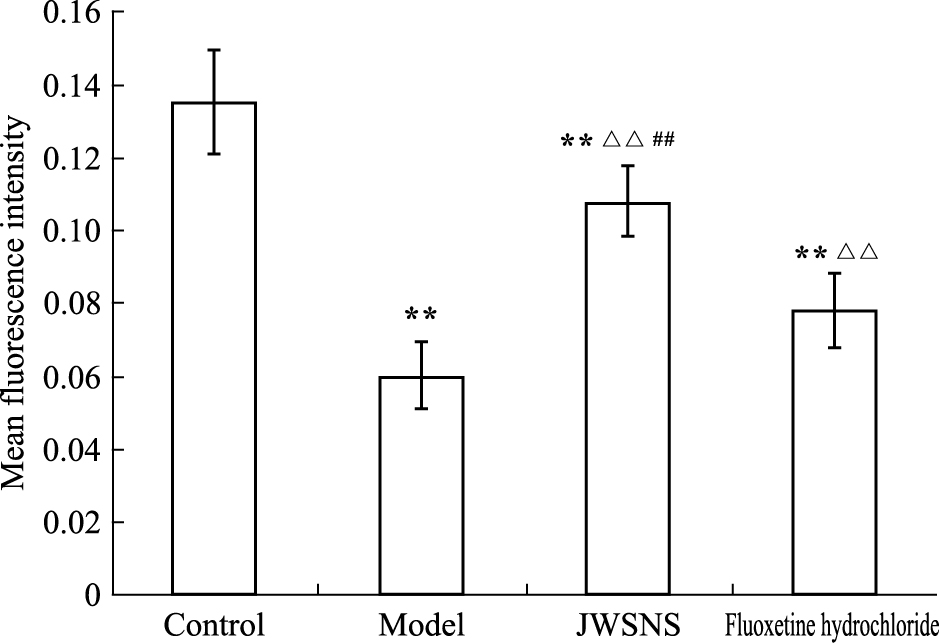
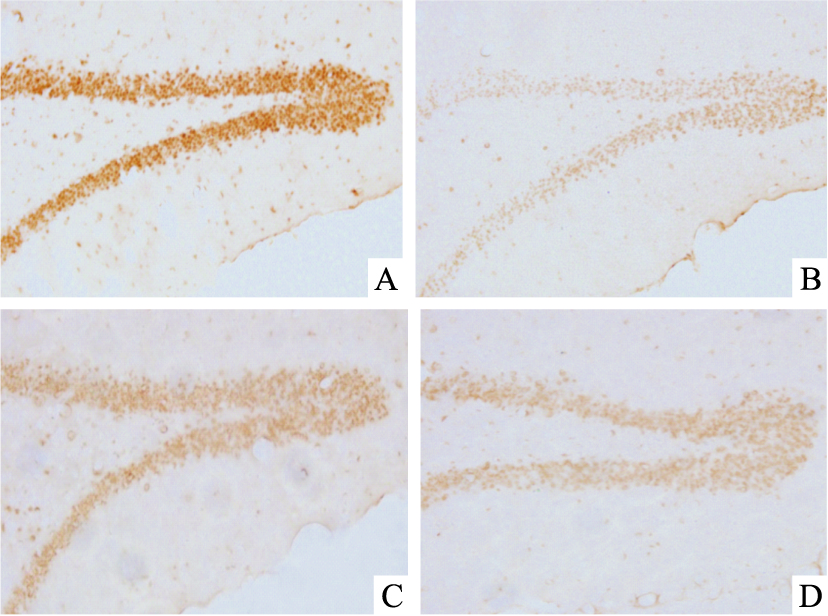
海马BDNF阳性表达的区域主要集中于CA3区和DG区。与正常组相比,模型组BDNF表达的平均荧光强度值明显减弱(P<0.01)。与模型组相比,JWSNS组和Fluoxetine hydrochloride组平均荧光强度明显升高(P<0.01),BDNF表达增强。与Fluoxetine hydrochloride组相比,JWSNS组BDNF表达明显增高(P<0.01,Fig 2,3)。
|
| Fig 2 Mean fluorescence intensity of BDNF expression in **P<0.01 vs control;△△P<0.01 vs model;##P<0.01 vs Fluoxetine hydrochloride |
|
| Fig 3 Expression of BDNF in hippocampal A:Control;B:Model;C:JWSNS;D:Fluoxetine hydrochloride |
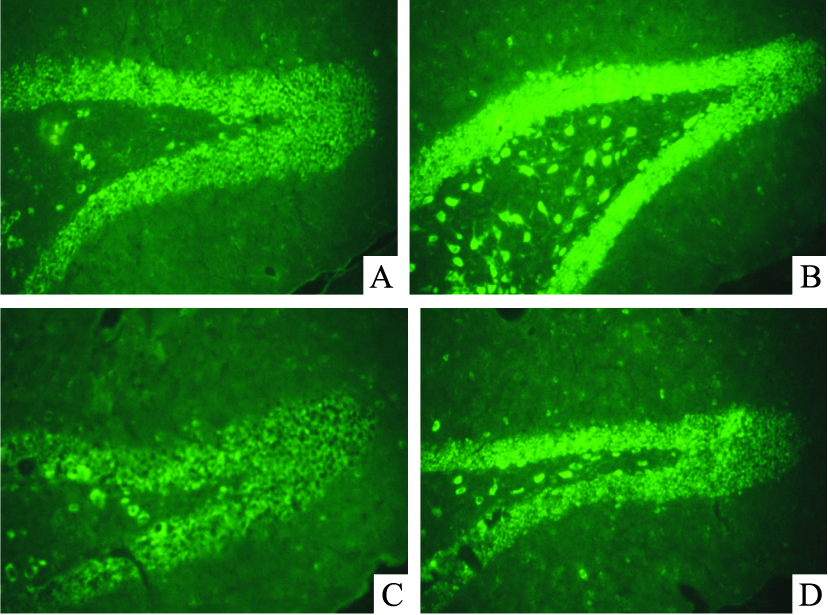
海马NMDA R1阳性表达的区域主要集中于CA3区和DG区。与正常组相比,模型组NMDA R1表达的平均荧光强度值明显升高(P<0.01)。与模型组相比,JWSNS组和Fluoxetine hydrochloride组平均荧光强度明显降低(P<0.01),NMDA R1表达减弱。JWSNS组与Fluoxetine hydrochloride组相比,差异无显著性(Fig 4,5)。

|
| Fig 4 NMDA R1 expression in hippocampal DG **P<0.01 vs control;△△P<0.01 vs model |
|
| Fig 5 Immunofluorescence tag of expression of NMDA A:Control;B:Model;C:JWSNS;D:Fluoxetine hydrochloride |
海马是情绪整合和高级精神活动中枢,海马DG区的颗粒细胞下层存在的神经前体细胞(neuronal progenitor cells,NPCs)可逐渐增殖、分化、迁移进入颗粒层,产生树、轴突并不断发生可塑性变化,与周围神经元形成突触联系,整合到海马功能的神经环路中。各类研究证实应激和抑郁症患者的海马体积发生改变,表现为海马萎缩及神经元的减少[6]。虽然目前尚未清楚海马萎缩与抑郁症之间的因果关系,但研究发现,抗抑郁药在细胞水平产生的一个明显效应就是促进成年海马的神经再生[7]。因此,成熟脑海马神经再生是抑郁障碍治疗的一个重要靶点。
BrdU标记平均荧光强度值主要反映单位面积中新增殖细胞的量的多少,而NeuN标记平均荧光强度值主要反映单位面积中神经细胞的量的多少。本研究发现,应激性抑郁症大鼠海马DG区中处于增殖状态的神经细胞数量以及单位面积的神经元数量出现下降,说明慢性应激能抑制海马前体细胞的增殖,导致海马神经元损伤和再生障碍。JWSNS和氟西汀能增加DG单位面积中神经元数目和新增殖细胞量,具有促进海马神经再生的效应。
脑源性神经营养因子(brain -derived neurotrophic factor,BDNF)广泛存在于中枢和外周神经系统,具有神经再生和修复功能。在动物实验中,慢性应激和促抑郁条件会导致海马部位BDNF表达减少,海马区神经元凋亡增加,再生能力降低[8]。大鼠DG区注入BDNF可以增加神经再生,并能在行为学上产生抗抑郁的效果;阻断BDNF的表达可以发现,海马DG区的神经再生受到抑制,并出现抑郁症相关的行为学改变[9]。因此,中枢BDNF表达水平的升高或降低与人或动物抑郁样行为的表现密切相关。本研究发现,应激性抑郁症大鼠海马DG区BDNF表达下降,而JWSNS和氟西汀能增强抑郁症大鼠BDNF的内源性合成和分泌表达。
谷氨酸是一种重要的兴奋性中枢神经递质,谷氨酸调控的突触及神经可塑性在抑郁症的神经生物学基础及抑郁症的治疗中都非常关键[10]。研究表明,其在精神分裂症、情感障碍和神经发育障碍中都占有重要的地位。谷氨酸受体分为离子型和代谢型,N-甲基-D-天冬氨酸(N-methyl-D-aspartate,NMDA)受体是离子型的谷氨酸受体。NMDA受体(NR)的亚基按基因型分为:NR1、NR2(A、B、C和D)和NR3(A和B)3个家族,其中,NR1为NR必需的功能亚基,而亚单位NR1、NR2B与抑郁症的关系最为密切[11]。应激可导致海马细胞外谷氨酸浓度的增加,使NR过度激活,NR兴奋时主要引起Ca2+、Na+内流以及K+外流,从而引起胞内信号通路激活,而过量的钙离子内流则会引起神经元的死亡,导致抑郁的发生[12]。激活NR可以抑制海马神经前体细胞增殖,阻断此受体会出现相反的结果。NR通过配体门控性Ca2+超载介导海马的神经再生过程。因此内源性的谷氨酸水平和NR的活性是维持神经再生的重要因素[6]。本研究发现,慢性应激使大鼠海马DG区NR1的表达明显升高,从而对DG区的神经元产生兴奋性毒性作用。JWSNS和氟西汀能逆转NR1的过度表达,减弱神经兴奋性毒性作用,提高神经细胞的存活率,促进海马神经再生。
综上所述,JWSNS能够促进慢性应激性抑郁症大鼠海马DG区神经细胞的增殖,并能通过增强BDNF表达和降低N R1表达,发挥促进海马DG区神经再生的效应。
(致谢:本文实验在广州中医药大学国家级重点学科中医基础理论治则治法实验室完成,参与人员除论文作者外,还有王剑研究员、硕士生刘书考、任雪梅,在此一并致谢!)
| [1] | Abrous D N, Koehl M, Le Moal M. Adult neurogenesis:from precursors to network and physiology[J]. Physiol Rev, 2005, 85(2):523-69. |
| [2] | Suk Y Y, Benson W M L, Tong J B, et al. Hippocampal neurogenesis and dendritic plasticity support running-improved spatial learning and depression-like behaviour in stressed rats[J]. PLoS One, 2011, 6(9):e24263. |
| [3] | Wu L L, Ran C L, Liu S K, et al. Jiaweisinisan facilitates neurogenesis in the hippocampus after stress damage[J].Neural Regen Res, 2013, 8(12):1091-102. |
| [4] | 吴丽丽, 严 灿, 丁胜元, 等.加味四逆散抗应激性抑郁效应及其海马NMDA受体通道机制的初步研究[J].中国药理学通报, 2007, 23(11):1425-31. Wu L L, Yan C, Ding S Y, et al. The initial research on the effect of anti-stressed depression of Jiaweisinisan and it's mechanism of N-methyl-D-aspartate receptor channel in hippocampus[J]. Chin Pharmacol Bull, 2007, 23(11):1425-31. |
| [5] | Willner P, Benton D, Brown E.Depression increases, craving for sweet rewards in animal and human models of depression and craving[J].Psychopharmacology, 1998, 136 (3):272-83. |
| [6] | 盖海军, 王秀艳, 袁 念, 等.成熟海马神经再生在抑郁症及应激发病机制中的作用[J].国际精神病学杂志, 2014, 41(4):225-8. Gai H J, Wang X Y, Yuan N, et al. Role of mature hippocampal neurogenesis in the pathogenesis of depression and stress[J]. Int J Psych, 2014, 41(4):225-8. |
| [7] | 高宇博, 李亮萍, 朱心红, 等.抑郁神经生物学机制研究新进展[J].生理学报, 2012, 64(4):475-80.Gao Y B, Li L P, Zhu X H, et al. Recent progress in neurobiological mechanisms of depression[J]. Acta Physiol Sin, 2012, 64(4):475-80. |
| [8] | Teche S P, Nuernberg G L, Sordi A O, et al. Measurement methods of BDNF levels in major depression:aqualitative systematic review of clinical trials[J]. Psychiatry Q, 2013, 84(4):485-97. |
| [9] | Taliaz D, Stall N, Dar D E, et al. Knockdown of brain-derived neurotrophic factor in specific brain sites precipitates behaviors associated with depression and reduces neurogenesis[J]. Mol sychiatry, 2010, 15(1):80-92. |
| [10] | 张 兵, 李 扬. 针对谷氨酸能系统的抗抑郁药物的研究进展[J]. 中国药理学通报, 2014, 30(9):1197-200. Zhang B, Li Y. Research progress of the antidepressants targeting the glutamate receptors[J].Chin Pharmacol Bull, 2014, 30(9):1197-200. |
| [11] | Costa B M, Irvine M W, Fang G, et al. A novel family of negative and positive allosteric modulators of NMDA receptors[J]. J Pharmacol Exp Ther, 2010, 335(3):614-21. |
| [12] | Goussakov I, Miller M B, Stutzmann G E.NMDA-mediated Ca2+ influx drives aberrant ryanodine receptor activation in dendrites of young Alzheimer's disease mice[J]. J Neurosci, 2010, 30(36):12128-37. |

