


肺炎支原体(mycoplasma pneumonia,MP)是引起呼吸道感染常见的病原体,其引起的肺炎支原体肺炎(mycoplasma pneumoniae pneumonia,MPP)占小儿肺炎发病率的20%以上,且呈逐年递增的趋势。由于其无细胞壁,目前临床上对于MPP的治疗主要应用大环内酯类抗生素,但是该类抗生素长期或反复使用不良反应大、副作用强,在杀灭支原体的同时对患者的机体造成一定的损伤,并且近年来有数据表明其耐药率呈逐年上升的趋势[1]。因此,开发一种既可以杀灭支原体,又可以促进受损肺组织修复的药物显得尤为重要。
芩百清肺浓缩丸(以下简称“芩百”,Qinbai)是我院自主研发,国家批准第一个用于临床研究治疗小儿支原体肺炎的中药新药。由黄芩、百部、地龙、桔梗、麦冬、紫菀6味中药组成,具有清热解毒、润肺止咳之功效。研究表明,其对支原体肺炎具有较好的治疗作用,并能够提高机体免疫功能,促进气道组织及上皮细胞的修复[2, 3, 4, 5]。
本研究通过比较给药前后,肺炎支原体感染大鼠肺组织中转化生长因子-β(transforming growth factorβ,TGF-β)和表面活性物质相关蛋白A(surfactant-associated protein A,SP-A)表达的变化,阐明芩百清肺浓缩丸对肺泡Ⅱ型上皮细胞(type Ⅱ alveolar epithelial cell,AEC-Ⅱ)的修复作用,从而为其促进肺组织修复、恢复肺功能的作用机制提供理论基础。
1 材料 1.1 试药芩百清肺浓缩丸(哈尔滨天合力制药有限公司,批号130701),本品为棕褐色的薄膜包衣浓缩水丸,经检查符合2010年版《中华人民共和国药典》丸剂下的各项规定。
1.2 试剂肺炎支原体国际标准株(ATCCFH15531,购自美国菌种保藏中心);PPLO培养基(Becton,Dickinson and Company,USA);IL-6、IL-8及TNF-α酶联检测试剂盒(Uscn公司);TRIzol试剂(美国Invitrogen,批号66211);Transcriptor first strand cDNA Synthesis Kit(Roche公司,批号1485422);FastStart Universal SYBR Green Master(ROX)(Roche公司,批号10277200);SP-A、TGF-β、β-actin引物(哈尔滨博仕生物技术有限公司);TGF-β多克隆抗体(ABCAM公司);SP-A多克隆抗体(SANTA公司);高效RIPA组织/细胞裂解液(北京索莱宝科技有限公司);PMSF(Calbiochem公司);BCA蛋白浓度测定试剂盒、SDS-PAGE凝胶配制试剂盒(碧云天公司);PVDF膜(Millipore公司)。
1.3 动物60只80~100 g的Wistar大鼠♀♂各半,长春亿斯实验动物技术有限公司提供,SPF级,许可证号:SCXK(吉)2011-0004。
1.4 仪器SorvaⅡ ST16低温离心机(Thermo公司);KD-TS3A自动组织脱水机(浙江金华科迪仪器设备有限公司);KD-BM生物组织包埋机(浙江金华科迪仪器设备有限公司);RM2235组织切片机(德国莱卡);BX4-1生物显微镜(OLYMPUS公司);DP-72组织生物信号采集分析系统(OLYMPUS公司);Infinite M200 Pro酶标仪(Tecan公司);9600定量PCR检测仪(杭州博日);VersaDoc 400mp凝胶成像系统(BIO-RAD公司);DYCZ-24DN电泳槽(北京六一仪器厂);PowerPac Universal电泳仪(BIO-RAD公司);半干转膜仪(BIO-RAD公司)。
2 方法 2.1 动物分组、造模及给药60只Wistar大鼠随机分为6组,每组10只,♀♂各半,分别为空白对照组,模型对照组,阳性对照药组,芩百高、中、低剂量组。大鼠适应性饲养1周后,用1%戊巴比妥钠腹腔注射麻醉,除空白对照组外,其余各组大鼠感染106 CCU/mL MP菌液50 μL,空白对照组滴入等量MP培养液。感染后d 2开始灌胃给药,每日1次,空白对照组和模型对照组灌胃等容积生理盐水;阳性对照组灌胃阿奇霉素(首次给药量为45 mg·kg-1·d-1,d 2~5为22.5 mg·kg-1·d-1),连续给药5 d;芩百高(3.2 g·kg-1·d-1)、中(1.6 g·kg-1·d-1)、低(0.8 g·kg-1·d-1)剂量组连续给药10 d。1%戊巴比妥钠麻醉,腹主动脉取血,分离血清-80℃冻存,用于检验血清中IL-6、IL-8及TNF-α的含量;剪取肺组织称重后取左肺组织4%甲醛固定,用于HE染色;取右肺组织中叶,用于提取RNA和蛋白质;剪取脾、胸腺称重,用于计算脏器指数。
2.2 HE染色实验取甲醛固定的肺组织,用乙醇梯度脱水,二甲苯透明2次,放入石蜡内进行包埋。蜡块修好后固定于石蜡切片机上切片,将完全展开的蜡片贴附于清洁载玻片上,常规HE染色,在显微镜下进行MP特异性病变间质性肺炎的病理组织学检查。
2.3 大鼠血清中IL-6、IL-8及TNF-α的测定采用ELISA法检测,操作程序按照ELISA试剂盒说明书进行。
2.4 大鼠肺组织TGF-β、SP-A mRNA检测以实时荧光定量PCR法检测TGF-β和SP-A mRNA的表达。提取RNA,用酶标仪对RNA纯度及浓度进行测定,根据RNA浓度调整总RNA的体积,使各样品逆转录体系所含的RNA量相同,将RNA逆转录为cDNA,以逆转录合成的cDNA为模板,进行聚合酶链反应。引物序列[6, 7, 8]:TGF-β上游5′-GGCGGTGCTCGCTTTGTA-3′,下游5′-GCCACTCAGGCGTATCAG-3′;SP-A上游5′-TAAGTGCTGCCCTCTGACCT-3′,下游5′-AGGAGCCATACATGCCAAAC-3′;β-actin上游5′-CGTTGACATCCGTAAAGAC-3′,下游5′-TGGAAGGTGGACAGTGAG-3′。
2.5 大鼠肺组织TGF-β、SP-A蛋白检测按试剂盒操作步骤提取并检测蛋白浓度,相同蛋白浓度加入12% SDS-PAGE凝胶分离并转印到PVDF膜上。PVDF膜用5%脱脂奶粉封闭3h,加入一抗稀释液,4℃孵育过夜,然后将膜与二抗稀释液在室温下摇床孵育1 h。最后用化学发光试剂显色,在凝胶成像仪中拍照。
2.6 统计学分析采用SPSS18.0软件进行统计学分析,数据用x± s 表示,组间均数比较采用F检验,两两比较用Dunnett’t检验。
3 结果 3.1 大鼠肺组织病理变化来自于动物左肺的组织全部被检玻片均随机化检测。评分系统由1个0~26分范围的可数评分组成[9],5个分类评价系统由管腔周围浸润而致的细支气管和支气管的数目、管腔周围浸润的程度、管腔内渗出的严重度、血管周围浸润的频度、实质性肺炎的严重度合并后记分,每张切片选择5个视野评分。
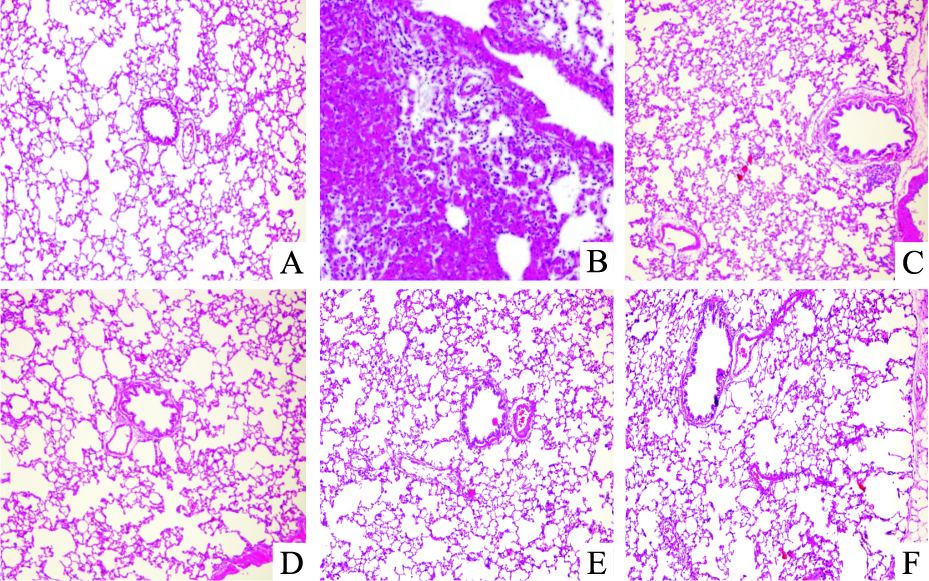
空白组可见肺泡结构清晰,肺泡壁薄,肺泡腔内未见水肿液,肺组织中未见炎性细胞浸润。模型组可见明显的炎症,病变性质为间质性肺炎和细支气管肺炎,肺泡壁增厚、水肿、脱落,气管支气管周围及其腔内、血管周围及肺泡腔内伴以淋巴细胞为主的炎性细胞浸润,严重者伴有红细胞渗入。而芩百各组的肺组织相对于模型组上述改变明显减轻,呈现明显的量效关系(Tab 1,Fig 1)。
| Group | Dose/g·kg-1·d-1 | Value |
| Blank | - | 0.6±0.7 |
| Model | - | 15.1±4.31△△ |
| Azithromycin | 1 st 0.045 | 5.6±2.80** |
| d 2~5 0.0225 | ||
| Qinbai (High) | 3.2 | 6.2±0.84** |
| Qinbai (Middle) | 1.6 | 9.2±1.48** |
| Qinbai (Low) | 0.8 | 11.6±1.14 |
| △△P <0.01 vs blank;**P <0.01 vs model | ||
|
| Fig 1 Pathological detection of lung tissue of rats(HE×20) A:Blank; B: Model; C: Azithromycin; D:Qinbai(High); E:Qinbai(Middle);F:Qinbai(Low) |
与空白组比较,模型组肺指数、脾指数明显增加(P <0.05),胸腺指数明显降低(P <0.01)。各给药组肺指数降低,但与模型组比较,差异无显著性;胸腺指数明显增加(P <0.05);脾指数明显降低(P <0.05)(见Tab 2)。
| Group | Dose/g·kg-1·d-1 | index of lung/g·kg-1 | index of thymus/g·kg-1 | index of spleen/g·kg-1 |
| Blank | - | 8.21±1.67 | 1.51±0.57 | 4.35±0.86 |
| Model | - | 10.65±2.14△ | 1.05±0.31△△ | 6.06±2.04△ |
| Azithromycin | 1 st 0.045 | 9.11±1.92 | 1.72±0.63** | 4.54±0.93* |
| d 2~5 0.0225 | ||||
| Qinbai(high) | 3.2 | 8.72±1.84 | 1.81±0.46** | 4.52±0.88* |
| Qinbai(middle) | 1.6 | 9.18±1.92 | 1.63±0.38** | 4.86±0.91* |
| Qinbai(low) | 0.8 | 9.71±2.01 | 1.49±0.44* | 5.12±0.62* |
| △P <0.05,△△P <0.01 vs blank;*P <0.05,**P <0.01 vs model | ||||
由Tab 3可知,与空白组比较,模型组大鼠血清中IL-6、IL-8和TNF-α水平均明显升高(P <0.05);与模型组比较,各给药组中3者数值均有所下调,其中阿奇霉素组及芩百高、中组对IL-6、IL-8的下调作用明显(P <0.05),而阿奇霉素组及芩百高剂量组对TNF-α的下调明显(P <0.05)。
| Group | Dose/g·kg-1·d-1 | IL-6/μg·L-1 | IL-8/μg·L-1 | TNF-α/μg·L-1 |
| Blank | - | 338.23±45.45 | 187.05±35.36 | 1.26±0.36 |
| Model | - | 421.77±42.35△ | 267.32±33.94△ | 2.12±0.54△ |
| Azithromycin | 1 st 0.045 | 365.92±51.27* | 200.18±29.65* | 1.43±0.65* |
| d 2~5 0.0225 | ||||
| Qinbai(high) | 3.2 | 353.28±43.25* | 195.25±36.74* | 1.38±0.57* |
| Qinbai(middle) | 1.6 | 368.72±39.76* | 211.69±34.23* | 1.74±0.62 |
| Qinbai(low) | 0.8 | 398.26±38.93 | 235.37±38.72 | 1.89±0.73 |
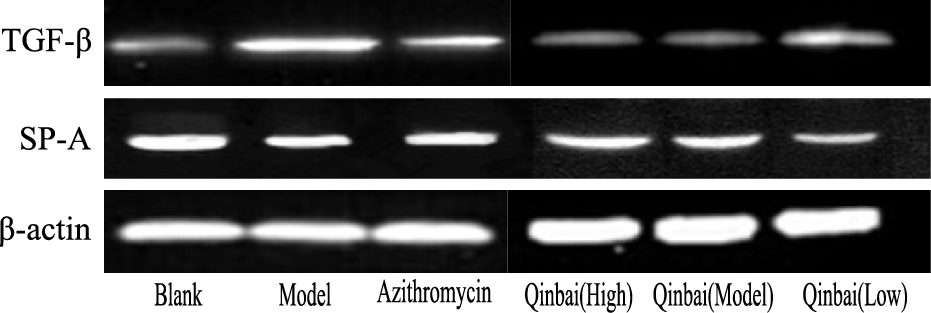
结果显示,与模型组比较,芩百各剂量组TGF-β基因和蛋白表达明显下降(P <0.05),且高剂量组下降明显;而SP-A基因和蛋白表达明显增加(P <0.05),同样,高剂量组表达更加明显(Tab 4,5,Fig 2)。
|
| Fig 2 Protein expression levels of TGF-β and SP-A in lung tissue of rats |
| Group | Dose/g·kg-1·d-1 | TGF-β /β-actin | SP-A /β-actin |
| Blank | - | 0.978±0.023 | 0.980±0.029 |
| Modle | - | 4.75±0.64△△ | 0.263±0.005△△ |
| Azithromycin | 1 st 0.045 d 2~5 0.0225 | 2.50±0.41** | 0.560±0.077* |
| Qinbai(high) | 3.2 | 2.49±0.43** | 0.748±0.047** |
| Qinbai(middle) | 1.6 | 2.64±0.46** | 0.490±0.051* |
| Qinbai(low) | 0.8 | 3.71±0.81* | 0.327±0.043 |
| △△P <0.01 vs blank;*P <0.05,**P <0.01 vs model. | |||
| Group | Dose/g·kg-1·d-1 | TGF-β /β-actin | SP-A /β-actin |
| Blank | - | 0.23±0.05 | 0.85±0.10 |
| Model | - | 0.79±0.16△ | 0.24±0.08△ |
| Azithromycin | 1 st 0.045 d 2~5 0.0225 | 0.33±0.04** | 0.68±0.10** |
| Qinbai(high) | 3.2 | 0.36±0.07** | 0.65±0.08** |
| Qinbai(middle) | 1.6 | 0.37±0.06** | 0.48±0.13** |
| Qinbai(low) | 0.8 | 0.66±0.02 | 0.31±0.12 |
| △△P <0.01 vs blank;*P <0.05,**P <0.01 vs model | |||
MPP的主要病理表现为间质性肺炎,通过本实验可以看出,芩百各剂量组能够明显减轻MP感染引起的大鼠肺部间质性炎症的改变,使肺组织形态结构趋向正常,损伤得到修复。对各组病理组织按照制定的评分标准进行半定量积分,与直接观察病理组织比较能更客观地评价疾病的轻重程度,评分后进行统计分析,可以更直观地比较各组之间的差异,使结果更具有统计学意义。通过对大鼠脏器指数的测定可知,芩百还可以改善肺指数、胸腺指数及脾指数,提示其能够杀灭清除体内的MP,对免疫器官刺激减轻,能够调节由MP引起的免疫紊乱情况。
MP侵入人体后,可刺激淋巴细胞等产生IL-2、IL-6、IL-8、IL-10及TNF-α等多种细胞因子。正常情况下,这些因子对机体具有保护作用,但如果过度分泌则会引起疾病的产生及炎症的加重。已有研究表明IL-6、IL-8及TNF-α的大量释放是引起继发性肺损伤的重要因素之一,目前已被研究人员和临床医生所认可,认为其作为MPP临床诊断指标更为敏感[10]。本实验结果表明,芩百能够明显降低大鼠血清中上述炎症因子的表达,从而减轻肺部炎症反应,肺损伤得到修复。
MP感染后反复发作,迁延不愈是临床治疗的难点,尤其多次复发后引起MP耐药是目前MPP治疗的最大难题。MPP的发病机制复杂,由MP感染引起的上皮间质转化可能是其难痊愈原因之一。AEC-Ⅱ是肺泡上皮的干细胞,是合成和分泌肺泡表面活性物质及其相关蛋白的主要细胞。当MP感染宿主时,MP与AEC-Ⅱ细胞膜上的SP-A结合,激活巨噬细胞等炎细胞吞噬作用,释放TGF-β等细胞因子,TGF-β与上皮细胞相应受体结合,细胞支架重排,促进AEC-Ⅱ发生上皮间质转化(EMT),其特征是失去上皮特性获得间质属性。AEC-Ⅱ损伤后,上皮通透性增加,肺表面活性物质相关蛋白的合成和分泌降低[11]。因此,TGF-β在AEC-Ⅱ发生EMT过程中起着非常重要的作用[12]。TGF-β能够诱导肺泡上皮细胞向间质转化,引发间质性肺炎,严重者导致肺纤维化,作用通路与Smad信号转导途径相关[6],也有研究报道TGF-β能激活非Smad介导的细胞信号途径[13]。还有人认为,TGF-β能够抑制上皮细胞增生,其表达升高可能减弱上皮细胞的再生能力,从而间接影响呼吸道的修复[14],而呼吸道生理结构的不完整又为MP再次感染提供了适宜条件。因此,对MPP的治疗不仅仅限于清除病原微生物上,更应该抑制炎症反应进程,促进各炎症因子间平衡制约,加快上皮细胞修复,使呼吸道微环境恢复至正常生理状态。本实验结果表明芩百各剂量组能够降低TGF-βmRNA和蛋白的表达,说明其能够抑制AEC-Ⅱ发生EMT,使AEC-Ⅱ得到修复,恢复其正常生理功能。
EMT的主要表现为上皮细胞丢失上皮标记物,其最具特征的表面标记物是表面活性蛋白(SP-A、SP-B和SP-C),而这些蛋白中SP-A最早被发现,且在AEC-Ⅱ中表达最强烈,信号最丰富的蛋白,约占SP总量的50%,是表面活性物质(PS)最重要的蛋白成分,其主要生理功能为降低肺泡表面张力,促进液体吸收,防止肺萎陷和肺水肿,以及对维持肺泡正常结构和稳定通气具有重要作用;还参与调节肺的局部免疫和炎症反应,并在多种因素致肺损伤中对肺泡具有保护作用。
MP感染宿主后,与SP-A结合,刺激巨噬细胞和中性粒细胞,产生大量细胞因子和炎症介质,打破了炎症介质/抗炎介质的平衡。此时,炎症介质对AEC-Ⅱ的作用使SP-A mRNA的表达受到影响,AEC-Ⅱ凋亡、裂解、坏死使AEC-Ⅱ数目减少,而AEC-Ⅱ在短时间内不能及时增生,凋亡、坏死的AEC-Ⅱ不能及时得到补充和代偿,所有这些导致SP-A mRNA下调。随着SP-A mRNA下调效应的积累、叠加与放大,AEC-Ⅱ内SP-A的生成减少,肺组织中SP-A蛋白表达逐渐下降。本实验结果表明,芩百各剂量组可使炎症介质水平降低,炎症介质对SP-A mRNA的抑制作用减弱,AEC-Ⅱ得到修复、增生使SP-A mRNA表达增强,同时随着SP-A基因表达的增多,被翻译蛋白量增加,其蛋白表达提高。
本研究阐明了芩百清肺浓缩丸通过降低TGF-β表达,抑制AEC-Ⅱ发生EMT,促进AEC-Ⅱ合成和分泌SP-A,SP-A表达增加,对肺组织起到保护和修复的作用,恢复其正常形态和生理功能。
(致谢:本实验在我院动物室、药理室完成,感谢以上科室崔花子、张志华两位老师的指导,张俊威、王博两位同事的帮助以及隋美娇同学的配合。)
| [1] | 马晓丽,郑跃杰.肺炎支原体对大环内酯类药物耐药研究[J].临床儿科杂志,2013,31(6):596-7. Ma X L,Zheng Y J. Study on Mycoplasma pneumoniae resistance to Macrolide[J].J Clin Pediatr Vol,2013,31(6):596-7. |
| [2] | 王伟明,张俊威,许庆瑞,等.芩百清肺浓缩丸体内外抗肺炎支原体作用的实验研究[J].中草药,2008,39(5):742-5. Wang W M,Zhang J W,Xu Q R,et al. Experiment study on Qinbaiqingfei concentrated pellets against Mycoplasma pneumoniae in vitro and vivo[J].Chin Tradit Herb Drugs,2008,39(5):742-5. |
| [3] | 王伟明,李继昌,张洪娟,等.呼畅清肺浓缩丸对肺炎支原体感染鼠肺组织钙粘附分子表达的研究[J].中国中药杂志,2005,30(21):1682-6. Wang W M,Li J C,Zhang H J,et al. Effect of Huchang Qingfei concentrated pellets on E-cadherin expression in lung tissue of mice infected with Mycoplasma pneumoniae[J]. China J Chin Mat Med,2005,30(21):1682-6. |
| [4] | Meng Y L,Huo J H,Lu W H,et al.Modulation of P1 and EGF expression by baicalin[J].Int J Mol Sci,2012,14(1):146-57. |
| [5] | 蒙艳丽,杨阳,王欣,等.芩百清肺浓缩丸对肺炎支原体感染模型小鼠和细胞肺表皮生长因子表达的影响[J].中华中医药杂志,2014,29(4):1089-92. Meng Y L,Yang Y,Wang X,et al. Qinbaiqingfei Pellets influence the epithelial growth factor on M.pneumoniae-infected cells or mice[J].China J Tradit Chin Med Pharm,2014,29(4):1089-92. |
| [6] | 徐国萍,徐达,李海霞,等.TGF-β1诱导的肺泡Ⅱ型上皮细胞向间质细胞转变[J].复旦学报(医学版),2007,34(2):223-7. Xu G P,Xu D,Li H X,et al. Epithelial-mesenchymal transition of type Ⅱ alveolar epithelial cells induced by TGF-β1[J]. Fudan Univ J Med Sci,2007,34(2):223-7. |
| [7] | 何蓉.高氧肺损伤新生大鼠肺组织中肺表面活性物质相关蛋白-A(SP-A)的mRNA和蛋白表达及布地奈德的干预作用[D].苏州:苏州大学硕士学位论文.2013:10-1.He R. Budesonide impact on the expression of pulmonary surfactant protein-A (SP-A) in hyperoxia-induced lung injury in neonatal rats[D]. Suzhou:Soochow University,2013:10-1. |
| [8] | Qiongjie H,Huilan Z,Shengdao X,et al.The alteration and significance of surfactant protein a in rats chronically exposed to cigarette smoke[J].J Huazhong Univ Sci Technol,2008,28(2):128-31. |
| [9] | Martin R J,Chu H W,Honour J M. Airway inflammation and bronchinal hyperresponsiveness after Mycoplasma pneumoniae infection in a murine model[J]. Am J Respir Cell Mol Biol,2001,24(5):577-82. |
| [10] | 滕宁燕.支原体肺炎患儿血清TNF-α、IL-6、IL-8的检测及临床意义[J].中华医院感染学杂志,2012,22(3):533-5. Teng N Y. Detection of TNF-α、IL-6、IL-8 levels in serum of chidren with Mycoplasma pneumoniae and its clinical significance[J].Chin Nosocomiol,2012,22(3):533-5. |
| [11] | 杨青,王桂芳.肺泡Ⅱ型上皮细胞功能的研究进展[J].复旦学报(医学版),2012,39(6):658-62.Yang Q,Wang G F.Advances in researches on the functions of alveodar epithelial type Ⅱcells[J]. Fudan Univ J Med Sci,2012,39(6):658-62. |
| [12] | Zhou B,Buckley S T,Patel V,et al. Troglitazone attenuates TGF-β1-induced EMT in alveolar epithelial cells via a PPARγ-independent mechanism[J].PLoS One,2012,7(6):e38827. |
| [13] | 刘理静,于小华,张平. 白藜芦醇通过TGF-β1/ADAMTS-1信号通路抑制肺纤维化[J].中国药理学通报,2013,29(3):425-31. Liu L J,Yu X H,Zhang P. Resveratrol inhibits pulmonary fibrosis through TGF-β1/ADAMTS-1 signaling pathway[J]. Chin Pharmacol Bull,2013,29(3):425-31. |
| [14] | 葛晓娜,熊密,黄召.香烟烟雾提取物对人胚肺成纤维细胞增殖及转化生长因子β1、表皮生长因子表达的影响[J].中华结核和呼吸杂志,2004,27(1):51-4. Ge X N,Xiong M,Huang Z. Effects of cigarette smoke extract on the proliferation and the expression of TGF-β1 and EGF in human embryonic lung fibroblasts[J]. Chin J Tuberc Respir Dis,2004,27(1):51-4. |

