


2. 湖北医药学院附属东风医院实验中心, 湖北 十堰 442000
2. Experiment Center of Medicine, Dongfeng Hospital, Hubei University of Medicine, Shiyan Hubei 442000, China
急性心肌梗死(acute myocardial infarction,AMI)仍然是全球范围内致死、致残的主要疾病之一[1]。AMI的治疗手段有药物、介入、手术、对症治疗及新兴的间充质干细胞移植治疗等,其目的是为了改善心肌的缺血缺氧,抑制心律失常,维持较好的心脏灌注[2]。尽管治疗方案较多,但所采用的前4种常规治疗都存在不能很好地修复梗死的心肌等突出问题。AMI触发的自发性血管新生反应是一个缓慢保护性反应的过程,只能部分地达到补偿阻塞冠脉以下的心肌,不能完全修复[3]。治疗性血管新生能进一步促进毛细血管的生长和侧支循环的建立,诱导血管新生的治疗被认为是恢复缺血区心肌氧气和营养供应,改善心功能和心室重构的有效方法。
人参等中药材常被用于预防和治疗心脑血管疾病、免疫失调、肝肺纤维化、糖尿病等[4]。人参含多种皂苷、多糖和黄酮,其中皂苷是其主要活性成分。人参总皂苷(total ginsenosides,TG)是从人参中分离的皂苷总和,包括人参皂苷Rb1、Rg1、Re等40多种皂苷单体。其中人参皂苷Rb1、Re等能够抑制心肌细胞凋亡,促进内皮细胞释放一氧化氮[5];人参皂苷Rg1能够上调大鼠心肌梗死区域及周边组织中血管内皮生长因子(vascular endothelial growth factor,VEGF)及其受体Flk-1的表达,增加微血管密度(microvessel density,MVD),改善心功能[6]。也有报道,TG具有抗心肌肥厚,抑制血管平滑肌细胞增殖的作用[7],但TG对心肌梗死后血管新生心室重构及心功能的影响及其分子机制尚不清楚,本文对此进行了探讨。
1 材料与方法 1.1 动物和试剂♂(Sprague-Dawley,SD)大鼠,清洁级,月龄2~3月,体质量200~250 g,由第三军医大学大坪医院实验动物中心提供(许可证:SCXK20080003);TG:北京天然药物研究院提供,为人参茎和叶提取所得(比色法测定,纯度97%;用JTY-300型反相制备色谱固定相分离,纯度>93%);其中含人参皂苷Rb1 5.26%、Rg1 5.20%、Re 21.60%、Rd1 3.65%及其它人参皂类化合物。用无菌生理盐水配制成2 g·L-1和4 g·L-1的储存液,4 ℃保存备用。逆转录试剂盒、VEGF和碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)基因扩增引物均购自大连宝生物公司;CD31单克隆抗体购自Santa Cruz公司;SYBRGREEN PCR Master Mix购自美国ABI公司。
1.2 主要仪器ALC-V8S小动物呼吸机,上海奥尔科特生物技术有限公司;Ken2 Cardico302心电图机,北京明成森木医疗器械有限公司;Sequoia 512彩色多谱勒超声诊断仪,德国SIEMENS ACUSON;2400PCR扩增仪和实时荧光定量PCR仪为美国ABI和BIO-RAD公司产品。
1.3 心脏彩色超声多普勒检查与动物筛选水合氯醛腹腔注射麻醉后,大鼠仰卧位固定,左胸前区以1.25 mol·L-1的硫化钠退毛。专人、双盲法,采用探头频率15 MHz的彩色多谱勒超声诊断仪监测超声心动图,取左室乳头肌短轴切面及左室长轴切面,将图像放大,M型取样左室前壁和左室后壁。选择清晰图像录像及磁盘存贮,分析测量:左心室舒张末期内径(left ventricular end diastolic dimension,LVDd)、左心室收缩末期内径(left ventricular end-systolic dimension,LVDs)、舒展末期左室容积(left ventricular end-diastolic volume,LVEDV)、收缩末期左室容积(left ventricular end-systolic volume,LVESV)及左室射血分数(ejection fraction,EF)、左室短轴缩短率(fractional shortening,FS)。选取心功能各项指标良好者进行实验,各组给予TG等治疗35 d,重复上述指标检测。
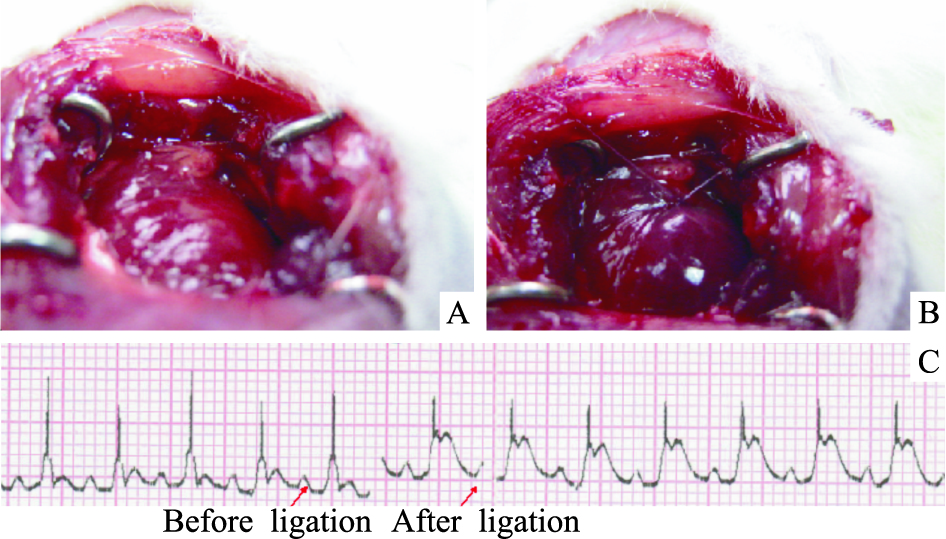
1.4 AMI模型制备和实验分组按照文献报道建立AMI模型[8]。气管插管连接小动物呼吸机,左心耳下缘与肺动脉圆锥距主动脉根部约2~3 mm处,结扎冠状动脉左前降支,心肌颜色变为暗红色和心电图示ST段抬高判断为制模成功(Fig 1);假手术组(sham组,8只)大鼠只开胸不结扎。模型成功大鼠随机分为3组,模型组(model组,12只),TG低剂量组(TG-L组,10只,腹腔注射TG 20 mg·kg-1·d-1),TG高剂量组(TG-H组,10只,腹腔注射TG 40 mg·kg-1·d-1),sham组和model组均腹腔注射生理盐水,术后d 1开始用药,连续给药35 d。
|
| Fig 1 The change of heart color and electrocardiogram(C) in AMI model rats before(A) and after(B) left coronary artery ligation |
处死大鼠,开胸、取心脏,沿冠状沟剪去心房,在结扎点以下,将左心室延冠状面横切为两部分,肉眼观察心室腔径和心室壁的变化,留取心尖组织经多聚甲醛固定、脱水、石蜡包埋、切片HE染色,显微镜下观察心肌组织病理学变化;Masson染色,观察蓝染的胶原纤维分布及数量改变,评价心肌纤维化程度。
1.6 免疫组化检测心肌组织MVD梗死区心肌组织切片常规脱蜡、水化及封闭内源性过氧化物酶活性,按照羊超敏二步法免疫组化检测试剂说明书,按1 ∶50稀释,滴加CD31单克隆一抗,孵育过夜,依次滴加试剂1(聚合物辅助剂)、试剂2(辣根酶标记抗山羊IgG多聚体),DAB显色,CD31阳性细胞表达呈棕色或褐色颗粒,阴性对照以PBS代替一抗。显微镜下观察左心室心肌梗死区域及其边缘CD31阳性细胞表达情况,计数单位面积内CD31阳性微血管数目(200倍视野),随机选取10个视野,计算平均值,即MVD。CD31阳性微血管计数标准:单个内皮细胞、内皮细胞簇、微小血管均予计数,带有较厚肌层区域的血管均不计数。
1.7 Real-time PCR检测基因表达按试剂盒说明书,用TRIzol提取心肌组织总RNA,紫外分光光度计测定A260与A280比值在1.8~2.0范围。逆转录,在稀释至7 mg·L-1的cDNA中加入SYBR®GREEN PCR Master Mix和相应基因扩增引物(序列见Tab 1),进行定量PCR检测,反应条件:95 ℃,5 min;60 ℃,20 s;72 ℃,1 min,4 ℃,40个循环。以目的基因域循环数(threshold cycle,Ct)值对同一样本的β-actin Ct值进行目的基因表达的相对定量分析。
| Gene | GenBank access | Forward primer(5′→3′) | Reverse primer(5′→3′) |
| VEGF | NM031836 | GCGTTCACTGTGAGCCTTGTT | AACGCGAGTCTGTGTTTTTGC |
| bFGF | NM 019305 | AGCGACCCACACGTCAAACT | GTTCGCACACACTCCCTTGAT |
| β-actin | NM 031144 | GGCCAACCGTGAAAAGATGA | CAGCCTGGATGGCTACGTACA |
应用SPSS16.0统计软件进行数据处理。所有数据均以x± s 表示,组间比较采用单因素方差分析,方差齐使用LSD检验。
2 结果 2.1 TG对AMI大鼠心功能的影响与sham相比,model组大鼠LVDd、LVDs、LVEDV、LVESV均明显增加(P <0.01),EF和FS明显减小(P <0.01),表现出明显的左心室收缩和舒张功能障碍。TG干预35 d后,与model组比较,TG-H组大鼠LVDd、LVDs、LVEDV、LVESV明显减小(P <0.05),反应左心室收缩功能的EF和FS则明显高于模型组(P <0.05和P <0.01);与model组比较,TG-L组大鼠EF和FS则明显增大(P <0.05,见Tab 2)。
| Group | LVDd/mm | LVDs/mm | LVEDV/cm3 | LVESV/cm3 | EF/% | FS/% |
| Sham | 6.75±0.33 | 4.14±0.32 | 0.71±0.11 | 0.19±0.04 | 73.20±4.90 | 38.30±4.30 |
| Model | 8.65±0.24## | 7.29±0.44## | 1.38±0.10## | 0.89±0.14## | 35.10±5.10## | 15.80±3.50## |
| TG-L | 8.44±0.55 | 6.62±0.65 | 1.45±0.26 | 0.72±0.15 | 53.70±5.10* | 24.70±3.10* |
| TG-H | 7.13±0.67* | 5.14±0.79* | 0.91±0.28* | 0.37±0.17* | 59.50±7.70** | 28.80±5.20* |
| #P < 0.05,##P <0.01 vs sham group;*P <0.05,**P <0.01 vs model group | ||||||
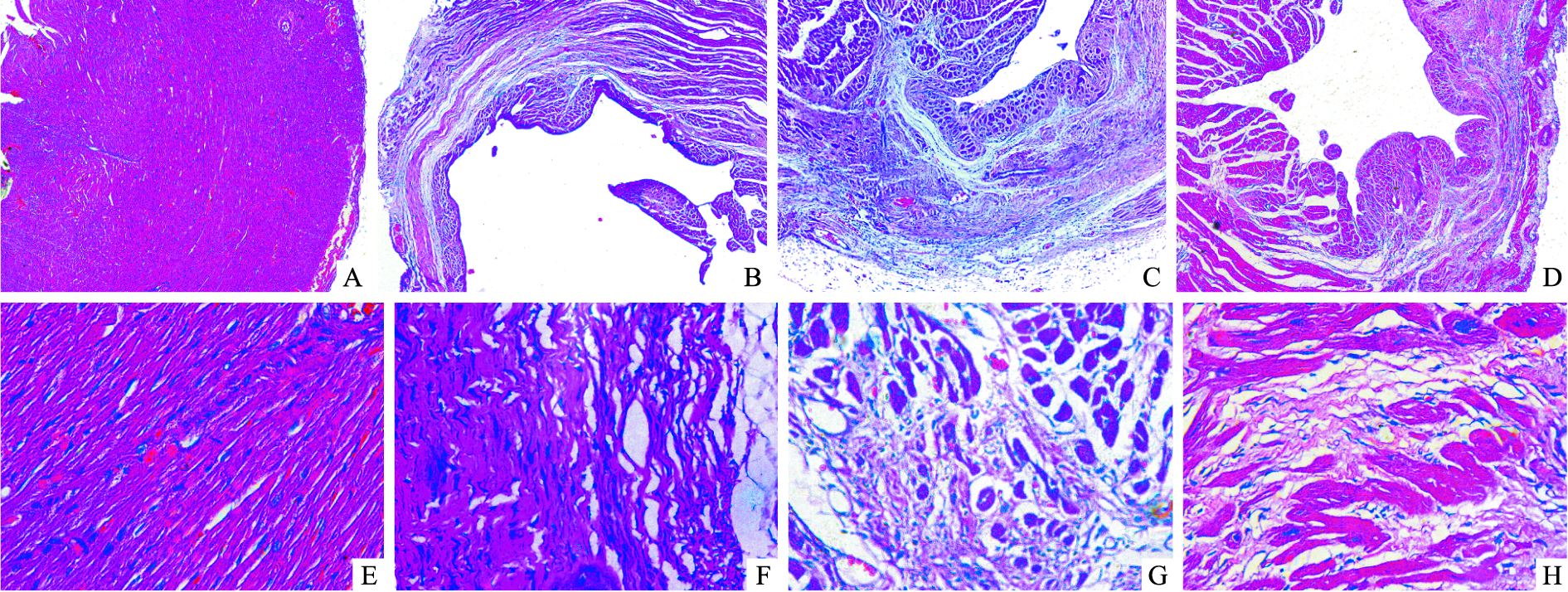
HE染色后,显微镜下观察,可见sham组大鼠心肌纤维排列整齐,无心肌纤维的破坏,胞质丰富均匀,细胞间隙正常;而model组大鼠心肌组织缺血梗死区心室壁变薄,心肌纤维消失,呈现大量局灶性梗死机化和瘢痕形成;TG-L组和TG-H组较model组心室壁明显增厚,心肌纤维保存较多,可见许多岛状存活的心肌组织,梗死机化和瘢痕形成面积较小(Fig 2)。Masson染色可见TG-L组和TG-H组蓝染的胶原纤维数量明显低于模型组(Fig 3A)。
|
| Fig 2 Effect of TG on histopathological change of left ventricle cardiac muscle in rats after AMI(HE staining) A:Sham(×50);B:Model(×50);C:TG-L(×50);D:TG-H(×50);E:Sham(×200);F:Model(×200);G:TG-L(×200);H:TG-H(×200) |
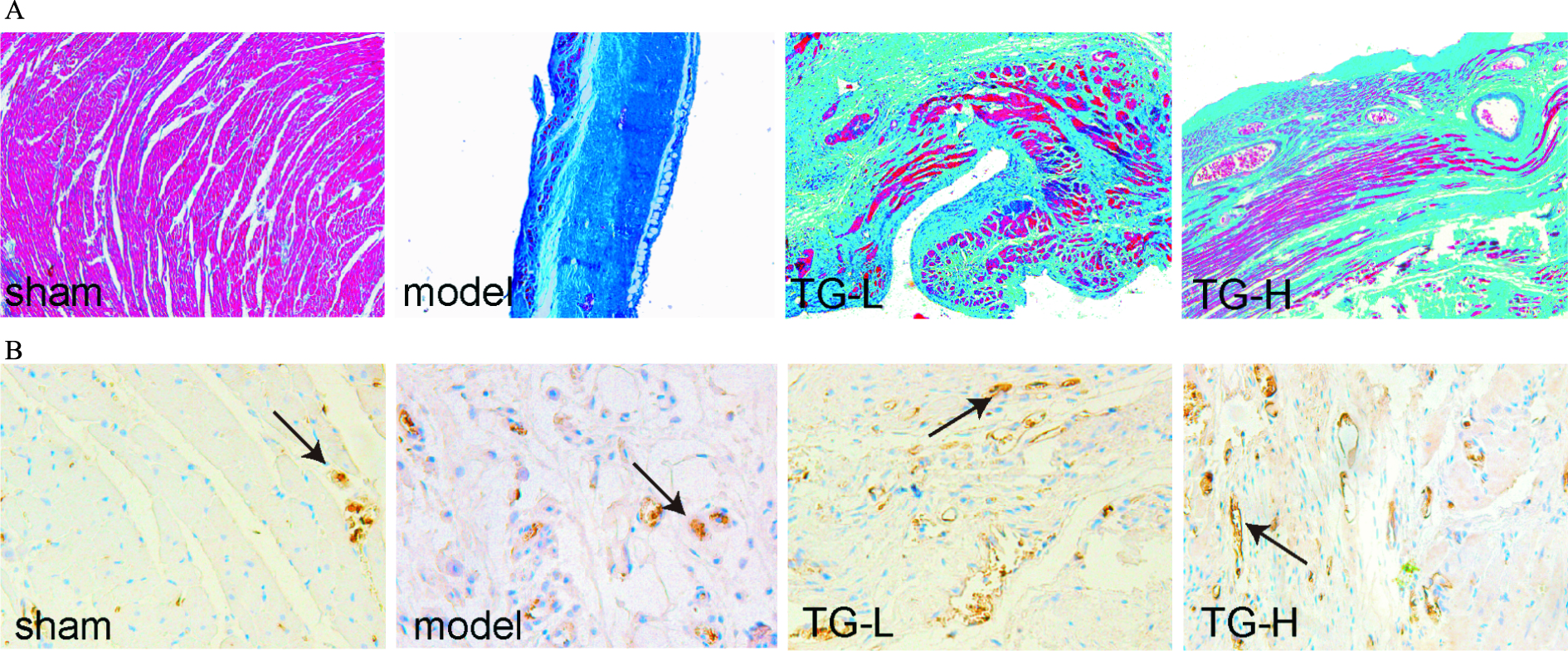
CD31为血管内皮细胞的标志,免疫组化结果显示,与sham组相比,model组和TG-L、TG-H组大鼠心肌组织CD31阳性微血管明显增多(P <0.01),4组心肌组织MVD分别为:1.75±0.96、7.40±0.89、11.40±1.11和13.46±1.82;而与model组相比,TG-L组和TG-H组心肌组织CD31阳性微血管增多更加明显(P <0.05,Fig 3B)。
|
| Fig 3 Effect of TG on fibrosis changes(A,×100, Masson staining) and MVD(B,×200, immunchistochemistry staining) of left ventricular left ventricle cardiac muscle in rats after AMI |
左心室心肌组织real-time PCR结果显示,以sham组基因表达水平的相对定量值为100,各组相同基因表达的相对定量值除以sham组基因表达水平的相对定量值×100表示。与sham组相比,model组左心室心肌组织VEGF和bFGF mRNA的表达水平无显著差异;与sham组和model组相比,TG-L组和TG-H组均可明显提高VEGF和bFGF mRNA的表达水平(P <0.01,见Tab 3)。
| Gene | Sham | Model | TG-L | TG-H |
| VEGF | 100.0±3.0 | 103.7±0.8 | 196.0±20.4** | 433.7±33.9** |
| bFGF | 100.0±7.0 | 116.5±2.8 | 377.0±4.6** | 220.3±31.1** |
| **P <0.01 vs model group | ||||
冠状动脉结扎导致心肌细胞缺血坏死,因心肌细胞再生能力有限,致坏死区域被纤维组织替代,发生心室重构,严重影响心脏功能。因此,增加血管新生和组织血液供应是AMI治疗的关键[9]。实验发现,TG治疗35 d,对大鼠AMI具有明显的保护作用,明显改善心功能和心室重构,AMI后大鼠EF和FS明显提高,尤其高剂量组,LVDd、LVDs、LVEDV、LVESV也明显减小,表明TG治疗后,AMI大鼠心脏舒缩功能较模型组明显提高。组织病理学也进一步证实,TG组心肌梗死面积明显缩小,梗死区心肌纤维化较轻,有大量心肌细胞存在,心室壁较厚,说明TG明显抑制了AMI大鼠的心室重构,这也是TG改善心功能的重要组织学基础。
微血管密度是反映侧支循环的最可靠指标,梗死范围的大小也间接反映侧支循环情况,梗死面积越小,侧支循环可能就越丰富。免疫组化染色结果显示,TG处理组大鼠梗死区域及其周边CD31阳性MVD明显增加,表明TG刺激AMI大鼠血管新生,促进侧支循环的建立。HE染色和Masson染色结果也证实,TG治疗后,心肌梗死区域减小,胶原纤维减少,存活心肌组织较多,说明TG促进AMI后梗死区及其周边血管新生,在较大程度上增加了缺血区血液供应,明显改善了AMI后的心室重构。
VEGF和bFGF是促进内皮细胞生长和分化的关键因素,在血管新生的过程中起着重要的作用[10]。缺血损伤上调VEGF和bFGF表达,导致内皮细胞有丝分裂因子活化,促进内皮细胞生长,诱导血管内皮细胞的分化和成熟,而bFGF则能上调整合素的表达,提高内皮细胞的黏附和迁移能力,最终形成新的血管[11, 12]。业已证明,VEGF和bFGF表达上调能够增加局部组织灌注和代谢,减轻缺血损伤,改善心功能[13]。实验中发现,TG处理组大鼠梗死区心肌组织VEGF和bFGF mRNA的表达明显增加,尤其是高剂量组增加更为明显,提示TG可剂量依赖性地上调AMI大鼠心肌组织中VEGF和bFGF mRNA的表达,而诱导血管新生,从而改善缺血区血液供应。
VEGF是内源性的促血管生成因子,心肌缺血发生后d 1即在梗死区域表达升高,诱导自发性的血管新生反应,但到梗死后d 14就下降到梗死前的水平[14]。实验中观察到,心梗后d 35,模型组VEGF水平与sham组相当,但TG处理组VEGF水平明显升高,提示TG处理,刺激VEGF持续高表达,可能以此来补充AMI激发的自发性血管新生的不足。
已有文献报道,人参皂苷中的Rg1、Re等具有血管生长因子样作用,Rg1可上调大鼠心肌梗死区的VEGF表达,Rb1则参与改善AMI所致的左室重构。由此推测,研究中TG所发挥的AMI治疗作用可能是其所含多种皂苷类物质共同作用的结果。
可见,通过上调VEGF和bFGF基因表达,诱导血管新生,改善心肌血液供应,减小心肌梗死面积,既是TG改善心肌梗死大鼠心脏功能的重要作用机制,也在AMI后减轻心肌纤维化和抑制心室重塑中发挥了明显作用。
[致谢:感谢遵义医学院药理教研室(贵州省基础药理重点实验室)吴芹和徐尚福老师给予的帮助!]
| [1] | Mozaffarian D, Benjamin E J, Go A S, et al. Heart disease and stroke statistics-2015 update:a report from the american heart association[J]. Circulation, 2015, 131(4):e29-322. |
| [2] | Kones R. Primary prevention of coronary heart disease:Integration of new data, evolving views, revised goals and role of rosuvastatin in management. A comprehensive survey[J]. Drug Des Devel Ther, 2011, 5:325-80. |
| [3] | Albrecht-Schgoer K, Schgoer W, Holfeld J, et al. The angiogenic factor secretoneurin induces coronary angiogenesis in a model of myocardial infarction by stimulation of vascular endothelial growth factor signaling in endothelial cells[J]. Circulation, 2012, 126(21):2491-501. |
| [4] | Liu Q, Li J, Wang J, et al. Effects and mechanisms of Chinese herbal medicine in ameliorating myocardial ischemiareperfusion injury[J]. Evid Based Complement Alternat Med, 2013, 2013:925625. |
| [5] | Xia R, Zhao B, Wu Y, et al. Ginsenoside Rb1 preconditioning enhances eNOS expression and attenuates myocardialischemia/reperfusion injury in diabetic rats[J]. J Biomed Biotechnol, 2011, 2011:767930. |
| [6] | Yin H, Liu Z, Li F, et al. Ginsenoside-Rg1 enhances angiogenesis and ameliorates ventricular remodeling in a rat model of myocardial infarction[J]. J Mol Med, 2011, 89(4):363-75. |
| [7] | 黄 警, 黄燮南, 张 纾, 等. 人参总皂苷对PDGF-BB所致血管平滑肌细胞增殖周期的影响[J]. 中国药理学通报, 2010, 26(6):787-91. Huang J, Huang X N, Zhang S, et al. Effect of total ginsenosides on the cell cycle of rat vascular smooth muscle cell proliferation induced by PDGF-BB[J]. Chin Pharmacol Bull, 2010, 26(6):787-91. |
| [8] | 郁秀娟, 朱红军, 黄飞燕, 等. 多西环素抑制基质金属蛋白酶对心肌梗死大鼠左室重构和心功能的影响[J]. 中国药理学通报, 2013, 29(6):841-5.Yu X J, Zhu H J, Huang F Y, et al. Doxycycline attenuates left ventricular remodeling and improves left ventricular function through inhibiting matrix metalloproteinases in post myocardial infarcted rats[J]. Chin Pharmacol Bull, 2013, 29(6):841-5. |
| [9] | Adluri R S, Thirunavukkarasu M, Zhan L, et al. Glutaredoxin-1 overexpression enhances neovascularization and diminishes ventricular remodeling in chronic myocardial infarction[J]. PLoS One, 2012, 7(3):e34790. |
| [10] | De Luca A, Carotenuto A, Rachiglio A, et al. The role of the EGFR signaling in tumor microenvironment[J]. J Cell Physiol, 2008, 214(3):559-67. |
| [11] | Ware J A, Simons M. Angiogenesis in ischemicheart disease[J]. Nat Med, 1997, 3(2):153-64. |
| [12] | Andersson H, Brittebo E. Proangiogenic effects of environmentally relevant levels of bisphenol A in human primary endothelial cells[J]. Arch Toxicol, 2012, 86(3):465-74. |
| [13] | Dragneva G, Korpisalo P, YläHerttuala S. Promoting blood vessel growth in ischemic diseases:Challenges in translating preclinical potential into clinical success[J]. Dis Model Mech, 2013, 6(2):312-22. |
| [14] | Cao R, Eriksson A, Kubo H, et al. Comparative evaluation of FGF-2-, VEGF-A-and VEGF-C-induced angiogenesis, lymphangiogenesis, vascular fenestrations, and permeability[J]. Circ Res, 2004, 94(5):664-70. |

