


阿魏酸(ferulic acid,FA)是一种酚类化合物,广泛应用于食物、饮料和医药行业[1]。文献报道,FA可以作为新型非肽类内皮素受体拮抗剂,拮抗内皮素收缩血管引起的冠心病,心绞痛等,也可降低氧自由基脂质过氧化损伤[1, 2]和癌症[2, 3]的发生率,且具有一定的镇静催眠[4]、解痉镇痛、活血化瘀、抗菌消炎[5]的作用。这些研究显示,FA有望成为治疗心血管系统疾病的一剂良药。然而,在治疗心血管疾病的同时,FA是否会通过其他途径对血管肌源性反应产生影响及其作用机制,目前尚不清楚。据此,本实验采用离体微血管张力测定法进一步探究其对冠状动脉平滑肌的作用特点,为临床应用FA治疗心血管疾病提供药理学基础。
1 材料 1.1 药品与试剂FA、血栓素A2类似物(U46619)、苯肾上腺素(PE)、四乙胺(TEA)、格列苯脲(Gli)、氯化钡(BaCl2)、4-氨基吡啶(4-AP)、L-硝基精氨酸甲酯(L-NAME)、吲哚美辛(Indo)、HEPES均购自美国Sigma公司,其余为市售分析纯。正常PSS液的成分为(mmol· L-1):NaCl 118,KCl 5,CaCl2 2.5,KH2PO4 1.2,MgCl2 1.4,NaHCO3 5,HEPES 5,Glucose 10。
1.2 实验动物正常♂SD大鼠,6周龄,体质量200~250 g,购自山西医科大学实验动物中心,合格证号为SCXK(晋)2009-0001,受试动物在本教研室观察室喂养2周后用于实验。
1.3 实验仪器PowerLab生物信号采集分析系统及张力换能器购自澳大利亚埃德仪器国际贸易有限公司,Multi Myograph System-610M微血管张力记录仪购自丹麦DMT公司,Nikon解剖显微镜购自日本Olympus公司,PHS-3C精密pH计、sartorius BS124S精密天平等。
2 方法 2.1 冠脉血管环标本的制备大鼠断头处死后即刻取出心脏,置于4℃、pH 7.38、氧饱和的PSS液中。在解剖显微镜下分离出大鼠冠状动脉的室间隔支、室壁支和前降支,剪成长约2 mm的血管环,通过两根直径为40μm的钢丝固定于DMT记录仪。具体制备方法、血管环标化及张力记录、活性检测参照文献[6]。
2.2 FA对离体大鼠冠状动脉静息及预收缩血管环张力的影响待血管环在盛有5 mL PSS液、37℃恒温、持续通入95% O2+5% CO2气体的浴槽中稳定1 h,期间通过顺时针旋转DMT的螺旋测微尺(每2 min一次,每次3~5格)逐步牵拉血管,调节血管跨壁压至80 mmHg,使其达到基础压力状态,即实验开始前的稳定状态。再将浴槽内PSS液更换为同体积KCl(60 mmol· L-1)刺激血管环发生收缩。当连续刺激3次血管环收缩幅度差别小于10%,收缩张力达2mN[7],认为该血管环的结构和功能符合实验标准,开始正式实验。在静息状态下,向浴槽内分别加入终浓度为1、1.5、2、2.5、3 mmol· L-1的FA,观察其对静息状态大鼠冠状动脉张力的影响;向浴槽内分别加入KCl(60 mmol· L-1)、U46619(1 μmol· L-1)、PE(10 μmol· L-1),当血管达到收缩坪台时,再向浴槽内累积加入上述浓度的FA,建立FA的浓度-舒张效应曲线,观察FA对预收缩冠脉血管环张力的影响。对照组分别加入相同体积的DMSO,排除溶剂对实验结果的影响。以冠脉血管环达坪台期的最大收缩幅度为100%,计算不同浓度FA的舒张百分数。
2.3 内皮对FA舒张PE预收缩冠状动脉作用的影响及L-NAME和Indo对其舒张作用的干预参照文献[8]所述,用直径小于冠状动脉的毛细管轻轻插入冠脉一端,温和的打入气泡,重复3~5次后,可机械去除冠脉血管环内皮。利用文献[9]方法检测内皮的完整性。在内皮完整组和去完整组分别加入PE(10 μmol· L-1),待血管收缩达到坪台后依次加入上述浓度的FA,观察内皮对FA舒张PE(10 μmol· L-1)预收缩冠状动脉作用的影响。以冠状动脉收缩达坪台期的幅度为100%,计算不同浓度FA的舒张百分率;在内皮完整组PE(10 μmol· L-1)预收缩达坪台后,分别加入L-NAME(0.1 mmol· L-1)和Indo(10 μmol· L-1)预孵15min,待冠脉收缩达到第2次坪台后再依次加入上述浓度的FA,观察L-NAME(0.1 mmol· L-1)和Indo(10 μmol· L-1)对FA舒张作用的影响。以加入L-NAME(0.1 mol· L-1)和Indo(10 μmol· L-1)后冠脉血管环收缩达坪台期的幅度为100%,计算不同浓度FA的舒张百分率。
2.4 预孵FA对外钙内流和内钙释放引起冠状动脉收缩的影响用KCl(60 mmol· L-1)刺激冠脉血管,当血管环收缩稳定后,用含EGTA的无钙PSS液洗脱血管环,15 min后血管环张力回到基线,使细胞外液达到一种无钙的理想状态;再将浴槽内的液体换成不含EGTA的无钙PSS液,排除EGTA对复钙后血管收缩反应的影响。15 min后将浴液更换为无钙的KCl(60 mmol· L-1)或U46619(1 μmol· L-1),预孵10 min加入CaCl2(2.5 mmol· L-1),血管收缩达坪台后重复上述操作,待血管环张力第2次回到基线,先加入FA预孵15min,再加入无钙的KCl(60 mmol· L-1)或U46619(1 μmol· L-1),10min后复钙,记录预孵FA前后无钙液中KCl(60 mmol· L-1)或U46619(1 μmol· L-1)的收缩幅度以及复钙后的幅度变化,比较FA对外钙内流和内钙释放引起冠状动脉收缩作用的影响。
2.5 4种钾通道阻断剂对FA舒张KCl或U46619预收缩冠状动脉作用的影响冠脉血管环稳定后向浴槽中加入KCl(60 mmol· L-1)或U46619(1 μmol· L-1),待血管收缩达坪台后,分别加入4种钾通道阻断剂TEA、Gli、BaCl2、4-AP,使其在浴槽内的终浓度分别为1、0.01、1、1 mmol· L-1,血管收缩再次达坪台后加入FA,观察4种钾通道阻断剂对FA舒张KCl或U46619预收缩冠状动脉作用的影响。以加入钾通道阻断剂后冠脉血管环收缩达坪台期的幅度为100%,计算不同浓度FA的舒张百分率。
2.6 统计学分析数据以x± s表示,采用GraphPad Prism 6作浓度-舒张效应曲线,SPSS19.0进行配对t检验及两因素重复测量方差分析。
3 结果 3.1 FA对离体大鼠冠状动脉静息及预收缩血管环张力的影响FA(1、1.5、2、2.5、3 mmol· L-1)对离体大鼠冠状动脉静息张力无明显影响(P>0.05);KCl(60 mmol· L-1)、U46619(1 μmol· L-1)、PE(10 μmol· L-1)可收缩大鼠离体冠状动脉,最大收缩幅度分别为(2.69±0.16)mN、(4.48±0.42)mN、(6.74±0.35)mN;FA可以浓度依赖性地舒张KCl(60 mmol· L-1)、U46619(1 μmol· L-1)、PE(10 μmol· L-1)引起的离体大鼠冠脉收缩,最大舒张百分率分别为(98.39±2.92)%、(95.03±2.86)%、(91.58±2.10)%,与溶剂对照组相比差异有显著性(P <0.01),与KCl组相比,PE组存在显著性差异(P <0.05),U46619组差异无显著性(P>0.05),见Fig 1。

|
| Fig 1 Effect of FA on resting and precontraction by KCl(60 mmol· L-1),U46619(1 μmol· L-1), PE(10 μmol· L-1) in isolated RCA rings(x± s , n=8) Relaxtions were expressed as percentages of the maximal contraction induced by KCl(60 mmol· L-1),U46619(1 μmol· L-1),PE(10 μmol· L-1),respectively. *P <0.05, **P <0.01 vs KCl. |
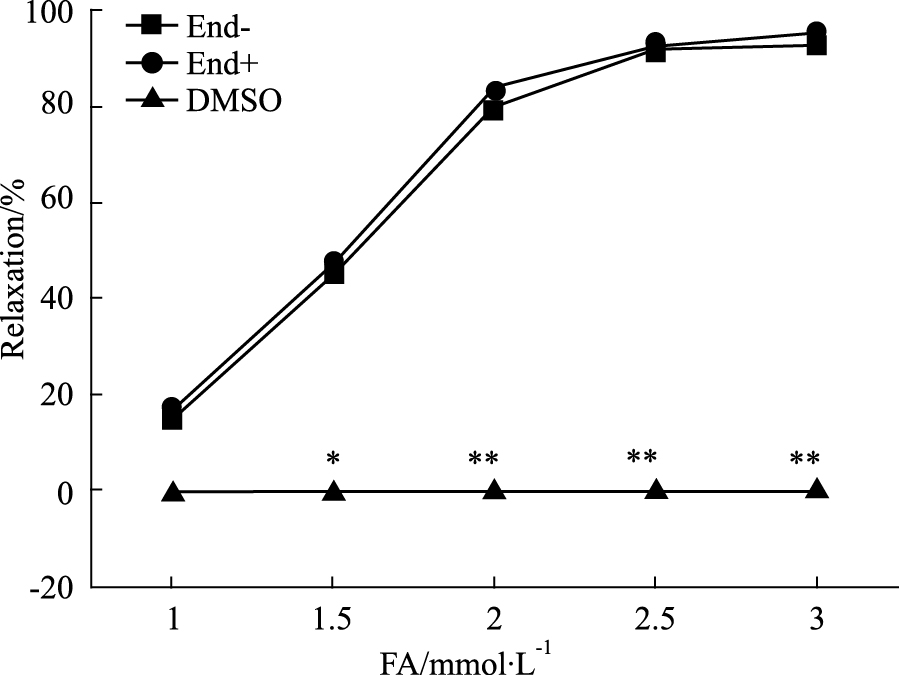
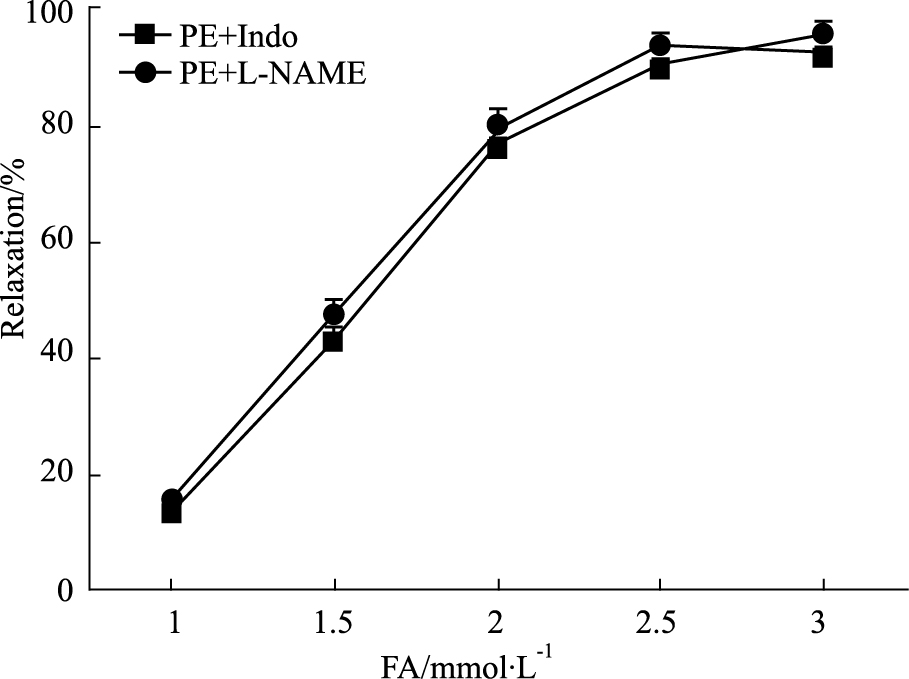
内皮完整组与去完整组FA舒张PE(10 μmol · L-1)预收缩冠状动脉作用差异无显著性(P>0.05),见Fig 2。预孵L-NAME(0.1 mol· L-1)和Indo(0.01 mol· L-1),血管环最大收缩强度分别达到(9.42±1.25)mN、(11.95±2.05)mN;但对FA舒张作用的影响无明显差异(P>0.05),见Fig 3。
|
| Fig 2 FA-induced relaxation in endothelium-intact (End+)or-denuded(End-) RCA rings precontracted with PE(10 μmol· L-1)(x± s , n=8) Relaxtions were expressed as percentages of the maximal contraction induced by PE(10 μmol· L-1). *P <0.05,**P <0.01 vs “End++FA”. |
|
| Fig 3 Effects of L-NAME(0.1 mol· L-1)and Indo(0.01 mol· L-1)on FA-induced relaxation in RCA rings(x± s , n=8) Relaxtions were expressed as percentages of the maximal contraction induced by PE(10 μmol· L-1)+L-NAME/Indo. |
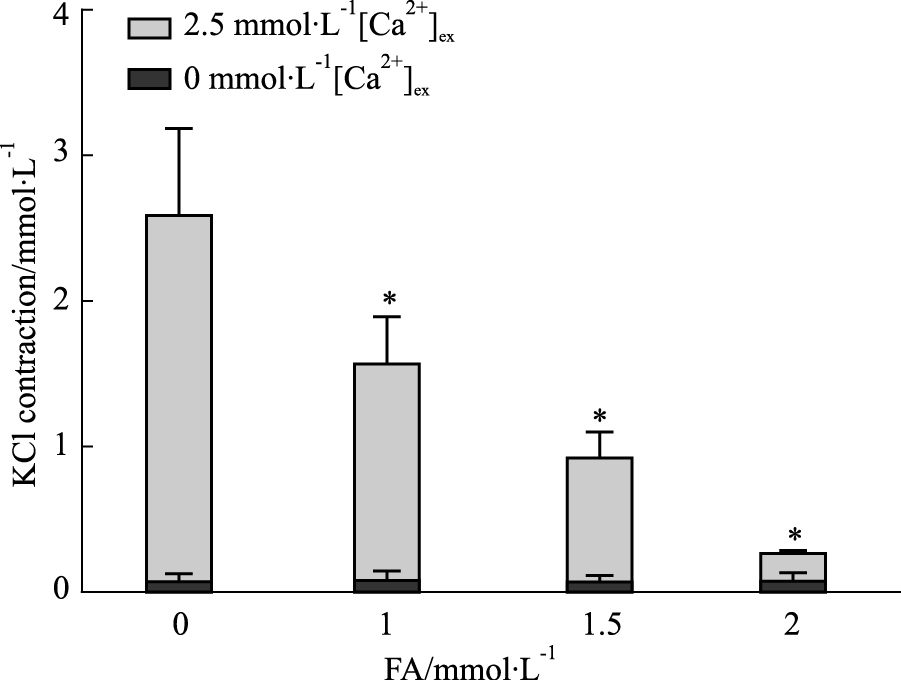
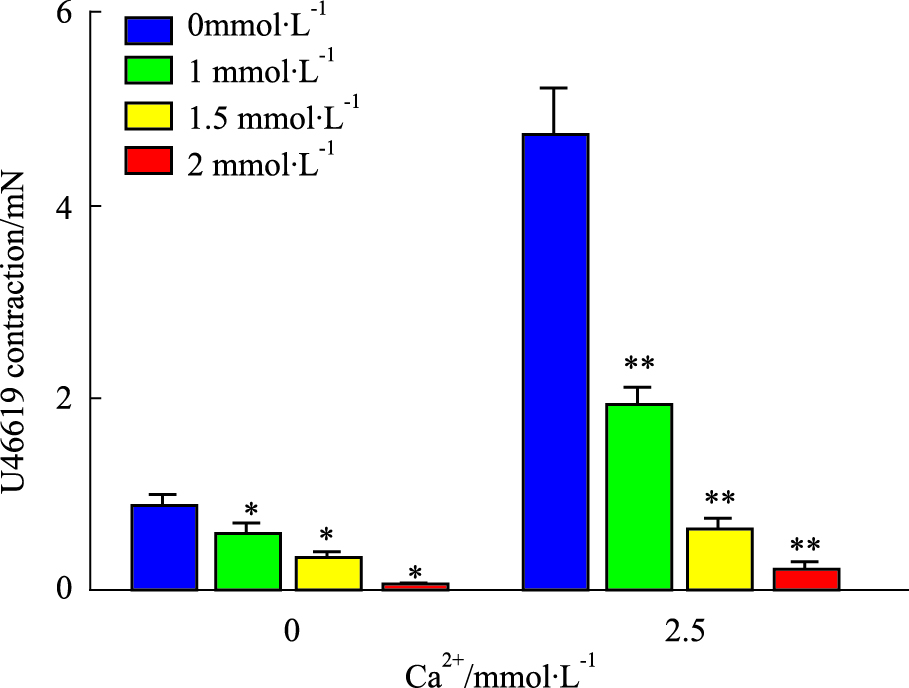
在无钙PSS液中,KCl(60 mmol· L-1)几乎不引起冠脉收缩,复钙(2.5 mmol· L-1 CaCl2)后冠脉发生收缩,且收缩幅度与正常PSS液中KCl(60 mmol· L-1)引起的收缩幅度相当。预孵FA(1、1.5、2 mmol· L-1)能够明显抑制KCl(60 mmol· L-1)在无钙PSS液中复钙后诱导的外钙依赖性血管收缩(见Fig 4),收缩率分别为(58.35±1.61)%、(32.90±1.63)%、(2.95±0.59)%;无钙PSS液中,U46619(1 μmol· L-1)引起冠脉收缩,最大收缩幅度为(0.84±0.07)mN,复钙后进一步收缩。预孵FA(1、1.5、2 mmol· L-1),能够抑制U46619(1 μmol· L-1)在无钙PSS液中引起的轻微血管收缩以及复钙后的收缩,收缩率分别为(69.35±1.52)%、(40.10±1.02)%、(6.74±0.36)%;(40.89±0.91)%、(13.74±0.43)%、(5.43±0.17)%,见Fig 5。
|
| Fig 4 Effects of FA on [Ca2+]ex-influx-induced contractions(mN)(x± s , n=8) *P <0.05 vs control. |
|
| Fig 5 Effects of FA on [Ca2+]in-efflux-induced and [Ca2+]ex-influx-induced contractions(mN)(x± s , n=8) *P <0.05,**P <0.01 vs control. |
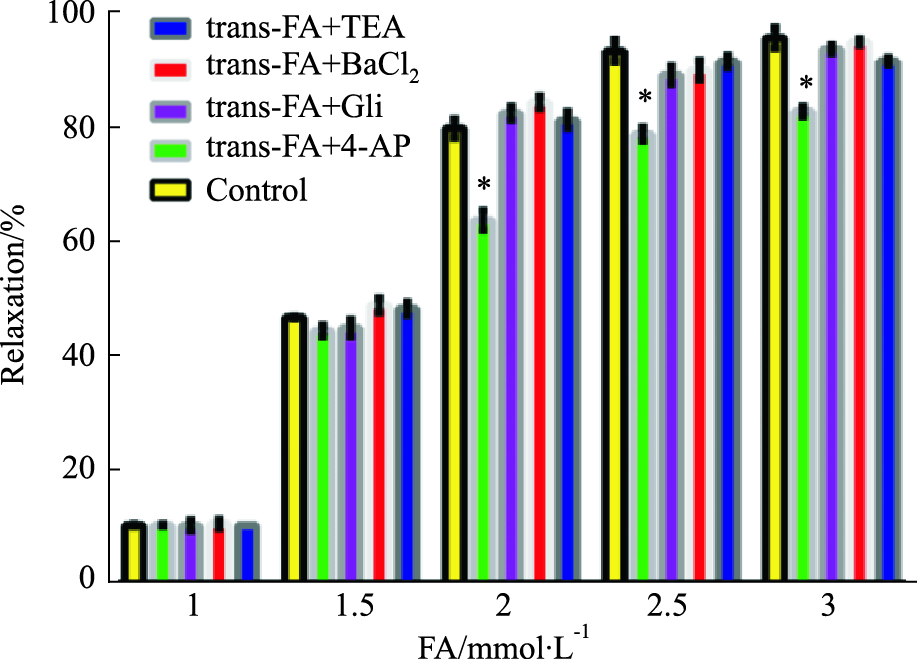
预孵BaCl2(1 mmol· L-1)、Gli(0.01 mmol· L-1)、TEA(1 mmol· L-1)均没有明显地影响FA对冠脉的舒张作用(P>0.05),但预孵4-AP(1 mmol· L-1)使FA对U46619(1 μmol· L-1)预收缩大鼠冠脉的舒张幅度减小26.46%(P <0.05,见Fig 6)。
|
| Fig 6 Effects of four K+ channel inhibitors on FA-induced relaxation in RCA rings(x± s , n=8) Relaxtions were expressed as percentages of the maximal contraction induced by U46619(1 μmol· L-1). *P <0.05 vs control. |
本实验结果显示:FA对静息状态的离体大鼠冠状动脉的肌张力无明显影响,可以舒张预收缩的大鼠冠状动脉,其舒张作用可能与激活血管平滑肌上KV通道、阻断电压依赖性的Ca2+通道(VOCC)、抑制钙操纵型Ca2+通道(SOC)有关,与内皮、NO及PGI2无关。
FA作为中药川穹等的生物碱提取物[10],有文献报道,FA能够降血压,缓解心绞痛,预防经皮冠状动脉治疗(PCI)术后再狭窄,改善心功能[11]等。我们的实验表明FA可以浓度依赖性的舒张预收缩的大鼠冠状动脉,提示其具有舒张血管的作用。
血管平滑肌分布着K+通道和Ca2+通道,是调节血管舒缩状态的重要机制。K+通道被抑制时,K+外流减少,细胞膜电位下降,引起VOCC的开放,钙内流导致细胞质内Ca2+浓度增加,引起血管平滑肌收缩,相反则舒张;Ca2+是平滑肌细胞兴奋-收缩偶联的关键因子,外钙内流和内钙释放是引起收缩的原因。细胞外钙内流主要依赖VOCC和受体操纵型Ca2+通道(ROCC),一般地,KCl引起的冠脉收缩主要是通过激活细胞膜上的VOCC通道,而内钙外流则主要是细胞肌浆网内钙离子的释放,即SOC的开放。为了探索FA舒张冠脉是否与K+通道和Ca2+通道有关,我们观察了4种特异性K+通道抑制剂4-AP、Gli、TEA、BaCl2以及Ca2+对FA舒张冠脉作用的影响。结果表明,4-AP(1 mol· L-1)可以抑制FA的舒血管作用,Gli(0.01 mol· L-1)、TEA(1 mol· L-1)、BaCl2(1 mol· L-1)对FA舒血管作用差异无显著性。FA能够抑制U46619(1 μmol· L-1)在无钙PSS液中引起的收缩,以及无钙PSS液中KCl和U46619复钙后的收缩作用。这些结果提示,FA对冠脉血管的舒张作用可能与激活KV通道、抑制VOCC和SOC通道有关。
在冠状动脉血管中,NO和PGI2是内皮依赖性的舒血管物质[12, 13]。NO是由L-精氨酸和分子氧化生成的一种自由基气体,能够穿透细胞膜到达靶细胞,激活NO合酶(NOS),从而引起细胞内cGMP含量升高。cGMP通过抑制Ca2+通道使细胞内Ca2+减少,舒张血管。NOS抑制剂L-NAME不能抑制FA对预收缩冠状动脉的舒张作用,证明其舒张作用与内皮-NO-cGMP途径无关;环氧合酶是PGI2合成的主要限速酶之一,其抑制剂Indo对FA舒张预收缩冠脉作用无影响,说明其舒张作用与PGI2途径无关。
综上所述,FA可以浓度依赖性的舒张预收缩SD大鼠离体冠状动脉,其舒张机制可能与KV通道激活、VOCC和SOC通道抑制有关,与内皮、NO系统和PGI2途径无关。
(致谢:本实验在山西医科大学基础医学院药理教研室完成。感谢我的导师张明升教授的耐心指导,感谢本教研室的侯晓敏老师、杨蓉老师、牛龙刚老师和田晴晴同学在实验过程中无私的帮助。也要感谢我的师妹范芳文、贺泽芳、石萌与我一起完成实验。)
| [1] | Kaur B, Chakraborty D, Kaur G, Kaur G. Biotransformation of rice bran to ferulic acid by pediococcal isolates[J]. Appl Biochem Biotechnol, 2013, 170(4):854-67. |
| [2] | Fukuda T, Kuroda T, Kono M, et al. Augmentation of ferulic acid-induced vasorelaxation with aging and its structure importance in thoracic aorta of spontaneously hypertensive rats[J]. Naunyn Schmiedebergs Arch Pharmacol, 2015, 388(10):1113-7. |
| [3] | 吴枝娟, 余 婧, 王瑞幸. 阿魏酸预处理对阿霉素诱导H9c2心肌细胞损伤的保护作用[J].中国药理学通报, 2014, 30(8):1059-65.Wu Z J, Yu J, Wang R X. Ferulic acid pretreatment on adriamycin induced H9c2 myocardial cell injury protection[J].Chin Pharmacol Bull, 2014, 30(8):1059-65. |
| [4] | Tu Y, Cheng S X, Sun H T, et al.Ferulic acid potentiates pento-barbital-induced sleep via the serotonergic system[J]. Neurosci Lett, 2012, 525(2):95-9. |
| [5] | Arvind T, Sushma C, Jeffrey W, Sunil P. Ferulic acid combined with aspirin demonstrates chemopreventive potential towards pancreatic cancer when delivered using chitosan-coated solid-lipid nanoparticles[J]. Cell Bioscience, 2015, 12(5):46. |
| [6] | Hou X M, Zhang M S. Enhancement of voltage-gated K+ channels and depression of voltage-gated Ca2+ channels are involved in quercetin-induced vasorelaxation in rat coronary artery[J]. Planta Med, 2014, 80(6):465-72. |
| [7] | Liu Y, Niu L, Zhang W, et al. Effects of taurine on contractions of porcine coronary artery[J]. Pharmacol Rep, 2009, 61(4):681-9. |
| [8] | Menendez C, Dueñas M, Galindo P, et al. Vascular deconjugation of quercetin glucuronide:the flavonoid paradox revealed?[J] Mol Nutr Food Res, 2011, 55(12):1780-90. |
| [9] | Bubolz A H, Li H, Wu Q, et al. Enhanced oxidative stress impairs cAMP-mediated dilation by reducing Kv channel function in small coronary arteries of diabetic rats[J]. Am J Physiol Heart Circ Physiol, 2005, 289(5):1873-80. |
| [10] | 吴建良, 沈敏敏, 杨水新.阿魏酸对小胶质细胞炎性反应的抑制作用[J].中国药理学通报, 2015, 31(1):97-102. Wu J L, Shen M M, Yang S X. Inflammatory reaction inhibition of Ferulic Acid on microglial cell[J]. Chin Pharmacol Bull, 2014, 31(1):97-102. |
| [11] | Barone E, Calabrese V, Mancuso C. Ferulic acid and its therapeutic potential as a hormetin for age-related diseases[J]. Biogerontology, 2009, 10(2):97-108. |
| [12] | Babettte B. Weksler prostanoids and NSAIDs in cardiovascular biology and disease[J]. Vascul Biol, 2015, 17:41. |
| [13] | Nakmareong S, Kukongviriyapan U, Pakdeechote P, et al. Antioxidant and vascular protective effects of curcumin and tetrahydrocurcumin in rats with L-NAME-induced hypertension[J]. Naunyn Schmiedebergs Arch Pharmacol, 2011, 383(5):519-29. |

