


2. 中央民族大学 生命与环境科学学院, 北京 100081
2. College of Life and Environmental Sciences, MINZU University of China, Beijing 100081, China
心肌缺血/再灌注(ischemia/reperfusion,I/R)损伤是指缺血心肌重新获得新鲜血液供给之后,心肌组织损伤反而进一步加重,甚至转为不可逆性损伤的现象[1,2]。研究发现,心肌I/R损伤发生机制复杂,涉及活性氧损伤、钙超载心肌细胞能量代谢障碍、线粒体损伤、细胞凋亡以及细胞自噬等多种机制[3,4]。其中细胞凋亡和细胞自噬及其相互作用在心肌I/R损伤发生发展中发挥非常关键的作用[5,6],是目前研究的热点。
苗药都木油(Ndut mongx youx)为陵齿蕨科乌蕨属植物乌蕨[Stenolomachusana(L.)Ching]的全草,收载于《广西中药志》、《滇南本草》、《中华本草-苗药卷》等,其单方和复方均具有清热、解毒、利湿、止血等功效[7]。现代药学研究发现,都木油中含有多种黄酮类化合物如荭草苷、芹菜素等,其中荭草苷因具有良好的抗氧化、抗细胞凋亡等药理作用[8,9],而被认为是苗药都木油作用于心血管系统的主要活性成分之一。前期研究发现,荭草苷具有很好的抗心肌I/R损伤和抗心肌细胞缺氧/复氧损伤的作用[10,11],但其给药方式多为治疗式给药,即在缺血和或再灌期给药[10],而且其抗心肌I/R损伤的作用机制主要集中在抗细胞凋亡上[8,10,11],而采用预给药方式的荭草苷抗心肌I/R损伤的作用机制是否与细胞自噬相关,还未见报道。本研究采用Langendorff法建立大鼠离体心脏缺血/再灌注模型,研究荭草苷对细胞自噬与细胞凋亡的调控作用,为荭草苷及苗药都木油防治I/R损伤提供药理学依据。
1 材料与方法 1.1 实验动物Wistar大鼠,♂,(240±20)g,SPF级,购自北京维通利华实验动物技术有限公司。
1.2 主要试剂和仪器荭草苷(纯度>98%,上海融禾医药科技发展有限公司),白藜芦醇(纯度> 99%,由长沙康隆生物制品有限公司赠送),渥曼青霉素(Wortmannin,美国Sigma公司),乳酸脱氢酶(LDH)试剂盒和肌酸激酶(CK-MB)试剂盒(中生北控生物科技股份有限公司),肝素(美国Sigma公司),戊巴比妥钠(美国Sigma公司),DeadEedTMFluorometric TUNEL检测试剂盒(美国Promega公司)。16道生理记录仪(ML880/P PowerLab16/30,澳大利亚AD Instruments公司);全自动生化仪(7020,日本日立公司);荧光显微镜(IX81,日本Olympus公司);电镜(TecnaiSpiri,美国FEI公司);半干转印仪(美国Bio-rad公司)。LC3抗体和Beclin 1抗体(美国Cell Signaling Technology公司)。
1.3 复制大鼠离体心脏I/R损伤模型采用Langendorff心脏灌注模型法建立大鼠离体心脏I/R损伤模型:腹腔注射戊巴比妥钠(30 mg·kg-1)麻醉动物,并腹腔注射肝素液抗凝(250 U·kg-1),开胸后快速取出心脏置Langendorff灌流架上进行逆行灌流。灌注液用95% O2和5% CO2饱和的K-H液(mmol·L-1:NaCl,118;KCI,4.7;KH2PO4,1.18;EDTA-Na2,0.5;NaHCO3,25;CaCl2,1.7;MgSO4· 7H2O,1.25;Glucose,11.1;pH,7.4±0.5),灌注压为75 cm H2O,灌注温度为37℃。待恒压灌流平衡30 min心脏参数稳定后,给予全心缺血30 min,再灌注120 min。离体心脏平衡灌注30 min后,心率低于200 BPM,发展压LVDP低于931 Pa,或出现心律不齐者舍弃不用。
1.4 动物分组及给药根据体重将大鼠随机分为7组(n=6):正常对照组(Control组)、心肌I/R模型组(I/R组)、不同剂量荭草苷组(1、2、4 mg·kg-1;Ori-1组,Ori-2组,Ori-4组)、自噬抑制剂组(OW组)以及阳性对照药组白藜芦醇组(1.5 mg·kg-1,Res组)。各组大鼠给予相应药物,每天腹腔注射给药1次,连续7 d,正常对照组及模型组给予等量生理盐水。自噬抑制剂组连续7 d腹腔注射2 mg·kg-1荭草苷后,于分离心脏前30 min腹腔注射0.015 mg·kg-1自噬抑制剂渥曼青霉素。各组通过Langendorff法制备离体心脏I/R损伤模型,缺血30 min,再灌注120 min,正常对照组不进行缺血处理。
1.5 血流动力学指标和心肌酶检测采用16道生理记录仪采集血流动力学数据,实验中选取平衡灌注30 min(Baseline)和再灌注120 min(R120)两个时间点,记录分析冠脉流量(coronary flow,CF)、左室发展压(left ventricular developed pressure,LVDP)、左室内压最大上升速率(+dp/dtmax)、左室内压最大下降速率(-dp/dtmax),并收集冠脉流出液,使用全自动生化分析仪测定LDH和CK-MB活性。
1.6 TUNEL法检测心肌细胞凋亡水平心脏复灌120min后,取左心室组织,4%多聚甲醛固定,乙醇梯度脱水,石蜡包埋并切片,按TUNEL试剂盒操作,用荧光显微镜观察心肌细胞凋亡情况,具体实验操作参考DeadEedTMFluorometric TUNEL检测试剂盒说明书。
1.7 电镜下观察大鼠心肌细胞超微结构改变及自噬体心脏复灌120 min后,取左心室组织,用戊二醛及锇酸双重固定,乙醇丙酮逐级脱水,环氧树脂包埋,LKB-V型超薄切片机制备超薄切片,超薄切片机切片,醋酸双氧铀和枸橼酸铅双重染色,在透射电镜下观察心肌细胞中的超微结构改变,并寻找心肌细胞内自噬体,并计数一铜网孔(约30 000 μm2)内自噬体数量,每个样本计数3个铜孔,取平均值。
1.8 Western blot法检测心肌细胞中自噬相关蛋白实验结束后,取心尖及左心室部分用RIPA 200 μL充分裂解提取蛋白,BCA法测样品蛋白浓度,均衡每组蛋白浓度后,以SDS-PAGE凝胶电泳分离。半干法转移蛋白至PVDF膜,5%脱脂奶粉封闭过夜,加入LC3抗体和Beclin 1抗体(1 :1 000)于4℃封闭袋中孵育过夜,二抗室温孵育1 h。ECL化学发光法显示结果,压片曝光,拍照,并对目的条带进行灰度分析,结果用目标条带与内参的比值表示。
1.9 统计学处理以x± s 表示,采用SPSS 18.0软件进行统计学处理,组间比较用单因素方差分析(One-Way ANOVA)。
2 结果 2.1 荭草苷对I/R损伤大鼠心脏血流动力学指标的影响如Tab 1所示,与Control组比较,缺血后再灌注120 min能明显引起大鼠离体心脏血流动力学指标变化:CF、LVDP、+dp/dtmax及-dp/dtmax均有不同程度下降(P < 0.01);而荭草苷能明显改善I/R大鼠心脏的血流动力学指标,与I/R组比较,差异有显著性,初步表明荭草苷能改善I/R损伤引起的心功能障碍;与Ori-2组比较,加用自噬抑制剂渥曼青霉素后,I/R大鼠心脏的LVDP及±dp/dtmax数值则明显降低(P <0.01)。
| Time | Control | I/R | Ori-1 | Ori-2 | Ori-4 | OW | Res | |
| CF/mL | Baseline | 10.79±2.14 | 10.90±1.08 | 10.96±1.06 | 11.15±1.19 | 11.38±0.95 | 11.39±1.13 | 10.98±1.93 |
| R120 | 8.75±2.47 | 6.15±1.27** | 7.40±1.31 | 7.80±1.65 | 8.20±1.72# | 6.64±1.27 | 7.15±1.74 | |
| LVDP/kPa | Baseline | 10.33±1.58 | 11.06±1.66 | 10.76±1.93 | 11.6±2.19 | 10.4±1.0 | 9.90±1.75 | 11.84±1.8 |
| R120 | 7.51±1.39 | 4.35±0.89** | 5.64±1.28# | 6.29±1.17 ## | 6.19±1.26 ## | 3.34±1.05△△ | 6.4±1.28## | |
| Heart Rate/bpm | Baseline | 310.40±32.78 | 279.73±21.26 | 293.62±49.25 | 288.45±26.62 | 296.31±33.61 | 301.51±28.72 | 291.31±21.96 |
| R120 | 295.46±21.11 | 268.99±32.31 | 271.79±45.24 | 277.54±31.16 | 271.57±19.32 | 264.48±58.18 | 265.78±35.49 | |
| +dp/dtmax/kPa·s-1 | Baseline | 453±76 | 488±38 | 401±81 | 450±85 | 431±40 | 442±44 | 487±118 |
| R120 | 369±75 | 183±50** | 231±45 | 283±42## | 264±46## | 122±41△△ | 271±62## | |
| -dp/dtmin/kPa·s-1 | Baseline | -248±56 | -263±43 | -256±53 | -275±61 | -247±35 | -238±59 | -287±59 |
| R120 | -158±35 | -90±14** | -115±30 | -127±25## | -126±26## | -68±18△△ | -136±27## | |
| *P<0.05,**P<0.01 vs control;#P<0.05,##P<0.01 vs I/R group;△P <0.05,△△P <0.01 vs ori-2 group | ||||||||
如Tab 2所示,与Control组相比,I/R大鼠心脏冠脉流出液中LDH及CK-MB漏出率明显升高(P <0.01);而荭草苷能明显减少I/R大鼠心肌冠脉流出液中的LDH和CK-MB水平(P <0.01),且呈一定的剂量依赖性,表明荭草苷能减轻I/R损伤引起的心肌损伤;与Ori-2组比较,OW组大鼠心脏冠脉流出液中LDH及CK-MB水平又明显升高(P <0.01),表明渥曼青霉素抑制了荭草苷对I/R损伤心肌的保护作用。
| Time | Control | I/R | Ori-1 | Ori-2 | Ori-4 | OW | Res | |
| LDH/U·L-1 | Baseline | 4.58±0.74 | 5.83±0.44 | 5.33±0.72 | 5.28±0.80 | 4.40±0.60 | 3.33±0.33 | 6.70±0.51 |
| R120 | 6.4 2±0.50 | 83.75±10.12** | 13.83±0.83## | 14.56±0.51## | 15.06±1.83## | 124.33±19.89△△ | 12.67±1.90## | |
| CK-MB/U·L-1 | Baseline | 3.67±0.62 | 3.33±0.82 | 3.67±0.47 | 3.75±0.50 | 3.07±0.26 | 1.87±0.56 | 3.24±0.79 |
| R120 | 1.67±0.29 | 29.30±4.01** | 5.67±0.47## | 7.33±1.54## | 6.87±1.86# | 57.56±9.73△△ | 9.42±1.17## | |
| **P<0.01 vs control;#P<0.05,##P<0.01 vs I/R group;△△P <0.01 vs Ori-2 group | ||||||||
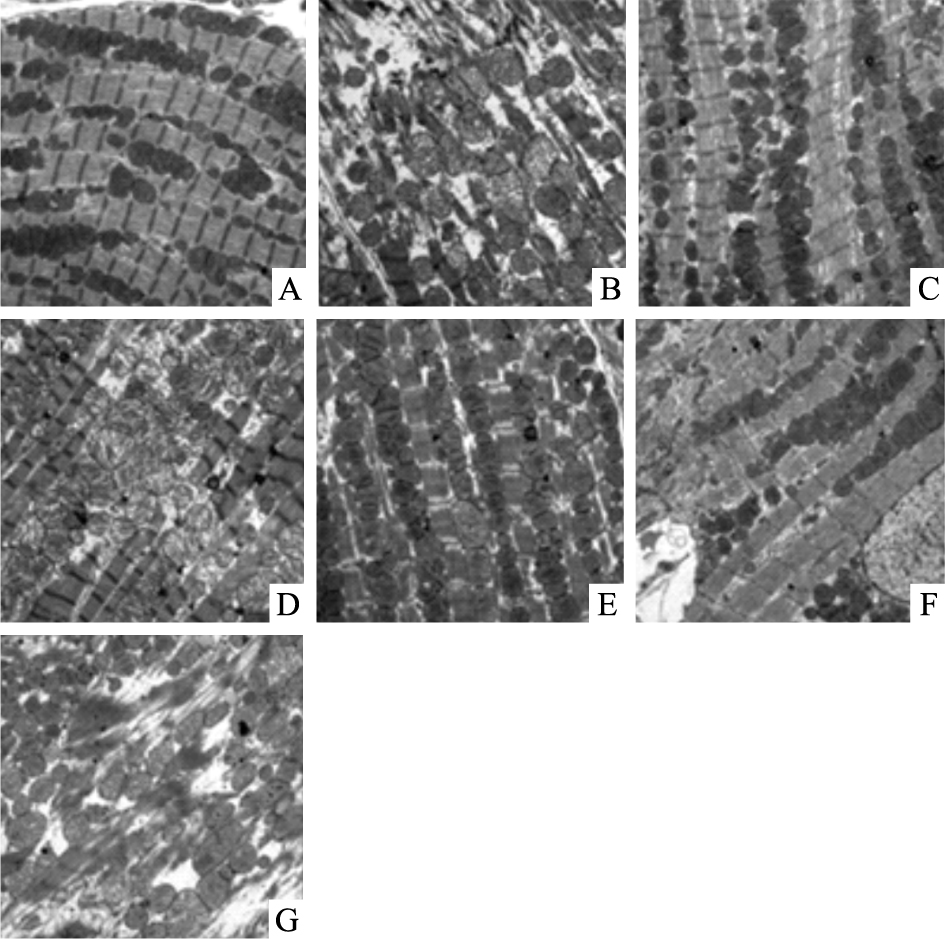
Control组大鼠的正常心肌细胞超微结构如Fig 1A所示:心肌纤维排列整齐且紧密,肌小节结构清晰可见,线粒体嵴丰富且完整,心肌间质无异常变化。I/R大鼠心肌细胞中心肌纤维排列紊乱且肌纤维溶解断裂;线粒体肿胀,基质稀疏,嵴密度降低,表明I/R引起了心肌细胞严重损伤。而荭草苷对I/R损伤导致的大鼠心肌细胞超微结构改变具有明显改善作用,大鼠心肌中肌原纤维排列整齐,肌小节完整,线粒体大小形态基本正常。在OW组中电镜观察显示其心肌细胞中肌纤维紊乱,部分肌丝溶解断裂,线粒体肿胀,嵴稀疏紊乱,进一步提示渥曼青霉素减弱了荭草苷对I/R心肌细胞的保护作用。
|
| Fig 1 Effects of orientin on ultrastructure of myocardial cells in MIRI rats Control group;B:I/R group;C:Ori-1 group;D:Ori-2 group;E:Ori-4 group;F:OW group;G:Res group(6 000×) |
由Fig 2可知,与Control组比较,心肌细胞I/R损伤能明显诱导心肌细胞凋亡(P <0.01);而荭草苷能明显抑制I/R损伤引起的心肌细胞凋亡,其中高剂量荭草苷的抑制效果更明显(P <0.01)。与Ori-2组比较,OW组的凋亡水平又明显上升(P <0.01),表明渥曼青霉素减弱了荭草苷的抗细胞凋亡作用。

|
| Fig 2 Orientin suppressed apoptosis of cardiomyocytes induced by MIRI ##P <0.01 vs I/R group;△△P <0.01 vs Ori-2 group |
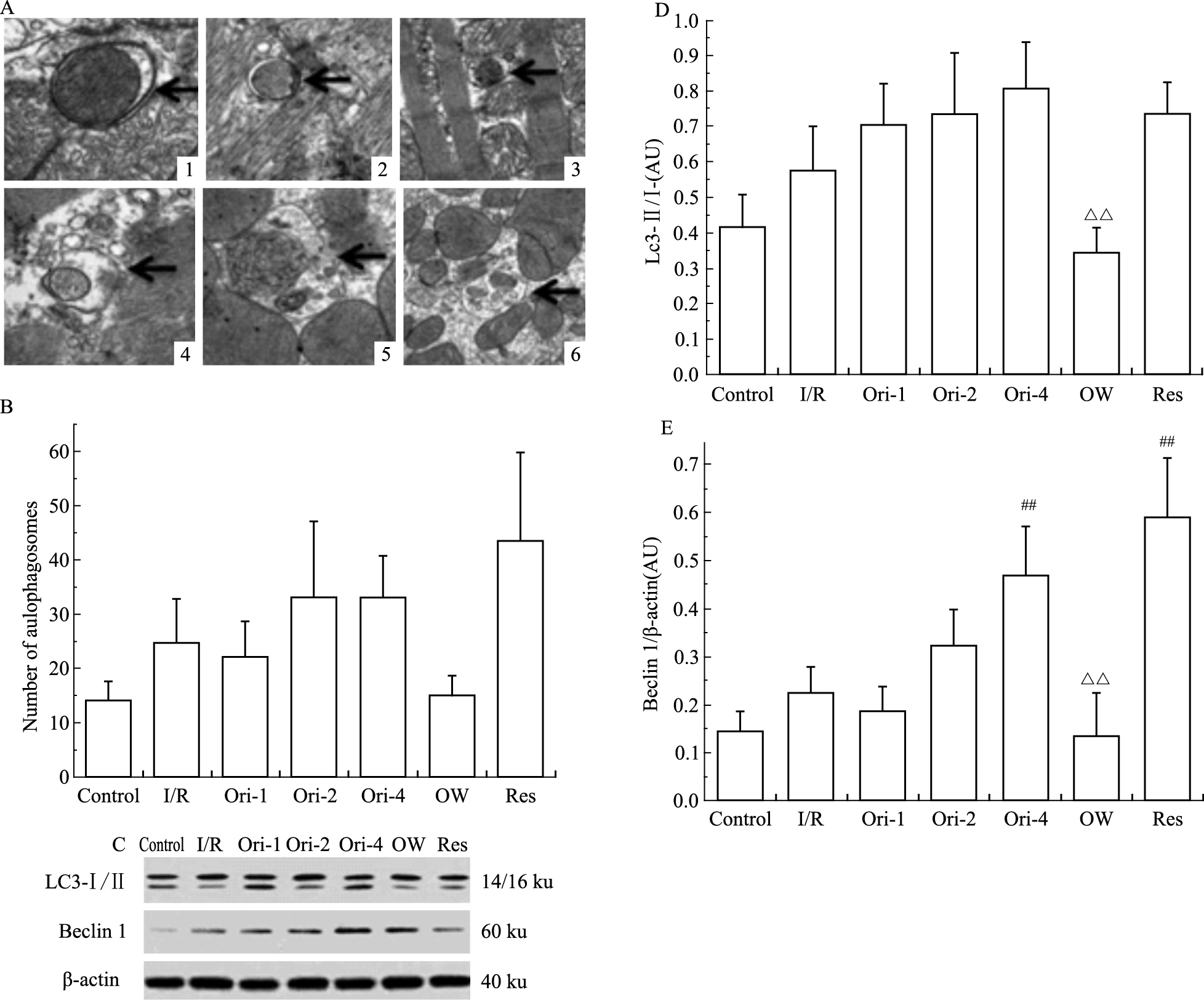
电镜下观察到心肌细胞内出现双层膜或单层膜结构内包含细胞器的自噬泡是鉴别细胞发生自噬的金标准[12]。Fig 3A为Ori-2组心肌细胞内发现的不同阶段自噬体。其中1和2为早期自噬体:双层膜结构内包裹有线粒体;3~6可能为晚期自噬体,即自噬溶酶体:单层膜内包裹有待降解的细胞器和细胞质。此外,本研究还对心肌细胞内自噬体的数量进行了统计(Fig 3B),在中高剂量荭草苷组中自噬体的数量有明显增加的趋势(差异无统计学意义),这提示荭草苷可能增强了细胞内的自噬程度。
|
| Fig 3 Orientin pretreatment induced autophagy A: Transmission electron micrographs of the myocardium of orientin(2 mg·kg-1)-treated samples showing autophagosomes(arrows);B: Quantification of the number of autophagosomes;C: Westernblot was performed with myocardial tissue lysate for expression of autophagic marker proteins;D: Quantification of LC3-Ⅱ/LC3-Ⅰ was performed by using the immunoreactive bands with QuantiOne imaging software(Biorad);E: Quantification of Beclin 1 was performed by using the immunoreactive bands with QuantiOne imaging software(Biorad).##P <0.01 vs I/R group;△△P <0.01 vs Ori-2 group. |
如Fig 3C~E所示,与Control组比较,在I/R组大鼠心肌细胞内LC3-Ⅱ/LC3-Ⅰ的比例及Beclin 1的表达水平都有上升的趋势,表明I/R损伤可诱导细胞自噬;而在荭草苷组大鼠心肌细胞内LC3- Ⅱ/LC3-Ⅰ的比例和Beclin 1的表达水平进一步增强,表明荭草苷可明显诱导自噬增强;与Ori-2组比较,在OW组大鼠心肌细胞内渥曼青霉素抑制了LC3-I向LC3-II的转化以及Beclin 1的表达,说明渥曼青霉素能抑制荭草苷诱导的心肌细胞自噬。
3 讨论心肌I/R发生时,易引发心功能障碍,血流动力学指数异常;而心肌酶(如LDH和CK-MB)的漏出量以及心肌细胞超微结构改变也是反映心肌损害程度的重要指标。在本实验中,荭草苷可明显缓解I/R引起心功能障碍,减少心肌酶的漏出,减轻心肌细胞超微结构改变,这表明荭草苷可以增强I/R后心肌功能,减轻I/R引起的心肌细胞损伤,对心肌I/R损伤有一定的预防作用。
研究认为,细胞凋亡参与了心肌I/R损伤的病理过程。心肌缺血和再灌注均可引起心肌细胞凋亡[13,14],对心脏造成不可逆的损伤,因此,细胞凋亡常被认为是心肌I/R损伤一个明显特征。前期研究表明,荭草苷的抗心肌I/R损伤的作用机制与其能抑制细胞凋亡有关,如付晓春等[10]通过建立心肌细胞缺氧/复氧损伤模型及心肌缺血/再灌损伤模型,发现荭草苷主要是通过阻止线粒体细胞凋亡途径激活来抑制心肌细胞缺氧/复氧和心肌缺血/再灌诱导的细胞凋亡;而卢娜等[11]则通过建立H9C2心肌细胞缺氧/复氧损伤模型,也发现荭草苷可明显降低缺氧/复氧损伤诱导的细胞凋亡。本实验结果表明,预给药荭草苷也能通过抑制细胞凋亡来减轻心肌I/R损伤,因此,抗细胞凋亡是荭草苷抗心肌I/R损伤的主要作用机制之一。
近年来研究发现,细胞自噬是一种与细胞凋亡不同又相关的细胞保护机制,也与心肌I/R损伤密切相关。细胞自噬是一个进化上高度保守的细胞内降解过程,主要用于降解细胞内长寿命或过度表达蛋白质以及受损细胞器。在正常生理条件下,自噬在细胞内是持续低水平进行的;但当细胞处于应激状态时,如饥饿胁迫、低氧环境或遭遇病原体感染等,自噬可被明显诱导。研究证明,心肌缺血、再灌注(或缺氧、复氧)均可诱导细胞自噬上调[4,15]。且研究进一步表明,自噬在心肌I/R损伤中起“双刃剑”作用:即在缺血期,心肌缺血缺氧可激活细胞自噬而对缺血心肌起保护作用;但在再灌注期,细胞自噬得到进一步增强,然而过度自噬会引起心肌细胞死亡,反而对心肌起损伤作用[4,15,16]。由于细胞自噬在本质上仍是一种促细胞存活机制[17],因此自噬的调控将决定其“双刃剑”的走向,自噬程度可能是其“双刃剑”作用的核心。目前,细胞自噬已成为抗心肌I/R损伤的一个新靶点。
LC3和Beclin 1是自噬体膜上的标志物,其中LC3-Ⅱ/LC3-Ⅰ的比例以及Beclin 1的表达水平与细胞内自噬水平成正比。在本实验中,荭草苷可明显诱导细胞自噬相关蛋白LC3II和Beclin 1表达上升,且增加心肌细胞内自噬体数量,这初步表明荭草苷诱导的细胞自噬对I/R损伤的心肌细胞起保护作用。由于渥曼青霉素是磷脂酰肌醇,-3激酶(PI3K)抑制剂,常用作自噬的抑制剂,因此本研究还通过加用渥曼青霉素的方法,进一步考察荭草苷抗心肌I/R损伤的保护作用与自噬的关系。在本实验中,与Ori-2组大鼠比较,OW组大鼠的血流动力学指标异常,LDH和CK-MB漏出量增加,心肌细胞超微结构出现病理学变化,表明渥曼青霉素在一定程度上减弱了荭草苷对心肌I/R损伤的保护性作用,也进一步证明了荭草苷的心肌细胞保护作用可能与细胞自噬有关,但其具体作用机制需进一步深入研究。
此外,本研究还表明:在I/R中,细胞自噬和细胞凋亡存在着复杂的相互作用。例如,在Ori-2组,I/R大鼠心肌细胞内自噬水平升高,而凋亡程度下降;而用渥曼青霉素抑制荭草苷诱导的细胞自噬后,细胞凋亡率又明显上升。这初步表明荭草苷能通过诱导细胞自噬来抑制细胞凋亡,但其具体作用机制仍需进一步探究。
综上所述,荭草苷对大鼠心脏I/R损伤具有明显保护作用,其保护机制可能与降低心肌细胞凋亡及增强细胞自噬有关。
(致谢:本文实验在北京市中央民族大学中国少数民族传统医学国家民委-教育部重点实验室完成,在此表示衷心感谢!)
| [1] | 邵莹, 吴启南, 周婧, 等. 淡竹叶黄酮对大鼠心肌缺血/再灌注损伤的保护作用[J].中国药理学通报, 2013,29(2):241-7.[1] Shao Y, Wu Q N, Zhou J, et al. Protective effects of total flavones from Lophatherum gracile onmyocardial ischemia-reperfusion injury in rats[J]. Chin Pharmacol Bull, 2013,29(2):241-7. |
| [2] | 韩笑, 刘建勋. 心肌缺血/再灌注损伤的细胞信号转导机制[J].中国药理学通报, 2004,20(1):4-7.Han X, Liu J X. Cellular signal transduction mechanisms ofmyocardial ischemia and reperfusion injury[J]. Chin Pharmacol Bull, 2004,20(1):4-7. |
| [3] | Yellon D M, Hausenloy D J. Myocardial reperfusion injury[J].N Engl J Med, 2007,357(15):1121-35. |
| [4] | Dong Y, Undyala V V, Gottlieb R A, et al. Autophagy:definition, molecular, machinery, and potential role in myocardial ischemia-reperfusion injury[J]. J Cardiovasc Pharmacol, 2010,15(3):220-30. |
| [5] | Hamacher-Brady A, Brady N R, Gottlieb R A. The interplay between pro-death and pro-survival signaling pathways in myocardial ischemia/reperfusion injury:apoptosis meets autophagy[J]. Cardiovasc Drugs Ther, 2006,20(6):445-62. |
| [6] | Xu J, Qin X, Cai X, et al. Mitochondrial JNK activation triggers autophagy and apoptosis and aggravates myocardial injury following ischemia/reperfusion[J]. Biochim Biophys Acta, 2015,1852(2):262-70. |
| [7] | 邱德文, 杜江, 夏同珩.中华本草-苗药卷彩色图谱[M]. 北京:中医古籍出版社, 2006.Qiu D W, Du J, Xia T H. Chinese Materia Medica-color atlas of Miao medicine[M]. Beijing:TCM Ancient Books Publishing House, 2006. |
| [8] | An F, Yang G D, Tian J M, et al. Antioxidant effects of the orientin and vitexin in Trolliuschinensis Bunge in D-galactose-aged mice[J]. Neural Regen Res, 2012,7(33):2565-75. |
| [9] | Fu X C, Wang M W, Li S P, et al. Anti-apoptotic effect and the mechanism of orientin on ischaemic/reperfused myocardium[J]. J Asian Nat Prod Res, 2006,8(3):265-72. |
| [10] | 付晓春. 竹叶提取物及荭草苷抗心肌缺血作用及其机制探讨[D]. 沈阳:沈阳药科大学, 2005. Fu X C. Studies on effects of anti-myocardial ischemia of bambooleaf extract and orientin andits mechanism[D]. Shenyang:Shenyang Pharmaceutical University, 2005. |
| [11] | 卢娜. 荭草素对缺血/再灌注损伤心肌细胞的保护作用及相关机制研究[D]. 杭州:浙江大学, 2011. Lu N. The protection and mechanisms of Orientin against ischemia/reperfusion (I/R) injury in cardiomyocytes[D]. Hangzhou:Zhejiang University, 2011. |
| [12] | Mizushima N. Methods for monitoring autophagy[J]. Int J Biochem Cell Boil, 2004,36(12):2491-502. |
| [13] | Gottlieb R A. Cell death pathways in acute ischemia/reperfusion injury[J]. J Cardiovasc Pharmacol Ther, 2011,16(3-4):233-8. |
| [14] | Singh S S, Kang P M. Mechanisms and inhibitors of apoptosis in cardiovascular diseases[J]. Curr Pharm Des, 2011,17(18):1783-93. |
| [15] | Ma S, Wang Y, Chen Y, et al. The role of the autophagy in myocardial ischemia/reperfusion injury[J]. Biochim Biophys Acta, 2015,1852(2):271-6. |
| [16] | Gurusamy N, Das D K.Is autophagy a double-edged sword for the heart[J]? Acta Physiol Hung, 2009,96(3):267-76. |
| [17] | Kang R, Zeh H J, Lotze M T, et al. The Beclin 1 network regulates autophagy and apoptosis[J]. Cell Death Differ, 2011,18(4):571-80. |

