


2. 遵义医学院附属医院病理科, 贵州 遵义 563000
2. Affiliated Hospital of Zunyi Medical College, Zunyi Guizhou 563000, China
高血压是心脑血管疾病发病与死亡的危险因素。肾脏既是引起高血压的重要器官,也是高血压损害的靶器官。高血压性肾损害指原发性高血压所导致的肾脏小动脉或肾实质的损害,是一个长时持续的过程,为高血压病的主要并发症。原发性高血压肾损害发病机制复杂,主要原因为血管活性物质平衡失调和肾小动脉硬化导致的肾血流动力学异常[1]。有研究报道,原发性高血压是引起高血压肾损伤并导致终末期肾衰竭的重要病因之一[2],在高血压的进程中引起的肾脏损伤与肾小管上皮细胞凋亡、氧化应激、能量代谢有关[3, 4]。Ica是淫羊藿的主要活性成分之一。现代药理学研究表明,Ica具有改善心脑血管功能、增强免疫功能、抗心肌细胞凋亡、抗SHR肾纤维化等作用[5, 6, 7]。故本研究拟用SHR的肾为研究对象,观察Ica对SHR肾小管上皮细胞凋亡的影响。
本研究使用14周龄♂ SHR,给予Ica灌胃至26周龄,采用HE染色观察肾脏病理学变化,观察Ica是否具有改善高血压肾损害的作用。采用TUNEL法观察Ica对SHR肾小管上皮细胞凋亡的影响。在确证其具有抗SHR肾小管上皮细胞作用的基础上,采用real time RT-PCR法和Western blot法检测肾Bcl-2、Bax、Bok、Active caspase-3的mRNA或蛋白变化,研究其抗凋亡的作用机制,旨在为Ica用于SHR肾损害的治疗提供基础药理学依据。
1 材料与方法 1.1 药品、试剂与仪器淫羊藿苷(纯度≥98%)购自南京泽朗医药有限公司;RNA逆转录试剂盒、荧光混合物、β-actin、Bcl-2、Bax、Bok引物购自TaKaRa生物工程公司;RNA扩增仪,美国Eppendorf公司;Bcl-2、Bax、Active caspase-3兔抗鼠抗体购自美国Abcam公司;HRP标记的β-actin抗体购自上海康成生物技术有限公司;ECL发光剂,七海生物有限公司;辣根过氧化物酶(HRP)标记山羊抗兔IgG,江苏碧云天生物技术研究所;原位细胞凋亡检测试剂盒(TdT-mediated dUTP Nick-End Labeling,TUNEL),德国ROCHE公司;Mini-PROTEAN3电泳仪、real time RT-PCR扩增仪、Mini Trans-Blot转移系统、CCD成像系统,美国 BIO-RAD公司;Olympus光学显微镜及照相系统,日本Olympus公司。
1.2 实验动物及标本制备14周龄的♂ SHR大鼠21只、WKY 大鼠7只,购自北京维通利华实验动物技术有限公司,许可证号:SCXK(京)2012-0001。SHR大鼠随机均分为3组,分别为模型组(n=7)、Ica低剂量组(20 mg·kg-1,n=7)和Ica高剂量组(40 mg·kg-1,n=7),WKY大鼠作为对照组(n=7)。所有大鼠适应性饲养1周后,Ica低剂量组与Ica高剂量组分别给予Ica 20、40 mg·kg-1,ig,bid至26周龄,模型组和对照组给予等体积双蒸水,实验结束后处死动物,取标本备用。
1.3 肾脏病理学给药至26周龄后,7%水合氯醛(0.35 g·kg-1)经腹腔注射麻醉成功后,取各组大鼠肾脏组织,置于4%甲醛溶液中固定48 h后,进行HE染色,光学显微镜下观察肾脏病理学的形态变化。
1.4 肾小管上皮细胞凋亡检测TUNEL法测定肾小管上皮细胞凋亡,光学显微镜下观察每组肾小管上皮细胞凋亡情况,正常细胞核显蓝色,凋亡阳性细胞核呈棕黄色,计算每400倍放大视野凋亡细胞数目与细胞总数的百分比。
1.5 Real-time RT-PCR法检测大鼠肾脏组织Bcl-2、Bax、Bok mRNA的表达取各组肾组织,置于1ml TRIzol中提取总RNA并纯化,经两步法-聚合酶链反应分别检测β-actin、Bcl-2、Bax、Bok mRNA的表达。所检测基因的引物序列参照GenBank中大鼠β-actin、Bcl-2、Bax、Bok序列设计,见Tab 1。目的基因表达用相对定量法:以PCR扩增过程中荧光信号强度达到阂值所需要的循环数(cycle threshold,Ct值)为统计参数,依次计算下列数据,Ct值的平均值=(Ctl+Ct2)/2(重复管);dCt=Ct值的平均值-中间值(相同检测基因的不同样品Ct值的平均值中居中的值);基因的表达=2-dct;相对定量=目的基因的表达/内参基因的表达×100,将WKY组的mRNA表达设为100。
| Gene | GeneBank accession No | Forward primer(5′-3′) | Reverse primer(5′-3′) |
| Bok | NM_017312.2 | TGGTTCATGCCCTGGTTGAC | TCTGTGCTGACCACACACTTGAG |
| Bcl-2 | NM_016993.1 | GACTGAGTACCTGAACCGGCATC | CTGAGCAGCGTCTTCAGAGACA |
| Bax | NM_017059.2 | CGAATTGGCGATGAACTGGA | CAAACATGTCAGCTGCCACAC |
| β-actin | NM_031144.2 | GGAGATTACTGCCCTGGCTCCTA | GACTCATCGTACTCCTGCTTGCTG |
取各组大鼠肾脏组织约0.1 g,剪碎后放入1 mL RIPA裂解液中,加入PMSF 10 μL,冰上匀浆后静置30 min,4℃离心12 000 r·min-1,20 min,取上清液,BCA法测定待测样品的总蛋白浓度。每孔上样量为30 μg蛋白配置为10 μL上样体系,SDS-聚丙烯酰胺凝胶,上层5%浓缩胶,下层12%分离胶。电泳后采用Bio-Rad Mini Trans-Blot转移系统PVDF膜转膜,5%蛋白封闭液封闭2.5 h,TBST洗膜10 min×3次,一抗结合:β-actin(1 ∶5 000)、Bcl-2(1 ∶200)、Bax(1 ∶1 000)、Active caspase-3(1 ∶2 000)4℃ 过夜;TBST洗膜10 min×3次,兔二抗(1 ∶2 000),常温浸泡1.5 h,ECL化学发光显色,Bio-Rad CCD成像系统获取图像。
1.7 统计学分析实验数据采用SPSS 17.0软件进行One-way ANOVA处理,方差齐用LSD法,方差不齐用Dunnett,T3法,P < 0.05认为有统计学意义。
2 结果 2.1 肾脏病理学HE染色显示WKY组肾小球毛细血管管腔开放良好,系膜基质及细胞无明显增生,肾小球囊无渗出。与WKY组比较,模型组肾小球囊腔狭窄且不规则,肾小球系膜基质增多,细胞排列紊乱,毛细血管扩张充血,个别肾小球出现皱缩,肾小管上皮细胞水肿,管腔狭窄;与模型组比较,Ica-L组肾小球囊腔略增宽,肾小球系膜基质减少,部分毛细血管扩张充血,细胞排列紊乱有所改善,肾小管管腔狭窄不明显;Ica-H组肾小球囊腔明显增宽,肾小球系膜基质无明显增生,细胞排列良好,毛细血管管腔开放良好,肾小管结构正常,见Fig 1。

|
| Fig 1 HE staining of kidney tissue and TUNEL staining of renal tubular epithelial cells(×400) A:WKY; B:Model; C:Ica-L; D:Ica-H, the scale is 50 um, and solid arrows indicate renal cysts, otherwise hollow arrows indicate mesangial matrix ; TUNEL solid arrow indicates the apoptotic cells |
与WKY组比较,模型组肾小管上皮细胞凋亡明显(P < 0.01),肾脏内凋亡阳性细胞主要见于肾小管上皮细胞和肾小球血管内皮细胞;与模型组比较,Ica-L组低、Ica-H组肾小管上皮细胞凋亡减少(P<0.01),见Tab 2,Fig 1。
( 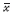 ± s, n=7) ± s, n=7) |
|
| Group | Apoptotic cell percentage/% |
| WKY | 9.01±1.18 |
| Model | 51.64±4.64## |
| Ica-L | 37.95±1.44** |
| Ica-H | 20.72±2.79** |
| ##P < 0.01 vs WKY;**P < 0.01 vs model | |
与WKY组比较,模型组Bok、Bax mRNA的水平均明显上调(P<0.01),Bcl-2 mRNA的水平明显下调(P<0.01);与模型组比较,Ica-L、Ica-H组Bok、Bax mRNA的水平均明显下调(P<0.01),Ica-H组Bcl-2 mRNA的水平明显上调(P<0.01),Ica-L组Bcl-2 mRNA的水平差异无统计学意义(P>0.05),见Fig 2。

|
Fig 2
Effects of Ica on expression of Bcl-2,Bax and Bok mRNA in kidney tissue( 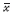 ± s, n=7)
##P < 0.01 vs WKY;**P < 0.01 vs model ± s, n=7)
##P < 0.01 vs WKY;**P < 0.01 vs model
|
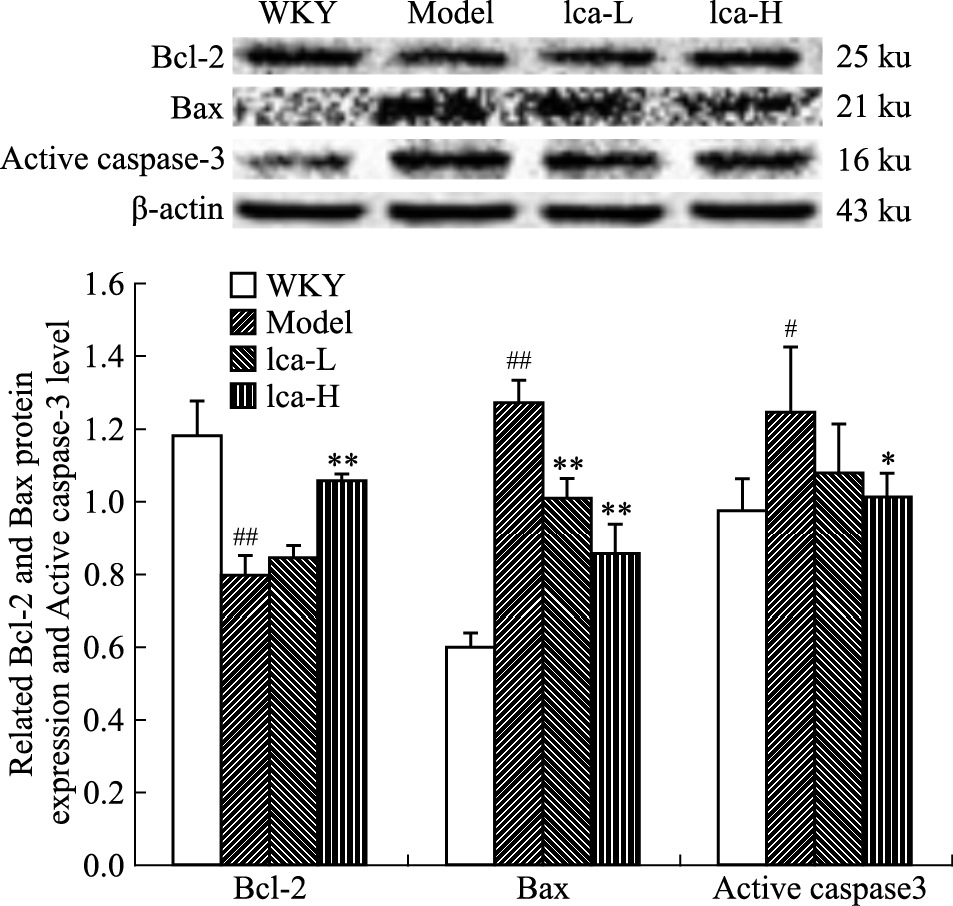
与WKY比较,模型组Bax、Active caspase-3蛋白的表达均明显上调(P<0.05或P<0.01),Bcl-2蛋白的表达明显下调(P<0.01);与模型组比较,Ica-L、Ica-H组Bax蛋白的表达均明显下调(P<0.01),Ica-H组Active caspase-3蛋白的表达明显下调(P<0.05),Ica-L组Active caspase-3蛋白的表达差异无统计学意义(P>0.05),Ica-H组Bcl-2蛋白的表达明显上调(P<0.01),Ica-L组Bcl-2蛋白的表达差异无统计学意义(P>0.05),见Fig 3。
|
Fig 3
Effects of Ica on expression of Bcl-2,Bax and Active caspase-3 protein in kidney tissue( 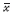 ± s, n=7)
#P < 0.05,##P< 0.01 vs WKY;*P< 0.05,**P< 0.01 vs model ± s, n=7)
#P < 0.05,##P< 0.01 vs WKY;*P< 0.05,**P< 0.01 vs model
|
SHR的发病机制和病理与人类高血压病相似,是目前研究原发性高血压应用最广泛的动物模型。本研究结果显示,与WKY组比较,SHR出现明显的高血压肾损害的病理改变,说明26周龄的SHR已出现肾损害。该结果与本实验室既往研究揭示的26周龄SHR出现肾损害的报道一致[7]。本研究中,Ica明显改善26周龄SHR的肾损害。有研究报道,Ica可减轻大鼠肾脏缺血/再灌注损伤[8]。
目前研究已证实,细胞凋亡参与了高血压靶器官损害,并在调节靶器官细胞数量,保护器官功能方面发挥着非常重要作用[9]。细胞凋亡是细胞在生理或病理状态下发生的一种自发性、程序性死亡的过程。已有研究报道,促进肾小管上皮细胞的凋亡可加重SHR、肾缺血/再灌注损伤等肾损害[8, 10]。本研究TUNEL染色结果显示,模型组肾脏发生细胞凋亡且凋亡细胞主要为肾小管上皮细胞,而Ica-L、Ica-H组肾脏细胞凋亡减少,特别是肾小管上皮细胞凋亡明显减少,提示Ica具有抗肾小管上皮细胞凋亡的作用。
线粒体通路在细胞存亡机制中起着至关重要的作用,尤其Bcl-2蛋白家族和含半胱氨酸的天冬氨酸蛋白水解酶(caspase)家族目前最受关注。Bcl-2家族成员按其功能可分为促凋亡蛋白和抗凋亡蛋白两种,Bcl-2是主要的抗凋亡蛋白,Bax、Bok是促凋亡蛋白,而Bax是促凋亡代表成员。已有研究表明,Bax和Bcl-2都是以线粒体为靶细胞器发挥作用[11, 12]。Bax蛋白多以非活性单体形式分布于胞质中,只有在接收到凋亡信号刺激被激活后,发生分子构象改变,移位并插入线粒体外膜后形成Bax 大孔道,破坏线粒体膜的完整性,并与Bcl-2 等抑制凋亡的蛋白对抗,阻止其抗凋亡作用的发挥[13]。caspase-3是ICE(白细胞介素1-β转化酶) 家族成员之一,又称为半胱氨酸蛋白酶32(CPP32),与Ced-3同源性最高,是多种凋亡途径的共同下游效应部分,在细胞凋亡过程中占据核心地位,被称为“死亡执行蛋白酶”[14]。Bcl-2、Bax蛋白位于线粒体上游,是线粒体膜的通透性改变的重要调控因素[15],其过度表达能控制cyt-C的释放和下游 caspase-3蛋白酶的活化,介导细胞的存活或死亡[16]。
淫羊藿系小檗科淫羊藿属植物,具有补肾阳,强筋骨,祛风湿的功效。有研究报道,Ica具有抗生殖细胞凋亡的作用[17],Ica还可通过抑制caspase-3激活减轻SHR心肌细胞凋亡[6],在5/6肾切除大鼠模型中,Ica通过调节Bax和Bcl-2的表达,改善肾脏功能[18]。本研究结果显示,与WKY组比较,模型组Bok、Bax mRNA的水平以及Bax、Active caspase-3蛋白的表达明显上调,Bcl-2 mRNA的水平以及Bcl-2蛋白的表达下调,提示肾组织Bcl-2、Bax、Active caspase-3、Bok表达的变化可能参与SHR肾损害的发生发展。Ica-L、Ica-H组Bok、Bax mRNA和Bax蛋白,Ica-H组Active caspase-3蛋白的表达均低于模型组,而Ica-H组Bcl-2 mRNA和蛋白的表达均高于模型组,提示Ica可能通过抑制肾组织的Bax、Bok、Active caspase-3的表达,上调Bcl-2的表达从而发挥抗SHR肾小管上皮细胞凋亡的作用。
综上,Ica对SHR肾损害的保护作用至少与其抑制其肾小管上皮细胞凋亡有关,其机制可能是抑制Bax、Bok、Active caspase-3的表达,促进Bcl-2的表达。本研究为中药淫羊藿的主要活性成分Ica用于肾损害的治疗提供基础药理学依据。
(致谢:本实验所有工作均在遵义医学院药理学教研室暨基础药理省部共建教育部重点实验室完成,感谢教研室的支持和帮助,感谢王俊逸、华亮、吴芹、高杨等提供的无私帮助!)
| [1] | 高秀林.高血压肾损害发病机制的研究进展[J].北京医学, 2007,29(9):559-61. Gao X L. Advances in the pathogenesis of hypertensive renal damage[J]. Beijing Medical Journal, 2007,29(9):559-61. |
| [2] | Gassanov N, Pollok M, Er F.Acute renal failure associated with malignant hypertension[J].Dtsch Med Wochenschr, 2009,134(44):2224-7. |
| [3] | 蒋嘉烨, 罗珊珊, 栗源, 等.SHR高血压进程中肾脏蛋白表达谱的变化[J].中国药理学通报, 2012,28(2):189-94. Jiang J Y, Luo S S, Li Y, et al. Study in the renal protein expressions during the developing progress of SHR[J]. Chin Pharmacol Bull, 2012,28(2):189-94. |
| [4] | 周巧玲, 唐荣, 朱莉莉, 等.冬虫夏草对自发性高血压大鼠肾脏Klotho表达和肾小管上皮细胞凋亡的影响[J].中华肾脏病杂志, 2009,25(4):305-12. Zhou Q L, Tang R, Zhu L L, et al. Effects of cordyceps sinensis on Klotho expression in kidneys and apotosis in renal tubular epithelial cells of spontaneously hypertensive rats[J]. Chin J Nephrol, 2009,25(4):305-12. |
| [5] | 龚其海, 杨丹莉, 石京山, 等.淫羊藿苷的神经药理作用及分子机制研究进展[J].中国新药与临床杂志, 2011,30(7):481-6. Gong Q H, Yang D L, Shi J S, et al. Advances in neuroharmacological effects and molecular mechanisms of icariin[J]. Chin J New Drugs Clin Rem, 2011,30(7):481-6. |
| [6] | 钱志强, 王颖婉, 李叶丽, 等.淫羊藿苷通过抑制caspase-3激活减轻自发性高血压大鼠心肌细胞凋亡[J].遵义医学院学报, 2015,38(5):450-3. Qian Z J, Wang Y W, Li Y L, et al. Icarrin attenuates myocardial apoptosis by inhibiting activation of caspase-3 in spontaneously hypertensive rats[J]. J Zunyi Med Univ, 2015,38(5):450-3. |
| [7] | 李叶丽, 王颖婉, 李意奇, 等.淫羊藿苷通过降低醛固酮水平减轻自发性高血压大鼠肾间质纤维化[J].中国药理学通报, 2014,30(4):519-22. Li Y L, Wang Y W, Li Y Q, et al. Icariin attenuates renal interstitial fibrosis by reducing aldosterone in SHR[J].Chin Pharmacol Bull, 2014,30(4):519-22. |
| [8] | 丰贵文, 刘龙山, 尚文俊.淫羊藿苷对大鼠肾脏缺血再灌注后炎性损伤的保护[J].中国组织工程研究, 2012,16(40):7496-502. Feng G W, Liu L S, Shang W J. Icariin alleviates renal ischemia-reperfusion injury in rats through inhibition of inflammation[J]. Chin J Tissue Engin Res, 2012,16(40):7496-502. |
| [9] | Hamet P, Richard L, Dam T V, et al. Apoptosis in target organs of hypertension[J]. Hypertension, 1995, 26:642-8. |
| [10] | Balasubramanian S, Jansen M, Valerius M T, et al. Orphan nuclear receptor Nur77 promotes acute kidney injury and renal epithelial apoptosis[J]. J Am Soc Nephrol, 2012,23(4):674-86. |
| [11] | Gupta S, Da S B, Sen S. Cardiac hypertrophy:mechanisms and therapeutic Opportunities[J]. Antioxid Redox Signal, 2007,9(6):623-52. |
| [12] | Renault T T, Teijido O, Missire F, et al. Bcl-xL stimulates Bax relocation to mitochondria and primes cells to ABT-737[J]. Int J Biochem Cell Biol, 2015,64:136-46. |
| [13] | Tan K O, Fu N Y, Sukumaran S K, et al. MAP-1 is a mitochondrial effector Of Bax[J].Proc Natl Acad Sci USA, 2005,102(41):14623-8. |
| [14] | Odonkor C A, Achilefu S. Modulation of effector caspase cleavage determinesresponse of breast and lung tumor cell lines to chemotherapy[J]. Cancer Invest, 2009,27(4):417-29. |
| [15] | Lin H H, Chen J H, Huang C C, et al. Apoptotic effect of 3, 4-dihydroxybenzoic acid on human gastric carcinoma cells involving JNK/p38MAPK signaling activation[J].Int Cancer, 2007,120(11):2306-16. |
| [16] | Scorrano L, Korsmeyer S J. Mechanisms of cytochrome c release by proapoptotic Bcl-2 family members[J]. Biochem Biophys Res Commun, 2003,304(3):437-44. |
| [17] | 章振保, 田生平, 杨镜秋, 等.淫羊藿苷与辜酮治疗亚急性衰老雄性大鼠的实验研究[J].中国男科学杂志, 2006,20(8):13. Zhang Z B, Tian S P, Yang J Q, et al. The experimental study on the treatment of sub一acutely aging male rats by Icariin and testosterone[J]. Chin J Androl, 2006,20(8):13. |
| [18] | 朱铁锤.淫羊藿苷对5/6肾切除大鼠Bcl-2、Bax表达的影响[J].中国老年学杂志, 2013(33):4206-7. Zhu T C. Icariin on 5/6 nephrectomized rats Bcl-2, Bax expression[J].Chin J Gerontol, 2013(33):4206-7. |

