


2. 广州市番禺区心血管疾病研究所, 广东 广州 511400;
3. 中山大学附属第一医院黄埔院区心血管内科CCU, 广东 广州 510070;
4. 中山大学附属第一医院心血管内科, 广东 广州 510080
 , CHEN Jing-fu3, HE Jie-yi1, 2, SONG Ming-cai1, 2, YU Sheng-long1, 2, ZHANG Wen-zhu1, 2, ZHENG Dong-dan3, LIAO Xin-xue4
, CHEN Jing-fu3, HE Jie-yi1, 2, SONG Ming-cai1, 2, YU Sheng-long1, 2, ZHANG Wen-zhu1, 2, ZHENG Dong-dan3, LIAO Xin-xue4

2. Cardiovascular Institute of Panyu District, Guangzhou 511400, China;
3. Cardiac Care Unit of Department of Cardiology, Huangpu Division, the First Affiliated Hospital, Sun Yat-sen University, Guangzhou 510070, China;
4. Dept of Cardiology, the First Affiliated Hospital, Sun Yat-sen University, Guangzhou 510080, China
ATP敏感性钾通道(ATP-sensitive K+ channel,KATP通道)是受细胞内ATP浓度调控的一种内向整流钾通道,于1983年由Noma首先在心肌细胞中发现[1]。最近,我们证实:HG可通过损伤KATP通道引起心肌细胞损伤;外源性硫化氢(hydrogen sulfide,H2S)可通过调控KATP通道对抗高糖引起的心肌细胞损伤[2]。KATP通道的心肌保护可能涉及多个与其关系密切的下游信号分子通路,进一步探讨KATP通道在H2S对抗高糖引起的心肌损伤中的分子作用机制,具有重要的意义。Akt是一种分子质量约为60 ku的丝氨酸/苏氨酸蛋白激酶[3],是多条信号通路的重要交叉点,调控细胞生长与存活、增殖与凋亡、糖类代谢等多种生物学效应。有研究指出:在链脲霉素诱导的糖尿病心肌病(diabetic cardiomyopathy,DCM)大鼠模型中,Akt的活性受到明显的抑制[4];另有研究证实:通过激活Akt通路可对心肌起保护作用[5, 6]。由此可见,Akt通路在心肌细胞的生理和病理生理过程中发挥非常重要的作用。另一方面,新型气体信号分子H2S是KATP通道的开放剂[7],其对脂肪细胞[8]和神经细胞[9, 10]的保护作用与其激活Akt通路有关。此外,Tang等[11]报道:H2S可通过调控KATP通道/PI3K/Akt通路保护神经细胞对抗1-甲基-4苯基吡啶离子(1-Methy-4-phenylpyridnium Ion,MPP+)引起的损伤。基于上述研究,我们推测,通过开放KATP通道继而激活Akt通路可能是外源性H2S保护心肌细胞对抗HG引起的损伤一个重要机制。
为此,本研究建立高糖损伤H9c2心肌细胞模型[12],旨在探讨:(1)HG对心肌细胞Akt信号通路的影响;(2)H2S能否减轻HG对Akt活性的抑制作用;(3)KATP通道和Akt通路之间的关系如何;(4)H2S是否通过调控KATP通道-Akt通路对抗高糖引起的心肌细胞损伤。
1 材料与方法 1.1 材料抗总(t)-Akt抗体、抗p-Akt抗体购自Cell Signaling Technology(USA);硫氢化钠(NaHS)、LY294002(Akt通路抑制剂)、双氯荧光素(2′,7′-dichlorfluorescein-diacetate,DCFH-DA)、Hoechst 33258和JC-1购自Sigma-Aldrich(USA);吡拉地尔(pinacidil,Pin)、格列本脲(glibenclamide,Gli)由Cayman Chemical Co.(USA)供应;细胞计数试剂盒8(cell counter kit-8,CCK-8)购自Dojindo Lab(Japan);DMEM培养基购自Hyclone公司(USA);特级胎牛血清购自Gibco BRL(USA)。H9c2 心肌细胞由中山大学实验动物中心提供。
1.2 细胞培养及实验分组H9c2心肌细胞来源于大鼠胚胎期的心脏组织,培养于含10%胎牛血清的DMEM培养基,置于5% CO2、37 ℃的温箱中培养。实验分为10组:(A)对照(control)组:DMEM培养基(5.5 mmol·L-1葡萄糖)处理心肌细胞24 h;(B)高糖(high glucose,HG)组:35 mmol·L-1葡萄糖处理H9c2心肌细胞24 h;(C)NaHS+HG组:400 μmol·L-1 NaHS作用心肌细胞30 min,撤去,PBS洗2次,接着35 mmol·L-1葡萄糖处理24 h;(D)Ly294002+NaHS+HG组:30 μmol·L-1 Ly294002作用心肌细胞30 min,撤去,PBS洗2次,后续实验步骤与(C)组相同;(E)NaHS组:400 μmol·L-1 NaHS作用心肌细胞30 min,撤去,PBS洗2次,接着DMEM培养基处理24 h;(F)Ly294002组:30 μmol·L-1 Ly294002作用心肌细胞30 min,撤去,PBS洗2次,接着DMEM培养基处理24 h;(G)Pin+ HG组:50 μmol·L-1 Pin作用心肌细胞30 min,撤去,PBS洗2次,接着35 mmol·L-1葡萄糖处理24 h;(H)Pin组:50 μmol·L-1 Pin作用心肌细胞30 min,撤去,PBS洗2次,接着DMEM培养基处理24 h;(I) Gli+NaHS+HG组:1 mmol·L-1 Gli作用心肌细胞30 min,撤去,PBS洗2次,后续实验步骤与(C)组相同;(J) Gli组:1 mmol·L-1 Gli作用心肌细胞30 min,撤去,PBS洗2次,接着DMEM培养基处理24 h。
1.3 Western blot 法检测Akt蛋白表达水平将H9c2心肌细胞接种于35 mm培养皿中,培养至80%满时,各实验组给予不同的处理因素后,用预冷的PBS洗3次,加入裂解液,4 ℃静置30 min,12 000 r·min-1离心10 min,取上清,然后采用BCA法进行蛋白定量。总蛋白经十二烷基硫酸钠聚丙烯酰胺凝胶电泳分离后,转移到PVDF膜上。用5%脱脂奶粉封闭60 min,随后分别加入抗t-Akt和抗p-Akt(1 ∶1 000)抗体,4 ℃过夜,然后用TBST洗3 次,5 min/次,与相应的二抗(1 ∶2 500)室温孵育1.5 h,用TBST洗3次,5 min/次。将PVDF膜用发光试剂ECL显色,暗室曝光到X线片上,凝胶成像系统扫描分析结果。实验重复5次。
1.4 CCK-8测定细胞存活率将H9c2心肌细胞接种于96孔培养板中,当心肌细胞生长到占培养孔面积大约80%时,按各分组处理后,于每孔中加入10 μL CCK-8和90 μL DMEM,轻摇,37 ℃孵育2.5 h,用酶标仪(λ=450 nm)记录各孔吸光度(A)。取5孔A值的平均数,按下列公式计算细胞存活率:细胞存活率/%=A处理组/A对照组×100%。实验重复5次。
1.5 Hoechst 33258核染色检测细胞凋亡将H9c2 心肌细胞接种于24孔培养板中,在细胞生长到占培养孔面积大约80%时,按各分组处理后,用PBS冲洗3次,然后用4%多聚甲醛于4 ℃环境中固定10 min,加入含5 mg·L-1 Hoechst 33258试剂,于37 ℃温箱孵育30 min,在荧光显微镜下(TE-2000′ Nikon′ Japan)摄片,鉴别正常的心肌细胞和凋亡的心肌细胞,随机选取视野,在荧光显微镜下摄片。实验重复5次。
1.6 DCFH-DA染色测定胞内ROS水平将H9c2心肌细胞接种于24孔培养板中,当细胞生长到培养孔面积大约80%时,经上述各实验组不同的处理因素后,PBS冲洗3次,用10 μmol·L-1 DCFH-DA染液于37℃温箱中孵育30 min,然后用PBS冲洗3次。在荧光显微镜下随机选取5个不重复区摄片,用ImageJ 1.47i软件分析5个视野绿色荧光强度的平均值,再对每组的各样本进行统计分析。实验重复5次。
1.7 JC-1染色测定MMP将H9c2 心肌细胞接种于24孔培养板中,当细胞生长到培养孔面积大约80%时,上述各实验组经不同的处理因素作用后,用PBS冲洗3次,用10 μg·L-1 JC-1的无血清培养基于37 ℃温箱中孵育45 min,然后用PBS冲洗3次。在荧光显微镜下随机选取5个不重复区摄片,细胞核周围绿色的亮点即为摄取了JC-1的线粒体。用Image J 1.47i软件分析5个视野绿色荧光强度的平均值,再对每组的各样本进行统计分析。实验重复5次。
1.8 统计学处理 实验数据用SPSS 17.0软件进行统计分析,所有结果以 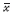 ± s表示,组间比较采用单因素方差分析(one-way ANOVA),用SNK-q进行均数之间的比较。
± s表示,组间比较采用单因素方差分析(one-way ANOVA),用SNK-q进行均数之间的比较。
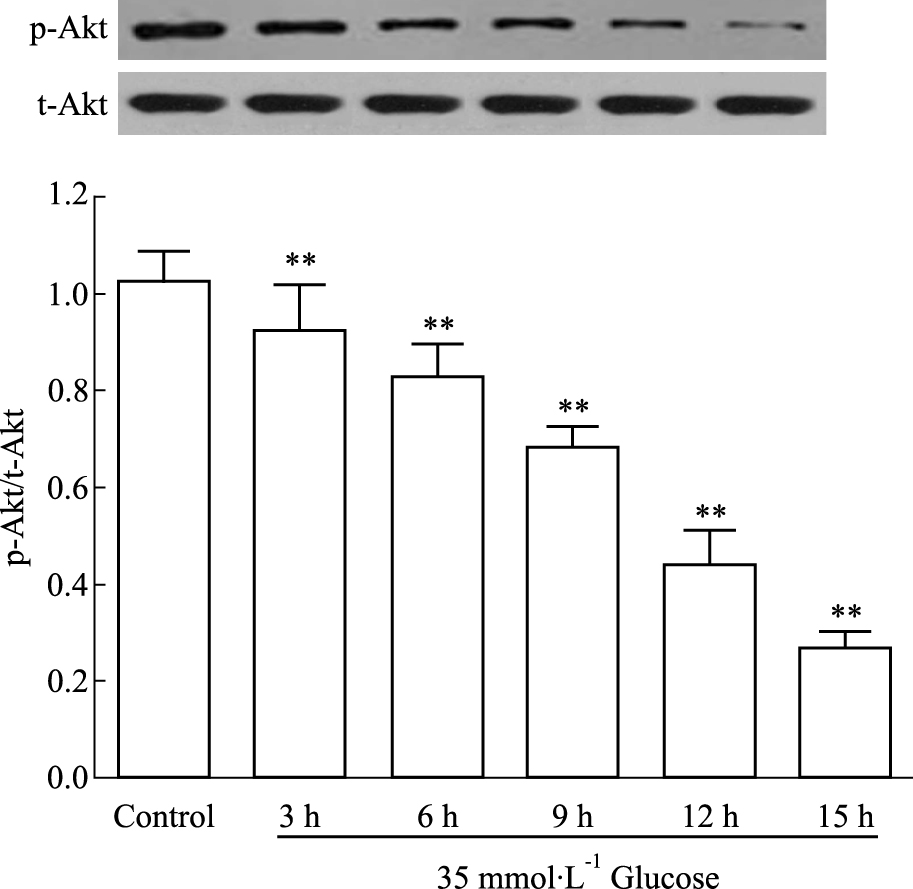
应用35 mmol·L-1葡萄糖(高糖,HG)分别处理H9c2心肌细胞0~24 h,其中,3 h开始p-Akt蛋白表达水平明显降低(P < 0.01),6、9、12 h时进一步降低(P < 0.01),HG作用24 h时,p-Akt降至最低水平(P < 0.01)(Fig 1)。但是,HG对心肌细胞的t-Akt的表达水平无明显的影响。
|
| Fig 1 HG inhibits expression levelof p-Akt in H9c2 cardiac cells(n=5) H9c2 cardiac cells were exposed to HG over a 24 h time period.**P < 0.01 vs control |
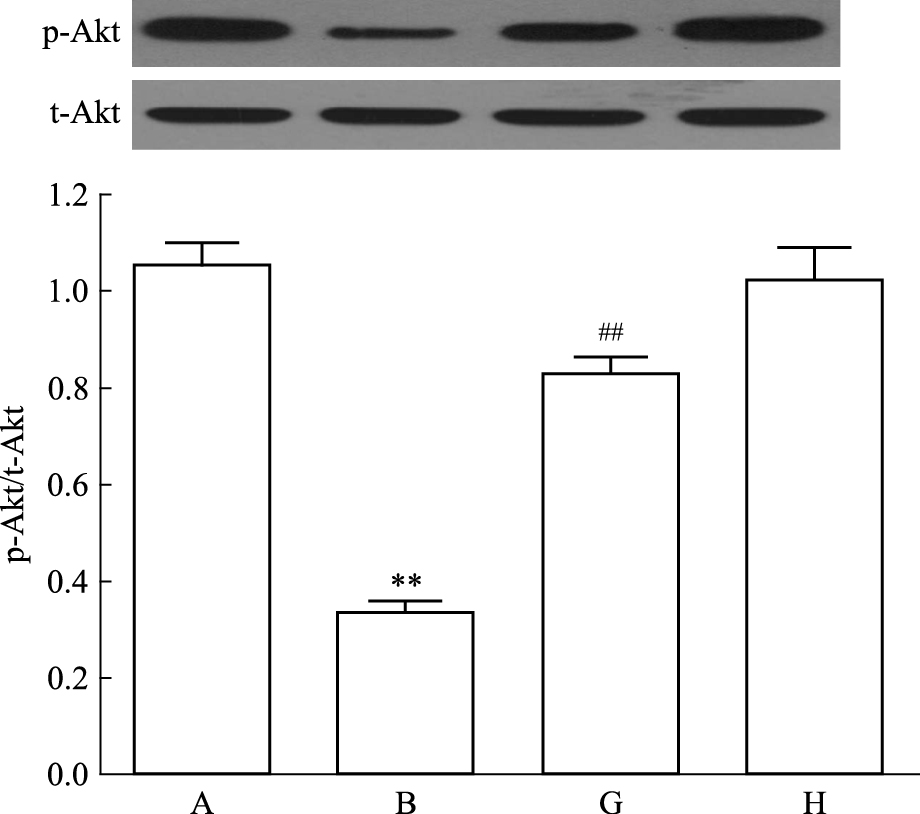
Fig 2显示,HG作用心肌细胞24 h可使p-Akt蛋白的表达明显减少,与对照组比较,差异有显著性(P < 0.01)。在HG作用心肌细胞前,应用50 μmol·L-1 KATP通道开放剂Pin预处理心肌细胞30 min,p-Akt蛋白的表达较HG处理组明显增多,两者差异有显著性(P < 0.01)。50 μmol·L-1 Pin本身对心肌细胞p-Akt蛋白的基础表达水平无明显的影响(Fig 2)。
|
| Fig 2 KATP channels attenuate HG-induceddown-regulation of p-Akt expression level(n=5) A: Control; B: Glucose 35 mmol·L-1; G: Pin 50 μmol·L-1+Glucose 35 mmol·L-1;H: Pin 50 μmol·L-1.**P < 0.01 vs control group;##P < 0.01 vs the HG-treated group |
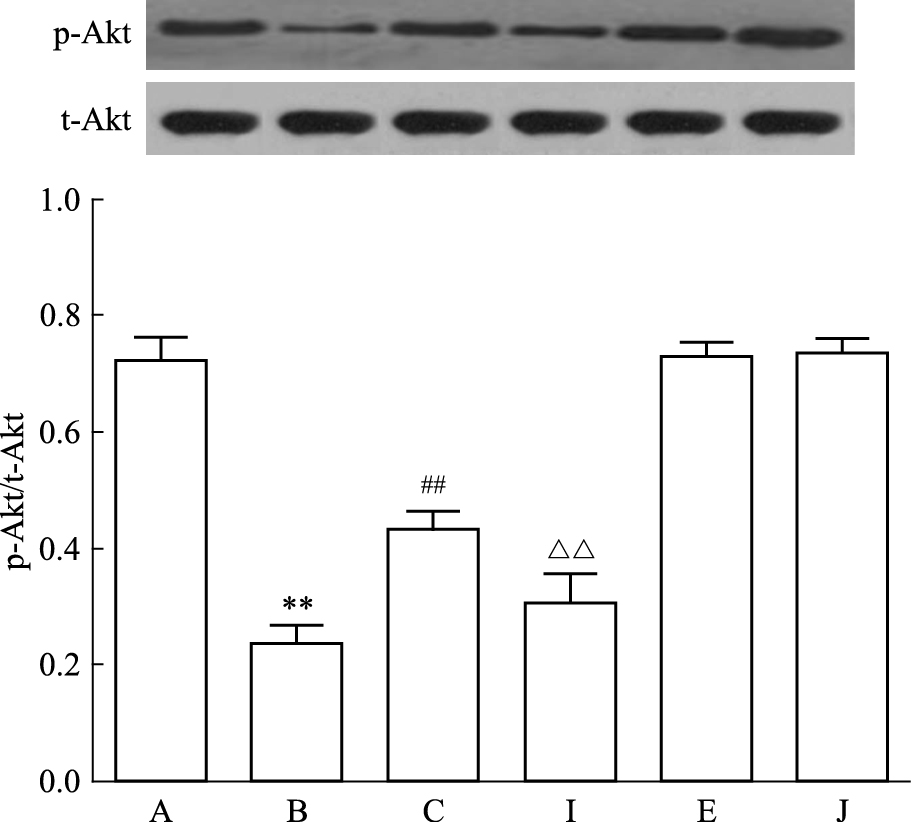
Fig 3显示,应用HG处理心肌细胞24 h可使p-Akt蛋白表达明显减少,与对照组比较,差异具有统计学意义(P < 0.01)。在HG处理心肌细胞前,应用400 μmol·L-1 NaHS预处理30 min,p-Akt蛋白的表达水平有所上升,与HG处理组比较,差异有显著性(P < 0.01)。但是,在NaHS预处理前,应用1 mmol·L-1 KATP通道阻断剂Gli作用心肌细胞30 min,p-Akt蛋白表达明显下降,与NaHS预处理组比较,差异有显著性(P < 0.01)。单纯应用400 μmol·L-1 NaHS或1 mmol·L-1 Gli本身对心肌细胞p-Akt蛋白的基础表达水平无明显的影响。
|
| Fig 3 KATP channels contribute to inhibitory effect ofH2S on high glucose (HG)-induced decrease inexpression level of p-Akt(n=5) A: Control; B: Glucose 35 mmol·L-1; C: NaHS 400 μmol·L-1+Glucose 35 mmol·L-1; I: Gli 1 mmol·L-1+NaHS 400 μmol·L-1+Glucose 35 mmol·L-1; E: NaHS 400 μmol·L-1; J: Gli 1 mmol·L-1.**P < 0.01 vs control group;##P < 0.01 vs the HG-treated group;△△P < 0.01 vs the NaHS+HG-treated group |
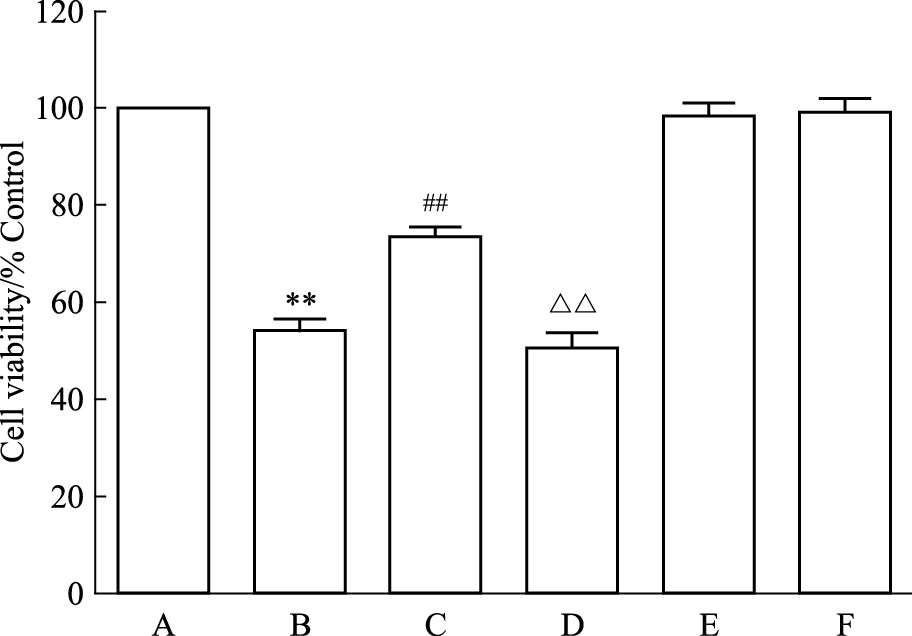
Fig 4显示,应用400 μmol·L-1 NaHS预处理心肌细胞30 min能使细胞存活率升高,与HG组处理组比较,差异具有统计学意义(P < 0.01)。但是,应用30 μmol·L-1 LY294002(Akt的抑制剂)预处理心肌细胞30 min,心肌细胞存活率较NaHS预处理组明显降低,两者差异具有统计学意义(P < 0.01)。NaHS或LY294002本身对细胞存活率无明显的影响。
|
| Fig 4 Akt pathway contributes to protectionof exogenous H2S against HG-inducedcytotoxicity in H9c2 cardiac cells(n=5) A: Control; B: Glucose 35 mmol·L-1; C: NaHS 400 μmol·L-1+Glucose 35 mmol·L-1; D: LY294002 30 μmol·L-1+NaHS 400 μmol·L-1+Glucose 35 mmol·L-1; E: NaHS 400 μmol·L-1; F: LY294002 30 μmol·L-1.**P < 0.01 vs control group;##P < 0.01 vs the HG-treated group;△△P < 0.01 vs the NaHS+HG-treated group |
Fig 5中Hoechst核染色的检测结果显示,正常的H9c2心肌细胞的染色质分布均匀,呈现弥散均匀的低密度荧光(Fig 5A)。心肌细胞经HG处理24 h,呈现典型的凋亡特征(即细胞核呈现浓缩致密的固缩形态或颗粒荧光)的细胞数量增多(Fig 5B),与正常对照组比较,差异具有统计学意义(P < 0.01)。应用400 μmol·L-1 NaHS预处理心肌细胞30 min,凋亡细胞的数量明显减少,与HG处理组比较,差异有统计学意义(P < 0.01,Fig 5C)。然而,在NaHS预处理前,采取30 μmol·L-1 Akt的抑制剂LY294002预处理心肌细胞30 min能使心肌细胞凋亡数量增加,与NaHS预处理组比较,差异具有统计学意义(P < 0.01,Fig 5D)。NaHS或LY294002本身对细胞凋亡数量无明显的影响(P>0.05)。

|
| Fig 5 Akt inhibitor blocks protectionof exogenous H2S against HG-inducedapoptosis in H9c2 cardiac cells(n=5) A: Control; B: Glucose 35 mmol·L-1; C: NaHS 400 μmol·L-1+Glucose 35 mmol·L-1; D: LY294002 30 μmol·L-1+NaHS 400 μmol·L-1+Glucose 35 mmol·L-1; E: NaHS 400 μmol·L-1; F: LY294002 30 μmol·L-1.**P < 0.01 vs control group;##P < 0.01 vs the HG-treated group;△△P < 0.01 vs the NaHS+HG-treated group |
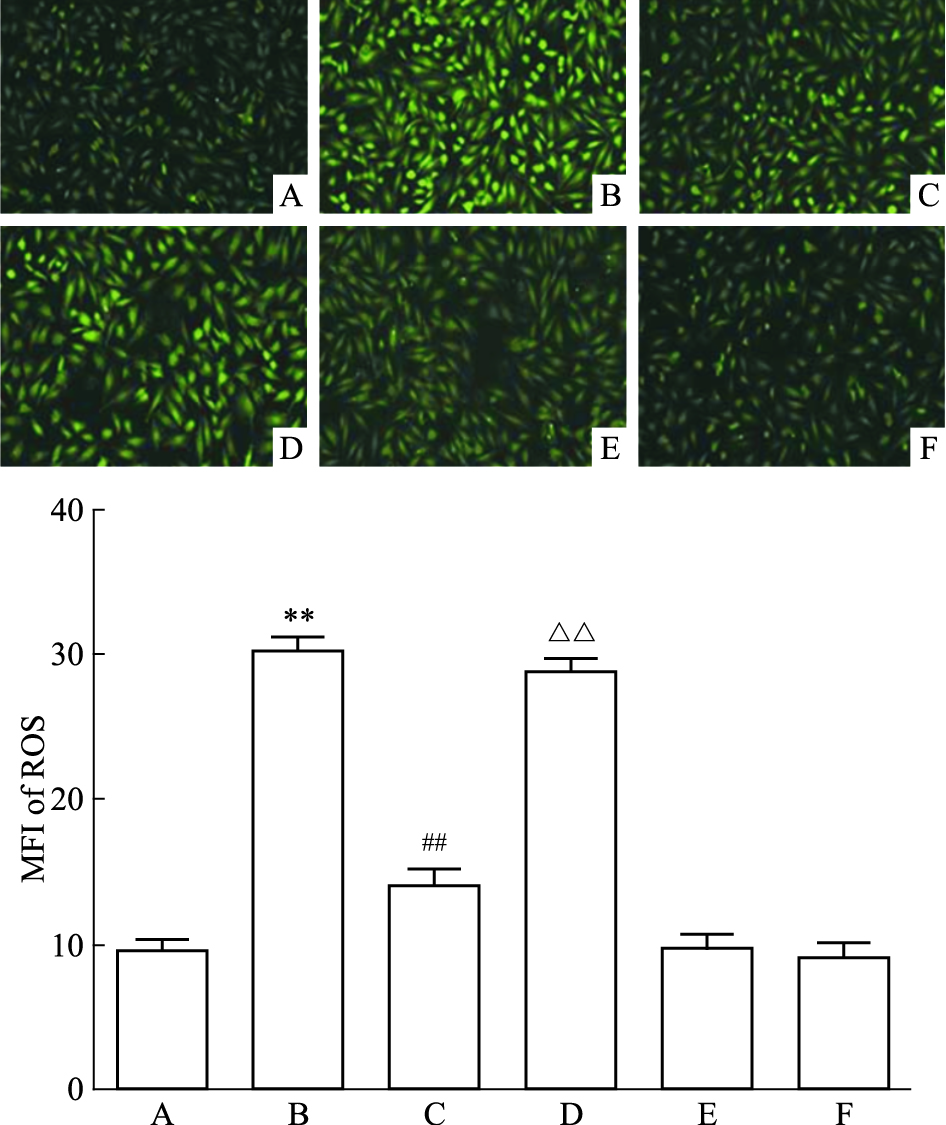
Fig 6B显示,采用HG作用H9c2心肌细胞24 h可使胞内DCFH的平均荧光强度(mean fluorescence intensity,MFI,能间接反映ROS水平)明显增强,与正常对照组(Fig 6A)相比,差异有显著性(P < 0.01)。然而,在HG作用前,应用400 μmol·L-1 NaHS预处理心肌细胞30 min,可使MFI由(30.1±0.95)%降低至(14.1±1.13)%,两者差异有显著性(P < 0.01,Fig 6C)。但是,先给予30 μmol·L-1 Akt的抑制剂LY294002预处理心肌细胞30 min,再采用NaHS预处理,心肌细胞的MFI增加至(28.9±0.86)%,与NaHS预处理组比较,差异具有统计学意义(P < 0.01,Fig 6D)。NaHS或LY294002本身对心肌细胞ROS的生成无明显的影响(P>0.05)。
|
| Fig 6 Akt pathway participates in protective effectof exogenous H2S against HG-induced increasein intracellular ROS generation in H9c2 cardiac cells(n=5) A: Control; B: Glucose 35 mmol·L-1; C: NaHS 400 μmol·L-1+Glucose 35 mmol·L-1; D: LY294002 30 μmol·L-1+NaHS 400 μmol·L-1+Glucose 35 mmol·L-1; E: NaHS 400 μmol·L-1; F: LY294002 30 μmol·L-1.**P < 0.01 vs control;##P < 0.01 vs the HG-treated group;△△P < 0.01 vs the NaHS+HG-treated group |
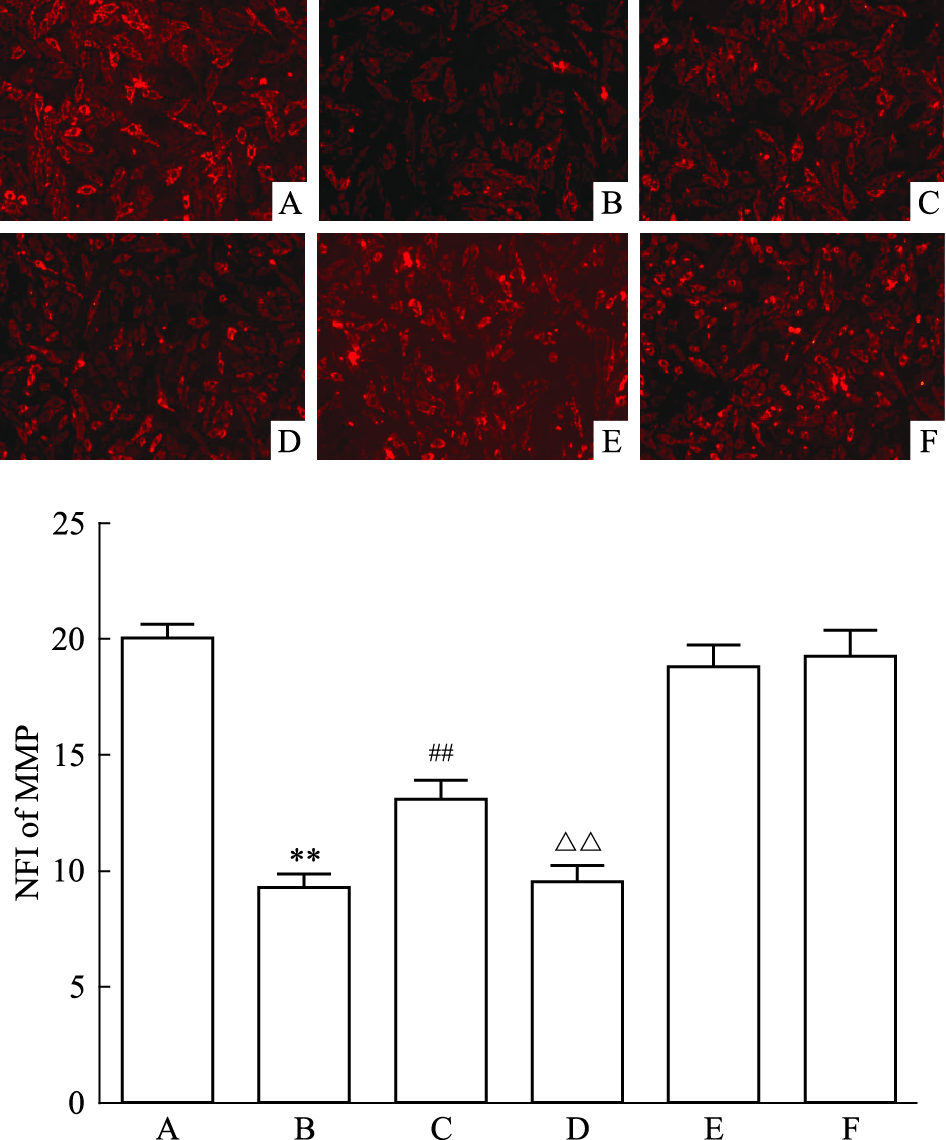
Fig 7显示,采用HG作用H9c2心肌细胞24 h,可使胞内JC-1的平均荧光强度(MFI,是反映MMP大小的指标)从(20.1±0.59)%(正常对照组,Fig 7A)降低至(9.3±0.61)%(Fig 7B),两组差异有统计学意义(P < 0.01)。采用400 μmol·L-1 NaHS预处理心肌细胞30 min,可使MFI升高至(13.1±0.86)%(Fig 6C),与HG处理组比较,差异有统计学意义(P < 0.01)。但是,在NaHS干预前,应用30 μmol·L-1 Akt的抑制剂LY294002预处理心肌细胞30 min,心肌细胞MFI降低至(9.5±0.70)%(Fig 7D),与NaHS预处理组比较,差异具有统计学意义(P < 0.01)。单纯NaHS或LY294002本身对心肌细胞MMP无明显的影响(P>0.05)。
|
| Fig 7 Akt pathway attributes to protectionof exogenous H2S against HG-induced dissipationof MMP in H9c2 cardiac cells(n=5) A: Control; B: Glucose 35 mmol·L-1; C: NaHS 400 μmol·L-1+Glucose 35 mmol·L-1; D: LY294002 30 μmol·L-1+NaHS 400 μmol·L-1+Glucose 35 mmol·L-1; E: NaHS 400 μmol·L-1; F: LY294002 30 μmol·L-1.**P < 0.01 vs control;##P < 0.01 vs the HG-treated group;△△P < 0.01 vs the NaHS+HG-treated group |
Akt信号通路是细胞内多条信号通路的交叉点,参与多种病理生理过程。有报道指出:链脲霉素诱导的大鼠糖尿病心肌病与Akt活性受到抑制有关[4]。本文在HG处理的H9c2心肌细胞模型观察到,HG呈时间依赖性地抑制心肌细胞Akt的活性,这从细胞水平上进一步证实高血糖对心肌细胞Akt通路的抑制作用。
最近,我们证实,抑制KATP通道是HG损伤心肌细胞的重要机制之一。有报道指出,KATP通道位于Akt通路的上游,KATP通道-Akt通路激活与减轻心肌缺血/再灌注损伤有关[5, 6],KATP通道开放剂可通过激活Akt通路对心肌起保护作用[6]。但是,在HG损伤心肌细胞的情况下,开放KATP通道能否对抗HG对Akt通路的抑制作用,迄今尚未见报道。为了探讨此重要的学术问题,本文观察了KATP通道开放剂(Pin)对HG抑制Akt通路活性的影响。结果表明,Pin能明显地减轻HG对心肌细胞Akt通路的抑制作用。结合我们近期的研究结果[2]及上述的结果(HG抑制Akt通路的活动),提示HG可通过抑制KATP通道-Akt通路损伤心肌细胞。
重要的是,我们进一步探讨了KATP通道-Akt通路在外源性H2S保护心肌细胞对抗HG损伤中的作用。越来越多的研究证实,H2S具有心肌保护作用,不仅能保护心肌细胞对抗缺血/再灌注引起的损伤[13, 14],也能抑制化学性缺氧引起的心肌细胞损伤[15]。最近,我们发现外源性H2S可通过激活心肌细胞KATP通道抑制HG诱导的损伤[2],表明KATP通道介导H2S的心肌细胞保护作用。Tang等[11]证实,H2S可通过调控KATP通道-Akt通路对抗MPP+引起的神经细胞毒性及细胞凋亡。但是,KATP通道-Akt通路在H2S对抗HG引起的心肌细胞损伤中的作用如何,目前尚未明确。为此,本研究观察了NaHS预处理对HG抑制Akt通路活动的影响。研究结果表明,外源性H2S能明显地减轻HG对心肌细胞Akt通路的抑制作用,提示通过激活Akt通路可能是H2S心肌细胞保护的另一个重要机制。此外,Akt通路的抑制剂LY294002 能拮抗H2S对HG引起的心肌细胞损伤的抑制作用,表现为细胞存活率降低、凋亡细胞数量与ROS 生成及MMP丢失增多。因此,前文[2]及本研究的上述结果清晰地表明,KATP通道-Akt通路在外源性H2S抑制HG引起的细胞毒性、细胞凋亡、氧化应激及线粒体损伤中起着重要的作用。
综上所述,抑制KATP通道-Akt通路可能是HG损伤心肌细胞的重要机制之一;外源性H2S可通过调控KATP通道-Akt通路对抗HG引起的心肌细胞损伤。
(致谢:本实验在中山大学中山医学院科技楼完成,全体作者均参与实验。在此,非常感谢实验室各位老师和师兄师姐、师弟师妹在实验中提供的帮助,尤其感谢中山大学中山医学院生理学教研室冯鉴强教授对本实验设计、文章书写给予的悉心指导!)
| [1] | Noma A. ATP-regulated K+ channels in cardiac muscle[J]. Nature, 1983, 305(5930):147-8. |
| [2] | 梁伟杰, 陈景福, 张稳柱, 等. ATP敏感性钾通道在硫化氢抑制高糖引起的心肌细胞损伤中的作用[J].中国病理生理杂志, 2015, 31(5):785-90. Liang W J, Chen J F, Zhang W Z, et al. Role of ATPsensitive potassium channels in inhibitory effect of hydrogen sulfide on high glucose-induced injury in H9c2 cardic cells[J]. Chin J Pathophysiol, 2015, 31(5):785-90. |
| [3] | Dummler B, Hemmings B A. Physiological roles of PKB/Akt isoforms in development and disease[J]. Biochem Soc Trans, 2007, 35:231-5. |
| [4] | Laviola L, Belsanti G, Davalli A M, et al. Effects of streptozocin diabetes and diabetes treatment by islet transplantation on in vivo insulin signaling in rat heart[J]. Diabetes, 2001, 50:2709-20. |
| [5] | Bian B, Yu X, Wang Q, et al. Atorvastatin protects myocardium against ischemia-reperfusion arrhythmia by increasing Connexin 43 expression:A rat model[J].Eur J Pharmacol, 2015, 2999(15):30254-5. |
| [6] | Ahmad N, Wang Y, Haider K H, et al. Cardiac protection by mitoKATP channels is dependent on Akt translocation from cytosol to mitochondria during late preconditioning[J]. Am J Physiol Heart Circ Physiol, 2006, 290(6):H2402-8. |
| [7] | Zhao W, Zhang J, Lu Y, et al. The vasorelaxant effect of H(2)S as a novel endogenous gaseous K(ATP) channel opener[J]. EMBO J, 2001, 20(21):6008-16. |
| [8] | Manna P, Jain S K.Hydrogen sulfide and L-cysteine increase phosphatidylinositol 3, 4, 5-trisphosphate(PIP3) and glucose utilization by inhibiting phosphatase and tensin homolog(PTEN) protein and activating phosphoinositide 3-kinase (PI3K)/serine/threonine protein kinase(AKT)/protein kinase Cζ/λ(PKCζ/λ) in 3T3l1 adipocytes[J]. J Biol Chem, 2011, 286(46):39848-59. |
| [9] | 孟金兰, 陈雅嘉, 陈 红, 等. PI3K/Akt信号通路在硫化氢保护PC12细胞对抗化学性缺氧损伤的作用[J]. 中国药理学通报, 2013, 29(2):257-61. Meng J L, Chen Y J, Chen H, et al. Role of PI3K/Akt in protective effect of hydrogen sulfide against PC12 cells injuries induced by chemical hypoxia[J]. Chin Pharmacol Bull, 2013, 29(2):257-61. |
| [10] | 兰爱平, 梅卫义, 孟金兰, 等. 硫化氢通过抑制p38?MAPK保护PC12细胞对抗化学性缺氧损伤[J]. 中国药理学通报, 2010, 26(10):1339-43. Lan A P, Mei W Y, Meng J L, et al. Hydrogen sulfide protects PC12 cells against hypoxia-induced injury by inhibiting p38MAPK[J]. Chin Pharmacol Bull, 2010, 26(10):1339-43. |
| [11] | Tang X Q, Zhuang Y Y, Fan L L, et al.Involvement of K(ATP)/PI(3)K/AKT/Bcl-2 pathway in hydrogen sulfide-induced neuroprotection against the toxicity of 1-methy-4-phenylpyridinium ion[J].J Mol Neurosci, 2012, 46(2):442-9. |
| [12] | Xu W, Wu W, Chen J, et al.Exogenous hydrogen sulfide protects H9c2 cardiac cells against high glucose-induced injury by inhibiting the activities of the p38 MAPK and ERK1/2 pathways[J]. Int J Mol Med, 2013, 32(4):917-25. |
| [13] | 杨洁琼, 胡明珠, 杜 斌, 等. AMPK/PGC-1α信号通路在硫化氢抗心肌缺血/再灌注损伤中的作用[J].中国药理学通报, 2015, 31(7):951-6. Yang J Q, Hu M Z, Du B, et al. Role of AMPK/PGC-1α pathway in cardioprotection of hydrogen sulfide against ischemia/reperfusion injury[J].Chin Pharmacol Bull, 2015, 31(7):951-6. |
| [14] | 杨海扣, 于 水, 米 琰, 等. 外源性硫化氢后处理对大鼠心肌缺血/再灌注损伤线粒体通透性转换孔的影响[J]. 中国药理学通报, 2010, 26(7):944-7. Yang H K, Yu S, Mi Y, et al. Effect of exogenous hydrogen sulfide postconditioning on the mitochondrial permeability transition pore against ischemia reperfusion injury in isolated rat heart[J]. Chin Pharmacol Bull, 2010, 26(7):944-7. |
| [15] | 廖新学, 杨春涛, 杨战利, 等. 硫化氢对抗化学性缺氧引起的心肌细胞损伤及其机制[J]. 中国药理学通报, 2009, 25(8):1012-7. Liao X X, Yang C T, Yang Z L, et al. Hydrogen sulfide protects H9c2 cells against chemical hypoxia-induced injury and the underlying mechanisms[J]. Chin Pharmacol Bull, 2009, 25(8):1012-7. |