


2. 应用心理学教研室, 山东 潍坊 261053
2. Dept of Psychology, Weifang Medical College, Weifang Shandong 261053, China
支气管哮喘是一种炎症性呼吸系统疾病,严重影响人类健康 [1, 2]。NF-κB/MAPK信号通路可介导炎症反应,在哮喘发生、发展中发挥重要作用[3, 4]。目前治疗哮喘以激素等为主,久用不良反应较大。中医中药在哮喘防治方面积累了大量经验,黄芪作为一种具备免疫调节功能的药物,在哮喘的防治上发挥着重要作用。黄芪提取物黄芪多糖(astragalus polysaccharide,APS)在多种疾病的动物模型中显示了良好的抗炎作用[5],课题组前期研究发现,APS可抑制支气管哮喘大鼠气道炎症并调节Th17/Treg 细胞因子表达[6]。但是,APS治疗哮喘的机制是否与调节NF-κB/MAPK信号通路有关未见报道,本研究拟就上述问题进行探索。
1 材料与方法 1.1 材料 1.1.1 实验动物与分组健康♂Wistar大鼠,体质量(200±20) g(山东大学实验动物中心,合格证号:SCXK鲁2003-0004),随机分为正常组、哮喘组、APS组,每组8只。
1.1.2 药品试剂与仪器卵蛋白(ovalbumin,OVA)购于美国Sigma公司,氢氧化铝购于淄博化学试剂公司,NF-κB p65、p-NF-κB p65、p-IκBα、ERK1/2、p-ERK1/2、JNK、p-JNK、p38 MAPK、p-p38 MAPK、IL-1β、IL-4、IL-5、IL-6及 IL-13酶联免疫试剂盒购于美国Cell Signaling公司、R&D公司、武汉华美公司及上海邦奕公司。雾化泵(德国PARI公司),H-7500 型透射电子显微镜(日立公司) 。
1.2 方法 1.2.1 模型制备哮喘组、APS组大鼠于分组后第1天(d 1),腹腔注射致敏液混悬剂2 mL(含有OVA 100mg,氢氧化铝200 mg),于d 8第2次注射致敏液。从d 15起,大鼠接受连续28 d的1% OVA雾化吸入(20 min,40 mL),每日1次。正常组仅腹腔注射及雾化吸入生理盐水。
1.2.2 药物治疗从d 1 开始,大鼠接受连续6周的药物干预。APS组予以腹腔注射APS 400 mg·kg-1·d-1 (多项动物实验显示,该剂量在大鼠体内可发挥多种药理学效应[7],课题组前期研究也发现,该剂量在大鼠体内具有免疫调节、抗炎等作用[6]),正常组及哮喘组腹腔注射等体积的生理盐水。
1.2.3 HE染色治疗结束处死大鼠,取右肺组织,10%多聚甲醛固定,常规石蜡包埋,切片(4 μm),进行HE染色,光镜分析病理变化。
1.2.4 电镜处死大鼠后,迅速取1 mm3大小的肺组织置于2.5%戊二醛前固定,继以1%锇酸后固定,脱水环氧树脂包埋,超薄切片(1 μm)铀铅染色,电镜观察肺泡Ⅰ型上皮超微结构。
1.2.5 肺泡灌洗液炎症细胞计数左侧肺脏以生理盐水(37 ℃)灌洗,收集灌洗液,2 500 r·min-1离心10 min。回收细胞进行瑞氏染色,光镜下分类计数炎症细胞数量。
1.2.6 ELISA检测取右肺新鲜组织,加入4 ℃生理盐水匀浆(1 g 组织加入2 mL生理盐水),2 500 r·min-1离心10 min,取上清液,ELISA法检测其中NF-κB p65、p-NF-κB p65、p-IκBα、ERK1/2、p-ERK1/2、JNK、p-JNK、p38 MAPK、p-p38 MAPK、IL-1β、IL-4、IL-5、IL-6及 IL-13含量。ELISA操作严格按说明书进行。
1.2.7 统计学处理计量资料以x±s表示,采用SPSS 13. 0软件对数据进行单因素方差分析,组间差异比较采用q检验。
2 结果 2.1 APS对BALF中炎症细胞数量的影响与正常组比较,哮喘组BALF中含有更多数量的巨噬细胞、嗜酸性粒细胞、淋巴细胞及中性粒细胞(P < 0.05);与哮喘组比较,APS组BALF中上述炎症细胞数量均明显降低(P < 0.05);但APS组上述炎症细胞数量仍明显高于正常组(P < 0.05)。见Tab1。
| Macrophages | Eosinophils | Lymphocyte | Neutrophil | |
| Normal | 6.07±1.14 | 0.06±0.01 | 10.24±1.63 | 3.41±0.55 |
| Asthma | 15.72±2.05 # | 1.96±0.30 # | 28.07±4.34 # | 6.80±0.69 # |
| APS | 10.35±2.10 #△ | 1.05±0.26 #△ | 17.84±2.95 #△ | 5.03±0.71 #△ |
| # P < 0.05 vs normal group; △ P < 0.05 vs asthma | ||||
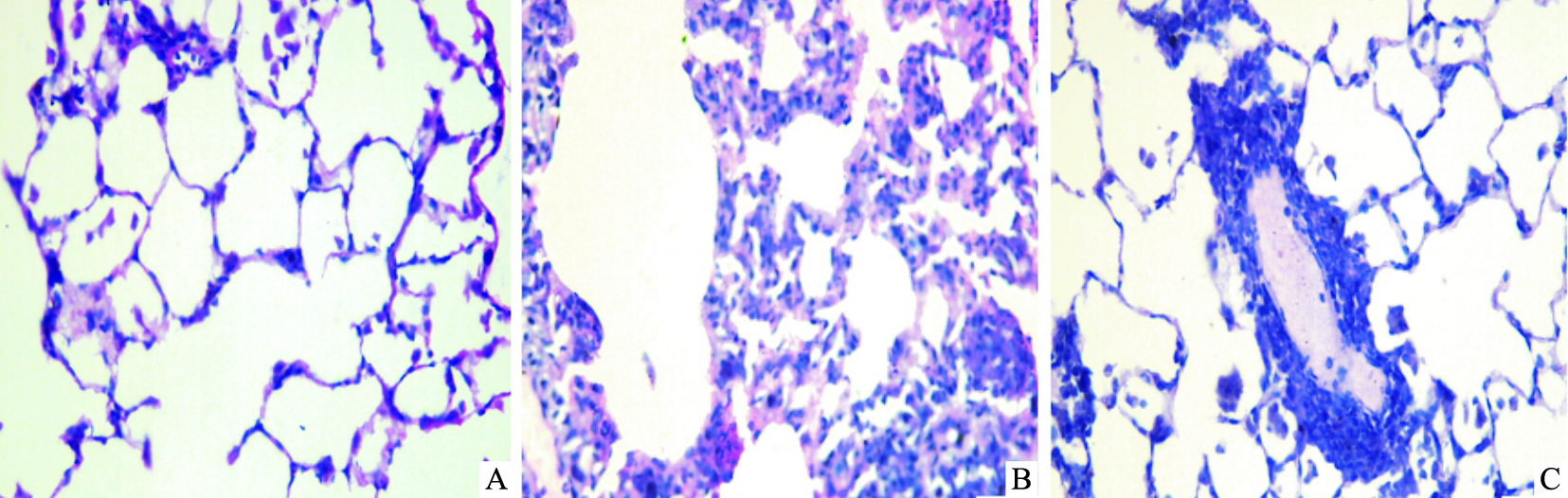
HE染色显示,正常组未见异常,肺泡轮廓完整清晰,未见明显的炎症细胞浸润。哮喘组肺泡轮廓欠清晰,肺泡壁明显水肿、增厚,部分肺泡扩张,大量炎症细胞浸润。与哮喘组比较,APS组肺泡轮廓较清晰,肺泡壁水肿明显减轻、炎症细胞浸润明显减轻;但与正常组比较,APS组仍存在较明显的肺泡壁水肿、炎症细胞浸润等表现。见Fig1。
|
| Fig 1 Effects of APS on histological changes of lung tissue A: Normal; B: Asthma; C: APS |
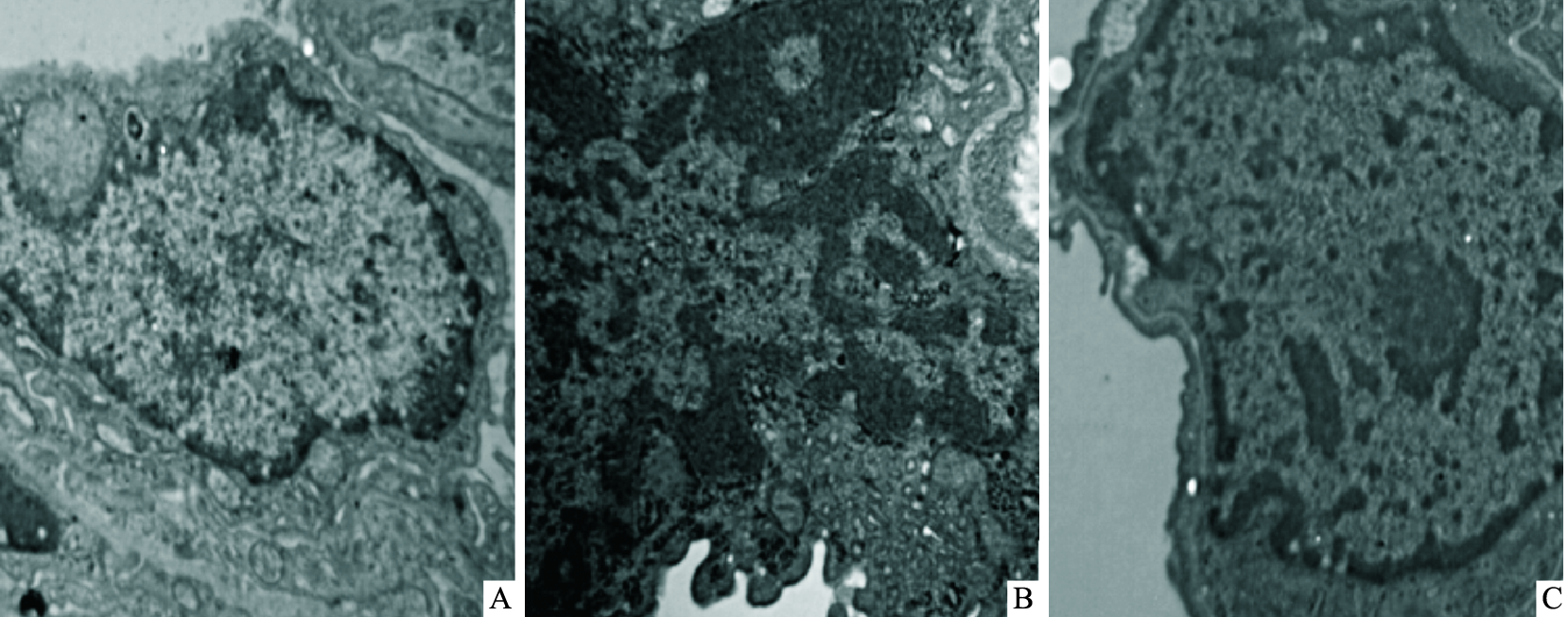
电镜下可见,哮喘组大鼠肺泡Ⅰ型上皮细胞线粒体肿胀、嵴模糊,高尔基复合体不发达,染色质聚集。与哮喘组比较,APS组大鼠肺泡Ⅰ型上皮细胞上述超微结构变化明显减轻。见Fig2。
|
| Fig 2 Effects of APS on ultrastructure of type Ⅰ pneumocyte A: Normal; B: Asthma; C: APS |
与正常组比较,哮喘组肺部NF-κB p65、p-NF-κB p65及p-IκBα含量明显升高(P < 0.05)。与哮喘组较,APS组肺部NF-κB p65、p-NF-κB p65及p-IκBα含量明显降低(P < 0.05);但APS组上述指标含量仍高于正常组(P < 0.05)。见Tab2。
| NF-κB p65/ng·L -1 | p-NF-κB p65/ng·L -1 | p-IκBα/ng·L -1 | |
| Normal | 39.55 ± 5.17 | 13.80 ± 2.10 | 11.16 ± 2.05 |
| Asthma | 82.09±11.20 # | 43.26±5.28 # | 33.71±5.39 # |
| APS | 59.14±7.06 #△ | 22.53±4.31 #△ | 20.80±3.51 #△ |
| # P < 0.05 vs normal group; △ P < 0.05 vs asthma | |||
与正常组大鼠比较,哮喘组肺部ERK1/2、JNK、p38 MAPK、p-ERK1/2、p-JNK及p-p38 MAPK含量明显升高(P < 0.05)。与哮喘组比较,APS组肺部上述指标含量明显降低(P < 0.05);但APS组上述指标含量仍高于正常组(P < 0.05)。见Tab3。
| ERK1/2/ng·L -1 | JNK/ng·L -1 | p38 MAPK/ng·L -1 | p-ERK1/2/ng·L -1 | p-JNK/ng·L -1 | p-p38 MAPK/ng·L -1 | |
| Normal | 33.01 ± 5.17 | 40.17 ± 5.83 | 52.71± 7.50 | 8.36 ± 1.58 | 11.96± 2.34 | 14.71 ±2.83 |
| Asthma | 54.77±6.83 # | 75.92±9.44 # | 95.60±9.82 # | 26.70±3.12 # | 36.41±4.88 # | 50.15±7.24 # |
| APS | 43.50±5.36 #△ | 56.80±7.33 #△ | 70.42±8.39 #△ | 15.38±2.66 #△ | 21.49±3.10 #△ | 30.70±5.89 #△ |
| # P < 0.05 vs normal group; △ P < 0.05 vs asthma group | ||||||
与正常组比较,哮喘组肺组织炎性细胞因子IL-1β、IL-4、IL-5、IL-6及IL-13含量明显增高(P < 0.05)。与哮喘组比较,APS组上述细胞因子含量明显降低(P < 0.05);但APS组含量仍高于正常组(P < 0.05)。见Tab4。
| IL-1β/ng·L -1 | IL-4/ng·L -1 | IL-5/ng·L -1 | IL-6/ng·L -1 | IL-13/ng·L -1 | |
| Normal | 79.33±10.74 | 51.08±8.29 | 49.93±7.39 | 69.52±8.13 | 41.83±6.05 |
| Asthma | 178.72±17.36 # | 147.36±18.55 # | 163.80±20.39 # | 152.04±18.29 # | 123.16±15.87 # |
| APS | 123.03±15.37 #△ | 101.58±14.80 #△ | 93.72±15.77 #△ | 114.60±14.58 #△ | 96.37±12.90 #△ |
| # P < 0.05 vs normal group; △ P < 0.05 vs asthma group | |||||
本研究首先观察了APS对哮喘大鼠肺部炎症的影响,结果表明,APS明显降低了哮喘大鼠BALF炎症细胞数量、抑制了肺组织炎症反应。肺泡Ⅰ型上皮对于维持正常的肺功能具有重要的作用,哮喘时该上皮易受累,导致呼吸功能下降。本研究结果显示,APS明显改善了OVA诱导的肺泡Ⅰ型上皮超微结构损伤。既往研究也就APS对哮喘的疗效进行了探讨,宋泽庆等发现APS对哮喘小鼠特异性免疫治疗具有增强作用。俞建芬等报道APS可改善哮喘小鼠气道高反应性及气道重塑。课题组前期研究显示APS可调节哮喘大鼠Th17/Treg细胞因子平衡[6]。这些研究均证明APS对哮喘具有治疗作用。
近年研究显示,NF-κB/MAPK信号通路过度激活在哮喘的发病中发挥作用[3, 4]。通常NF-κB被IκB抑制,以非活性形式存在于细胞质。当IκB发生磷酸化,失去了对NF-κB的抑制作用,活化的磷酸化-NF-κB可转位至细胞核,促进基因转录,继而增加炎性细胞因子表达,促进哮喘发展。本研究显示,哮喘组NF-κB p65、p-NF-κB p65及p-IκBα表达升高,表明NF-κB通路过度激活。其他研究也显示哮喘动物NF-κB通路活性较正常动物增加[9, 10],与本研究结果一致。本研究中,APS组大鼠NF-κB p65、p-NF-κB p65及p-IκBα表达较哮喘组明显降低,表明APS可明显抑制NF-κB通路活性。MAPK信号通路在炎症反应中发挥重要作用,MAPK信号通路主要包括分别由ERK1/2、JNK、p38 MAPK介导的三条级联反应,该通路的激活可促进炎症细胞因子的生成而加剧炎症反应。有研究表明哮喘动物MAPK信号通路较正常动物活性增强[11]。本研究显示,哮喘组大鼠肺部ERK1/2、JNK、p38 MAPK、p-ERK1/2、p-JNK及p-p38 MAPK含量较正常组明显升高,这与既往报道相一致[11, 12, 13]。本研究中,APS明显降低了哮喘大鼠肺部ERK1/2、JNK、p38 MAPK、p-ERK1/2、p-JNK及p-p38 MAPK含量,表明APS可抑制OVA诱导的MAPK信号通路过度激活。
本研究尚检测了大鼠肺部NF-κB/MAPK信号通路下游炎性细胞因子IL-1β、IL-4、IL-5、IL-6及IL-13的表达。结果表明哮喘组大鼠上述细胞因子水平明显升高,这同既往其他研究报道一致[14, 15, 16]。在本研究中,与APS抑制NF-κB/MAPK信号通路的过度激活相一致,APS也明显抑制了哮喘大鼠炎性细胞因子IL-1β、IL-4、IL-5、IL-6及IL-13表达。
综上所述,OVA引起了大鼠NF-κB/MAPK信号通路过度激活以及炎性细胞因子过度分泌。与文献报道一致,上述通路的激活以及炎性细胞因子的过度分泌,可引起炎症级联反应、加剧肺部炎症,促进肺上皮损伤,增加气道反应性,并引起气道重构 [3, 4, 17, 18]。针对此,大量研究以药物对哮喘进行干预,旨在降低NF-κB/MAPK信号通路的过度激活及炎症因子的过度分泌,结果表明能改善上述靶点的药物,可明显减轻哮喘病变[3, 4, 19]。本研究中,APS亦明显降低了OVA引起的NF-κB/MAPK信号通路过度激活及炎症因子过度分泌,同时减轻了肺部炎症以及肺泡Ⅰ型上皮细胞超微结构损伤,理论上推测大鼠哮喘表现的好转可能与APS抑制NF-κB/MAPK信号通路及炎症因子水平有关。在既往报道中,虽然有众多的中药提取物表现出了一定的抗哮喘作用,但与阳性对照药物糖皮质激素比较,多数提取物均未达到或优于糖皮机制激素的疗效[20, 21]。与此类似,本研究中APS虽然明显抑制了NF-κB/MAPK信号通路及炎症因子分泌,但其水平仍明显高于正常对照组,与此一致,APS组虽然肺部炎症得到缓解,但与正常组比较,仍然存在显著的炎症,故APS对哮喘时的肺部炎症仅有部分缓解作用。
总之,APS可明显缓解哮喘大鼠肺部炎症反应,同时减低了NF-κB/MAPK信号通路活性。故推测,APS改善哮喘的作用可能与抑制NF-κB/MAPK信号通路有关。
(致谢:本研究在山东省潍坊医学院应用药理学实验室完成。)
| [1] | 李良昌, 朴红梅, 延光海, 等. 芝麻素抗哮喘炎症作用研究[J].中国药理学通报, 2015,31(3):411-5.[1] Li L C, Piao H M, Yan G H, et al. Sesamin attenuates inflammation response in a murine model of asthma[J]. Chin Pharmacol Bull, 2015,31(3):411-5. |
| [2] | 王雅娟, 赵一婷, 戴斌, 等. 两种大鼠哮喘模型的比较[J].中国药理学通报, 2014,30(8):1175-8. Wang Y J, Zhao Y T, Dai B, et al. Comparison of two asthma models in rats[J]. Chin Pharmacol Bull, 2014,30(8):1175-8 |
| [3] | Yan G H, Choi Y H. Phellinus linteus extract exerts anti-asthmatic effects by suppressing NF-κB and p38 MAPK activity in an OVA-induced mouse model of asthma[J]. Immune Netw, 2014,14(2):107-15. |
| [4] | Yang X, Li Y, He Y, et al. Cordycepin alleviates airway hyperreactivity in a murine model of asthmaby attenuating the inflammatory process[J]. Int Immunopharmacol, 2015,26(2):401-8. |
| [5] | Lu J, Chen X, Zhang Y, et al. Astragalus polysaccharide?induces anti-inflammatory effects dependent on AMPK activity in palmitate-treated RAW264.7 cells[J]. Int J Mol Med, 2013,31(6):1463-70. |
| [6] | 李承德, 周文宾, 孙艳, 等. 黄芪多糖对哮喘大鼠Th17/Treg细胞因子及肺部炎症的影响[J].中国药理学通报, 2013,29(9):1275-8. Li C D, Zhou W B, Sun Y, et al. Effects of astragalus polysaccharide on Th17/Treg associated cytokines and airway inflammation in OVA-induced asthmatic rats[J]. Chin Pharmacol Bull, 2013,29(9):1275-8. |
| [7] | 刘端勇, 黄敏芳, 徐荣, 等. 黄芪多糖对结肠炎大鼠小肠PP结中T淋巴细胞亚群的调节作用[J].中国药理学通报, 2015,31(9):1328-9. Liu D Y, Huang M F, Xu R, et al. Effect of astragalus polysaccharides in regulating the T lymphocyte subgroup in intestinal PPs of rat with colitis[J]. Chin Pharmacol Bull, 2015,31(9):1328-9. |
| [9] | Lee C H, Kim Y S, Kang N I, et al. IgG immune complex induces the recruitment of inflammatory cells into the airway and TNF-mediated late airway hyperresponsiveness via NF-κB activation in mice[J]. J Asthma, 2011,48(8):757-66. |
| [10] | Lai G, Wu C, Hong J, et al. 1, 25-Dihydroxyvitamin D(3) (1, 25-(OH)(2)D(3)) attenuates airway remodeling in a murine model of chronic asthma[J]. J Asthma, 2013,50(2):133-40. |
| [11] | Xiong Y, Wang J, Yu H, et al. Anti-asthma potential of crocin and its effect on MAPK signaling pathway in a murine model of allergic airway disease[J]. Immunopharmacol Immunotoxicol, 2015,37(3):236-43. |
| [12] | Alam R, Gorska M M. Mitogen-activated protein kinase signalling and ERK1/2 bistability in asthma[J]. Clin Exp Allergy, 2011,41(2):149-59. |
| [13] | Chung K F. p38 mitogen-activated protein kinase pathways in asthma and COPD[J]. Chest, 2011,139(6):1470-9. |
| [14] | Chung K F. Targeting the interleukin pathway in the treatment of asthma[J]. Lancet, 2015,386(9998):1086-96. |
| [15] | Walsh G M. Anti-IL-4/-13 based therapy in asthma[J]. Expert Opin Emerg Drugs, 2015,20(3):349-52. |
| [16] | Chu D K, Al-Garawi A, Llop-Guevara A, et al. Therapeutic potential of anti-IL-6 therapies for granulocytic airway inflammation in asthma[J]. Allergy Asthma Clin Immunol, 2015,11(1):14. |
| [17] | Rajajendram R, Tham C L, Akhtar M N, et al. Inhibition of epithelial CC-family chemokine synthesis by the synthetic chalcone DMPF-1 via disruption of NF-κB nuclear translocation and suppression of experimental asthma in mice[J]. Mediators Inflamm, 2015,2015:176926. |
| [18] | Schuliga M. NF-kappa B signaling in chronic inflammatory airway disease[J]. Biomolecules, 2015,5(3):1266-83. |
| [19] | Chung K F. Targeting the interleukin pathway in the treatment of asthma[J]. Lancet, 2015,386(9998):1086-96. |
| [20] | Quan Z, Lee Y J, Yang J H, et al. Ethanol extracts of Saururus chinensis suppress ovalbumin-sensitization airway inflammation[J]. J Ethnopharmacol, 2010,132(1):143-9. |
| [21] | Lee S H, Seo M J, Choi S M, et al. DA-9201 shows anti-asthmatic effects by suppressing NF-kappaB expression in an ovalbumin-induced mouse model of asthma[J]. Arch Pharm Res, 2005,28(12):1350-7. |

