


2. 云南中医学院中药学院, 云南 昆明 650500
曹丽(1966-), 女, 博士, 研究员, 研究方向:天然药物抗肿瘤药理学, Tel:010-57833222, E-mail:lcao@implad.ac.cn
 , HE Xiao-shan2, ZHANG Li-jing1, HUO Xiao-wei1, LIU Dong-yu1, HAN Jia-yuan1, LI Li-yong1, CAO Li1
, HE Xiao-shan2, ZHANG Li-jing1, HUO Xiao-wei1, LIU Dong-yu1, HAN Jia-yuan1, LI Li-yong1, CAO Li1
2. College of Traditional Chinese Medicine, Yunnan University of Traditional Chinese Medicine, Kunming 650500, China
茯苓为多孔菌科真菌poria cocos(schw)wolf的干燥菌核,根据记载茯苓具有利水渗湿、健脾和胃、宁心安神之功效,为一种药食两用的传统中药材[1]。茯苓多糖(pachyman)是茯苓的主要成分,其含量占茯苓干重的80%以上[2, 3]。天然茯苓多糖经氢氧化钠、氯乙酸醚化、再加碱二次醚化最后乙醇沉淀,合成羧甲基茯苓多糖(carboxymethylpachymaran,CMP),修饰后茯苓多糖分子量变小,黏度降低,取代度增加,水溶性升高,抗肿瘤及免疫活性等也增强[4]。大量研究发现,茯苓多糖在免疫调节、抗肿瘤、抗炎、抗氧化等多方面具有良好的药理活性[5, 6, 7]。在肠道免疫方面,茯苓多糖能够影响免疫抑制小鼠CD4+、CD8+细胞亚群比例及肠派氏结T、B淋巴细胞比例和细胞因子水平[8]。
氟尿嘧啶(fluorouracil,5-Fu)是临床上治疗消化道肿瘤和乳腺癌的基本药物。然而,临床应用发现,5-Fu具有较强的毒副作用,如造成胃肠道黏膜炎、骨髓抑制、肝、肾及心脏毒性、机体免疫功能及造血功能低下等[9]。为观察CMP是否具有改善5-Fu所致的小鼠肠黏膜炎及肠道保护作用,本实验采用腹腔注射5-Fu建立小鼠肠黏膜炎模型,通过检测CMP对小鼠肠推进作用、派氏集合淋巴结(PPs)匀浆上清中脂质过氧化、细胞因子分泌水平及结肠病理、炎症、凋亡相关指标的影响,探讨CMP对5-Fu所致小鼠肠黏膜炎的改善及肠道功能的保护作用及可能作用机制,为茯苓多糖的临床应用及茯苓药用价值的深入开发提供依据。
1 材料与方法 1.1 药品与试剂CMP(湖南补天药业股份有限公司);氟尿嘧啶注射液(上海旭东海普药业有限公司);活性氧类(ROS)、谷胱甘肽(GSH)、过氧化氢酶(CAT)和谷胱甘肽过氧化物酶(GSH-Px)均购于南京建成生物工程有限公司;ELISA试剂盒IL-1β购于武汉华美生物工程有限公司;山羊抗鼠一抗NF-κB、p-p38购于Santa Cruz公司;山羊抗鼠二抗、山羊抗兔二抗均购于北京康为世纪生物技术有限公司;冰醋酸、甲醛及其他试剂,均为国产分析纯。
1.2 仪器生物洁净工作台(北京东联哈尔仪器制造有限公司,型号:BCN-1360);二氧化碳培养箱(美国Napco公司,型号:5410);酶标仪(美国Bio-Tek公司,型号:MQX 200);荧光倒置显微镜(日本Olympus,型号:CKX 41);离心机(德国Heraeus公司,型号:Labofuge 400R)。
1.3 动物♂ ICR小鼠,SPF级,16-18g,购自北京维通利华实验动物技术有限公司,许可证号SCXK(京)2012-0001。按啮齿类动物饲养方法和条件饲养于SPF级动物房。
1.4 方法 1.4.1 分组、给药健康♂ ICR小鼠32只,随机分为4组:正常对照组、5-Fu(25 mg·kg-1)组、CMP(200 mg·kg-1)组、CMP(200 mg·kg-1)+5-Fu(25 mg·kg-1)组,每组8 只。正常组灌胃给予蒸馏水,20 mL·kg-1,每日1次,CMP组灌胃给予CMP,20 mL·kg-1,每日1次,5-Fu组,腹腔注射给药,10 mL·kg-1,每两日1次,CMP+5-Fu组,灌胃给予CMP,20 mL·kg-1,每日1次,同时腹腔注射给予5-Fu,10 mL·kg-1,每两日1次,各组均给药至14 d。
1.4.2 CMP对5-Fu模型小鼠肠道推进作用的影响给药最后1 d,提前6 h禁食,正常饮水。末次给药1.5 h后,每只小鼠灌胃炭末混悬液(质量分数为10%的阿拉伯胶和质量分数为5%的活性炭充分混匀)0.2 mL。灌胃后20 min颈椎脱臼处死,剖腹取小肠,测量炭末推进前端的位置及小肠的总长度,计算推进的距离与小肠全长的比值为炭末推进百分率/%:炭末推进百分率/%=炭末前端与幽门的距离/小肠全长×100%
剪取盲、结直肠,分别测量结肠长度和总长度,并将结肠部分组织置于体积分数为10%的甲醛溶液中固定,做组织病理切片观察及免疫组化。
1.4.3 CMP对5-Fu模型小鼠派氏集合淋巴结(PPs)中ROS、GSH含量和CAT、GSH-Px活性及细胞因子IL-1β含量的影响剪取小肠外壁上隆起的派氏集合淋巴结(PPs),称取一定重量,按1:9加入生理盐水,冰浴、充分匀浆,4℃,3 000 r·min-1,离心15 min,取上清-80℃保存,按照脂质过氧化试剂盒和ELISA试剂盒操作要求测定相应指标。
1.4.4 免疫组化方法检测5-Fu模型小鼠结肠组织中蛋白NF-κB和p-p38的表达末次给药后,摘眼球取血、脱臼处死动物,剪取结肠部分测量长度后,剪取结肠前段部分约1.5 cm,置于体积分数为10%的甲醛溶液中固定,将固定好的组织进行流水冲洗、梯度酒精脱水,浸蜡,包埋,6 μm切片,烤干,脱蜡,HE 染色,中性树脂封片。免疫组化镜检观察,结肠组织中NF-κB和p-p38一抗、二抗的表达情况;然后,对于蛋白阳性表达部分(棕褐色细胞)用ImagePro-Plus 6.0软件 (Media Cybernetics,Rockville,MD,USA)进行量化。
1.4.5 统计结果处理实验数据用x±s表示,采用统计软件SPSS 17.0进行单因素方差分析,组间两两比较用SNK法。
2 结果 2.1 CMP对5-Fu模型小鼠小肠长度及推进功能的影响Tab1结果显示,与正常组比,各组小肠总长度没有明显变化,但5-Fu组小鼠的肠推进长度明显缩短,肠推进率明显降低,差异有统计学意义(P < 0.05)。相比5-Fu组,给予CMP后小鼠的肠推进率则明显升高,且差异有显著性(P < 0.05),说明CMP能够明显改善5-Fu所致的肠道推进功能障碍。
| Group | Dose/mg·kg -1 | Small intestine length/cm | Advancing length/cm | Advancing rate/% |
| Normal | - | 51.30±2.73 | 31.15±4.38 | 60.51±6.00 |
| 5-Fu | - 25 | 50.76±2.91 | 26.61±2.96 * | 52.53±6.31 * |
| CMP | 200 - | 47.20±2.97 | 30.02±4.97 | 63.71±10.52 |
| CMP+5-Fu | 200 + 25 | 53.32±2.96 | 33.22±3.91 | 62.46±8.04 # |
| * P < 0.05 vs normal; # P < 0.05 vs 5-Fu | ||||
Tab2结果显示,与正常组相比,单用CMP能够增加结直肠总长度和结肠长度,其中结肠长度增加明显(P < 0.05);单用5-Fu明显缩短结直肠总长度和结肠长度,且差异有统计学意义(P < 0.05)。与5-Fu组相比,给予CMP 后小鼠的结直肠总长度和结肠长度均明显增加,且差异均有显著性(P < 0.01)。
| Group | Dose/mg·kg -1 | Total length ofcolorectum/cm | Colon length/cm |
| Normal | - | 8.90±0.55 | 2.30±0.31 |
| 5-Fu | - 25 | 8.10±0.27 * | 1.96±0.11 * |
| CMP | 200 - | 9.30±0.71 | 2.66±0.29 * |
| CMP+5-Fu | 200 + 25 | 8.80±0.33 ## | 2.50±0.28 ## |
| * P < 0.05 vs normal; ## P < 0.01 vs 5-Fu | |||
Tab3结果显示,与正常组比较,5-Fu组ROS的含量明显增加(P < 0.01),GSH含量、CAT和GSH-Px的活性均明显降低(P < 0.05或P < 0.01);表明小鼠肠道发生明显的脂质过氧化损伤;与5-Fu组相比,CMP能使ROS含量明显减少(P < 0.05),GSH含量明显增加(P < 0.05),CAT和GSH-Px活性明显升高(P < 0.01或P < 0.05),提示CMP能明显减轻5-Fu所致的小鼠氧化损伤。
| Group | Dose/mg·kg -1 | ROS/mmol·g -1 | CAT/kU·g -1 Pro | GSH/μmol·g -1 Pro | GSH-Px/kU·g -1 Pro |
| Normal | - | 61207.40±396.46 | 3.83±0.25 | 76.83±11.08 | 145.33±48.91 |
| 5-Fu | - 25 | 61885.40±146.66 ** | 2.96±0.44 ** | 59.12±7.52 * | 65.95±37.14 * |
| CMP | 200 - | 60855.60±292.74 | 3.41±0.54 | 77.95±26.18 | 230.73±94.79 |
| CMP+5-Fu | 200 + 25 | 61611.00±244.36 # | 4.09±0.33 ## | 87.51±22.16 # | 136.73±61.66 # |
| * P < 0.05, **P < 0.01 vs normal; # P < 0.05, ##P < 0.01 vs 5-Fu | |||||
Tab4结果显示,与正常组比较,5-Fu组IL-1β的含量明显增加(P < 0.05),表明小鼠肠道发生炎症性损伤;与5-Fu组相比,CMP明显降低IL-1β含量(P < 0.01),提示CMP能够减轻5-Fu所致的小鼠肠黏膜炎。
| Group | Dose/mg·kg -1 | IL-1β/ng·L -1 |
| Normal | - | 40.09±22.91 |
| 5-Fu | - 25 | 76.28±27.45 * |
| CMP | 200 - | 44.16±23.58 |
| CMP+5-Fu | 200 + 25 | 36.92±23.57 ## |
| * P < 0.05 vs normal; ## P < 0.01 vs 5-Fu | ||
Fig1结肠病理切片显示,正常小鼠肠黏膜绒毛表面完整,固有层可见小血管、毛细血管、淋巴管。黏膜下层疏松结缔组织,富有血管、淋巴管,肌层和浆膜层次清晰。相比正常组,5-Fu组小鼠结肠肠黏膜表面不完整,上皮杯状细胞丢失严重,炎症细胞浸润达黏膜肌层。相比单用5-Fu,给予CMP处理后结肠黏膜组织病变、上皮杯状细胞丢失、炎症细胞浸润及细胞损伤等均明显减轻,结肠黏膜表面相对完整。

|
| Fig 1 Effect of CMP on HE in colon tissues in model mice induced by 5-Fu(Left:40×, Right:100×) |
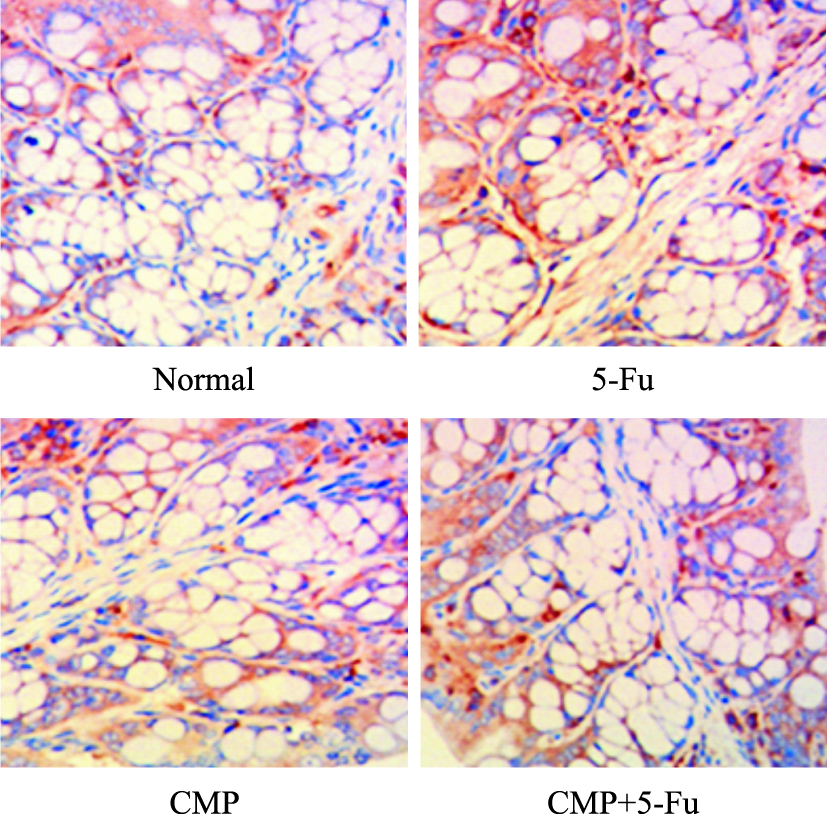
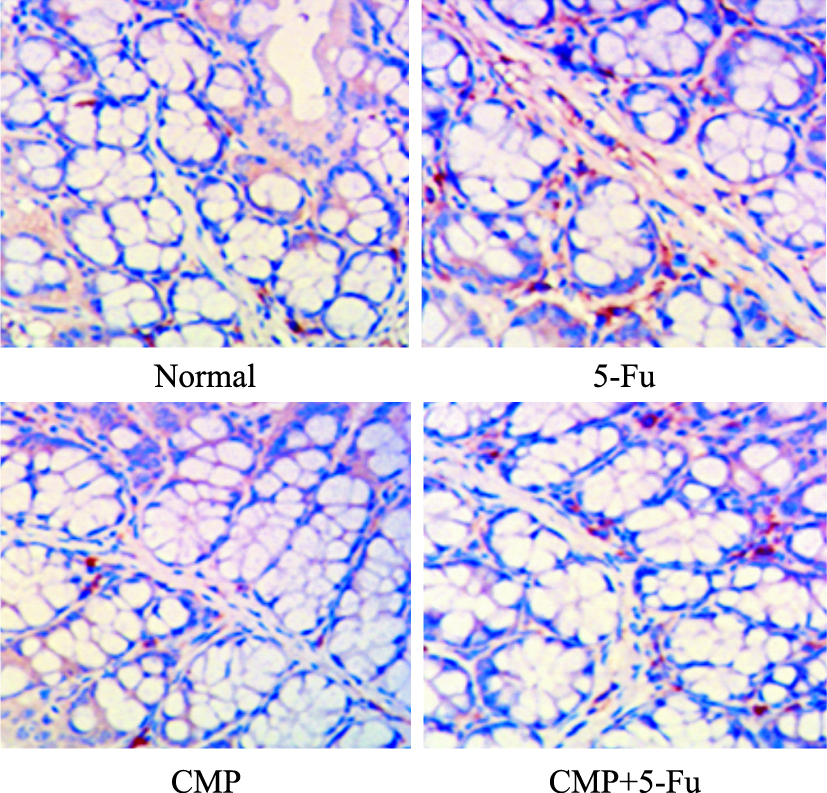
Fig2~5小鼠结肠组织中NF-κB和p-p38免疫组化的结果显示,相比5-Fu组,CMP能明显减少NF-κB和p-p38的表达,表明CMP能够明显减轻5-Fu所致小鼠肠黏膜炎。
|
| Fig 2 Effect of CMP on expression of NF-κBoncolon tissuesin model mice induced by 5-Fu(400×) |

|
| Fig 3 Statistical result of effect of CMP on expression ofNF-κBoncolon tissues in model mice induced by 5-Fu(x±s, n= 3) **P < 0.01 vs normal;#P < 0.05 vs 5-Fu |
|
| Fig 4 Effect of CMP on expression of p-p38 on colon tissuesin model mice induced by 5-Fu(400×) |
|
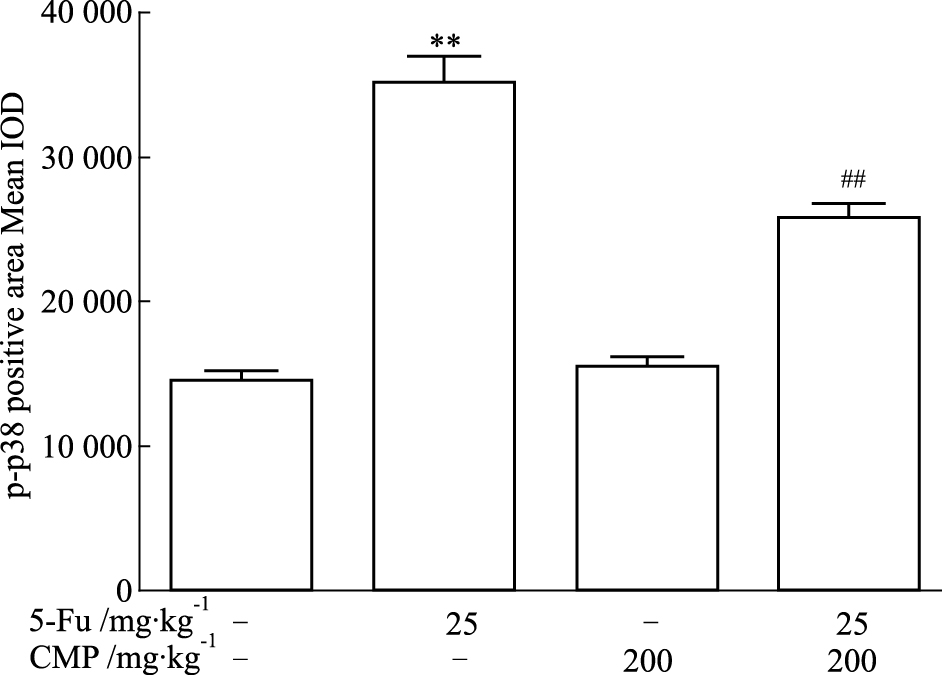
| Fig 5 Statistical result of effect of CMP on expression of p-p38on colon tissues in model mice induced by 5-Fu(x±s,n= 3) **P < 0.01 vs normal;##P < 0.01 vs 5-Fu |
氟尿嘧啶是治疗消化道肿瘤和乳腺癌的基本药物,但其有较严重的副作用。如骨髓抑制、心脏毒性、腹泻、肝损伤和黏膜炎,其中黏膜炎是影响化疗疗效的主要毒副作用[11]。5-Fu对肠黏膜屏障的损伤主要包括:直接损伤肠黏膜,绒毛萎缩,吸收、传递功能降低,出现腹泻;毛细血管组织缺血,释放大量氧自由基ROS,损伤膜结构,使机体循环被破坏、清除自由基能力降低,进而发生氧化损伤[12, 13]。肠炎发生的主要作用机制与p38MAPK通路的过度激活[14]及NF-κB通路的激活有关,NF-κB信号能够调节许多炎症因子基因的表达[15],促进炎症因子TNF-α、IL-1β、IL-6等的释放[16]。
本研究结果显示,CMP能改善5-Fu所致小肠推进功能的降低;并增加5-Fu模型小鼠结肠长度,说明CMP能够改善5-Fu所致小鼠肠道传输功能的障碍。CMP明显减轻5-Fu所致结肠黏膜组织病变、上皮杯状细胞丢失及炎症细胞浸润等病理损伤,使结肠黏膜表面相对完整,并且明显降低派氏集合淋巴结过氧化物ROS含量,增加抗氧化物GSH含量和抗氧化物酶CAT和GSH-Px的活性;提示CMP能够明显减轻5-Fu所致小鼠肠道过氧化损伤和结肠黏膜炎病理状态。另外,CMP还能明显降低炎症因子IL-1β的释放;明显减少结肠组织中NF-κB蛋白的表达,提示CMP能够通过抑制NF-κB信号通路的激活,降低细胞炎症因子IL-1β的释放,进而减轻炎症的发生,与文献报道一致[16];CMP还能通过抑制p38MAPK信号通路的激活,减少结肠组织p-p38的表达,对结肠组织的细胞凋亡起到保护作用。以上结果均提示,CMP能够促进小鼠肠道蠕动,减轻化疗药物所致肠道黏膜免疫功能低下带来的过氧化病理损伤和炎症。证实CMP能通过调节小鼠肠道免疫功能,进而抑制氧化损伤及炎症产生并起到保护肠道的作用。
综上所述,CMP能够减轻临床常用化疗药物5-Fu的肠道毒副作用,提示在氟尿嘧啶化疗时,辅以CMP在减轻肠道毒性,提高肠道免疫功能,改善生活质量等方面具有积极意义;而CMP亦具有抗癌作用,提示CMP可能对肿瘤治疗具有减毒增效作用,但其具体作用机制有待进一步证实。
(致谢:本实验在中国医学科学院药用植物研究所药理毒理中心完成。曹丽老师负责指导本实验的设计及论文修改;王灿红主要负责动物造模、给药、生化、病理实验以及论文的撰写;何晓山老师协助本实验设计思路的制订;张丽静、霍小位、刘冬羽、韩嘉媛和李立勇均参与动物实验处理及相关指标检测。)
| [1] | 国家药典委员会.中华人民共和国药典一部[M].北京:北京化学工业出版社, 2005:166.[1] Chinese Pharmacopoeia Commission.Pharmacopoeia of the People's Republic of China, Volume 1[M].Beijing:Beijing Chemical Industry Press, 2005:166. |
| [2] | Hamuro J J, Maeda Y Y, Arai Y, Fukuoka F.The significance of the higher structure of the polysaccharides lentinan and pachymaran with regard to their anti-tumor activity[J].Chem Biolog Interact, 1971,3(1):69-71. |
| [3] | Wang Y F, Zhang L N.Chain conformation of carboxymethylated derivatives of(1, 3)-β-D-glucan from Poriacocossclerotium Carbohydrate[J].Polymers, 2006,65(4):504-9. |
| [4] | 石清东, 蒋先明.二次碱化法制备羧甲基茯苓多糖[J].天然产物研究与开发, 1996,8(2):78-81. Shi Q D, Jiang X M.Twice alkalization method for preparation of carboxymethyl pachymaran[J].Nat Prod Res Devel, 1996,8(2):78-81. |
| [5] | Wei Y Y, Hu T J, Su Z J, Yun Z.Immunomodulatory and antioxidant effects of carboxymethylpachymaran on the mice infected with PCV2[J].Int J Biolog Macromol, 2012,50(3):713-9. |
| [6] | Lu M K, Cheng J J, Lin C Y.Purification, structural elucidation, and anti-inflammatory effect of a water-soluble 1, 6-branched 1, 3-α-d-galactan from cultured mycelia of Poriacocos[J].Food Chem, 2010,118(2):349-56. |
| [7] | 高贵珍, 汪俊博, 姜芳, 李光坤.硫酸化茯苓多糖对MPTP诱导帕金森小鼠的神经保护作用研究[J].中国药理学通报, 2015,31(12):1699-704. Gao G Z, Wang J B, Jiang F, Li G K.Neuroprotective effect of sulfated pacchymaran on the MPTP-induced Parkinson mice[J].Chin Pharmacol Bull, 2015,31(12):1699-704. |
| [8] | 孙晓雨, 崔子寅, 张明亮, 孙长江.枸杞多糖和茯苓多糖对免疫抑制小鼠免疫增强及对肠道黏膜的免疫调节作用[J].中国兽医学报, 2015,35(3):450-5. Sun X Y, Cui Z Y, Zhang M L, Sun C J.Effect of Lyciumbarbarumpolysaccharides and pachymaran on immune function and intestinal mucosal system in immunosuppressivemice[J].Chin J Veter Sci Med, 2015,35(3):450-5. |
| [9] | 蒙烨, 黄永坤.化疗药物对肠黏膜屏障的损伤及其防治[J].医学综述, 2012,18(9):1325-7. Meng Y, Huang Y K.Chemotherapeuticsimpairment on intestinal mucosal barrier and the prevention and treatment[J].Med Recapitul, 2012,18(9):1325-7. |
| [10] | Bensinger W, Schubert M, Ang K K, Brizel D.NCCN task force report prevention and management of mucositis in cancer care[J].J Nat Compreh Cancer Network, 2008,6(1):S1-21. |
| [11] | Tsuyuki S, Kawaguchi K, Kawata Y, Yamaguchi A.Usefulness of antimycotic agents itraconazole in chemotherapy induced mucositis of breast cancer patients[J].Gan To Kagaku Ryoho, 2012,39(9):1369-73. |
| [12] | 刘端勇, 黄敏芳, 徐荣, 王馨.黄芪多糖对结肠炎大鼠小肠PP结中T淋巴细胞亚群的调节作用[J].中国药理学通报, 2015,31(9):1328-9. Liu D Y, Huang M F, Xu R, Wang X.Effect of Astragalus polysaccharides in regulating the T lymphocyte subgroup in intestinal PPs of ratwith colitis[J].Chin Pharmacol Bull, 2015,31(9):1328-9. |
| [13] | 何玲, 孙桂波, 孙潇, 孙静.木犀草苷对阿霉素诱导乳鼠心肌细胞损伤的保护作用[J].中国药理学通报, 2012,28(9):1229-34. He L, Sun G B, Sun X, Sun J.Protective effects of luteolin-7-0-glucoside on neonatalratcardiomyocytes damage induced by Adriamycin[J].Chin Pharmacol Bull, 2012,28(9):1229-34. |
| [14] | Abdelali D, Enrique M P, Mercedes O G, Borja O.The nutritional supplement active Hexose correlated compound(AHCC) hasdirect immunomodulatory actions on intestinal epithelial cells andmacrophages involving TLR/MyD88 and NF-κB/MAPK activation[J].Food Chem, 2013,136:1288-95. |
| [15] | Sharif O, Bolshakov V N, Raines S, Newham P.Transcriptional profiling of the LPS induced NF-κB response in macrophages[J].BMC Immunol, 2007,12(8):1. |
| [16] | 王琳琳, 韦巧珍, 连淑君, 唐清.谷氨酰胺对内毒素血症幼鼠肠道核因子-B活化及肿瘤坏死因子-α、白介素-6表达的影响[J].实用儿科临床杂志, 2010,25(19):1479-81. Wang L L, Wei Q Z, Lian S J, Tang Q.Effect of G lutamine on activation of nuclear factor-κB and expression of tumor necrosis factor-α, interleukin-6 in infant rats with endotoxemia[J].J Appl Clin Pediaty, 2010,25(19):1479-81. |