


2. 湖南中医药大学医学院, 湖南长沙 410208
2. Medical College of Hunan University of Chinese Medicine, Changsha 410208, China
内皮功能障碍(endothelial dysfunction,ED)与冠心病、动脉粥样硬化等心脑血管疾病密切相关,其本质是内皮损伤和修复之间动态平衡被破坏。内皮祖细胞(endothelial progenitor cell,EPC)是修复内皮损伤的重要细胞,可作为种子细胞用于血管内皮受损的修复治疗。但由于局部微环境的改变和EPC数量和功能的异常而影响EPC对受损血管内皮的修复效率[1, 2],因而增加EPC的数量和改善局部微环境成为促进受损血管内皮修复的重要措施。目前能促进EPC修复受损血管内皮的措施还很少。现代研究表明,中医活血化瘀法对血管内皮功能具有保护作用,能修复内皮损伤。血府逐瘀汤是中医行气活血法的代表方剂,研究表明血府逐瘀汤能调节血管内皮活性因子,改善血管内皮病变程度,保护血管内皮[3],对冠状动脉粥样硬化性心脏病患者有很好疗效[4]。但有关该方能否促进EPC对血管内皮受损的修复作用还不清楚。因此,为进一步了解血府逐瘀汤对EPC修复受损血管内皮的调控作用,深入探讨该方治疗心脑血管疾病的机制,本文研究了该方对体外输注EPC修复受损血管内皮的影响。
1 材料与方法 1.1 材料 1.1.1 实验动物成年♂ SD大鼠,体质量180~200 g,湖南斯莱克景达实验动物有限公司,合格证号:scxk(湘)2011-0003。
1.1.2 主要试剂和仪器Percoll淋巴细胞分离液(ρ=1.083) (TBD,天津),内皮细胞培养基(Endothelial Basal Medium-2,EBM-2),内皮细胞生长因子套装(EGM-2-MV-SingleQuots)(LONZA Inc. Switzerland),纤联蛋白(fibronectin,FN),FITC标记的荆豆凝集素-1(FITC-UAE-1),四甲基吲哚羰基花青高氯酸盐(1,1′-dioctadecy1-3,3,3′,3′-tetramethylindocarbocyanine perchlorate,Dil)标记的乙酰化低密度脂蛋白(Dil-ac-LDL)(Biomedical Technologies,USA); 4′,6-二脒基-2-苯基吲哚(4′,6-diamidino-2-phenylindole,DAPI) (Vector Laboratories,USA);β-半乳糖苷酶 (senescence-associated β-galactosidase,SA-β-Gal) 染色试剂盒( Beyotime,中国);小鼠抗大鼠内皮型一氧化氮合酶抗体(eNOS)(Boster,中国);兔抗鼠β-actin单克隆抗体(Bioworld,中国);兔抗鼠多克隆基质细胞衍生因子-1(stromal cell-derived factor-1,SDF-1)抗体(R&D Systems,Inc.,USA);兔抗鼠单克隆趋化因子受体-4(CXC chemokine receptor 4,CXCR-4)抗体(abcam,USA);超敏化学放光显色试剂盒、封闭蛋白干粉、羊抗鼠二抗、羊抗兔二抗、蛋白印迹膜再生液,以上试剂均来自博士德公司(Boster,中国)。血脂和血钙检测试剂盒均来自中生北控生物科技股份有限公司。
1.2 方法 1.2.1 EPC的培养、鉴定和标记参考文献方法[5],大鼠颈椎脱臼处死,采用改良密度梯度离心法获取骨髓单个核细胞后培养,72 h后半量换液,14 d左右见细胞铺满培养瓶后可进行鉴定或传代。(1)功能学鉴定:按照文献方法[6],取培养细胞,PBS漂洗5min 3次。加入Dil-ac-LDL(终浓度10 mg·L-1 )37℃ 孵育4 h。PBS漂洗后以4%多聚甲醛固定。PBS漂洗后加入FITC-UAE-1(终浓度80 mg·L-1)37℃孵育1 h。PBS漂洗晾干后荧光显微镜观察。细胞吸收Dil-ac-LDL后荧光显微镜下可见红色,结合FITC-UAE-1后可见绿色,采用图像分析系统将同视野的吸收Dil-ac-LDL和结合FITC-UAE-1的照片重合后出现橙色即为EPC。本实验细胞计数双阳性细胞达(91.5±4.3)%(n=5)。(2)细胞表面标志物鉴定:按照文献方法[7],收集细胞,4%多聚甲醛固定,PBS洗涤、离心,5%羊血清4℃封闭,离心后以PBS重悬细胞,进行CD34/CD133细胞表面标志物的鉴定。本研究细胞培养7、14、21 d细胞CD34/CD133的双阳性表达分别为16.9%、22.6%、19.71%,CD34/CD133双阳性表达细胞即为具有干细胞表型且能分化为成熟内皮细胞的EPC。(3)EPC标记:参考文献[8],取培养14 d的EPC,将荧光染色剂DAPI(终浓度50 g·L-1)加入EPC中,在37℃ CO2培养箱中孵育24 h,标记后的EPC用无菌PBS冲洗6次,除去未结合的DAPI,荧光显微镜下观察标记的EPC。
1.2.2 血管内皮衰老模型建立根据文献建立大鼠血管内皮衰老模型[9]:大鼠以配方为2%胆固醇、0.5%胆酸钠、3%猪油、0.2%丙基硫氧嘧啶和94.3%基础饲料的高脂饲料喂养,辅以VitD腹腔注射,7×105 U·kg-1,分2次注射,高脂喂养14 d后第1次注射,28 d后第2次注射,持续高脂饲料喂养12周。随机取5只大鼠,采用形态学方法观察内膜形态,检测内膜厚度,SA-β-Gal法检测内皮衰老情况,可见大鼠主动脉内膜增厚,出现动脉粥样硬化样改变,内皮衰老检测呈阳性,据此确认造模成功。
1.2.3 血府逐瘀汤的制备按原方剂量取药材6倍量,置于5 000 mL烧瓶中加8倍量蒸馏水进行回流加热提取两次,提取时间分别为60 min。滤过,合并两次滤液,将滤液置于旋转蒸发仪浓缩约440 mL。将上述两份浓缩液加95%乙醇调至含醇浓度85%,得水醇液,放置沉淀(出现大量黄褐色粘性沉淀),24 h后抽滤,醇液减压回收乙醇并蒸干水至无醇味。反复处理、沉淀3次,最后一次调乙醇浓度达90%,放置至无沉淀物再生成,抽滤,滤液回收乙醇,并蒸干至无醇味后,置于重量已知的蒸发皿中90℃水浴蒸至近干,放置于真空干燥箱中,真空干燥至全干,称重备用。
1.2.4 分组、给药及处理模型成功后将大鼠随机分为模型组(M组)、单纯EPC输注组(E组)、单用血府逐瘀汤组(X组)、血府逐瘀汤联合EPC组(Y组),并设立空白对照组(C组),共5组。X组、Y组灌胃血府逐瘀汤(生药7.5 g·kg-1)具体给药剂量参考文献[10]及动物给药的体表面积折算法确定;E组、M组及C组灌胃蒸馏水,灌胃药物及水均每天1次,连用30 d,每周称体重调整灌胃药量。在灌胃给药的d 8,给予E组、Y组尾静脉一次性输注以1 mL PBS混悬,数量约为2×106的DAPI标记的EPC、X组、M组、C组输注1 mL PBS予以对照。药物干预30 d后处死动物取材进行检测。
1.2.5 血管内膜增生的测定取胸主动脉,按以往研究方法[11]检测血管内膜厚度以反映内皮损伤和修复。masson染色法观察血管内膜形态,采用图像分析法计量内膜增生情况,按组织学划分,内弹力膜以内为内膜。内膜厚度=[(内弹力膜周径-管腔周径)/2π],以MIAS医学图像分析系统测量内膜厚度。取血管壁内膜最厚处测量,以3个不同横截面的平均值表示该血管内膜的厚度。
1.2.6 内皮衰老测定根据试剂盒方法测定血管SA-β-gal活性以评价内皮衰老状况:大鼠胸主动脉标本石蜡切片,常规方法脱蜡和水化处理后加入适量的β-半乳糖苷酶染色固定液,以充分盖住组织为宜,室温固定不少于15 min。用PBS浸泡洗涤组织3次,每次不少于5 min。吸除PBS,加入适量染色工作液。将切片充分浸泡在染色工作液中37℃孵育过夜,在普通光学显微镜下观察,阳性表达可见血管内膜呈颗粒状蓝色。
1.2.7 EPC归巢的测定参考文献[12]取培养14 d的EPC用荧光染色剂DAPI标记后尾静脉输注大鼠体内。4周后取胸主动脉冰冻切片标本荧光显微镜下观察EPC在受损血管内皮的归巢情况。
1.2.8 血脂血钙测定实验结束后眼眶静脉丛取血,分离血清按试剂盒说明书测定血脂、血钙。
1.2.9 Western blot检测血管内皮eNOS、SDF-1、CXCR4蛋白表达各组大鼠于给药30 d后即末次给药后次日,麻醉后处死,取出胸腹主动脉,按试剂盒说明提取蛋白,Bradford 法测定蛋白质含量。将样品蛋白煮沸变性后进行SDS-PAGE电泳,电转法将蛋白转移至PVDF膜,5%蛋白封闭液封闭。加入3mL用TBST稀释的一抗(eNOS1:500、SDF-1 1:200、 CXCR4 1:1 000、 β-actin 1:2 000),4℃缓慢摇动过夜后加入羊抗鼠、羊抗兔第二抗体3 mL(1:4 000),37℃孵育1 h。用化学发光试剂进行显色,用凝胶成像系统将曝光后胶片进行扫描,用图像分析软件IPP6.0对图像进行光密度分析。以目的蛋白与β-actin光密度值的比值作为该目的蛋白的相对表达量。
1.3 统计分析方法运用统计学软件spss17.0进行数据分析,实验结果所有数据均采用±s表示,多组间均数比较用单因素方差分析,组间两两比较方差齐者用LSD法,方差不齐者先将数据进行自然对数转换后再作单因素方差分析和两两比较。
2 结果 2.1 各组血管内皮形态及内膜厚度比较血管形态观察显示,模型组可见血管内膜增厚,部分增厚部位出现泡沫细胞等动脉粥样硬化样改变,中膜萎缩,血管环状肌层结构破坏,表明造模方法可造成血管内膜损伤。与模型组比较,各药物组血管内膜增生、中膜变薄明显改善。其中EPC输注组及血府逐瘀汤联合EPC组改善明显(Fig1)。

|
| Fig 1 Vascular morphology of each group(masson stanining,×100) C:Control group;M:Model group;E:EPC alone infusion group;X:XFZYD alone group;Y:XFZYD joint EPC group |
与空白组比较,模型组内膜增厚(P < 0.01),提示造模后血管内皮损伤,内膜增生。与模型组比较,EPC组、血府逐瘀汤组以及血府逐瘀汤联合EPC组内膜厚度均明显减小(P < 0.01);与单用EPC组比较,血府逐瘀汤联合EPC组内膜厚度减小(P < 0.05);与单用药物组比较,血府逐瘀汤联合EPC组内膜厚度明显下降(P < 0.01)。结果提示血府逐瘀汤联用EPC后修复损伤血管内皮的效果优于单用EPC组和单用药物组。
| Group | n | Intima Thickness/μm |
| C | 6 | 8.2±1.4 |
| M | 7 | 106.5±18.9 ** |
| E | 8 | 12.8±1.7 △△ |
| X | 8 | 35.2±8.9 △△● |
| Y | 8 | 8.9±1.1 △△●## |
| C:Control group,M:Model group,E:EPC alone infusion group,X:XFZYD alone group,Y:XFZYD joint EPC group. ** P < 0.01 vs control group; △△ P < 0.01 vs model group; ● P<0.01 vs EPC group; ## P < 0.01 vs group X | ||
为进一步了解该方在抑制内膜增生方面是否与EPC有交互作用,本研究进行了交互作用分析,方法如下:以模型组的均数为基础值,模型组均数与EPC组均数的差值为单用EPC的效应,模型组均数与单用中药组均数的差值为单用中药的效应,二者相加为其联合应用的理论效应值。模型组均数与联合组的均数差值为联合应用的实际效应值。如果实际效应值<理论效应值为拮抗作用,实际效应值≈理论效应值(误差≤10%)为相加,实际效应值﹥理论效应值为协同作用。交互作用分析结果显示:血府逐瘀汤与EPC联用后在拮抗内膜增生方面具有相加作用。
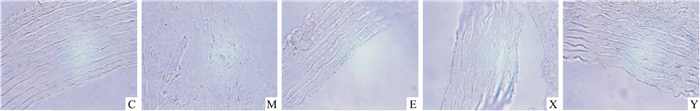
2.2 各组血管内皮衰老的比较结果显示,M组血管内膜增生,增生内膜中可见泡沫细胞,部分血管可见动脉粥样硬化病变,细胞内膜和内膜细胞可见衰老阳性表达颗粒呈蓝色。而空白组表达呈阴性,且无增生。药物干预4周后,与模型组比较,各实验组细胞衰老情况改善明显,可见血府逐瘀汤联合EPC组、EPC组血管各层细胞排列较整齐,内膜层稍有折叠,血管各层细胞均未见阳性表达;血府逐瘀汤组与模型组相比内膜损伤亦明显改善,未见明显粥样硬化样病变,但血管纤维排列较紊乱,内膜、中膜层阳性颗粒偶见(Fig2)。
|
| Fig 2 Endothelial cell senescence markers in each group(SA-β-gal stanining,×400) Note see Fig1. |
荧光显微镜下血府逐瘀汤联合EPC组、单用EPC输注组血管管壁可见蓝色荧光,尤其是在内膜部位及损伤严重部位的荧光表达更强;结合血管形态学及管壁计量检测结果可见输注EPC的各组损伤修复较好,由此可知,输注的EPC归巢到损伤血管分化为内皮细胞参与了损伤血管内皮的修复(Fig3)。

|
| Fig 3 EPC homing to vascular intima(Fluorescence method,×100) Y:XFZYD joint EPC group; E:EPC alone infusion group. |
由Tab2可知,与空白组比较,模型组血脂明显升高,差异有统计学意义(P < 0.05),提示高脂喂养加注射维生素D导致血脂升高。与模型组比较,药物组及药物联合EPC组均有下调总胆固醇及甘油三酯的作用,差异有统计学意义(P < 0.05),而单独输注EPC组在下调上述两个指标上差异无显著性,提示活血方可能是降低血脂的主要有效物质。药物组及药物联合EPC组均能上调高密度脂蛋白(HDL-ch)的水平,而单独EPC组HDL-ch无明显变化。由此可见,血府逐瘀汤还具有上调高密度脂蛋白的作用。
| Group | n | Total cholesterol | Triglyceride | High density lipoprotein | Low density lipoprotein | Serum calcium |
| C | 6 | 1.92±0.46 | 1.2±0.31 | 0.65±0.06 | 0.51±0.05 | 2.45±0.51 |
| M | 7 | 2.29±0.38 * | 1.55±0.54 * | 0.59±0.12 * | 0.53±0.19 | 4.02±0.83 ** |
| E | 8 | 2.17±0.22 | 1.2±0.13 | 0.57±0.04 | 0.46±0.02 | 3.40±0.76 △ |
| X | 8 | 1.64±0.23 △● | 0.83±0.12 △△● | 0.68±0.11 △ | 0.49±0.08 | 2.98±0.65 △ |
| Y | 8 | 1.78±0.26 △● | 0.63±0.19 △△●# | 0.84±0.13 △●# | 0.5±0.11 | 2.74±0.57 △△● |
| Note see Tab 1. * P < 0.01, **P < 0.01 vs control group; △ P < 0.05, △△P < 0.01 vs model group; ● P < 0.01 vs EPC group; # P < 0.01 vs Group X. | ||||||
与E组比较,药物联合EPC组在降低总胆固醇及甘油三酯的水平方面差异有显著性(P < 0.05)。与单用药物组比较,血府逐瘀汤联合EPC组降低甘油三酯的水平,升高高密度脂蛋白水平的作用更为明显(P < 0.05),从而提示中药复方联合EPC后调节血脂作用增强。血钙结果分析表明,与空白组比较,模型组的血钙浓度明显增加(P < 0.01);药物组与模型组比较血钙浓度明显降低(P < 0.05);单纯EPC组与药物EPC联合组相比,后者血钙下降更为明显,差异有统计学意义(P < 0.05),提示血府逐瘀汤能下调血管内皮损伤模型的血钙水平。
交互作用分析结果显示:在调节高密度脂蛋白和甘油三酯方面,血府逐瘀汤与输注EPC具有协同作用;在调节血钙方面未见交互作用。
由上可知,在调节血脂血钙方面,其作用可能来自于活血方,而血府逐瘀汤联合EPC后,在修复血管内皮损伤方面具有交互作用,可能与该方能调节血脂,改善内环境,从而为EPC归巢分化提供有利条件有关。
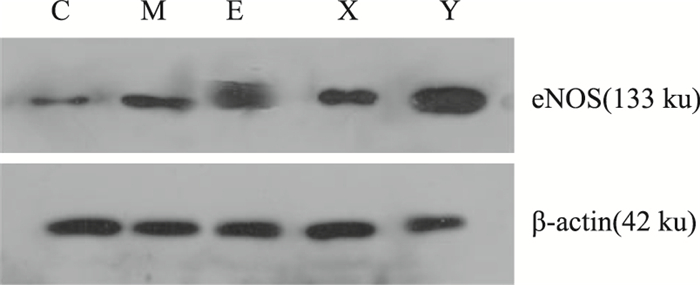
2.5 各组血管eNOS表达的比较与空白对照组比较,模型组eNOS蛋白表达无明显变化(P>0.05);与模型组比较,各治疗组eNOS表达均明显增强(P<0.05)。与E组比较,活血方联用EPC组的eNOS蛋白表达明显增加(P < 0.05)。与单用药物组比较,活血方联用EPC组eNOS蛋白表达明显增强(P < 0.05)。结果表明,血府逐瘀汤联合EPC后可提高eNOS蛋白表达水平,各药物组治疗后eNOS蛋白表达水平明显提高,从而提示损伤血管内皮得到修复,内皮功能得到恢复(Fig4,Tab3)。
|
| Fig 4 eNOS expression profile of each group Note see Fig1. |
| Group | n | eNOS/β-actin(IOD) |
| C | 6 | 0.47±0.09 |
| M | 7 | 0.53±0.06 ● |
| E | 8 | 0.73±0.12 △△ |
| X | 8 | 0.71±0.06 △● |
| Y | 8 | 1.13 ±0.10 △△●## |
| Note see Tab 1.△ P < 0.05,△△P < 0.01 vs model group,● P < 0.01 vs EPC group;## P < 0.01 vs Group X. | ||
交互作用分析结果如下:血府逐瘀汤在上调eNOS表达方面与EPC具有相加作用。
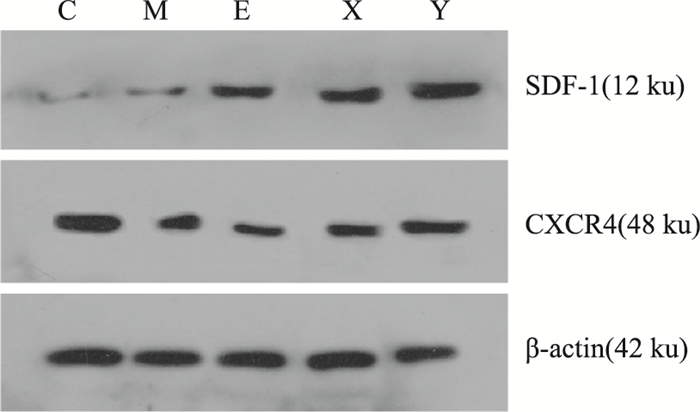
2.6 各组SDF-1、CXCR-4表达的比较与空白对照组比较,SDF-1蛋白表达明显升高(P < 0.05)。与模型组比较,血府逐瘀汤组和血府逐瘀汤联合EPC组SDF-1蛋白表达明显升高(P < 0.01或P < 0.05),而单用EPC组与模型组比较无统计学意义(P>0.05)。与单用EPC组比较,血府逐瘀汤联合EPC组SDF-1表达明显增高。与单用药物组比较,血府逐瘀汤联合EPC组与血府逐瘀汤之间的差异无统计学意义(P>0.05,Fig5)。
|
| Fig 5 SDF-1 and CXCR-4 proteinexpression profiles in each group |
| Group | n | SDF-1/β-actin(IOD) | CXCR4/β-actin(IOD) |
| C | 6 | 0.23±0.15 | 0.80±0.12 |
| M | 7 | 0.50±0.10 * | 0.51±0.11 * |
| E | 8 | 0.57±0.12 | 0.57±0.20 |
| X | 8 | 0.61±0.09 △ | 0.60±0.16 |
| Y | 8 | 0.68±0.12 △● | 0.57±0.14 |
| Note see Tab 1. * P < 0.01 vs control group; △ P < 0.01 vs model group; ● P < 0.01 vs EPC group | |||
在CXCR-4蛋白表达方面,与空白组比较,模型组CXCR-4表达明显降低(P < 0.05),其它各组CXCR-4表达也明显降低(P < 0.05)。与模型组比较,各治疗组CXCR-4变化无统计学意义(P>0.05)。
为进一步了解两类活血方在调节SDF-1、CXCR-4的表达方面是否与EPC有交互作用,本研究进行了交互作用分析,结果如下:在上调血管SDF-1的表达方面,血府逐瘀汤与输注EPC具有相加作用;在调节血管CXCR-4的表达方面,中药复方与输注EPC无交互作用。
2.7 各组PI3K、磷酸化Akt表达的比较Tab5结果表明:与空白对照组比较,模型组PI3K蛋白表达差异无统计学意义(P>0.05)。与模型组比较,血府逐瘀汤联合EPC组PI3K蛋白表达增强(P < 0.05),而单用EPC组和单用血府逐瘀汤组差异无统计学意义(P>0.05)。与单独药物组比较,药物联合EPC组PI3K蛋白表达均明显增强(P < 0.01或P < 0.05)。与单纯EPC组比较,活血方联用EPC组PI3K蛋白表达均增强(P < 0.05)。与空白对照组比较,模型组p-Akt表达差异无显著性(P>0.05),与模型组比较,各治疗组p-Akt表达均增强(P < 0.05或P < 0.01)。与单纯EPC组比较,活血方联合EPC组p-Akt表达均明显增强(P < 0.01);与单用两类活血方组比较,两类活血方联合EPC组p-Akt表达均明显增强(P < 0.01)。交互作用分析结果如下:血府逐瘀汤联合输注EPC在上调PI3K、p-Akt蛋白表达方面均有协同作用(Fig6)。

|
| Fig 6 PI3K and p-AKT protein expression profiles in each group Note see Fig1. |
| Group | n | PI3K/β-actin(IOD) | p-Akt/β-actin(IOD) |
| C | 6 | 0.81±0.09 | 1.12±0.09 |
| M | 7 | 0.80±0.07 | 1.01±0.11 |
| E | 8 | 0.86±0.09 | 1.50±0.12 △ |
| X | 8 | 0.74±0.07 | 1.23±0.11 △ |
| Y | 8 | 1.12±0.06 △●## | 1.75±0.09 △△●## |
| Note see Tab 1.△ P < 0.05,△△P < 0.01 vs model group;● P < 0.01 vs EPC group;## P < 0.01 vs Group X. | |||
中医药防治血管内皮损伤,“本在气血,标为瘀”。故本研究选用活血化瘀的代表方:行气化瘀之血府逐瘀汤,研究其防治内皮损伤性疾病的作用。血府逐瘀汤亦载于清代王清任《医林改错》,重在行气活血化瘀。方中当归、赤芍、川芎、桃仁、红花活血化瘀;牛膝祛瘀、通血脉,并引瘀血下行;柴胡疏肝解郁、升达清阳;桔梗、枳壳开胸引气,气行则血行;生地黄凉血清热,配当归养血润燥,使瘀祛而不伤阴;甘草缓急,通百脉以调和诸药。红花、桃仁、赤芍、川芎4味药为活血化瘀法的核心,而以桔梗主升、枳壳畅中、牛膝主下,贯通上、中、下气血,再用当归、生地黄养血补血活血,加甘草和中防止伤胃气。本方不仅行血分之瘀滞,又解气分之郁结,活血而不耗血,祛瘀而又能生新,合而用之,使气行瘀祛,诸证可愈。该方在调节血脂方面具有良好的作用,能联合西药可有效提高高脂血症的临床疗效,能改善血脂和血流流变学指标,增加颈动脉血流量[13]。
本文实验结果表明,从血管形态学评价和血管内膜厚度比较可知,血府逐瘀汤联合EPC使受损内膜增生明显下降、损伤减轻,并促进EPC在受损血管的归巢。提示中药复方联合EPC后可促进EPC对血管内皮的修复,中药联合EPC具有一定的相加作用。血管内皮eNOS蛋白表达分析也表明,血府逐瘀汤联合EPC可进一步上调血管内皮eNOS表达,交互作用分析表明,中药复方联合EPC均具有相加作用。在调节血脂、血钙方面该方联合EPC的作用优于单纯EPC组,但与单用两类活血方组差异无显著性。综上所述,从血管形态学、血脂血钙、血管内皮功能检测结果并结合交互作用分析可知,血府逐瘀汤联合EPC可以增加修复损伤血管内皮的作用,其机制可能与该方通过改善局部微环境,促进了EPC的归巢与分化从而促进了EPC对损伤内皮的修复有关。
在分析其机制方面,已有研究表明,SDF-1/CXCR-4轴在内皮祖细胞的归巢、动员和分化中发挥着关键作用[14]。血府逐瘀汤联合EPC输注组的SDF-1表达高于单独输注EPC组,亦高于单独药物组。提示药物联合EPC可能通过上调SDF-1的表达而促进EPC迁移、归巢,促进了损伤内皮的修复。在内皮损伤后血管内膜的CXCR-4表达上调,这可能是血管本身适应性改变,目的是为EPC修复内皮创造条件。各药物及EPC输注并不能影响CXCR-4的表达,推测一是可能与CXCR-4仅在内皮祖细胞表面的表达而本研究的标本来自于内皮祖细胞归巢分化后修复的损伤血管,二是可能与检测的时间点有关,如选择输注后细胞分裂期可能会检测到对CXCR-4表达的影响,这也是本研究进一步深入研究的内容和方向。
磷脂酰肌醇3 激酶/蛋白激酶B(phosphatidylinositol 3′-kinase/protein kinase B,PI3K/Akt)信号通路是调节各种细胞生长、代谢、分化的重要信号通路[15, 16]。血府逐瘀汤联合EPC后,PI3K表达增强,磷酸化Akt水平增加,提示该方联合EPC后可进一步激活PI3K/Akt,促进EPC的增殖、分化,增强了EPC对受损内皮的修复作用。PI3K/Akt信号通路可能是该方联合EPC促进内皮修复的主要机制。
| [1] | Kunz G A, Liang G, Cuculi F, et al.Circulating endothelial progenitor cells predict coronary artery disease severity[J].Am Heart J, 2006, 152(1):190-5. |
| [2] | 李玉娟, 刘建勋.内皮祖细胞的鉴定及培养方法[J].中国药理学通报, 2009, 25(10):1383-5. Li Y J, Liu J X.The identification and culture methods of endothelial progenitor cells[J].Chin Pharmacol Bull, 2009, 25(10):1383-5. |
| [3] | 耿兆辉, 寿保栋, 刘辉, 等.血府逐瘀汤对动脉粥样硬化大鼠血脂及血管活性物质的影响[J].河北大学学报, 2011, 31(3):304-8. Geng Z H, Shou B D, Liu H, et al.Effect of Xuefu Zhuyu Decoction on the expression of blood-lipid and vasoactive substances in the rats with atherosclerosis[J].J Hebei Univ, 2011, 31(3):304-8. |
| [4] | 刘喜梅.血府逐淤汤对冠状动脉粥样硬化性心脏病Hcy、LP(a)的临床研究[J].中医临床研究, 2013, 5(14):27-8. Liu X M.A clinical research of the effect of the Xuefu Zhuyu decoction on Hcy and LP(a) level in coronary atherosclerotic heart disease[J].Clin J Chin Med, 2013, 5(14):27-8. |
| [5] | Yin T, Ma X L, Zhao L, et al.Angiotensin II promotes NO production, inhibits apoptosis and enhances adhesion potential of bone marrow-derived endothelial progenitor cells[J].Cell Res, 2008, 18:792-9. |
| [6] | Zhao M, Wang X X, Wan W H.Effects of the ginkgo biloba extract on the superoxide dismutase activity and apoptosis of endothelial progenitor cells from diabetic peripheral blood[J].Genet Mol Res, 2014, 13(1):220-7. |
| [7] | Zhang J C, Lyu G.Effect of 17β estradiol in rat bone marrowderived endothelial progenitor cells[J].Mol Med Rep, 2013, 8(1):178-82. |
| [8] | Zhu Z, Chen G, Li X, et al.Endothelial progenitor cells homing to the orthotopic implanted liver tumor of nude mice[J].J Huazhong Univ Technol Med Sci, 2012, 32(5):675-9. |
| [9] | 王先酉, 赵秀华, 王峰, 等.高脂饮食引起大鼠动脉血管内皮细胞衰老[J].国际病理科学与临床杂志, 2010, 30(4):118-22. Wang X X, Zhao X H, Wang F, et al.Endothelial cellular senescence caused by high-fat diet in rats[J].Int J Pathol Clin Med, 2010, 30(4):118-22. |
| [10] | 樊星花, 石卫州, 程允相, 等.血府逐瘀汤对大鼠肝脏抗氧化酶及药物代谢酶的影响[J].中国中药杂志, 2014, 39(22):4453-8. Fan X H, Shi W Z, Cheng Y X, et al.Effects of Xuefu Zhuyu decoction on antioxidant and drug-metabolizing enzymes in liver of rats[J].China J Chin Mat Med, 2014, 39(22):4453-8. |
| [11] | Wu L, Zhang W, Tang Y H, et al.Effect of total saponins of "panax notoginseng root" on aortic intimal hyperplasia and the expressions of cell cycle protein and extracellular matrix in rats[J].Phytomedicine, 2010;17(3-4):233-40. |
| [12] | Yu J X, Huang X F, LYU W M, et al.Combination of stromal-derived factor-1alpha and vascular endothelial growth factor gene-modified endothelial progenitor cells is more effective for ischemic neovascularization[J].J Vasc Surg, 2009, 50(3):608-16. |
| [13] | 俞雪梅, 杨光辉, 李萍.血府逐瘀汤对高血脂症患者的降脂作用机制研究[J].辽宁中医杂志, 2014, 41(4):289-90. Yu X M, Yang G H, Li P.Mechanism of lowering blood lipids of xuefuzhuyu decoction in patients with hyperlipidemia[J].J Liaoning Chin Med, 2014, 41(4):289-90. |
| [14] | Wojakowski W, Tendera M.Mobilization of bone marrow-derived progenitor cells in acute coronary syndromes[J].Folia Histochem Cytobiol, 2005, 43(4):229-32. |
| [15] | Li L X, Zhang X F, Bai X, et al.SDF-1 promotes ox-LDL induced vascular smooth muscle cell proliferation[J].Cell Biol Int, 2013, 37(9):988-94. |
| [16] | 秦臻, 黄水清.当归补血汤含药血清对内皮祖细胞功能及其PI3K/Akt通路影响的研究[J].中国药理学通报, 2013, 29(9):1320-3. Qin Z, Huang S Q.Influence of drug-serum containing Dangguibuxue decoction on functional activity and PI3K/Akt pathway of endothelial progenitor cells[J].Chin Pharmacol Bull, 2013, 29(9):1320-3. |

