


2. 河北以岭医药研究院国家中医药管理局重点研究室, 河北石家庄 050035;
3. 河北医科大学附属以岭医院, 河北石家庄 050091
2. Dept of Cardiology, Yiling Medical Institute of Hebei Province, Key Laboratory of State Administration of Traditional Chinese Medicine, Shijiazhuang 050035, China;
3. Yiling Hospital of Hebei Medical University, Shijiazhuang 050091, China
近年关于动脉粥样硬化(atherosclerosis,AS)的研究,已经由聚焦于血管内膜的“由内向外”(inside-out)炎症反应机制逐步转变为“由外向内”(outside-in),血管外膜在AS发病机制中的作用越来越受到重视,大中动脉管壁外膜及中膜外1/3上存在微血管,滋养中膜外1/2至2/3的区域[1],保障管壁自身的物质代谢及能量代谢。Gssl等[2]利用Micro-CT检测方法发现,高脂组的血管滋养管密度和内中膜层厚度较正常组均明显增多;而新生滋养血管的破裂使得巨噬细胞积累、脂质/坏死核心扩大,导致斑块不稳定,已经被确定为斑块进展和斑块破裂并发症的启动因子,管壁微血管的分布密度与AS病变的严重程度呈正相关。此外研究显示在AS早期外膜微血管滋生过程中,外膜局部氧化及抗氧化酶活性发生改变[3]要早于整体氧化还原系统。桂芍通络是以营卫学说与血脉理论指导制定的营卫通络方,我们试图围绕氧化应激作用,探讨AS早期外膜滋养血管新生机制及桂芍通络的干预作用。
1 材料与方法 1.1 动物清洁级日本大耳白兔84只,♀♂各半,体质量(2.0±0.3) kg,购自北京富豪实验动物养殖中心,实验动物许可证号:SCXK(京)2010-0010。单笼饲养于河北络病重点实验室。每天12 h间隔照明,温度20~25℃,湿度40%~70%,每日通风,定时消毒。
1.2 药品、试剂与仪器阿托伐他汀片(辉瑞制药有限公司,批号:L14578);通心络超微粉(石家庄以岭药业股份有限公司,批号:S-130901);桂芍通络超微粉(石家庄以岭药业股份有限公司,将桂芍通络按临床所用剂量比例称取,采用水提、醇提、提油等制备工艺,浓缩干燥制成胶囊原粉);VEGF鼠抗兔单克隆抗体(英国Abcam公司,批号:ab1316);VEGFR-2山羊多克隆抗体(美国Santa Cruz公司,批号:sc-48161);柠檬酸钠(阿拉丁,生产批号:6132-04-3);50×Denhardts(北京索莱宝,生产批号:D1080);蛋白酶K(Beyotime,生产批号:ST532);7080全自动生化分析仪(日本日立公司);3K15型高速冷冻离心机(Sigma);MDF-U50V型-80℃冰箱(SANYO);
1.3 方法 1.3.1 动物分组及造模适应性喂养1周后,将84只实验兔随机分为正常组、高脂组、外膜损伤组、桂芍通络高剂量(GH)组、桂芍通络中剂量(GM)组、阿托伐他汀(ATO)组、通心络(TXL)组,每组12只。正常组给予普通饲料,高脂组给予高脂饲料[4](胆固醇1%、猪油5%、胆固醇7.5%及基础饲料86.5%)喂养建立早期高脂血症模型,外膜损伤组及各用药组实施高脂饮食复合右侧颈动脉硅胶管包裹术。3%戊巴比妥钠(1 mL·kg-1)耳缘静脉注射麻醉后,将实验兔仰卧固定于手术台,备皮后消毒,沿颈部正中剪开皮肤,钝性分离,暴露气管右侧搏动的颈总动脉鞘,用眼科镊配合玻璃分针仔细游离出右颈动脉(RCA)2.5 cm,将消毒后的硅胶管(内径1.7 mm,外径3.2 mm,长2 cm)纵向剖开后,包裹于右侧颈动脉,避免损伤鞘膜内的迷走神经、交感神经,局部滴加链霉素,逐层缝合伤口,术后连续3 d行2次/日局部消毒。实验室每日按时通风消毒。
1.3.2 标本采集术后4周时取材,标本采集前禁水禁食12 h,3%戊巴比妥钠(1 mL·kg-1)耳缘静脉注射麻醉,腹主动脉取血。备皮消毒后,行颈部正中切口,迅速分离取下术侧颈动脉,生理盐水洗净,一部分置入4%多聚甲醛溶液固定,用于荧光原位杂交检测及苏木精-伊红(HE)染色。另一部分液氮冻存以备Western blot检测。
1.3.3 血脂测定取全血,4℃、3 500 r·min-1离心10 min,取上清液分装入EP管,采用日立7080全自动生化分析仪测定TC、TG和LDL-C水平。
1.3.4 HE染色观察血管内中外膜病理形态变化将已固定的标本脱水浸蜡包埋,切片脱蜡,PBS冲洗,苏木精液浸染2 min,流水冲洗,0.3%盐酸乙醇分化,自来水返蓝,伊红染液4 min,封片,光镜下观察。
1.3.5 血清SOD、MDA、T-AOC表达水平采用黄嘌呤氧化酶法检测超氧化物歧化酶(SOD),TBA法检测丙二醛(MDA),化学比色法检测总抗氧化能力(T-AOC)。详细的检测步骤按照试剂盒说明书操作。
1.3.6 荧光原位杂交检测p22phox和gp91phox mRNA的定位与表达探针由上海诺辰生物技术有限公司合成,序列信息如下:gp91phox,5′FITC+ ACCATTTTATGAAAAGTGAGATTTCTG;p22phox,5′FITC+ CCAGGAGCTTCAGCACGGCGGTCAGGTAGCG。将已固定的标本脱水浸蜡包埋,切片脱蜡后浸入蛋白酶K液,置入37℃水浴锅中孵育20 min,室温漂洗后,梯度酒精脱水;将切片置于盛有变性液的染色缸内75℃孵育8 min,同时将含有RNA探针的杂交液于75℃孵育8 min,梯度酒精脱水;干燥后在玻片的标本区加入50 μL已变性的探针,放入湿盒,42℃烘箱杂交过夜(12~16 h);杂交后洗脱、酒精梯度脱水风干,荧光镜下观察。
1.3.7 Western blot检测VEGF、VEGFR-2蛋白表达取出液氮冻存标本,于预冷的PBS液中剔除周围组织,纵向剖开血管,剥离外膜干燥后称重;取100 mg标本,1 mL细胞裂解液充分裂解后,进行蛋白定量,SDS聚丙烯酰胺凝胶电泳结束后,将凝胶半干转膜至PVDF膜上;5%脱脂奶粉封闭后,与VEGF/VEGFR-2抗体4℃孵育过夜;室温洗膜后,与相应二抗室温孵育2 h,洗膜后,抗体结合区带用化学发光法检测。以GAPDH为内参,以目的基因吸光度值/GAPDH吸光度值的比值表示所检测标本目的蛋白的相对含量,进行数据统计分析。
1.3.8 统计学处理采用SPSS 19.0统计软件进行数据处理。计量资料用x ± s表示,组间比较用单因素方差分析(One-Way ANOVA),首先对数据进行正态性和方差齐性检验,方差齐性两两比较采用最小显著差法(LSD),方差不齐用Dunnett’s T3法。
2 结果 2.1 各组血脂水平比较Tab 1示,高脂组和外膜损伤组的血清TC、TG及LDL-C水平较正常组明显升高(P<0.01);与外膜损伤组相较,各药物组均降低血脂水平,且差异具有统计学意义(P<0.01);药物组之间两两比较差异无统计学意义。
| Group | TC/mmol·L-1 | TG/mmol·L-1 | LDL-C/mmol·L-1 |
| ##P<0.01 vs normal; **P<0.01 vs model | |||
| Normal | 2.70±0.32 | 0.78±0.29 | 1.00±0.23 |
| High-fat | 36.36±3.52## | 4.61±0.77## | 16.78±3.11## |
| Adventitial injury | 42.72±10.99## | 6.01±1.40## | 21.21±6.46## |
| GH | 22.77±5.40** | 2.65±0.50** | 5.97±0.99** |
| GM | 26.68±5.46** | 2.93±0.43** | 7.29±2.94** |
| ATO | 16.66±2.29** | 2.16±0.35** | 5.79±1.19** |
| TXL | 21.98±5.39** | 2.27±0.74** | 5.98±2.37** |
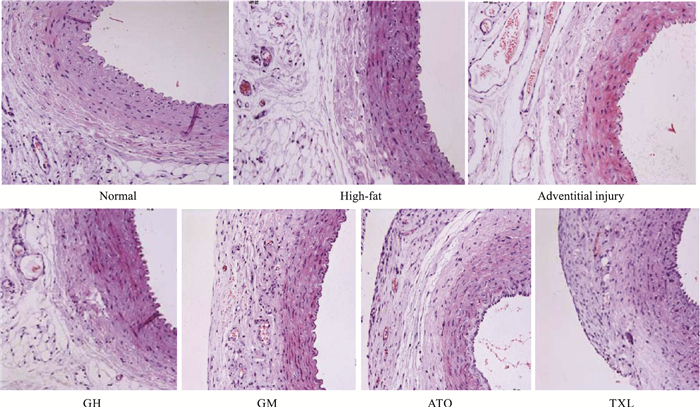
如Fig 1所示,正常组颈动脉内膜光滑,内皮细胞完整连续,中膜以平滑肌细胞为主;高脂组内膜增生,中膜间隙增宽,外膜微血管表达数量增多;外膜损伤组内膜弥漫性增生,内皮细胞脱落,可见少量泡沫状巨噬细胞形成,中膜间隙增宽,内弹力板弯曲严重,平滑肌细胞和弹力纤维排列紊乱,外膜滋养血管丰富;与外膜损伤组比较,各用药组内膜层部分增厚,中膜走形较清晰,外膜滋养血管数量减少。
|
| Fig 1 Appearance of carotid artery morphology in all groups (HE staining ×400) |
Tab 2示,与正常组相比,高脂组和外膜损伤组血清SOD、T-AOC活性明显下降,MDA含量明显升高(P<0.01);与外膜损伤组相比,GH组、GM组、ATO组及TXL组SOD、T-AOC活性明显升高,MDA含量降低;各药物组间差异无统计学意义。
| Group | SOD/kU·L-1 | MDA/μmol·L-1 | T-AOC/kU·L-1 |
| ##P<0.01 vs normal; **P<0.01 vs model | |||
| Normal | 282.97±42.98 | 4.25±0.97 | 11.36±2.31 |
| High-fat | 188.24±33.92## | 18.45±2.46## | 4.55±1.37## |
| Adventitial injury | 153.92±34.88## | 24.37±4.13## | 2.94±0.88## |
| GH | 243.81±51.91** | 10.52±2.66** | 7.82±1.92** |
| GM | 219.04±58.69** | 15.45±2.94** | 5.80±0.58** |
| ATO | 263.67±32.87** | 7.39±1.28** | 8.76±1.49** |
| TXL | 254.06±59.98** | 9.09±1.53** | 8.43±1.57** |
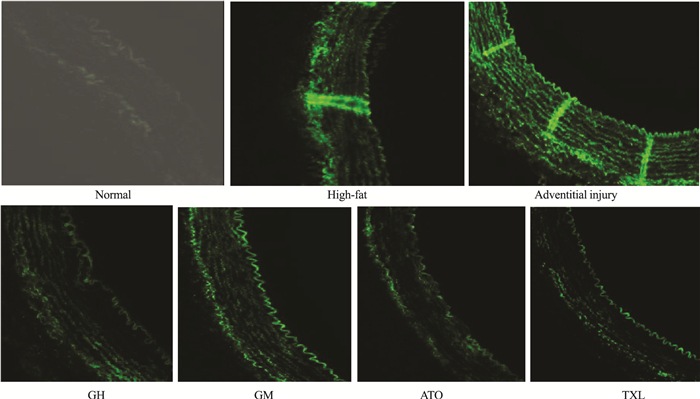
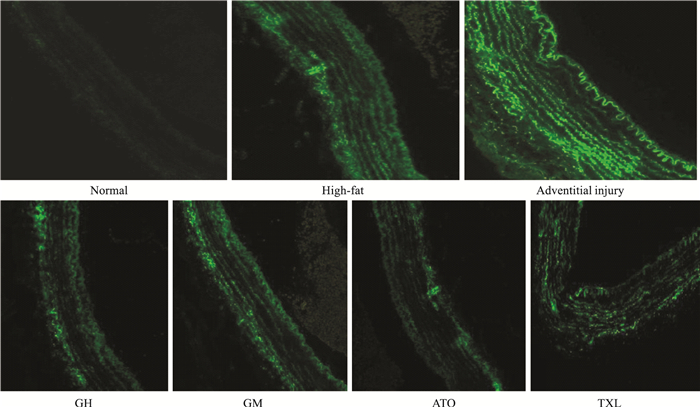
正常组gp91phox和p22phox基因杂交信号表达极少,高脂组和外膜损伤组的gp91phox和p22phox表达呈强阳性,主要分布在新生内膜和外膜微血管附近,在血管外膜gp91phox基因杂交信号分布较p22phox更为密集。GH组、GM组、ATO组及TXL组gp91phox和p22phox基因杂交信号在外膜的表达均减弱(Fig 2、3)。
|
| Fig 2 Localization and expression of gp91phox mRNA in rabbit carotid arteries by in situ hybridization (×200) The elastic laminae fluoresce green. |
|
| Fig 3 Localization and expression of p22phox mRNA in rabbit carotid arteries by in situ hybridization (×200) The elastic laminae fluoresce green. |
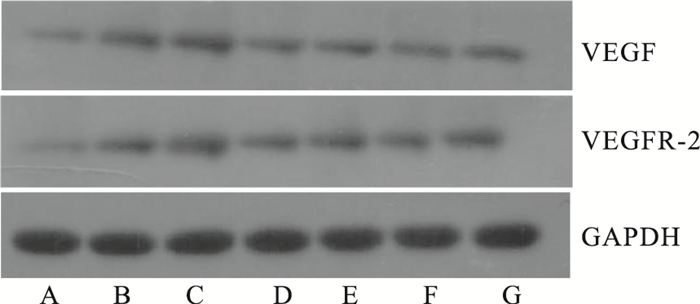
与正常组相比,高脂组VEGF、VEGFR-2蛋白表达明显增高(P<0.01,P<0.05);与高脂组相比,外膜损伤组VEGF、VEGFR-2蛋白水平明显上调(P<0.01);与外膜损伤组相比,GH组、GM组、ATO组及TXL组VEGF、VEGFR-2蛋白表达均明显降低(P<0.01),各药物组间差异无统计学意义(Fig 4,Tab 3)。
|
| Fig 4 Expression of VEGF and VEGFR-2 protein in adventitia of common carotid artery in various groups A: Normal B: High-fat C: Adventitial injury D: GH E: GM F: ATO G: TXL |
| Group | VEGF | VEGFR-2 |
| #P<0.05, ##P<0.01 vs normal; ??P<0.01 vs high-fat; **P<0.01 vs model | ||
| Normal | 0.10±0.01 | 0.13±0.03 |
| High-fat | 0.24±0.03## | 0.26±0.06# |
| Adventitial injury | 0.41±0.07?? | 0.45±0.10?? |
| GH | 0.16±0.02** | 0.19±0.02** |
| GM | 0.23±0.04** | 0.22±0.04** |
| ATO | 0.13±0.03** | 0.14±0.03** |
| TXL | 0.17±0.04** | 0.17±0.04** |
小鼠和人类的正常心肌内血管并不存在滋养血管,滋养血管主要存在于超过29层的动脉壁或管腔直径>0.05 mm的血管外膜及外膜内侧层。Hyuck Moon Kwon等运用Micro-CT技术重建器官内血管空间分布,证实高胆固醇饮食喂养猪在冠状动脉病变形成之前存在外膜滋养血管异常增生,一级与二级滋养血管数量比值发生逆转,形成密度增加、紊乱而不规则的微血管网络,其密度增加使得中、内膜层增厚,表明新生滋养血管与AS病变发展密切相关。我们采用高脂饮食喂养建立高脂血症模型,利用高脂饮食复合右侧颈总动脉硅胶管包裹术[5]在短时间内建立AS早期血管外膜损伤模型。实验结果显示,高脂组和外膜损伤组血清TC、TG、LDL-C水平明显升高(P<0.01),HE染色内膜增厚,外膜微血管数量增多,VEGF、VEGFR-2蛋白升高(P<0.05,P<0.01),表明高脂血症模型及外膜损伤模型建立成功。既往研究已证实他汀类药物、通心络具有降脂作用,且能够通过保护微血管内皮而抑制微血管异常增生,采用阿托伐他汀和通心络作为阳性对照,以进一步验证“营卫通络方”桂芍通络对AS早期外膜滋养血管及氧化应激机制的干预作用。
血管内皮生长因子(vascular endothelial growth factor,VEGF)是最主要的促进血管生成的生长因子,在正常组织中低表达,在胚胎和有血管生成的组织中高表达。VEGF家族受体主要包括非酪氨酸激酶受体和酪氨酸激酶受体两大类,后者主要包括VEGF-R1、VEGF-R2、VEGF-R3[6]。VEGF主要通过诱导内皮细胞增殖、迁移来特异性促进血管新生[7]。抑制血管新生药物的使用明显抑制了滋养血管新生及VEGF的表达,导致血管面积分数、中、内膜厚度明显减少[8]。而氧化应激通过激活MAPK信号转导通路,引起胞外信号调节激酶(ERK)、氨基末端激酶(JNK)和核转录因子NF-κB,参与VEGF诱导动脉壁血管新生[9]。ROS是与氧化应激密切相关的自由基,其生成或清除可引起机体或细胞内氧化应激反应,而起关键作用的ROS大多是NADPH氧化酶源性。NADPH氧化酶是多亚单位复合体酶,由gp91phox、p22phox、p47phox、p67phox、p40phox和Rac 6种亚基组成[10],膜结合亚基gp91phox和p22phox形成的异元二聚体是NADPH氧化酶的核心[11]。有研究证实,p22phox基因敲除诱发小鼠肿瘤血管新生障碍;在小鼠后肢缺血模型中,gp91phox基因敲除可以阻滞毛细血管密度的增加,可能与抑制gp91phox结合actin肌动蛋白有关[12]。SOD是清除自由基的主要防御酶,维持正常生物体内氧化系统与还原系统的动态平衡[13]。细胞被自由基攻击,细胞壁破裂、细胞膜磷脂降解形成最终裂解产物MDA,间接反映自由基的生成量和对组织的氧化程度。T-AOC能够反映机体酶及非酶促体系总抗氧化能力水平。在AS早期外膜滋养血管新生阶段,gp91phox和p22phox基因杂交信号阳性表达明显升高,血清SOD、T-AOC活性明显下降、MDA活性上调,表明NADPH氧化酶活性升高促进的外膜氧化应激是诱导管壁微血管新生的重要机制。
桂芍通络胶囊是撷取东汉张仲景调和营卫及历代医家运用通络法治疗血脉病变的用药经验调制的经验方,以桂枝与白芍为基础,一通卫阳,一理营阴,合以薤白疏畅营卫气机运行以防络气郁滞,以达营卫畅达,气血流行;辅以丹参、姜黄活血通络,剔除络中淤血。桂芍通络能够明显减少VEGF、VEGFR-2蛋白表达,有效下调gp91phox和p22phox基因杂交信号在外膜的表达,上调血清SOD、T-AOC活性,减少MDA表达;与阿托伐他汀组和通心络组的差异无统计学意义(P>0.05),表明“调和营卫方”桂芍通络一定程度上能够通过抑制外膜氧化应激水平,提高血管系统和外膜局部的抗氧化能力,而抑制管壁血管新生,延缓AS病变进程。
(致谢:本实验于河北省络病重点实验室完成,衷心感谢河北以岭医药研究院药理室王宏涛博士、张军方博士、张会欣博士、刘克剑博士、刘焕、单星阁、崔雯雯、郭佳禄、刘文正等其他成员在实验过程中给予的热情帮助。)
| [1] | Heistad D D, Marcus M L, Larsen G E, et al.Role of vasa vasorum in nourishment of the aortic wall[J].Am J Physiol, 1981, 241(5):H781-7. |
| [2] | Gössl M, Herrmann J, Tang H, et al.Prevention of vasa vasorum neovascularization attenuates early neointima formation in experimental hypercholesterolemia[J].Basic Res Cardiol, 2009, 104(6):695-706. |
| [3] | 谢莲娜, 曾定尹, 张海山, 等.硅胶管包裹大鼠颈动脉对血管收缩功能的影响[J].中国医科大学学报, 2010, 39(9):698-702. Xie L N, Zeng D Y, Zhang H S, et al.Effect of the collar-induced adventitia injury on vasoconstriction of rat carotid artery[J].J China Med Univ, 2010, 39(9):698-702. |
| [4] | 肖维刚, 张秋艳, 郎艳松, 等.通心络对高脂血症兔甲襞微循环血流速度的影响[J].微循环杂志, 2013, 23(4):8-11. Xiao W G, Zhang Q Y, Lang Y S, et al.Effects of Tongxinluo on nail fold microcirculation in hyperlipemia rabbit[J].Chin J Microcircul, 2013, 24(4):8-11. |
| [5] | 杨琼, 唐志晗, 武春燕, 等.异常剪切应力促兔总颈动脉粥样硬化模型的建立[J].中南医学科学杂志, 2011, 39(3):258-61. Yang Q, Tang Z H, Wu C Y, et al.Establishment of new zealand rabbits carotid atherosclerosis model induced by abnormal shear stress[J].J Med Sci Cent S China, 2011, 39(3):258-61. |
| [6] | 肖维刚.动脉管壁"孙络-微血管"滋生在动脉粥样硬化早期病变中的作用及通络药物干预研究[D].河北医科大学, 2014. Xiao W G.The role of vasa vasorum angiogenesis in early atherosclerosis and intervention studies with tongxinluo[D].Hebei Medical University, 2014. |
| [7] | 郎艳松, 秘红英, 刘红利, 等.通心络联合阿托伐他汀、阿司匹林对家兔动脉粥样硬化早期血管外膜滋养血管新生的干预作用[J].中国药理学通报, 2015, 31(1):71-6. Lang Y S, Mi H Y, Liu H L, et al.Interventional effects of tongxinluo combined with atorvastatin and aspirin (ATS) on the angiogenesis of vasa vasorum in the early stage of atherosclerosis [J].Chin Pharmacol Bull, 2015, 31(1):71-6. |
| [8] | Gössl M, Zamir M, Ritman E L.Vasa vasorum growth in the coronary arteries of newborn pigs[J].Anat Embryol, 2004, 208(5):351-7. |
| [9] | Ushio-Fukai M, Tang Y, Fukai T, et al.Novel role of gp91phox-containing NAD(P)H oxidase in vascular endothelial growth factor-induced signaling and angiogenesis[J].Cir Res, 2002, 91(12):1160-7. |
| [10] | Krause K H, Lambeth D, Krnke M.NOX enzymes as drug targets[J].Cell Mol Life Sci, 2012, 69(14):2279-82. |
| [11] | Vignais P.The superoxide-generating NADPH oxidase:structural aspects and activation mechanism[J].Cell Mol Life Sci, 2002, 59(9):1428-59. |
| [12] | Coso S, Harrison I, Harrison C B, et al.NADPH oxidases as regulators of tumor angiogenesis:current and emerging concepts[J].Antioxid Redox Signal, 2012, 16(11):1229-47. |
| [13] | Ye N, Liu S, Lin Y, et al.Protective effects of intraperitoneal injection of TAT-SOD against focal cerebral ischemia/reperfusion injury in rats[J].Life Sci, 2011, 89(23-24):868-74. |

