


糖尿病肾病(diabetic nephropathy,DN)是一种巨噬细胞激活介导的慢性炎症性疾病[1, 2]。在糖尿病的高糖环境中,体内游离氨基之间发生非酶促糖基化反应,最终生成晚期糖基化终末产物(AGEs)。研究表明,AGEs的聚集增加可诱发巨噬细胞的活化,是导致DN发生发展的重要原因。转化生长因子β激活激酶1(TAK1)是一种丝氨酸/苏氨酸激酶,是细胞丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)和核因子-κB(nuclear factor-kappa B,NF-κB)信号通路上游炎症和免疫信号途径的共同关键调节子[3]。有研究表明,MAPK和NF-κB信号通路是参与巨噬细胞激活的细胞内信号转导途径[4, 5]。但是TAK1是否参与AGEs诱导巨噬细胞活化及其机制研究,目前尚未见报道,本实验以BMMs为研究对象,体外模拟糖尿病肾病病理状态,观察TAK1抑制剂对BMMs中相关信号通路蛋白及炎症因子的影响,探讨TAK1信号通路在AGEs诱导巨噬细胞激活中的具体机制。
1 材料与方法 1.1 实验动物清洁级♂ C57BLKS/J小鼠24只,同窝清洁级♂野生对照小鼠12只,6~8周龄,体质量30~40 g,南京大学动物模式中心,动物合格证号:SCKX(苏)2010-0001。
1.2 药品与试剂AGEs、牛血清白蛋白(BSA)(北京博奥森生物技术公司),胎牛血清(FBS),RPMI 1640(加拿大WISENT公司),小鼠成纤维细胞L929(中科院上海细胞库),5Z-7-oxozeaenol(美国EMD Billerica公司),抗鼠F4/80抗体,抗鼠/人CD11b抗体,抗鼠CD11c抗体(美国Bio Legend公司),TRIzol试剂(美国Life Technology公司),荧光定量试剂盒(美国Bio-Rad公司),RT-PCR引物(上海,生工),兔抗p-TAK1多克隆抗体、兔抗TAK1多克隆抗体、兔抗TAB1多克隆抗体、鼠抗ED-1单克隆抗体(美国Abcam公司)、小鼠抗p-p38MAPK单克隆抗体、兔抗p38MAPK多克隆抗体、兔抗NF-κB p65多克隆抗体(美国Cell Signaling公司)、兔抗MCP-1多克隆抗体、兔抗TNF-α多克隆抗体、小鼠抗β-actin单克隆抗体、辣根酶标记羊抗兔IgG、辣根酶标记羊抗小鼠IgG(武汉三鹰生物技术公司)
2 方法 2.1 骨髓来源巨噬细胞提取C57小鼠麻醉后颈椎脱臼处死,分离并剪断股骨及胫骨的两端,用含2%FBS的冷PBS冲洗出骨髓,过筛离心后加入红细胞裂解液,冰上孵育10min;再以4℃离心5 min;弃上清,使用RPMI 1640培养基+15%L929上清+10%FBS+双抗培养基重悬细胞后计数,细胞浓度调整至1×109 cells·L-1接种到6孔板,于5% CO2,37℃孵箱中培养。7 d后,0.25%胰酶消化并收集非贴壁细胞。
2.2 流式细胞术分析BMMs纯度无血清培养基同步化BMMs 24 h,200 mg·L-1 AGEs刺激24 h后收集[6],经离心洗涤,加入抗小鼠CD16/32Fcγ受体20min阻断细胞膜上Fc受体;再加入FITC标记的F4/80抗体,APC标记的CD11b和PE标记的CD11c,避光室温孵育30 min,离心洗涤2次,重悬于500 μL PBS中,使用美国BD FACS Calibur流式细胞仪分别检测F4/80、CD11b和CD11c阳性细胞百分比。
2.3 抑制剂对巨噬细胞活力影响按照CCK-8(cell counting kit)细胞毒性试剂盒说明书进行,取BBMs对数期生长细胞(每孔1×104)接种于96孔板,同步化培育24 h,分别加入不同浓度(10~1 000 nmol·L-1)的TAK1抑制剂或DMSO(对照组),37℃孵育1 h后,AGEs干预24 h;每孔加入10 μL CCK-8溶液,孵育4 h;用酶标仪测490 nm处各孔吸光度,重复3次,计算平均细胞活力。
2.4 实时荧光定量PCR检测各组巨噬细胞的MCP-1及TNF-α mRNA的表达选TAK1抑制剂浓度30、100及300 nmol·L-1,作用于AGEs刺激的BBMs,分别加入1 mL TRIzol试剂,提取总RNA,进行RNA纯度和浓度鉴定,使OD260/OD280在1.8~ 2.0之间;将RNA通过反转录系统A3500逆转录成cDNA,采用SYBR Green PCR试剂盒进行PCR测定。GAPDH:上游序列5′- GGTGAAGGTCG GTGTGAACG-3′,下游序列5′-CTCGCTCCTGGAAGATGGTG-3′;TNF-α:上游序列5′-GCTGAGCTCAAACCCTGGTA-3′,下游序列5′-CGGACTCCG CAAAGTCTAAG-3′;MCP-1:上游序列5′-TTGACCCGTAAATCTGAAG CTAAT-3′,下游序列5′-TCACAGTCCGAGTCACACTAGTTCAC-3′。每个样本设3个复孔,取均值,获得平均Ct值,以GAPDH作为内参照校正,用2-△△Ct法分析基因的相对表达。
2.5 巨噬细胞实验分组通过预实验摸索最佳抑制剂浓度为300 nmol·L-1,及各组蛋白表达最佳时间点。细胞培养至70%~80%融合时,同步化24 h,进行细胞分组:正常对照组(normal control,NC,RPMI 1640培养基);BSA组(200 mg·L-1BSA,BSA);AGEs组(200 mg·L-1 AGEs,AGEs);AGEs+OZ组(200 mg·L-1 AGEs+OZ300)。
2.6 激光共聚焦显微镜分析将BMMs以1×105/孔的密度接种在玻璃皿底,4%多聚甲醛4℃下固定10 min,5%驴血清白蛋白阻断2 h,加入抗iNOS抗体4℃孵育过夜。PBST洗3次后,加入Alexa Fluor 647标记的F4/80和FITC标记的二抗避光孵育2 h,DAPI染核,漂洗封片后,在德国Leica TCS SP5激光共聚焦显微镜下观察采像。
2.7 Western blot检测各组的蛋白表达AGEs刺激同步化后的巨噬细胞,相应的时间点收集蛋白;并将蛋白电转移至NC膜,使用丽春红染色判断有无条带,将NC膜取出并置于TBST配制的5%脱脂奶粉于37℃封闭2 h;加入p-TAK1抗体(1 :1 000)、TAK1(1 :1 000)、TAB1(1 :1 000)、pJNK(1 :1 000)、JNK(1 :2 000)、p-p38MAPK(1 :1 000)、p38MAPK(1 :2 000)、NF-κBp65(1 :1 000)、β-actin抗体(1 :2 000)、4℃过夜;洗膜后加入用TBST稀释的辣根酶过氧化物标记的羊抗兔IgG(1 :2 000),37℃孵育45 min;洗膜3次后使用ECL反应30 s,在Tanon 4500SF成像系统中显影。用Tanon公司LabWorks 4.5软件对Western blot条带进行半定量分析。以β-actin作为内参照,所有的结果至少重复3次。
2.8 统计学分析实验数据用x± s 表示,方差齐性检验用Levene法,统计学处理应用单因素方差分析,组间差异检验采用LSD分析。
3 结果 3.1 骨髓来源巨噬细胞纯度鉴定L929细胞上清液中含巨噬细胞集落刺激因子(M-CSF),加入小鼠骨髓来源干细胞,d 7时,诱导成BMMs,经流式细胞仪检测巨噬细胞表面标记物F4/80和CD11b,双标阳性率达到99.35%(Fig 1)。

|
| Fig 1 Purity detection of bone marrow derived macrophages |
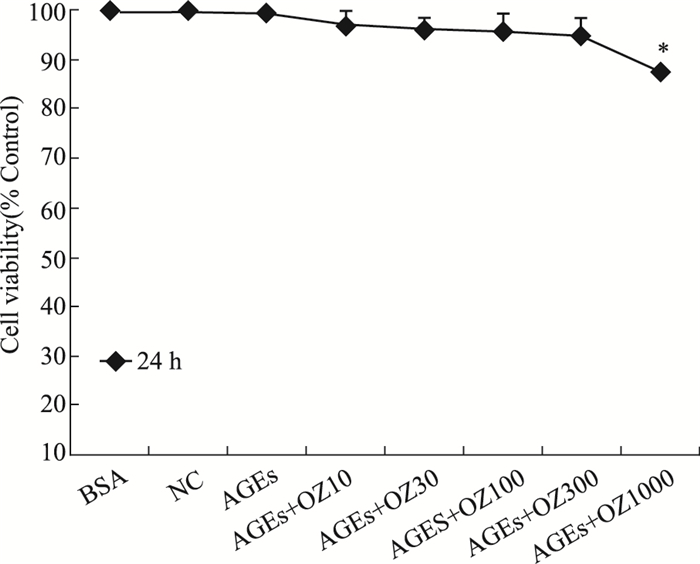
选取10 nmol·L-1到1 000 nmol·L-1之间5种抑制剂浓度,Fig 2表明5Z-7-oxozeaenol浓度在10~300 nmol·L-1对AGEs刺激的BMMs活性无影响(P>0.05),5Z-7-oxozeaenol 1 000 nmol·L-1时对AGEs刺激的BMMs活性有影响(P <0.05)。
|
| Fig 2 Viability analysis of BMMs after treatment with 5Z-7-oxozeaenol (10~1 000 nmol·L-1) in AGEs-induced BMMs *P < 0.05 vs AGEs group (AGEs). |
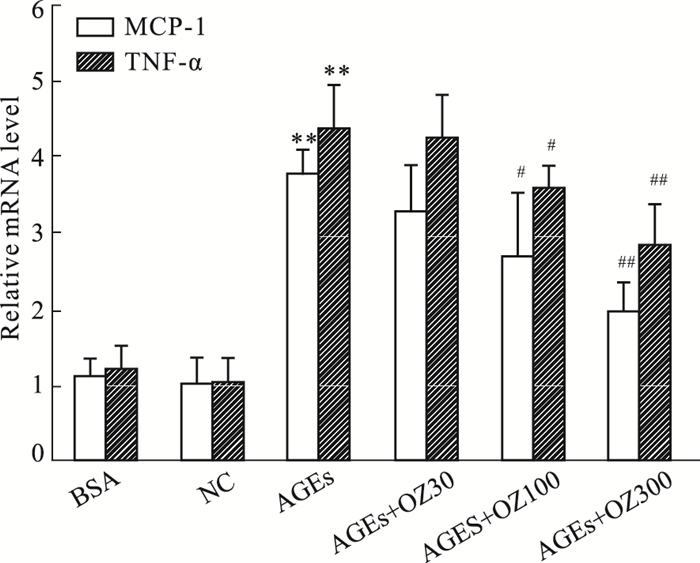
RT-PCR结果显示,与对照组比较,AGEs刺激组BMMs MCP-1和TNF-α的mRNA表达明显上调(P <0.01),这一结果表明AGEs可以增加巨噬细胞炎症因子的产生;随5Z-7-oxozeaenol浓度(30、100、300 nmol·L-1)的升高,MCP-1、TNF-α mRNA表达呈下降趋势,其中300 nmol·L-1的5Z-7-oxozeaenol对炎症因子抑制作用最强(P <0.01),故5Z-7-oxozeaenol可以降低AGEs诱导的BMMs炎症因子的表达,见Fig 3。
|
| Fig 3 Real time PCR analyses effects of OZ on MCP-1 and TNF-α mRNA expression of BMMs under AGEs **P < 0.01 vs normal group (NC);#P < 0.05,##P < 0.01 vs AGEs group (AGEs). |
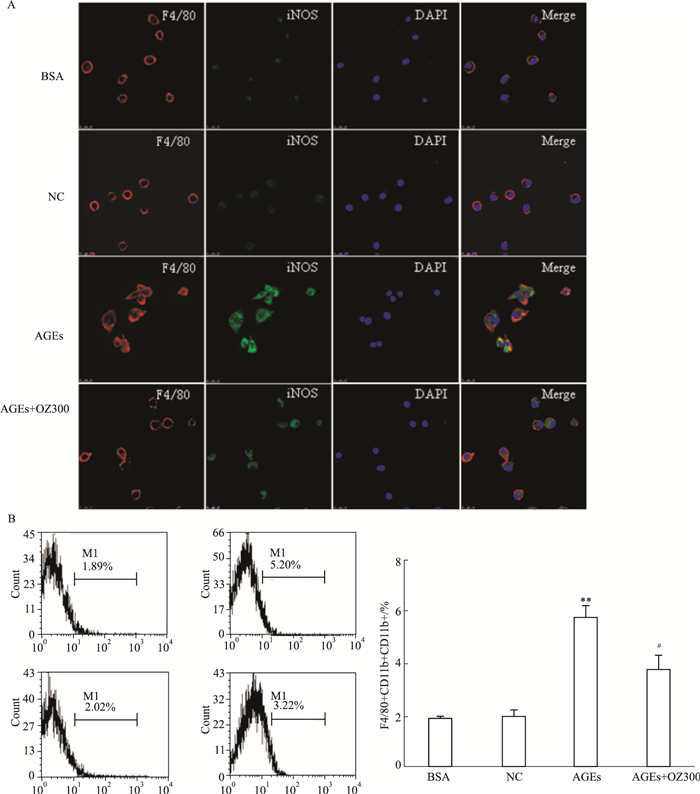
Fig 4A系激光共聚焦显微镜分析结果,提示AGEs组iNOS荧光强度明显高于对照组,AGEs+OZ300组iNOS荧光强度明显减弱;但F4/80在所有组别的BMMs上均表达。流式细胞术显示,AGEs组的F4/80、CD11b和CD11c三标的M1型巨噬细胞百分比较对照组明显升高(P <0.01),说明AGEs刺激可成功诱导BMMs功能表型向M1型活化;AGEs+OZ300组M1型巨噬细胞百分比明显降低(P <0.01),提示5Z-7-oxozeaenol可抑制AGEs对巨噬细胞的活化作用,见Fig 4B。
|
| Fig 4 Effects of 5Z-7-oxozeaenol on macrophage activation in AGEs-induced BMMs A:Effects of 5Z-7-oxozeaenol on expression of the macrophage cytoplasmic markers. The markers were measured by confocal microscopy. Double staining with F4/80 and iNOS. B:Effects of 5Z-7-oxozeaenol on expression of the macrophage surface markers. The markers of F4/80,CD11b,and CD11c was measured by FCM. **P < 0.01 vs normal group (NC);#P < 0.05 vs AGEs group. |
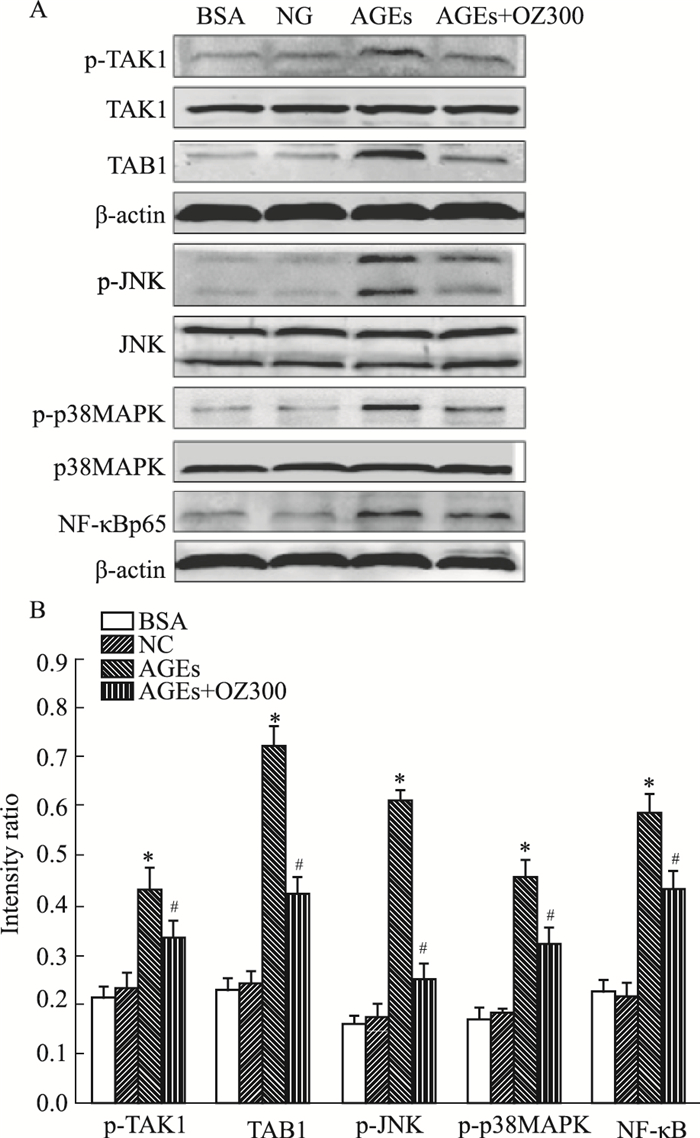
Western blot印迹条带分析显示AGEs组p-TAK1、p-JNK、p-p38MAPK、TAB1和NF-κB p65蛋白表达较对照组增加(P <0.05),5Z-7-oxozeaenol干预可使巨噬细胞上述蛋白表达与AGEs组相比下降(P <0.05),见Fig 5。
|
| Fig 5 Effects of OZ on p-TAK1,TAB1,p-JNK,p-p38MAPK protein in AGEs-induced BMMs analysed by Western blot *P < 0.05 vs normal group (NC);#P < 0.05 vs AGEs group. |
巨噬细胞的活化和浸润是DN炎症反应的特征性表现之一。经典激活型(classically activated,M1型)巨噬细胞是促炎及促纤维化的巨噬细胞表型,在早期炎症反应阶段,浸润的巨噬细胞通过分泌IL-12、IL-23、TNF-α、IL-1β、活性氧(ROS),诱导型一氧化氮合酶(iNOS)及MCP-1等促炎因子引起的肾脏组织结构的损伤和破坏,参与DN间质炎症反应及肾小球纤维化的发生[7]。糖尿病环境下生成的AGEs可以通过与细胞表面特异性受体结合,激活氧化应激及MAPK、NF-κB等信号传导途径,诱导细胞因子的表达及细胞外基质的聚集,导致肾小球纤维化、炎性细胞浸润和蛋白尿产生[8, 9, 10]。故巨噬细胞的活化和AGEs的聚集与DN发生发展有着密切的关系。本实验采用AEGs孵育巨噬细胞24 h,模拟体外糖尿病肾病炎症状态。F4/80、CD11b表示巨噬细胞的成熟度,iNOS和CD11c在活化的巨噬细胞中高表达,可作为M1型巨噬细胞表面标志[11]。激光共聚焦显示AGEs组上述M1型巨噬细胞表面标志的百分比明显高于对照组,说明AGEs刺激可成功诱导BMMs向M1型巨噬细胞分化。作为免疫反应的主要效应细胞,M1型巨噬细胞产生多种炎性细胞因子,如TNF-α和IL-1β,TNF-α具有介导生长、炎症、免疫调节等多方面生物学效应[12]。最近的一项研究显示,在单核/巨噬细胞中,AGEs通过上调mRNA水平并释放促炎细胞因子IL-1β和TNF-α,进而诱导人单核细胞表达单核细胞趋化因子-1(monocyte chemoattractant protein-1,MCP-1),它对单核巨噬细胞具有很强的趋化激活作用[12, 13, 14]。前期预实验结果显示,10、30、100及300 nmol·L-1的5Z-7-oxozeaenol对AGEs刺激的BMMs活性无影响,在安全剂量范围内选用30、100及300 nmol·L-1 3种浓度作用于AGEs刺激的BMMs,RT-PCR法检测炎症因子TNF-α、MCP-1的表达,较AGEs组均有降低(P <0.05),其中300 nmol·L-1时的炎症因子的表达最弱(P <0.01),故后期的实验分组中5Z-7-oxozeaeno的浓度选为300 nmol·L-1,而AGEs+OZ300组M1型巨噬细胞表面标志较AGEs组明显降低(P <0.01),提示5Z-7-oxozeaenol可抑制AGEs刺激的巨噬细胞的活化及TNF-α和MCP-1的产生,但具体的分子机制尚不清楚。
TAKl为苏氨酸/丝氨酸蛋白激酶,在序列与功能上属于丝裂原激活蛋白激酶家族成员。TAK1作为调节多种促炎因子信号转导通路,在促炎因子,如TNF-α、IL-1β、TGF-β、Toll样受体(TLR)配体的参与下,首先通过激活MAP2Ks家族的MEK3/6和MEK4/7,然后MEK3/6和MEK4/7信号分别激活MAPK家族的应激活化激酶(JNK)、p38MAPK激酶进而激活转录因子激活蛋白1(AP-1)[15]。TAK1又可以通过与结合蛋白TAB1的共表达而被激活,磷酸化修饰被认为是TAK1依赖的信号转导过程中重要调节机制[16]。NF-κB是转录因子家族中的成员,被AGEs产生的ROS激活,与靶基因上特定的DNA序列结合并调节基因转录,产生和释放各种细胞因子,如MCP-1及TNF-α等,后者可进一步增加ROS的产生,二者形成级联反应,构成恶性循环,导致NF-κB活性持续升高[17, 18]。Hofmann等[19]的研究发现,DN患者外周血单个核细胞NF-κB的活性较DM患者明显增强,并与蛋白尿程度相关,表明NF-κB活性与DN的发生及其程度密切相关。在UUO致肾小管间质纤维化小鼠模型中,JNK、p38MAPK、NF-κB信号通路在肾脏组织被激活以及下游的炎症因子IL-1α、TNF-α、NOS2和CCL2mRNA表达增加,同时巨噬细胞浸润明显增加。利用基因敲除技术使UUO小鼠模型TAK1基因敲除,结果JNK、p38MAPK、NF-κB信号通路被抑制,炎症因子的释放减少以及巨噬细胞的浸润明显降低[8]。体内研究表明,TAK1抑制剂可以阻止损伤导致的TAK1和NF-κBp65的磷酸化[20],TAK1基因敲出小鼠细胞的TNFR1、IL-1R和TLR3通路功能缺陷,下游信号NF-κB、JNK和IKKβ不能被激活[21]。因此,TAK1基因在调节JNK、p38MAPK和NF-κB通路及其下游炎症因子的表达上发挥重要作用。本实验通过Western blot法探讨TAK1抑制剂对BMMs中TAK1、MAPK和NF-κB信号通路的影响,与对照组相比较,AGEs组的p-TAK1、TAB1表达明显升高,同时JNK、p38MAPK及NF-κB的磷酸化水平均增加,给予300 nmol·L-1 TAK1抑制剂治疗后,上述信号通路蛋白的表达均降低,说明TAK1通过磷酸化介导在调节MAPK及NF-κB信号通路中发挥至关重要的作用。
综上所述,本研究模拟体外糖尿病病理环境,AGEs可以激活巨噬细胞中TAK1、MAPK及NF-κB信号通路,初步证实TAK1抑制剂可以干预巨噬细胞MAPK及NF-κB信号转导通路的活化以及炎症因子TNF-α、MCP-1的表达,从而抑制糖尿病炎症反应,且为临床上控制糖尿病炎症的激活提供理论基础。但是TAK1、MAPK及NF-κB信号通路之间是否存在相互作用,以及肾脏巨噬细胞分离进一步验证TAK1在糖尿病肾病中的作用机制需要进一步的探讨。
| [1] | Chow F Y, Nikolic-Paterson D J, Atkins R C, et al.Macrophages in streptozotocin-induced diabetic nephropathy:potential role in renal fibrosis[J].Nephrol Dial Transplant, 2004, 19(12):2987-96. |
| [2] | Fang Q, Zhao L, Wang Y, et al.A novel chalcone derivative attenuates the diabetes-induced renal injury via inhibition of high glucose-mediated inflammatory response and macrophage infiltration [J].Toxicol Appl Pharmacol, 2015, 282(2):129-38. |
| [3] | Chow F Y, Nikolic-Paterson D J, Ozols E, et al.Monocyte chemoattractant protein-1 promotes the development of diabetic renal injury in streptozotocin-treated mice [J].Kidney Int, 2006, 69(1):73-80. |
| [4] | Banba N, Nakamura T, Matsumura M, et al.Possible relationship of monocyte chemoattractant protein-1 with diabetic nephropathy [J].Kidney Int, 2000, 58(2):684-90. |
| [5] | Wang Q Y, Chen F Q.Clinical significance and different levels of urinary monocyte chemoattractant protein-1 in type 2 diabetes mellitus[J].Diabetes Res Clin Pract, 2009, 83(2):215-9. |
| [6] | Qin Q, Niu J, Wang Z, et al.Astragalus membranaceus inhibits inflammation via phospho-P38 mitogen-activated protein kinase (MAPK) and nuclear factor (NF)-κB pathways in advanced glycation end product-stimulated macrophages[J].Int J Mol Sci, 2012, 13(7):8379-87. |
| [7] | 罗邦雨, 熊俊.巨噬细胞在肾脏纤维化中的调节作用[J].中华肾脏病杂志, 2012, 28(8):657-60.Luo B J, Xiong J.Regulation of macrophages in renal fibrosis[J].Chin J Kidney Dis, 2012, [HTH]28(8):657-60 |
| [8] | Ma F Y, Tesch G H, Ozols E, et al.TGF-β1-activated kinase-1 regulates inflammation and fibrosis in the obstructed kidney[J].Am J Physiol Renal Physiol, 2011, 300(6):1410-21. |
| [9] | Ma F Y, Liu J, Nikolic-Paterson D J.The role of stress-activated protein kinase signaling in renal pathophysiology[J].Braz J Med Biol Res, 2009, 42(1):29-37. |
| [10] | Mezzano S, Aros C, Droguett A, et al.NF-kappaB activation and overexpression of regulated genes in human diabetic nephropathy[J].Nephrol Dial Transplant, 2004, 19(10):2505-12. |
| [11] | Ying W, Cheruku P S, Bazer F W, et al.Investigation of macrophage polarization using bone marrow derived macrophages[J].J Vis Exp, 2013, (76):e50323. |
| [12] | Hickey F B, Martin F.Diabetic kidney disease and immune modulation[J].Curr Opin Pharmacol, 2013, 13(4):602-12. |
| [13] | Sugimoto K, Yasujima M, Yagihashi S.Role of Advanced Glycation End Products in Diabetic Neuropathy [J].Curr Pharm Des, 2008, 14(10):953-61. |
| [14] | Labonte A C, Tosello-Trampont A C, Hahn Y S.The role of macrophage polarization in infectious and inflammatory diseases[J].Mol Cells, 2014, 37(4):275-85. |
| [15] | Ajibade A A, Wang H Y, Wang R F.Cell type-specific function of TAK1 in innate immune signaling[J].Trends in Immunol, 2013, 34(7):307-16. |
| [16] | Sakurai H.Targeting of TAK1 in inflammatory disorders and cancer[J].Trends Pharmacol Sci, 2012, 33(10):522-30. |
| [17] | Chen L, Zhang J, Zhang Y, et al.Improvement of inflammatory responses associated with NF-kappa B pathway in kidneys from diabetic rats[J].Inflammation Res, 2008, 57(5):199-204. |
| [18] | Nam J S, Cho M H, Lee G T, et al.The activation of NF-kappaB and AP-1 in peripheral blood mononuclear cells isolated from patients with diabetic nephropathy[J].Diabetes Res Clin Pract, 2008, 81(1):25-32. |
| [19] | Hofmann M A, Schiekofer S, Isermann B, et al.Peripheral blood mononuclear cells isolated from patients with diabetic nephropathy show increased activation of the oxidative-stress sensitive transcription factor NF-kappaB[J].Diabetologia, 1999, 42(2):222-32. |
| [20] | Song Z, Zhu X, Jin R, et al.Roles of the kinase TAK1 in CD40-mediated effects on vascular oxidative stress and neointima formation after vascular injury[J].PLoS One, 2014, 9(7):e101671. |
| [21] | Shim J H, Xiao C, Paschal A E, et al.TAK1, but not TAB1 or TAB2, plays an essential role in multiple signaling pathways in vivo[J].Genes Devel, 2005, 19(22):2668-81. |
