


2. 天津市第三中心医院, 天津 300170;
3. 天津市职业与环境危害生物标志物重点实验室, 天津 300309
2. Dept of Gastroenterology and Hepatology, Tianjin Third Central Hospitaln, Tianjin 300170, China;
3. Tianjin Key Laboratory for Biomarkers of Occupational and Environmental Hazard, Tianjin 300309, China
原发性肝癌(简称肝癌)是临床中最常见的恶性肿瘤之一。蟾酥为宝贵的中药之一,已被作为药物使用近千年,《本草纲目》记载“蟾酥,疗疳积,消臌胀,解疔毒之药也”。而华蟾毒配基(cinobufagin)是中药蟾酥的主要抗癌活性成分之一,目前是我国临床治疗中晚期肝癌的首选中药制剂,药物作用靶点为细胞膜表面钠钾ATP酶(Na+,K+-ATPase)[1]。研究证实非小细胞肺癌、神经胶质瘤、肝细胞癌和乳腺癌等肿瘤细胞中钠钾ATP酶呈现高表达状态,参与调控肿瘤细胞的发生和发展[2, 3]。前期的研究显示华蟾毒配基可下调肝癌细胞周期蛋白 A(cyclin A)表达引发细胞周期S期阻滞现象[4, 5]。然而蟾酥制剂在治疗肝癌中的作用机制仍然不明确。因此,研究华蟾毒配基抑制肝癌细胞生长,探讨其作用机制,意义重大。
1 材料与方法 1.1 材料与试剂人肝癌细胞株HepG2购自协和基础医学院细胞库,华蟾毒配基为Sigma公司产品,无水乙醇溶解成母液,浓度为1 mmol·L-1,-20 ℃避光保存;H-DMEM培养基,胎牛血清购自Gibco公司。TRIzol为Invitrogen公司产品;四甲基偶氮唑盐(MTT)、碘化丙啶(PI)和二甲基亚砜(DMSO)购自于Sigma公司;PrimeScriptTM RT逆转录试剂购自于TaKaRa公司;SYBR Green Ⅰ染料为Roche公司产品,一抗兔抗人Mre11、Nbs1、Rad50和p53单克隆抗体购自Abcam公司,二抗和ECL化学发光试剂购自KPL公司。
1.2 免疫组化检测肝癌组织与肝癌旁组织中钠钾ATP酶α1亚单位表达90例肝癌与癌旁组织样本,年龄(49.8±8.8),均为原发性肝癌肿瘤。常规处理,石蜡包埋切片,高压蒸汽抗原修复,3% H2O2室温孵育30 min;兔血清封闭10 min,Na+,K+-ATPase α1羊单克隆抗体,4℃孵育过夜,二抗室温孵育30 min,3,3-二氨基联苯胺(DAB)显色5 min,冲洗,乙醇脱水,二甲苯透明,中性树脂封片,每张切片随机选取3个视野LeicaBM2500拍照,图像数据由Image-Pro Plus 6.0软件分析,测量阳性结果区域面积和积分光密度值,计算样本的平均光密度值,分析肝癌与癌旁组织中Na+,K+-ATPase α1亚单位表达水平。
1.3 单细胞电泳检测DNA双链断裂程度实验分组同前,第1层胶制作:取0.5 %常温熔点琼脂糖溶液熔化后包被载玻片,冷却充分凝固。第2层胶制作:100 μL 0.5 %低熔点琼脂糖溶液中混合500个细胞,均匀滴在第1层胶上,充分冷却。玻片浸入预冷裂解液 [10 mmol·L-1 Tris-HCl(pH 7.5)2.5 mol·L-1 NaC1,100 mmol · L-1 四甲基乙二胺四乙酸二钠,1 %Triton X-100和10 %二甲基亚砜],4 ℃,2 h。置于水平电泳槽中,加入电泳液(1 mmol·L-1 四甲基乙二胺,300 mmol·L-1 氢氧化钠),静置20 min,25 V电泳30 min。25 g·L-1碘化丙啶(PI)75 μL 染色,荧光显微镜下观察结果。采用CASP1.2软件分别计算彗星头部和尾部积分面积(Head Area和Tail Area)与荧光强度(Head DNA and Tail DNA Amount),计算各自荧光密度值,同时检测彗星尾部迁移长度(Tail Moment)。通过分析彗星头部光密度值和彗星尾部长度与荧光密度值评估DNA损伤。
1.4 RNA提取和Real time-PCR检测Mre11、Nbs1、Rad50和p53 mRNA表达实验分组同前,TRIzol法提取细胞总RNA,按PrimeScriptTM RT试剂反转录合成cDNA。反应体系为20 μL (上、下游引物各 1 μL,模板1 μL,SYBR green 试剂 4 μL,ddH2O 12 μL)。引物序列见Tab 1,反应条件:95 ℃ 变性10 min:95 ℃变性5 s,65 ℃退火15 s,72 ℃延伸15 s,共40个循环。通过相对定量法(2-△△Ct)分析实验组目的基因表达丰度。
| Gene | Sequences of PCR primers | Amplication length(bp) | |
| Mre11 | Sense | 5′-GCCTTCCCGAAATGTCACTA-3′ | 172 |
| Antisense | 5′-TTCAAAATCAACCCCTTTCG-3′ | ||
| Nbs1 | Sense | 5′-AGAATGGCTTTTCCCGAACT-3′ | 106 |
| Antisense | 5′-CAAGAAGAGCATGCAACCAA-3′ | ||
| Rad50 | Sense | 5′-CTTGGATATGCGAGGACGAT-3′ | 215 |
| Antisense | 5′-CCAGAAGCTGGAAGTTACGC-3′ | ||
| p53 | Sense | 5′-CCGCAGTCAGATCCTAGCG-3′ | 118 |
| Antisense | 5′-AATCATCCATTGCTTGGGACG-3′ | ||
| GAPDH | Sense | 5′-AATGTCACCGTTGTCCAGTTG-3′ | 94 |
| Antisense | 5′-GTGGCTGGGGCTCTACTTC-3′ |
实验分组同前,蛋白印迹实验参考以前方法[6],每组60 μg蛋白通过10% SDS-PAGE分离,Bio-rad半干转印系统转膜,经抗体孵育,经ECL液化学发光,暗室X线曝光、显影、定影。Bandscan 5.0软件进行灰度值分析。
1.6 流式细胞术检测细胞周期接种1×105个HepG2细胞,培养24 h后加药,实验分组同前,药物作用6、12和24 h后,收集细胞,75 % 冷乙醇固定,PBS洗1次,加入终浓度为50 mg· L-1 RNA酶和5 g·L-1 碘化乙啶(PI)溶液,孵育20 min,流式细胞仪检测细胞周期变化。
1.7 统计学处理数据采用 x±s表示,SPSS14.0软件进行分析处理。两组数据间比较采用t检验,多组间数据采用方差分析。
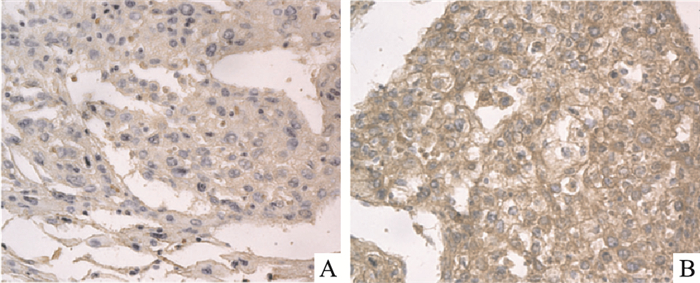
2 结果 2.1 人肝癌组织与正常肝组织钠钾ATP酶α1亚单位的差异化表达通过IPP6.0软件分析肝癌与癌旁组织中钠钾ATP酶α1亚单位表达的平均光密度。Fig 1显示,肝癌组织钠钾ATP酶α1亚单位密度值为184.74 ± 17.22,癌旁组织为67.21 ± 8.41,肝癌组织中钠钾ATP酶α1亚单位与正常肝脏癌旁组织相比呈现高表达状态,差异有统计学意义(P<0.05)。
|
|
Fig 1
Expression level of Na+,K+-ATPase α1
subunit in normal liver tissues and hepatoma tissue by|
Immunohistochemistry(×400)
A: Adjacent to hepatocellular carcinoma liver tissue( |
5 μmol·L-1 华蟾毒配基可引起HepG2细胞DNA损伤(Fig 2)。药物组细胞电泳后可见彗星状拖尾,对照组呈现明亮的圆点无拖尾,经CASP 1.2软件分析测量对照组彗星头部荧光强度为84.21±9.76,尾部荧光强度4.87±0.58,彗星无拖尾迁移现象发生;药物作用6、12和24h后,头部荧光强度分别为43.2±5.32、38.46±5.74、18.52±3.21,尾部荧光强度分别为23.2±3.12、31.46±4.64、38.52±6.21;彗星尾部长度依次为(26.21±2.47)、(28.42±3.14)、(31.22±5.31) μm,差异具有统计学意义(P<0.05)。研究证实,5 μmol·L-1华蟾毒配基可诱发HepG2细胞DNA双链断裂。

|
| Fig 2 Levels of DNA double-strand breaks in HepG2 cells treated with 5 μmol·L-1 cinobufagin for different time by SCGE(×400) A: 0 h;B: 6 h;C: 12 h;D: 24 h. |
通过相对定量法(2-△△Ct)计算各实验组HepG2细胞的相关基因表达(Tab 2),5 μmol·L-1华蟾毒配基作用HepG2细胞6、12和24 h 3个检测点中,Mre11基因水平分别是对照组的1.29、2.53和7.67倍;Nbs1基因水平分别是对照组的1.16、1.34和1.72倍;Rad50基因水平分别是对照组的1.49、2.97和3.71倍;p53基因水平分别是对照组1.37、3.58和5.94倍。结果显示,5 μmol·L-1华蟾毒配基可明显上调DNA损伤感应相关基因Mre11、Rad50、Nbs1和p53 mRNA表达(P<0.05)。
| (x±s) | |||
| Gene | Relative amount(2 -△△Ct) | ||
| Expose time/h | |||
| 6 | 12 | 24 | |
| Mre11 | 0.37±0.21 * | 1.34±0.37 * | 2.94±0.34 ** |
| Nbs1 | 0.22±0.12 | 0.42±0.14 ** | 0.78±0.27 ** |
| Rad50 | 0.58±0.23 | 1.57±0.31 ** | 1.89±0.42 ** |
| p53 | 0.45±0.32 * | 1.84±0.37 ** | 2.57±0.49 ** |
| *P<0.05;**P<0.01 vs control group | |||
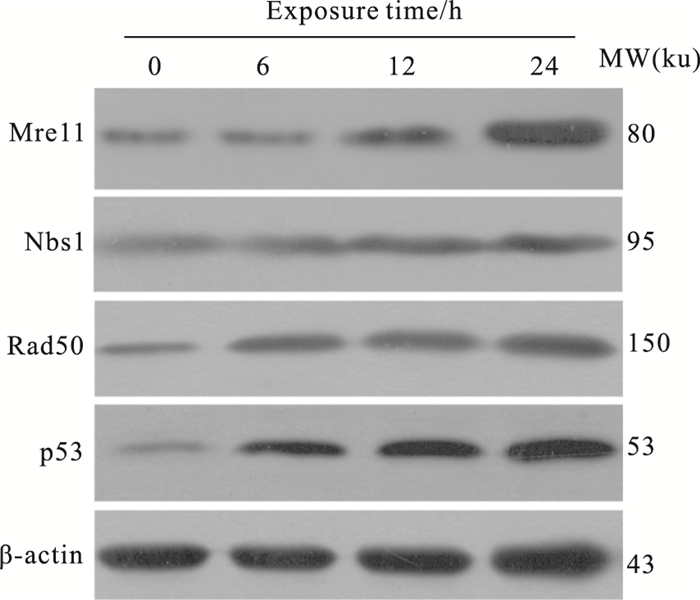
Western blot 结果显示(Fig 3),与对照组细胞相比,5 μmol·L-1华蟾毒配基作用HepG2细胞后,可上调DNA损伤感应基因Mre11、Nbs1、Rad50和p53 蛋白表达,差异有统计学意义(P<0.05),以作用24 h处理组差异更为明显(P<0.01)。
|
| Fig 3 Mre11, Nbs1, Rad50 and p53 protein levels in HepG2 treated with 5 μmol·L-1 cinobufagin for different time by Western blot |
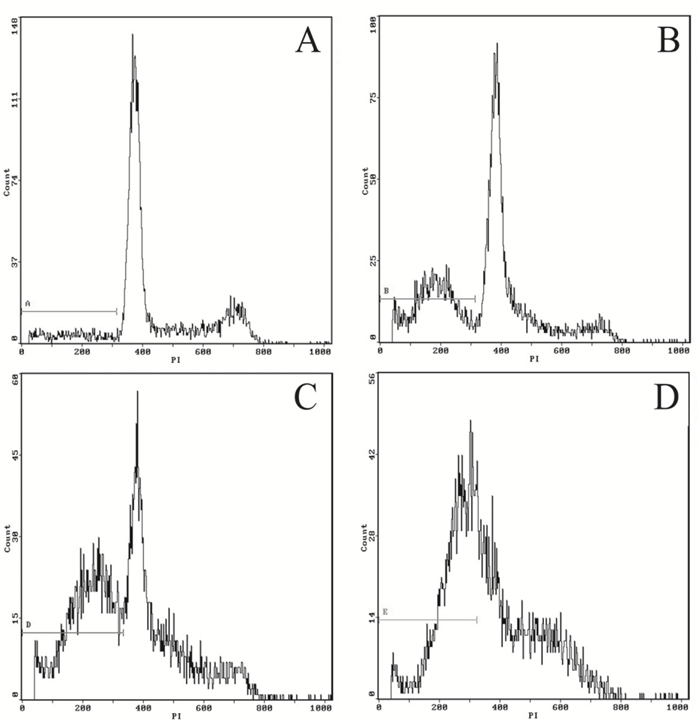
Fig 4所示,流式细胞术分析细胞周期对照组S期细胞比例为(21.32 ± 4.21)%,5 μmol·L-1华蟾毒配基处理6 h后为(33.25 ± 5.72)%,处理12 h后为(56.72 ± 6.29)%,作用24 h后为(67.32 ± 9.42)%,结果显示5 μmol·L-1华蟾毒配基引起HepG2细胞发生S期阻滞现象,差异具有统计学意义(P<0.05)。
|
| Fig 4 Effect of cell cycle on HepG2 cells treated with 5 μmol·L-1 cinobufogenin for different time by flow cytometry A: 0 h;B: 6 h;C: 12 h;D: 24 h |
蟾酥及相关制剂作为抗肿瘤中药在我国广泛用于肝癌、结肠癌、乳腺癌和胃癌等恶性肿瘤的中晚期治疗,疗效显著,蟾酥的主要抗癌有效成分为蟾毒配基类,如华蟾毒配基(cinobufagin)和蟾蜍灵(bufalin)等,属于强心甾类固醇(cardiotonic steroids,CTS)。以华蟾素(混合制剂)为代表的药物在市场中占有重要份额,国际上关于CTS抗癌作用研究取得重要进展,比利时从非洲植物大牛角瓜中提取的CTS经半合成得到的新型钠钾ATP酶抑制剂UNBS1450,作为高活性抗癌药进入欧洲临床,显示了巨大潜力[7, 8, 9] 。
研究显示[1, 2, 3],钠钾ATP酶α1亚单位在正常组织和肿瘤组织呈现出差异化表达,在人前列腺癌PC-3、DU-145细胞系,非小细胞肺癌A549细胞系,神经胶质瘤Hs683、U373-MG、U87-MG和T98G细胞系中钠钾ATP酶α1亚单位都呈现出高表达状态,课题组研究发现在肝癌组织中钠钾ATP酶α1亚单位亦呈现高表达状态,我们前期应用哇巴因与华蟾毒配基作用肝癌细胞后,细胞内游离Ca2+和氧自由基(reactive oxygen species,ROS)浓度增加,损伤细胞DNA,以Cyclin D1为代表的细胞周期调控蛋白生成减少和细胞周期抑制因子p21CIP1引起细胞周期S期阻滞。华蟾毒配基可抑制钠钾ATP酶活性,继发性引起细胞内K+ 浓度减少,同时伴随Na+浓度增加,从而使细胞膜Na+-Ca2+ 交换器启动,诱发细胞内Ca2+持续性升高,破坏线粒体膜电位,氧自由基浓度升高。这些细胞内离子物质是损伤细胞DNA的主要物质[10, 11, 12]。
由细胞DNA 损伤转变成细胞周期阻滞信号并引起周期阻滞过程,主要有DNA 损伤的识别(感受损伤)和效应蛋白分子变化(效应器蛋白)两个部分构成[13, 14]。本研究发现华蟾毒配基可引起肝癌细胞DNA分子双链断裂,损伤感受蛋白Mre11,Nbs1和Rad50基因和细胞周期负调控因子p53表达上调。而Mre11/Rad50/Nbs1(MRN)复合体能将检测到的DNA损伤的情况传递给效应器蛋白分子ATM激酶,其对DNA双链断裂产生应答反应,可将信息传导到p53 蛋白,p53 激活,半衰期延长,促进p21CIP1表达,p21CIP1与CyclinA/CDK2/PCNA激酶复合体结合,抑制其活性,产生细胞出现S期阻滞现象,争取更多的修复时间,在修复无法完成时细胞走向最终的凋亡途径。
综上所述,以华蟾毒配基为代表的钠钾ATP酶抑制因子可能将成为一类新的抗肝癌候选药物,通过破坏癌细胞离子平衡、能量供应,损伤癌细胞DNA分子,引起细胞周期阻滞,诱导细胞凋亡。
(致谢:本文实验在武警后勤学院中心实验室完成,徐瑞成主任为研究项目国家自然科学基金项目负责人,徐忠伟老师为主要实验操作人员,王凤梅主任负责肝癌与癌旁组织样本实验检测,王聪聪老师完成实验数据统计分析与论文审校工作。)
| [1] | Fernandez-Moncada I, Barros L F.Non-preferential fuelling of the Na(+)/K(+)-ATPase pump [J].Biochem J, 2014, 460(3):353-61. |
| [2] | Magpusao A N, Omolloh G, Johnson J, et al.Cardiac glycoside activities link Na(+)/K(+) ATPase ion-transport to breast cancer cell migration via correlative SAR[J].ACS Chem Biol, 2015, 10(2):561-9. |
| [3] | Mijatovic T, Roland I, Van Quaquebeke E, et al.The α1 subunit of the sodium pump could represent a novel target to combat non-small cell lung cancers [J].J Pathol, 2007, 212(2):170-9. |
| [4] | Lefranc F, Kiss R.The sodium pump α1 subunit as a potential target to combat apoptosis-resistant glioblastomas[J].Neoplasia, 2008, 10(3):198-206. |
| [5] | 高默洁, 徐忠伟, 王凤梅, 等.钠钾泵抑制剂通过调节细胞周期相关蛋白的生成介导肝癌HepG2细胞周期S期阻滞与凋亡[J].中国药理学通报, 2010, 26(4):452-6.Gao M J, Xu Z W, Wang F M, et al.The linkage between cell cycle S phase arrest and apoptosis on human hepatocellular carcinoma HepG2 induced by Na+, K+-ATPase inhibitors via regulating proteins associated with cell cycle[J].Chin Pharmacol Bull, 2010, 26(4):452-6. |
| [6] | 买霞, 徐忠伟, 陈小义, 等.土槿乙酸抑制人卵巢癌SKOV_3细胞增殖并诱导G_2/M期阻滞[J].中国药理学通报, 2012, 28(4):508-12.Mai X, Xu Z W, Chen X Y, et al.Growth inhibition and G2/M phase arrest in human ovarian cancer SKOV3 cells induced by pseudolaric acid B [J].Chin Pharmacol Bull, 2012, 28(4):508-12. |
| [7] | Xu Z W, Wang F M, Gao M J, et al.Targeting the Na+/K+-ATPase α1 subunit of hepatoma HepG2 cell line to induce apoptosis and cell cycle arresting [J].Biol Pharm Bull, 2010, 33(5):743-51. |
| [8] | Mijatovic T, Van Quaquebeke E, Delest B, et al.Cardiotonic steroids on the road to anti-cancer therapy [J].Biochimica Biophysica Acta, 2007, 1776(1):32-57. |
| [9] | Prassas I, Diamandis EP.Novel therapeutic applications of cardiac glycosides [J].Nat Rev Drug Discov, 2008, 7(11):926-35. |
| [10] | 徐瑞成, 王娜, 徐忠伟, 等.哇巴因抑制钠泵β1亚单位和VE-cadherin减弱血管内皮细胞连接功能[J].中国药理学通报, 2008, 25(8):701-5.Xu R C, Wang N, Xu Z W, et al.Ouabain reduces the function of cell junction in vascular endothelial cells through inhibiting the expression of Na+, K+-ATPase β1 subunit and VE-cadherin[J].Chin Pharmacol Bull, 2008, 25(8):701-5. |
| [11] | 徐瑞成, 张敏.哇巴因信号的传递及其对细胞生长和死亡的影响[J].中国药理学通报, 2005, 21(2):149-52.Xu R C, Zhang M.The ouabain signal transduction and its role in cell growth and death[J].Chin Pharmacol Bull, 2005, 21(2):149-52. |
| [12] | 陈小义, 徐忠伟, 王娜, 等.哇巴因对血管内皮细胞ECV304细胞凋亡及胞内游离钙离子和活性氧浓度的影响[J].中国药理学与毒理学杂志, 2010, 24(4):241-8.Chen X Y, Xu Z W, Wang N.Effect of ouabain on human vascular endothelial ECV304 cell apoptosis and on concentrations of intracellular free calcium ion and reactive oxygen species[J].Chin J Pharmacol Toxicol, 2010, 24(4):241-8. |
| [13] | Deng Y, Guo X, Ferguson D O, et al.Multiple roles for MRE11 at uncapped telomeres [J].Nature, 2009, 460(7257):914-8. |
| [14] | Hopfner K P.DNA double-strand breaks come into focus [J].Cell, 2009, 139(1):25-7. |

