


2. 南通大学药学院药理学系, 江苏 南通 226001
2. Dept of Pharmacology, School of Pharmacy, Nantong University, Nantong Jiangsu 226001, China
一氧化氮(NO)是细胞中参与神经和心血管信号传导的重要分子[1, 2, 3],但是在炎症病变中,过量NO能损伤机体功能,例如,研究发现体内积累过量的NO能损坏线粒体功能并诱导细胞凋亡[4, 5];在严重败血症中,高浓度NO会导致细胞损伤和永久性低血压[6]。因此,控制体内NO含量对避免NO毒性作用的出现具有重要意义。NO在体内主要由一氧化氮合酶(NOS)合成,包括诱导型一氧化氮合酶(iNOS)、神经元一氧化氮合酶(nNOS)和内皮一氧化氮合酶(eNOS)[7]。其中,iNOS在刺激因子如脂多糖(LPS)的作用下表达明显增加[8]。LPS与细胞表面TLR4受体结合后,引起IKK激活;激活的IKK使IκB磷酸化并降解,最终导致NF-κB入核,并与iNOS启动子结合,促进iNOS基因转录[9]。我们之前的研究发现,热休克蛋白70(Hsp70)C末端底物结合活性抑制剂2-phenylethynesulfonamide(pifithrin-μ)能明显抑制由LPS引起的巨噬细胞和小胶质细胞iNOS等炎症因子表达[10, 11],基于此,我们推测激动Hsp70对巨噬细胞iNOS表达也可能有调控作用,但具体是什么样的作用,还不得而知。本研究对这一问题作了包括分子机制在内的详细探讨,有望进一步阐明Hsp70在炎症调控中的作用,同时也有助于Hsp70激动剂多样化药理学作用的评价。
1 材料与方法 1.1 试剂SW02、LPS、DMSO、TRIzol提取试剂盒购自美国Sigma公司。iNOS、IκB-α、NF-κB、GAPDH抗体购自美国Cell Signaling公司。兔抗大鼠荧光二抗购自Odyssey公司。DMEM 培养基购自美国Hyclone公司。Griess Reagent试剂盒、逆转录聚合酶链反应试剂盒等购自美国Invitrogen公司。DNA提取试剂盒购自Tiangen公司。胎牛血清购自美国Gibco公司。细胞核/质分离试剂盒、MTT、BCA蛋白浓度测定试剂盒、青-链霉素等购自江苏海门碧云天生物技术研究所。
1.2 方法 1.2.1 细胞培养和实验分组RAW264.7小鼠巨噬细胞源自美国ATCC。细胞培养基为DMEM/F12+10%胎牛血清+1×105 IU·L-1青霉素G+100 mg·L-1链霉素,每隔1~2 d换液1次,生长环境为37℃含95%空气和5% CO2的细胞培养箱。细胞分为DMSO预处理组、DMSO+LPS处理组、SW02预处理组、SW02+LPS处理组。浓度依赖实验中,SW02分别是1、5、10 μmol·L-1,预处理时间为30 min,LPS工作浓度1 mg·L-1。
1.2.2 MTT法检测细胞活力巨噬细胞生长至可传代的密度后,平均接种到96孔板中,每孔体积约200 μL。在用相应药物处理过的孔中加入MTT溶液20 μL,继续培养4 h。弃去每孔中上清,再每孔加入150 μL DMSO,震荡10 min使结晶充分溶解。在波长为490 nm酶标仪上读数。
1.2.3 Western blot用冷PBS收集细胞,3 000×q室温离心3~5 min,随后去除上清,加入RIPA裂解液(50 mmol·L-1 Tris-HCl,pH 7.4,1 mmol·L-1 EDTA,100 mmol·L-1 NaCl,20 mmol·L-1 NaF,3 mmol·L-1 Na3VO4,1 mmol·L-1 PMSF,1% NP-40,protease inhibitor cocktail),冰上裂解30 min。裂解完成后12 000×q 4℃离心15 min,将上清液转至新管,取适量蛋白液进行浓度测定,其余根据浓度计算配比等质量样品。95℃ 5 min蛋白变性。150 V电泳1 h后转膜。取膜,并在5%脱脂牛奶中室温封闭1 h,TBST洗3次,加入一抗4℃过夜。d 2去除一抗,TBST洗3次,加入1%脱脂牛奶稀释的荧光二抗,室温下孵育2 h,TBST洗3次。最后用Odyssey CLx Western blot检测系统进行条带显影检测。
1.2.4 NO测定根据Griess Reagent试剂盒说明书,将20 μL Griess试剂、150 μL各实验组细胞培养液和130 μL去离子水混合于96孔板中,以20 μL Griess试剂加280 μL去离子水作为空白对照。室温下放置30 min,用分光光度仪测量各组混合液的吸光度(波长548 nm)并校正曲线。
1.2.5 细胞核、质分离PBS洗1遍,用细胞刮子刮下细胞。离心收集细胞,吸尽上清。每20 μL沉淀加入200 μL添加了PMSF的细胞质蛋白抽提试剂A。剧烈振荡5 s,把细胞沉淀完全悬浮并分散开。冰浴15 min,加入细胞质蛋白抽提试剂B 10 μL,剧烈振荡5 s,冰浴1 min,随后再剧烈振荡5 s,4℃ 12 000×q离心5 min。立即吸取上清至一预冷的塑料管中,即为抽提得到的细胞质蛋白。对于沉淀,完全吸尽残余的上清,加入50 μL添加了PMSF的细胞核蛋白抽提试剂,剧烈振荡20 s,把细胞沉淀完全悬浮并分散开,然后放回冰浴中,每隔2 min剧烈振荡20 s,共30 min。4℃ 12 000×q离心10 min,立即吸取上清至一预冷塑料管中,作为抽提得到的细胞核蛋白,再用Western blot法检测SW02处理前后细胞核、细胞质NF-κB表达情况。
1.2.6 实时定量PCR检测细胞iNOS mRNA表达:总RNA按照TRIzol抽提试剂说明书进行。一定比例稀释后加样测定所提取的RNA浓度,使得260/280值在1.8~2.0之间。测量得到浓度后,按照最低浓度水平用无RNA酶水稀释其它样品。取10 μL做凝胶电泳,其余置-80℃冷冻保存。PCR反应体系条件如下:预变性94℃ 30 s,变性94℃ 30 s,退火60℃ 30 s,延伸72℃ 1 min,25个循环,最后延伸72℃ 7 min。结束后,反应产物经1%琼脂糖凝胶电泳(95 V,30 min)鉴定,用凝胶成像仪进行灰度扫描分析。引物序列如下:iNOS(557 bp)上游:5′-CCATGTCAAAACCCGTGGTGAATG-3′,下游:5′-A TGGGAGTTGGGCAGTCATCAG-3′;GAPDH(107 bp)上游:5′-TAAAGAACAGGCTCTTAGCACA-3′,下游:5′-AGTCTTGGAAATGGATTGTCTC-3′。
1.2.7 染色质免疫共沉淀(ChIP)ChIP实验方法主要参考我们已经发表的研究论文[12],简述如下:用1%甲醛(福尔马林)室温孵育细胞10 min,加甘氨酸至终浓度0.125 mol·L-1,室温下放置5 min终止交联。用冷PBS洗2次,收集细胞于离心管中,4℃ 3 500×q离心6 min。去上清,加入低张溶液重悬,冰上裂解10 min,随后冰上匀浆25~30次,4℃ 3 500×q离心5 min。取上清,去除沉淀,将取出的上清继续离心:4 ℃,12 000×q离心5 min。剩下的沉淀为细胞核,将其溶解在40 μL裂解液中裂解10 min。经超声处理后,取ChIP稀释液稀释后的样品20 μL,加入NF-κB抗体(1 ∶200),4℃摇床过夜。d 2取珠子,用ChIP稀释液清洗珠子2次,每次2 min。弃上清,加ChIP稀释液,室温摇匀2 h。随后用高盐和低盐溶液清洗,并加入稀释缓冲液简单混匀,室温孵育15 min。12 000×q离心3 min,小心取出上清,将其转入另一管。65℃,过夜交联,随后加入10 μL 0.5 mol·L-1 EDTA、20 μL 1 mol·L-1 Tris-HCl和2 μL 10 g·L-1 Proteinase K到上述液体中,45℃孵育1 h。最后提取DNA,用上游引物5′-C AAGCCAGGGTATGTGGTTT-3′和下游引物5′-GCAG CAGCCATCAGGTATTT-3′(290 bp)检测NF-κB。
1.2.8 统计学分析实验数据以x±s表示,采用SPSS 11.0统计软件对数据进行单因素方差分析(ANOVA)。
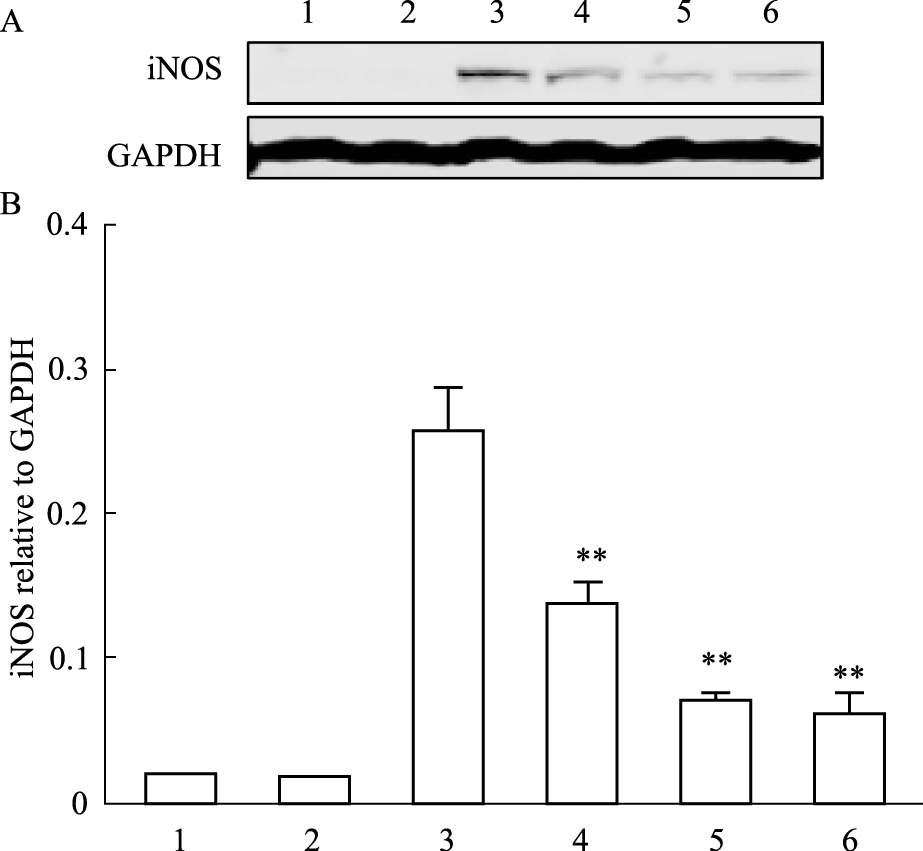
2 结果 2.1 SW02抑制LPS诱导的RAW264.7细胞iNOS蛋白表达RAW264.7细胞经1 mg·L-1 LPS处理24 h后,iNOS蛋白被明显诱导出来(Fig1)。不同浓度SW02(1、5、10 μmol·L-1)预处理30 min后,iNOS诱导被明显抑制(P < 0.01或P < 0.05)。结果提示,SW02能抑制LPS诱导的巨噬细胞iNOS蛋白表达,并呈剂量依赖方式,浓度越高,抑制效应越明显,在10 μmol·L-1时效果最佳(Fig1)。
|
| Fig.1 SW02 inhibited LPS-induced iNOS protein expression in RAW264.7 cells(n=3) A: The dose-dependent effect of SW02 on iNOS protein expression in LPS-treated cells; B:The quantitative analysis of iNOS protein expression in cells upon SW02 and/or LPS treatment.1:Control;2:SW02(10 μmol·L-1);3:DMSO+LPS;4:LPS+SW02(1 μmol·L-1);5:LPS+SW02(5 μmol·L-1);6:LPS+SW02(10 μmol·L-1).**P < 0.01 vs DMSO+LPS group |
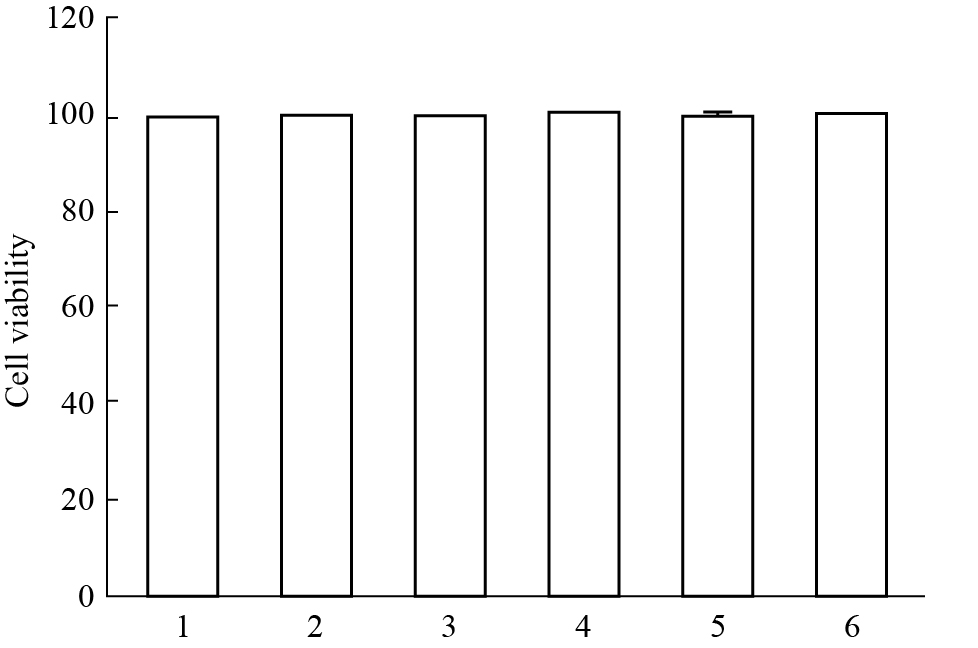
为了判断iNOS蛋白减少是否与SW02和(或)LPS引起细胞减少有关,我们检测了各给药组细胞活力,发现10 μmol·L-1 SW02处理和各浓度SW02(1、5、10 μmol·L-1)、LPS共处理均不影响细胞活力(P>0.05),提示SW02处理后iNOS蛋白表达减少与细胞损伤无关(Fig2)。
|
| Fig.2 SW02 and/or LPS did not affect cell viability(n=5) 1:Control;2:SW02(10 μmol·L-1);3:DMSO+LPS;4:LPS+SW02(1 μmol·L-1);5:LPS+SW02(5 μmol·L-1);6:LPS+SW02(10 μmol·L-1). |
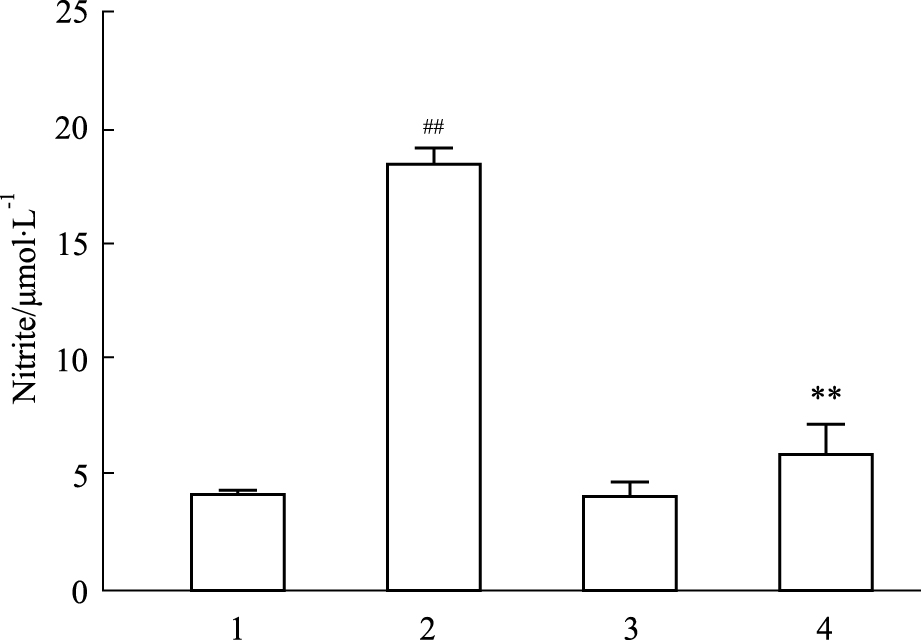
对照组细胞用1 mg·L-1 LPS处理24 h后,NO生成量明显增加(P < 0.01)(Fig3);SW02组细胞根据剂量依赖实验选取合适浓度的SW02(10 μmol·L-1)预处理30 min,随后用1 mg·L-1 LPS处理24 h,发现SW02+LPS组细胞NO生成量与SW02组比差异无显著性(P>0.05),但明显低于DMSO+LPS组(P < 0.01)(Fig3)。结果提示SW02能抑制LPS诱导的巨噬细胞NO生成。
|
| Fig.3 SW02 inhibited LPS-induced NO production in RAW264.7 cells(n=5) 1:Control;2:DMSO+LPS;3:SW02(10 μmol·L-1);4:LPS+SW02(10 μmol·L-1).##P < 0.01 vs control;**P < 0.01 vs LPS alone-treated group. |
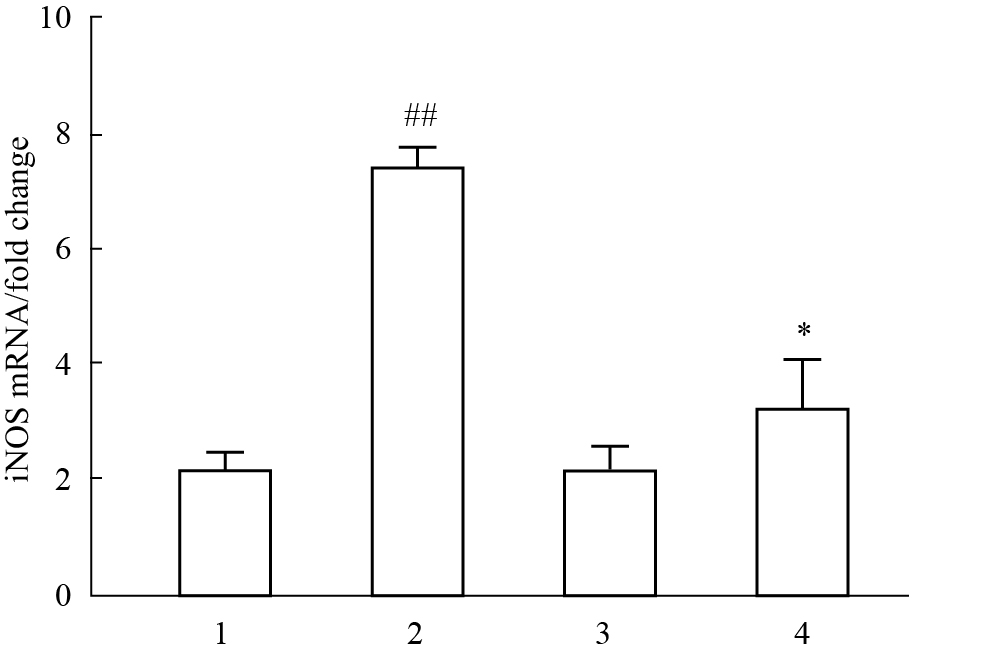
对照组细胞用1 mg·L-1 LPS处理4 h后,iNOS mRNA表达量明显增加(P < 0.01)(Fig4);SW02组细胞用10 μmol·L-1 SW02预处理30 min,随后用1 mg· L-1 LPS处理4 h,发现SW02+LPS组细胞iNOS mRNA表达量与SW02组比差异无显著性(P>0.05),但明显低于DMSO+LPS组(P < 0.05)(Fig4)。结果提示SW02能抑制LPS诱导的巨噬细胞iNOS mRNA表达。
|
| Fig.4 SW02 inhibited LPS-induced iNOS mRNA expression in RAW264.7 cells(n=3) 1:Control;2:LPS;3:SW02(10 μmol·L-1);4:LPS+SW02(10 μmol·L-1).##P < 0.01 vs control;*P < 0.05 vs LPS alone-treated group. |
对照组细胞用1 mg·L-1 LPS处理30 min后,IκB-α表达量明显减少(P < 0.05)(Fig5A,B);SW02组细胞用10 μmol·L-1 SW02预处理30 min,随后用1 mg·L-1 LPS处理30 min,发现SW02+LPS组细胞IκB-α表达量明显低于SW02组(P < 0.01),但与DMSO+LPS组比差异无显著性(P>0.05)(Fig5A,B),提示SW02并不影响LPS诱导的巨噬细胞IκB-α降解。对照组细胞用1 mg·L-1 LPS处理30 min后,DMSO+LPS组细胞质NF-κB表达量明显低于对照组(P < 0.05,Fig5C,D),而细胞核NF-κB表达量明显高于对照组(P < 0.01,Fig5C,E);在SW02存在的情况下,由LPS刺激引起的NF-κB出入核情况没有受到明显影响(SW02+LPS组细胞质、细胞核NF-κB表达量与SW02组比差异有显著性,P < 0.05;与DMSO+LPS组比差异无显著性,P>0.05,Fig5C-E),提示SW02并不影响LPS诱导的巨噬细胞NF-κB核转位。

|
| Fig.5 SW02 did not affect LPS induced-degradation of IκB-α and nuclear translocation of NF-κB in RAW264.7 cells(n=3) A:The effect of SW02 on LPS induced-degradation of IκB-α in RAW264.7 cells;B:The quantitative analysis of IκB-α protein levels in cells upon SW02 and/or LPS treatment; C:The effect of SW02 on LPS induced-nuclear translocation of NF-κB in RAW264.7 cells; D:The quantitative analysis of cytoplasmic NF-κB protein levels in cells upon SW02 and/or LPS treatment; E:The quantitative analysis of nuclear NF-κB protein levels in cells upon SW02 and/or LPS treatment. #P < 0.05,##P < 0.01 vs control;*P < 0.05,**P < 0.01 vs SW02 group. 1:Control;2:DMSO+LPS;3:SW02(10 μmol·L-1);4:LPS+SW02(10 μmol·L-1). |
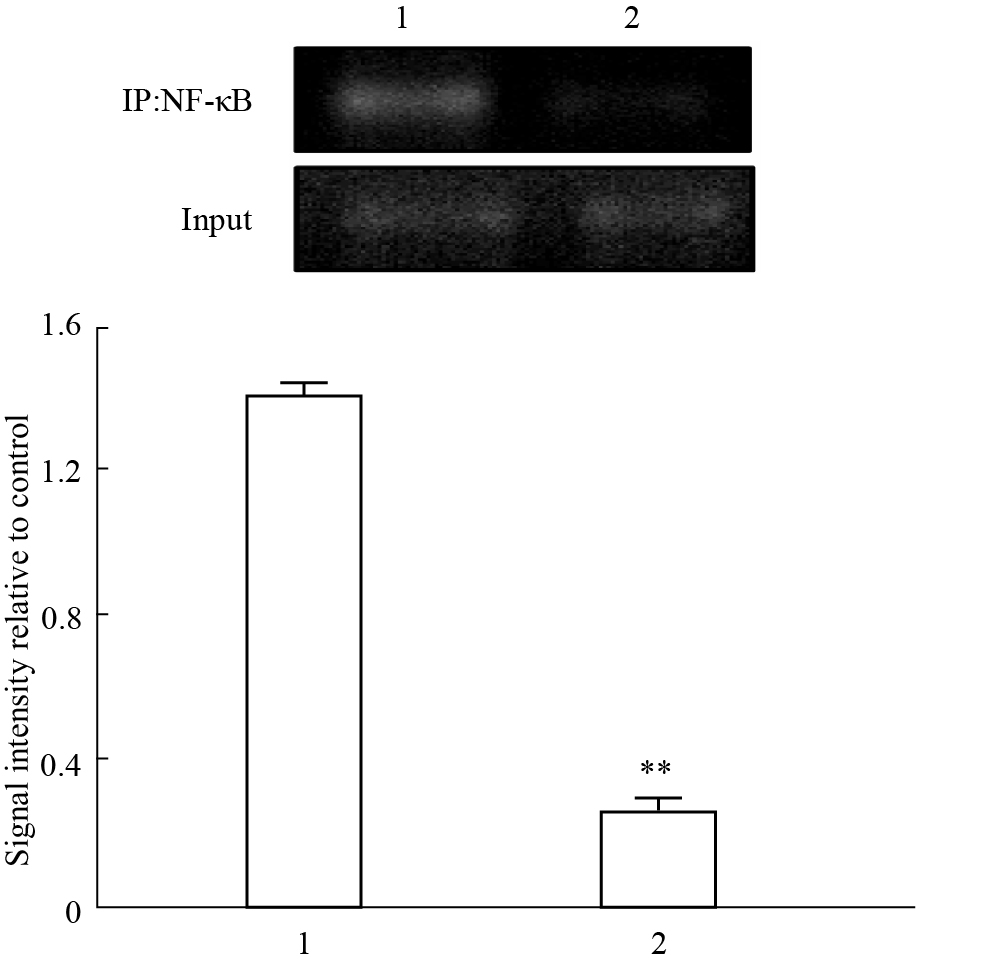
首先用10 μmol·L-1 SW02预处理细胞30 min,随后1 mg·L-1 LPS处理1 h,发现SW02+LPS组细胞NF-κB与iNOS启动子结合量明显低于DMSO+LPS组(P < 0.01)(Fig6)。结果提示SW02能抑制NF-κB与iNOS启动子的直接结合。
|
| Fig.6 SW02 inhibited LPS-induced binding of NF-κB to iNOS promoter in RAW264.7 cells(n=3) 1:DMSO+LPS;2:LPS+SW02(10 μmol·L-1).**P < 0.01 vs DMSO+LPS group. |
NO作为一种具有生物活性的气体分子,在大量生成的情况下与炎症密切相关[4, 5]。NO生成量主要取决于一氧化氮合成酶的多少与活性。在体内,NOS可分为诱生型(iNOS)、神经型(nNOS)和内皮型(eNOS)3种[7]。在活化的巨噬细胞中,iNOS活性与表达量直接决定着NO生成量。因此,研究iNOS表达调控机制也就显得十分重要。在本实验中,我们选择研究Hsp70激动剂SW02在LPS诱导的巨噬细胞iNOS表达和NO生成中的作用及信号机制。这一研究主要是建立在我们前期发现Hsp70选择性抑制剂2-phenylethynesulfonamide明显抑制巨噬细胞和小胶质细胞iNOS表达基础上的[10, 11],在国内外尚未见文献报道。
SW02是一种Hsp70特异性激动剂,能通过激动Hsp70 N末端ATP酶活性抑制Aβ聚集[13],将来有可能作为一种潜在的抗神经退行性疾病药物进行开发。在本研究中,我们发现SW02能抑制由LPS诱导的巨噬细胞iNOS蛋白表达,且这种作用主要由iNOS mRNA减少引起。SW02抑制巨噬细胞iNOS蛋白表达这一事实体现了SW02在iNOS诱导调控中的重要性,为今后研究SW02调控iNOS/NO介导的相关疾病,如血管麻痹综合征、感染性休克等提供了参考依据。此外,由于免疫系统iNOS/NO在阿尔茨海默病等神经退行性疾病的发生、发展中具有重要作用[14, 15],本研究为我们今后了解SW02的多样化作用及分子机制提供了理论参考。然而,SW02抑制巨噬细胞iNOS表达是否通过激动Hsp70 N末端ATP酶来实现,还不得而知。如果后续实验证明是通过激动Hsp70 N末端ATP酶发挥作用,那么这将丰富我们对Hsp70调控炎症反应的理解,因为我们已经证明Hsp70 C末端底物结合活性抑制剂能抑制巨噬细胞和小胶质细胞炎症反应[10, 11]。当然,也有可能存在脱靶的可能性,也就是说SW02通过不依赖于Hsp70 N末端ATP酶的方式发挥iNOS调控作用,这些猜测有待进一步研究。
细胞基因转录受抑往往是由阻断转录因子活化过程中一个或多个信号分子引起的[9, 10]。在LPS刺激的炎症细胞中,SW02并不影响由LPS引起的IκB-α降解和NF-κB细胞核转位,表明SW02可能是通过干扰NF-κB核转位下游信号实现iNOS表达调控的。与预期相一致的是,在ChIP实验中,我们发现SW02能明显抑制由LPS诱导的NF-κB与iNOS DNA启动子之间的结合。概括来说,SW02调控iNOS表达的关键环节在基因转录起始阶段,这一结论合理解释了如下现象,即为什么SW02处理的细胞中IκB-α-NF-κB信号通路没有受到任何影响,而iNOS基因转录最终却是减弱的。
综上所述,我们的研究结果显示,SW02能明显抑制由LPS诱导的巨噬细胞iNOS表达,这一过程与IκB-α-NF-κB信号通路无关,主要是通过抑制NF-κB与iNOS基因启动子区结合来实现的,这些发现为深入研究和开发与Hsp70相关的免疫炎症调控分子奠定了基础。这部分内容是我们关于Hsp70调控免疫炎症反应系列工作的延伸,国内外尚未见报道,其中更为深入的分子生物学机制,还需要做大量工作。
| [1] | Chow B S,Chew E G,Zhao C,et al.Relaxin signals through a RXFP1-pERK-nNOS-NO-cGMP-dependent pathway to up-regulate matrix metalloproteinases:the additional involvement of iNOS[J].PLoS One,2012,7(8):e42714. |
| [2] | 胡 军,张 野,蒋玲玲,等.NO/cGMP信号通路在鞘内吗啡预处理减轻大鼠心肌缺血/再灌注损伤中的作用[J].中国药理学通报,2005,21(8):901-4. Hu J,Zhang Y,Jiang L L,et al.Role of NO/cGMP in the cardioprotective effects of intrathecal morphine preconditioning against myocardial ischemia-reperfusion injury in rats[J].Chin Pharmacol Bull,2005,21(8):901-4. |
| [3] | Haldar S M,Stamler J S.S-nitrosylation:integrator of cardiovascular performance and oxygen delivery[J].Clin Invest,2013,123(1):101-10. |
| [4] | Banuls C,Rocha M,Rovira-Llopis S,et al.The pivotal role of nitric oxide:effects on the nervous and immune systems[J].Curr Pharm Des,2014,20(29):4679-89. |
| [5] | Dodson M,Darley-Usmar V,Zhang J.Cellular metabolic and autophagic pathways:traffic control by redox signaling[J].Free Radic Biol Med,2013,63:207-21. |
| [6] | Su C F,Yang F L,Chen H I.Inhibition of inducible nitric oxide synthase attenuates acute endotoxin-induced lung injury in rats[J].Clin Exp Pharmacol Physiol,2007,34(4):339-46. |
| [7] | O'Connor DM,O'Brien T.Nitric oxide synthase gene therapy:progress and prospects[J].Expert Opin Biol Ther,2009,9(7):867-78. |
| [8] | Kleinert H,Pautz A,Linker K,Schwarz P M.Regulation of the expression of inducible nitric oxide synthase[J].Eur J Pharmacol,2004,500(1-3):255-66. |
| [9] | Hayden M S,Ghosh S.Signaling to NF-κB[J].Genes Dev, 2004,18(18):2195-224. |
| [10] | Huang C,Wang J,Chen Z,et al.2-phenylethynesulfonamide prevents induction of pro-inflammatory factors and attenuates LPS-induced liver Injury by targeting NHE1-Hsp70 complex in mice[J].PLoS One,2013,8(6):e67582. |
| [11] | Huang C,Lu X,Wang J,et al. Inhibition of endogenous heat shock protein 70 attenuates inducible nitric oxide synthase induction via disruption of heat shock protein 70/Na(+)/(+) exchanger 1-Ca(2+)-calcium-calmodulin-dependent protein kinase II/transforming growth factor β-activated kinase 1-nuclear factor-κB signals in BV-2 microglia[J]. J Neurosci Res, 2015, 93(8):1192-202. |
| [12] | Huang C,Wang Y Z,Wang J,et al.TSG(2,3,4',5-tetrahydroxystilbene 2-O-β-D-glucoside)suppresses induction of pro-inflammatory factors by attenuating the binding activity of nuclear factor-κB in microglia[J].J Neuroinflammation,2013,10:129. |
| [13] | Jinwal U K,Miyata Y,Koren J 3rd,et al.Chemical manipulation of hsp70 ATPase activity regulates tau stability[J]. J Neurosci, 2009, 29(39):12079-88. |
| [14] | Heppner F L,Ransohoff R M,Becher B.Immune attack:the role of inflammation in Alzheime disease[J].Nat Rev Neurosci,2015,16(6):358-72. |
| [15] | Phani S,Loike J D,Przedborski S. Neurodegeneration and inflammation in Parkinson's disease[J].Parkinsonism Relat Disord,2012,18(Supp11):S207-9. |

