


抑郁症是以明显而持久的心境低落为主要临床特征的心境障碍疾病。随着现代社会生活与工作的压力越来越大,抑郁症的发病率逐渐提高,预计到2020年,抑郁症将会成为继心脑血管疾病后的第二大致残性疾病[1]。目前临床的治疗手段远不能达到有效治愈的目标,多达65%的抑郁患者遭受反复发作的痛苦[2]。因此,深入探讨抑郁症的发病机制,寻找更加有效的预防策略及治疗方案成为目前关注的焦点。
严重或持久的应激对健康十分不利,尤其是慢性应激是诱发抑郁症的重要因素[3]。应激所致抑郁的发生机制非常复杂,其中免疫炎症抑郁假说提出内部炎性状态以及各种生理、心理性外部刺激等,在激活机体的免疫系统之后,提高炎症反应及氧化应激水平,从而参与调控抑郁症的发生发展过程[4],这为抑郁症病因学提供了新方向,也开启了炎症因子拮抗剂和抗炎剂在抑郁症治疗中的实验与应用,其中环氧酶2(cyclooxygenase-2,COX-2)抑制剂备受关注。COX-2是介导炎症反应的关键酶,在炎症因子和有丝分裂原刺激下催化花生四烯酸(arachidonic acid,AA)生成前列腺素类
(prostaglandins,PGs)产物,PGs通过各自特殊的G蛋白偶联受体发挥不同生物学效应[5]。迄今为止的研究指出,选择性COX-2抑制剂在抑郁症治疗中具有较高的反应率和缓解率[6],而在和其他抑郁症治疗药物的联合运用中具有协同作用[7]。我们的前期实验[8]也发现,选择性COX-2抑制剂美洛昔康对慢性应激诱导的抑郁行为有明显的改善作用,然而,其具体机制还不明确。应激促发免疫炎症反应,使患者出现抑郁症状,动物表现出抑郁样行为,这不仅与免疫炎症诱导的细胞因子和炎症介质释放增加影响神经形成和HPA轴活化有关,还与其引起单胺类神经递质如多巴胺(dopamine,DA)、去甲肾上腺素(norepinephrin,NE)、5-羟色胺(5-hydroxytryptamine,5-HT)等释放关系密切[9]。那么,美洛昔康改善应激大鼠抑郁行为的机制是否与皮层神经递质系统相关呢?目前还尚未见研究报道。
为此本研究采用慢性温和不可预知性应激(chronic unpredictable mild stress,CUMS)大鼠抑郁模型,在观察美洛昔康对大鼠抑郁行为改变的基础上,进一步观察其对大鼠皮层组织中PGE2、TNF-α含量,单胺类神经递质及其代谢产物NE、DA、3,4-二羟基苯乙酸(3,4-dihydroxyphenylacetic acid,DOPAC)、5-羟吲哚乙酸(5-hydroxyindoleacetic acid,5-HIAA)含量以及5-羟色胺1A 受体(5-hydroxytryptamine 1A receptor,5-HT1AR)蛋白表达的影响,拟从炎症反应/单胺递质系统平衡方面初步探讨美洛昔康的抗抑郁作用机制。
1 材料与方法 1.1 材料 1.1.1 动物选取清洁级♂SD大鼠50只,2月龄,体质量180~220 g,购于重庆医科大学实验动物中心,动物生产许可证编号:SCXK(渝)2012-0001。在标准的实验环境下:温度(22±2)℃,湿度(50±10)%,明暗交替各12 h。正常饮食饮水,饲养7 d以适应实验环境。
1.1.2 主要药品与试剂美洛昔康(昆山龙灯瑞迪制药有限公司),PGE2与TNF-α ELISA 试剂盒(武汉华美生物工程有限公司),山羊抗大鼠多克隆5-HT1A抗体(CST,美国),SP试剂盒与DAB染色试剂盒(北京中杉金桥生物技术有限公司),NE、DA、DOPAC与5-HIAA标准品[西格玛奥德里奇(上海)贸易有限公司]。
1.1.3 主要仪器无盖木制方箱,自制大鼠强迫游泳仪,-80℃超低温冰箱(SANYO公司,日本),ELX-800全自动酶标仪( Bio-Tek公司,美国),光学显微镜( Nikon公司,日本),5810R超低温离心机(Eppendorf公司,德国),高效液相色谱仪(岛津,日本)。
1.2 方法 1.2.1 分组与给药正式实验之前选取旷场实验水平活动得分在40~100的♂清洁级SD大鼠50只,并将其随机分为5组(n=10),即正常对照组、模型组、阳性药物对照组、美洛昔康1 mg·kg-1组和美洛昔康3 mg·kg-1组。分组完成后,正常对照组大鼠大笼饲养,每笼5只,自由摄水进食且不给予任何刺激,其余4组大鼠孤养并给予42 d CUMS。从造模d 22开始,给药组大鼠分别灌胃给予舍曲林(5 mg·kg-1)、美洛昔康(1、3 mg·kg-1),模型组与正常组则以相同的方式给予等体积0.5%羧甲基纤维素钠(sodium carboxymethyl cellulose,CMC-Na),每天1次,连续给药至42 d。大鼠每周称1次体重,灌胃剂量根据体重调节。
1.2.2 慢性温和不可预知性应激大鼠模型综合文献[8, 10]所述方法并稍加改进后建立应激抑郁大鼠模型。模型组、阳性药物对照组、美洛昔康(1、3 mg·kg-1)组大鼠每笼单只饲养,连续给予42 d温和刺激,包括:夹尾1 min、昼夜颠倒24 h、潮湿垫料24 h、禁食水24 h、冰水游泳(4℃,5 min)、热水游泳(45℃,5 min)、噪声(92 dB,1500 Hz)刺激2 h、鼠笼倾斜45° 24 h共8种刺激,每日随机选择一种,3 d内不重复,刺激在同楼远离饲养室房间给予。
1.2.3 行为学测定(1)旷场实验(open-field test):实验在安静且可见度为5m的暗室中进行,实验装置为四周与底面均黑漆覆盖,长×宽×高为100 cm×100 cm×50 cm的无盖木箱,底部由白线均分为25个20 cm×20 cm 大小的方格。实验开始时,大鼠被放置于中央方格内,观察其在300 s内的活动情况:①水平运动(horizontal movement):以穿行的方格数记录水平运动次数,穿行方格的定义为大鼠4只脚都进入同一格子中。②垂直运动(vertical movement):以大鼠后肢直立即两前爪腾空或攀爬墙壁的总次数为垂直运动次数。每只大鼠测试完结束后,使用75%酒精对木箱底面进行清洁消毒。(2)强迫游泳实验(force swimming test):将单只大鼠放入内径30 cm,高50 cm圆柱形透明水桶中,桶内水深30 cm,水温(24±2)℃。使其适应游泳2 min后,从第3 min开始记录大鼠300 s内在水中静止不动状态持续时间,不动状态是指大鼠在水中停止挣扎时呈漂浮的状态,或为使其头部浮在水面仅有细小的肢体活动。每只大鼠测试完后均清洗水桶并换水。
1.2.4 PGE2、TNF-α含量检测每组各随机选取6只大鼠断头处死,用于PGE2、TNF-α含量测定。取皮层称重后按质量体积比1 ∶9加入PBS,于冰面玻璃匀浆器中匀浆,5 000×g,4℃离心5 min,取上清液,-20℃冻融,严格参照ELISA测试盒说明书测定PGE2和TNF-α含量。
1.2.5 高效液相色谱法测定NE、DA、DOPAC、5-HIAA的含量变化与ELISA共用组织测定NE、DA、DOPAC、5-HIAA的含量,皮层临用前解冻称重,按照6 μL/mg加入0.1 mol·L-1高氯酸(内标浓度为1 mg·L-1),用玻璃匀浆器匀浆,在4℃条件下,以20 000×g离心15 min,取上清液进样20 μL。色谱的条件为:依利特ODS2色谱柱(E2118047,4.6 mm×250 mm,5 μm);流动相为 A 乙腈 ∶B 水(含 0.1%甲酸)等度洗脱,0~3 min(10 ∶90 V/V),流速为 1 mL·min-1。
1.2.6 免疫组化每组随机选取4只大鼠灌注后取脑,于4%多聚甲醛溶液中固定24 h,脑组织脱水后石蜡包埋,冠状面切片约4 μm厚。免疫组化实验观察皮层5-HT1AR的表达情况,5-HT1A抗体浓度为1 ∶100。具体步骤按SP法操作进行,DAB显色后中性树胶封闭,显微镜下观察蛋白阳性表达情况,用Image-pro plus 6.0软件分析免疫组化图片,将10×40倍光镜下3个不同视野进行光密度分析。
1.3 统计学处理所有实验数据以x±s的形式表示,采用SPSS 17.0统计软件进行统计学分析,组间比较用方差分析和Dunnett's t检验。
2 结果 2.1 美洛昔康对慢性应激抑郁大鼠水平和垂直运动的影响与正常组相比,CUMS组大鼠水平活动(P < 0.01)和垂直活动明显减少(P < 0.01);给予美洛昔康1 mg·kg-1连续灌胃21 d,大鼠水平活动(P < 0.01)与垂直活动增加(P < 0.05),美洛昔康3 mg·kg-1组大鼠水平活动和垂直活动增加更明显(P < 0.01),见Tab1。
| Group | Vertical movement | Horizontal movement |
| Control | 15.70±9.31 | 92.20±17.35 |
| CUMS | 3.10±1.20 ** | 12.40±4.23 ** |
| CUMS+Sertraline(5 mg·kg -1) | 9.70±5.54 ## | 65.80±18.51 ## |
| CUMS+Meloxicam(1 mg·kg -1) | 5.40±0.84 # | 45.30±10.18 ## |
| CUMS+Meloxicam (3 mg·kg -1) | 9.40±4.37 ## | 63.40±17.15 ## |
| ** P < 0.01 vs control; # P < 0.05, ## P < 0.01 vs CUMS | ||
与正常组相比较,CUMS组大鼠静止不动时间增加(P < 0.01),美洛昔康1、3 mg·kg-1治疗能明显减少大鼠不动时间(P < 0.01),见Tab2。
| Group | Immobility time/s |
| Control | 95.90±21.22 |
| CUMS | 209.30±30.64 ** |
| CUMS+Sertraline(5 mg·kg -1) | 136.10±25.96 ## |
| CUMS+Meloxicam (1 mg·kg -1) | 121.80±25.48 ## |
| CUMS+Meloxicam (3 mg·kg -1) | 138.20±28.13 ## |
| ** P < 0.01 vs control; ## P < 0.01 vs CUMS | |
与正常组比较,CUMS组大鼠皮层中PGE2、TNF-α含量明显增加(P < 0.01);与CUMS组相比,美洛昔康1 mg·kg-1组大鼠皮层组织PGE2(P < 0.05)、TNF-α(P < 0.01)明显降低,美洛昔康3 mg·kg-1组PGE2、TNF-α含量减少更为明显(P < 0.01),见Tab3。
| PGE 2/ng·L -1 | TNF-α/ng·L -1 | |
| Control | 22.11±5.07 | 433.79±34.99 |
| CUMS | 63.06±11.59 ** | 539.82±57.16 ** |
| Sertraline(5 mg·kg -1) | 52.34±7.40 | 471.53±25.63 # |
| Meloxicam (1 mg·kg -1) | 47.22±12.60 # | 391.35±30.12 ## |
| Meloxicam (3 mg·kg -1) | 31.86±11.07 ## | 310.41±17.57 ## |
| ** P < 0.01 vs control; # P < 0.05, ## P < 0.01 vs CUMS | ||
与正常组比较,CUMS组大鼠皮层中NE、DA、DOPAC、5-HIAA的含量明显减少(P < 0.01);美洛昔康1 mg·kg-1组皮层DA和DOPAC含量明显增加(P < 0.05),NE和5-HIAA含量有增加,但差异无统计学意义; 美洛昔康3 mg·kg-1组NE(P < 0.05)、DA(P < 0.01)、5-HIAA(P < 0.01)、DOPAC(P < 0.01)的含量均明显增加,见Tab4。
| Group | NE/ng·g -1 | DA/ng·g -1 | DOPAC/ng·g -1 | 5-HIAA/ng·g -1 |
| Control | 971.47±150.31 | 162.00±25.89 | 399.78±19.75 | 236.77±24.21 |
| CUMS | 571.10±21.96 ** | 86.04±9.69 ** | 230.54±22.07 ** | 152.70±23.00 ** |
| Sertraline( 5mg·kg -1) | 751.29±92.43 # | 130.81±11.17 # | 328.45±20.30 ## | 204.39±13.54 ## |
| Meloxicam( 1mg·kg -1) | 688.08±38.83 | 116.64±12.40 # | 270.18±25.21 # | 170.17±16.90 |
| Meloxicam( 3mg·kg -1) | 737.14±96.25 # | 124.60±13.48 ## | 300.18±30.75 ## | 192.80±11.80 ## |
| ** P < 0.01 vs control; # P < 0.05, ## P < 0.01 vs CUMS | ||||
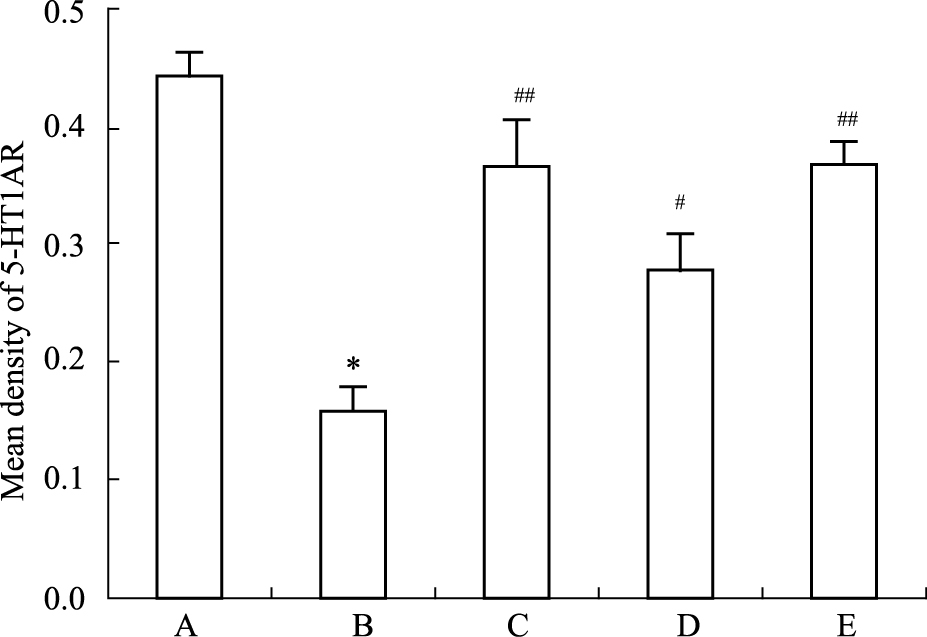
正常大鼠皮层组织中5-HT1AR阳性神经细胞较多,胞质染色较深,呈黄棕色。CUMS组大鼠皮层5-HT1AR阳性神经细胞较少,且细胞质染色较浅。COX-2抑制剂美洛昔康使给予组大鼠皮层5-HT1AR阳性神经细胞增多,染色加深,见Fig1。平均光密度值(average optical density,AOD)分析结果统计显示,与正常组相比,CUMS组5-HT1AR(P < 0.05)阳性神经细胞AOD减少;与CUMS组相比,美洛昔康1 mg·kg-1组大鼠皮层5-HT1AR(P < 0.05)阳性细胞AOD明显增加,3 mg·kg-1美洛昔康组大鼠皮层5-HT1AR(P < 0.01)阳性细胞AOD增加更明显,见Fig2。

|
| Fig.1 Effect of meloxicam on 5-HT1AR protein expression of cortex in rats (400×) A:Control;B:CUMS;C:Sertraline (5 mg·kg-1); D: Meloxicam (1 mg·kg-1); E:Meloxicam (3 mg·kg-1) |
|
| Fig.2 Effect of meloxicam on 5-HT1AR protein expression of cortex in rats (x±s,n=4) A:Control;B:CUMS;C:Sertraline (5 mg·kg-1); D: Meloxicam (1 mg·kg-1); E:Meloxicam (3 mg·kg-1).*P < 0.05 vs control group;#P < 0.05,##P < 0.01 vs CUMS group |
CUMS大鼠抑郁模型模拟了人类抑郁症心境低落、动力低下、快感缺失、行为绝望等核心症状,目前广泛应用于抑郁症发病机制研究、抗抑郁药物筛选及新药研发。本实验通过CUMS方法建立大鼠抑郁模型,观察美洛昔康改善抑郁大鼠行为与炎症反应/神经递质系统的关系。实验结果表明,CUMS致大鼠旷场试验中水平与垂直活动明显减少,强迫游泳时静止不动时间明显延长,同时大脑皮层炎症因子PGE2、TNF-α含量明显增加,说明造模成功,且CUMS大鼠脑皮层出现炎症反应,这与O’Connor等[11]的研究结果相似,心理应激刺激机体免疫炎症反应激活,能升高外周及中枢情绪相关脑区内炎性因子的浓度,从而引发炎症级联反应,致使脑损伤加剧,证实了抑郁症的发生与炎症反应激活密切有关。给予美洛昔康治疗后,不仅改善了应激大鼠的抑郁行为,还逆转了皮层PGE2、TNF-α含量的升高,提示美洛昔康改善抑郁大鼠行为的作用机制可能在于抑制皮层COX-2酶活性的同时抑制炎症反应损伤,阻碍小胶质细胞释放炎症因子,从而干扰炎症反应瀑布效应造成的脑损伤[12];也从另一方面提示抗抑郁治疗可能与控制炎症因子的表达关系密切。
NE、5-HT、DA是中枢神经系统中重要的单胺类神经递质,对觉醒、情绪、记忆、疼痛、摄食和运动等多种正常生理过程起调节作用,因此神经元突触间隙单胺递质的浓度与其相应作用时间的精密调节对中枢神经系统正常功能的维持十分重要。一旦单胺类神经递质与其代谢物的释放和相关受体表达受阻,则会直接导致NE能、DA能、5-HT能3个系统之间的功能紊乱,这是引起抑郁症发生的重要因素,因此目前临床上使用的大多抗抑郁药物主要是通过升高单胺递质的水平而发挥作用。在我们的实验中,CUMS致大鼠皮层NE、DA、DOPAC、5-HIAA的含量明显下降,5-HT1AR表达减少,提示抑郁大鼠皮层出现神经系统单胺的合成和降解、储存和重摄取及其受体功能受到影响,导致单胺能神经递质网络系统失衡,这与人类抑郁症患者尸检发现及抑郁症患者脑脊液中单胺类神经递质水平下降的结果相一致[13, 14]。给予CUMS组大鼠COX-2抑制剂美洛昔康治疗后,NE、DA、DOPAC、5-HIAA的含量明显增加,5-HT1AR表达上调,提示美洛昔康改善应激抑郁行为与其逆转皮层单胺类神经递质减少及恢复单胺能神经元功能不足相关。
研究表明,促炎细胞因子及炎症介质(如PGE2)不仅能促进5-HT分解、5-HTlAR的表达减少,导致5-HT在突触间隙的水平降低、利用受阻[15],还会通过NO影响神经系统四氢生物蝶呤的含量,进而使不同脑区DA的生成减少[16]。除此之外,逐渐增多的数据显示炎症还可影响神经元五羟色胺转运体(serotonin transporter,5-HTT)和去甲肾上腺素转运体(norepinephrine transporter,NET)的活性等,如TNF阻滞剂能使类风湿性关节炎患者脑组织5-HTT密度减小[17],这表明TNF对5-HTT的表达有影响,炎症反应能干扰5-HTT对5-HT的重摄取。这些研究表明炎症反应与单胺神经递质系统关系密切。我们的结果,结合其他的研究报道,提示美洛昔康能重建CUMS大鼠皮层神经递质系统平衡,可能与其减少皮层炎症因子PGE2、TNF-α等的释放,从而减轻炎症反应相关。
综上所述,美洛昔康能改善由CUMS引起的大鼠抑郁行为及皮层神经损伤,可能与其抑制皮层炎症反应,改善单胺神经递质系统功能紊乱相关。
| [1] | Simon G E.Social and economic burden of mood disorders[J].Blol Psychiat,2003,54(3):208-15. |
| [2] | Yiend J,Paykel E,Merritt R,et al. Long term outcome of primary care depression[J].J Affect Disorders,2009,118(1-3):79-86. |
| [3] | Grippo A J,Johnson A K.Stress,depression,and cardiovascular dysregulation:a review of neurobiological mechanisms and the integration of research from preclinical disease models[J].Stress,2009,12(1):1-21. |
| [4] | Maes M,Galecki P,Chang Y S,et al.A review on the oxidative and nitrosative stress (O&NS) pathways in major depression and their possible contribution to the (neuro)degenerative processes in that illness[J].Prog Neuropsychopharmacol Biol Psychiatry,2011,35(3):676-92. |
| [5] | Milatovic D,Montine T J,Aschner M.Prostanoid signaling:dual role for prostaglandin E2 in neurotoxicity[J].Neurotoxicology,2011,32(3):312-9. |
| [6] | Abbasi S H,Hosseini F,Modabbernia A,et al. Effect of celecoxib add-on treatment on symptoms and serum IL-6 concentrations in patients with major depressive disorder:randomized double-blind placebo-controlled study[J].J Affect Disord,2012,141(2-3):308-14. |
| [7] | Miller A H,Maletic V,Raison C L. Inflammation and its discontents:the role of cytokines in the pathophysiology of major depression[J].Biol Psychiatry,2009,65(9):732-41. |
| [8] | 罗 文,马庆阳,韦丽佳,等.美洛昔康对慢性应激大鼠抑郁行为的影响[J].中国药理学通报,2012,28(1):123-7. Luo W,Ma Q Y,Wei L J,el at.Protective effect of meloxicam on CUMS-induced behavioral alterations in rats[J].Chin Pharmacol Bull,2012,28(1):123-7. |
| [9] | Schiepers O J,Wichers M C,Maes M.Cytokines and major depression[J].Prog Neuropsychopharmacol Biol Psychiatry,2005,29(2):201-17. |
| [10] | Jiang P,Zhang W Y,Li H D,et al. Stress and vitamin D:altered vitamin D metabolism in both the hippocampus and myocardium of chronic unpredictable mild stress exposed rats[J].Psychoneuroendocrino,2013,38(10):2091-8. |
| [11] | O'Connor K A,Johnson J D,Hansen M K,et al.Peripheral and central proinflammatory cytokine response to a severe acute stressor[J].Brain Res,2003,991(1-2):123-32. |
| [12] | Milatovic D,Zaja-Milatovic S,Gupta R C,et al.Oxidative damage and neurodegeneration inmanganese-induced neurotoxicity[J].Toxicol Appl Pharmacol,2009,240(2):219-25. |
| [13] | Rosa-Neto P,Diksic M,Okazawa H,et al. Measurement of brain regional alpha-[11C]methyl-L-tryptophan trapping as a measure of serotonin synthesis in medication-free patients with major depression[J].Arch Gen Psychiatry,2004,61(6):556-63. |
| [14] | Meyer J H,McNeely H E,Sagrati S,et al. Elevated putamen D2 receptor binding potential in major depression with motor retardation:an[11C]raclopride positron emission tomography study[J].Am J Psychiatry,2006,163(9):1594-602. |
| [15] | Müller N,Myint A M,Schwarz M J. Inflammatory biomarkers and depression[J].Neurotox Res,2011,19(2):308-18. |
| [16] | Kitagami T,Yamada K,Miura H,et al. Mechanism of systemically injected interferon-alpha impeding monoamine biosynthesis in rats:role of nitric oxide as a signal crossing the blood-brain barrier[J].Brain Res,2003,978(1-2):104-14. |
| [17] | Cavanagh J,Paterson C,McLean J,et al. Tumour necrosis factor blockade mediates altered serotonin transporter availability in rheumatoid arthritis:a clinical,proof-of-concept study[J].Ann Rheum Dis,2010,69(6):1251-2. |

