


心肌肥大(cardiac hypertrophy)是心脏应对长期压力超负荷缓慢产生的一种代偿机制,常伴随蛋白质合成增加、心脏结构重构和细胞器的功能障碍,主要表现为心肌细胞体积增大、胶原纤维形成的肌节增加及胚胎基因的再表达,是先天性心脏病、高血压、心肌梗死、心力衰竭等多种心血管疾病共有的病理过程。自噬(autophagy)是指细胞在自噬相关基因(autophagy related gene,Atg)的调控下,利用溶酶体降解自身受损的蛋白质和细胞器的过程。自噬是生物维持蛋白代谢平衡及细胞环境稳定的共同机制,广泛参与了各种生理和病理过程[1]。研究表明[2, 3],自噬参与调控心肌肥大,但其具体作用及机制目前尚不明确。
G蛋白偶联受体(G protein coupled receptors,GPCRs)/甘油二酯(diacylglycerol,DAG)/蛋白激酶C(protein kinase C,PKC)信号通路在调控心肌肥大的发展进程中发挥非常重要的作用。甘油二脂激酶(diacylglycerol kinase,DGK)是DAG的磷酸激酶,通过磷酸化DAG,减少DAG的可利用性,可以削弱DAG对PKC的激活,是负调节磷脂酰肌醇信号通路的关键信号分子。我们以往的研究显示[4],DGK在心肌组织分布的主要亚型DGK-ζ 明显抑制内皮素1(endothelin-1,ET-1)诱导的心肌肥大,但其机制尚未完全阐明。新近有研究表明,DGK的抑制剂R59022能诱导神经细胞株NG108-15的自噬[5],提示DGK可能通过调节心肌细胞自噬,进而影响心肌肥大。为研究DGK 调节的心肌细胞自噬在心肌肥大中的作用,本实验首先观察了 R59022对ET-1诱导的原代乳鼠心肌细胞肥大的影响,并探讨其可能分子机制。
1 材料与方法 1.1 材料 1.1.1 动物出生1~3 d的清洁级SD大鼠,♀♂不拘,广东省医学实验动物中心提供,许可证:SCXK粤2013-0002。
1.1.2 主要试剂高糖DMEM、胎牛血清(FBS)购自Gibco;ET-1、R59022、5-溴脱氧尿嘧啶核苷(BrdU)、氯喹(chloroquine,CQ)、三甲基腺嘌呤(3-methyl adenine,3-MA)、胰蛋白酶、F-actin-鬼笔环肽等试剂均购自Sigma;雷帕霉素(rapamycin,RAPA)购自上海浩然生物技术有限公司;LC3、beclin-1、p62、p-Akt、Akt 、p-AMPK、AMPK等抗体以及ECL发光液均购自Cell Signaling Technology;β-actin购自Bioworld;逆转录相关试剂购自TaKaRa;PCR引物由Invitrogen公司合成。
1.2 方法 1.2.1 新生大鼠原代心肌细胞分离、培养及药物处理出生1~3 d SD大鼠,无菌开胸取心脏,剪碎,胰酶反复多次消化后,收集消化的心肌细胞悬液,于4 ℃离心收集细胞。用含质量分数为10% FBS的DMEM重悬细胞,差速贴壁法除去贴壁的成纤维细胞,未贴壁的心肌细胞以合适密度接种于细胞培养皿或孔板中,置于细胞培养箱内培养24 h,换无血清培养基饥饿24 h后,以ET-1(10-7 mol·L-1)作用细胞24 h诱导乳鼠心肌细胞肥大,CQ(5 μmol·L-1)、3-MA(5 mmol·L-1)、RAPA(10 nmol·L-1)和R59022(10-5 mol·L-1)分别于加入ET-1前0.5 h加入,以观察其对自噬相关蛋白表达及心肌肥大的影响。
1.2.2 Western blot法检测蛋白表达药物处理后,用RIPA裂解液裂解细胞,提取总蛋白。BCA法测定蛋白浓度后,取等量蛋白行SDS-PAGE凝胶电泳,电泳结束后将蛋白转移至PVDF膜上,剪取目的条带,以脱脂奶粉室温封闭1 h,随后加入LC3、beclin-1、p62、p-Akt、Akt、β-actin一抗4 ℃孵育过夜,TBST洗膜后,室温孵育相应二抗1 h,TBST洗膜后,用ECL试剂盒检测蛋白表达水平,Quantity one软件分析灰度值,以目的条带的灰度值与β-actin的灰度值的比值表示目的蛋白的表达水平。
1.2.3 细胞免疫荧光检测心肌细胞表面积药物处理后,除去培养基,细胞经固定、破膜、封闭后,用TRITC-鬼笔环肽避光孵育以标记F-actin,于荧光显微镜下观察并记录结果。每组随机选取30个细胞,用图像分析软件Image-Pro Plus 6.0计算心肌细胞表面积。
1.2.4 RT-PCR法检测心肌肥大标记物BNP、β-MHC的mRNA表达水平TRIzol裂解细胞提取总RNA,逆转录成cDNA后,取逆转录产物进行PCR扩增,条件:95 ℃变性 3 min,95 ℃ 30 s,55 ℃ 30 s,72 ℃ 30 s,共35个循环,72 ℃ 延伸 10 min。反应完成后,取PCR产物行琼脂糖凝胶电泳(含溴化乙锭0.5 mg·L-1),用BI2000凝胶成像系统分析,以目的基因条带的积分光密度值(IOD)与β-actin的 IOD之比确定目的基因BNP、β-MHC的mRNA表达水平。
1.3 统计学处理结果以x±s表示,用Graph Pad Prism 6.0进行统计学处理,各组间的比较采用One-way AVOVA分析。
2 结果 2.1 ET-1诱导心肌细胞自噬如Fig1所示,给予ET-1分别作用心肌细胞0~12 h,ET-1对自噬相关蛋白LC3-II/I、beclin-1及p62表达没有明显影响,但与0 h相比,ET-1作用细胞24 h明显诱导LC3-II/I、beclin-1表达上调(P<0.05,Fig1A、1B),并使p62表达明显降低(P<0.05,Fig1B);预先给予自噬溶酶体的抑制剂CQ抑制溶酶体降解后,较未经CQ预处理细胞相比,ET-1作用各时间点LC3-II/I的表达有增加趋势,且在24 h明显增加(P<0.01,Fig1A),表明ET-1明显诱导心肌细胞自噬及自噬流。

|
| Fig.1 Effects of ET-1 on expression of autophagy-related proteins(n=3~8) A: Effects of ET-1 on expression of LC3II/I in the presence or absence of CQ pretreatment; B:Effects of ET-1 on expression of beclin-1 and p62. *P < 0.05 vs ET 0 h; #P < 0.05, ##P < 0.01 vs ET+CQ 0 h; △P < 0.05 vs ET 24 h |
如Fig2所示,与control组相比,ET-1明显促进心肌细胞表面积增加(P<0.01,Fig2A)及肥大基因BNP、β-MHC的mRNA表达水平的上调(P<0.01,Fig2B、2C),诱导心肌细胞肥大;自噬抑制剂CQ、3-MA对上述指标发挥明显抑制作用(P<0.01,Fig2A、2B),而自噬激动剂RAPA则发挥明显的促进作用(P<0.01,Fig2A、2C)。提示自噬激活促进ET-1诱导的心肌细胞肥大。

|
| Fig.2 Effects of 3-MA,CQ and RAPA on ET-1-induced myocardial hypertrophy(n=3~4) A: Effects of 3-MA,CQ,RAPA on cardiomyocyte size; B: Effects of 3-MA,CQ on mRNA levels of BNP and β-MHC; C: Effects of RAPA on mRNA levels of BNP and β-MHC. *P<0.05,**P<0.01 vs control; ##P<0.01 vs ET |
如Fig3所示,与control组相比,ET-1作用于心肌细胞24 h,LC3-II/I及beclin-1表达明显上调(P<0.05,P<0.01);R59022预处理明显促进ET-1诱导的上述指标上调(P<0.05,P<0.01)。

|
| Fig.3 Effects of R59022 on expression of autophagy-related proteins(n=6) *P<0.05,**P<0.01 vs control; #P<0.05,##P<0.01 vs ET |
如Fig4所示,R59022预处理促进ET-1诱导的心肌细胞表面积增加(P<0.01,Fig4A)及BNP、β-MHC 的mRNA表达水平的上调(P<0.05,Fig4B),促进ET-1诱导的心肌细胞肥大。

|
| Fig.4 Effects of R59022 on ET-1-induced myocardial hypertrophy(n=3~4) A: Effects of R59022 on cardiomyocyte size; B: Effects of R59022 on mRNA levels of BNP and β-MHC. *P<0.05, **P<0.01 vs control; #P<0.05, ##P<0.01 vs ET. |
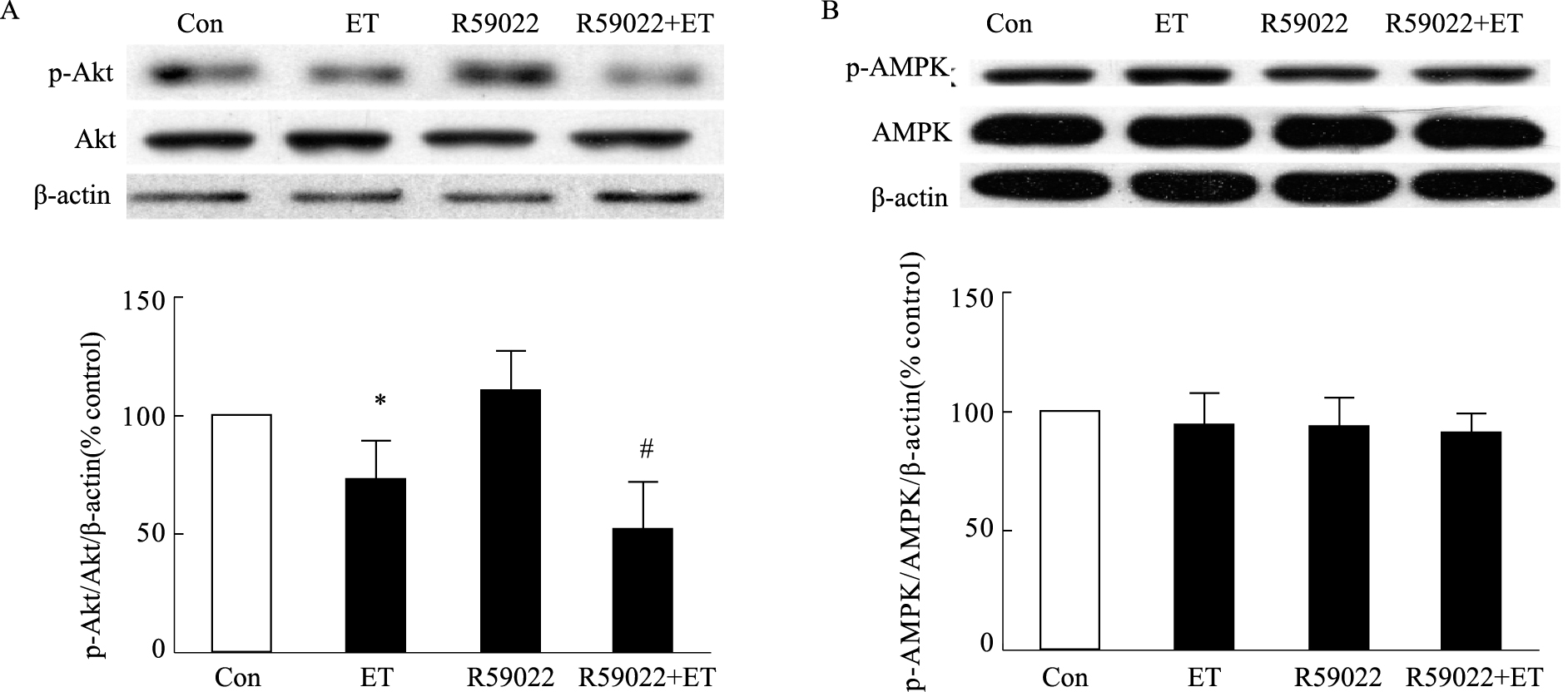
如Fig5所示,与control组相比,ET-1明显下调Akt的磷酸化水平(P<0.05,Fig5A),R59022预处理促进ET-1诱导的Akt磷酸化水平的下调(P<0.05,Fig5A);而对AMPK的磷酸化水平,ET-1及R59022均未见明显影响(P>0.05,Fig5B)。
|
| Fig.5 Effects of R59022 on expression of Akt and AMPK(n=4~5) A:Effects of R59022 on expression of Akt; B: Effects of R59022 on expression of AMPK.*P<0.05 vs control;#P<0.05 vs ET. |
心肌肥大是心肌重构的关键组成部分,是导致心源性猝死和心力衰竭风险明显升高的危险因素[6],其发生机制复杂,目前尚不完全明确。ET-1是公认的促肥大因子[7],通过与其特异性的受体结合,在介导心肌肥大的发生、发展过程中发挥重要作用[8]。本研究结果证实,ET-1作用原代乳鼠心肌细胞24 h明显增大心肌细胞表面积,增加肥大基因BNP、β-MHC 的mRNA表达水平,诱导原代乳鼠心肌细胞肥大。
近年的研究显示,自噬参与调控心肌肥大的发生发展,但其对心肌肥大的具体作用目前尚不明确。有研究认为自噬激活起促进心肌肥大的作用[9],也有研究认为自噬激活对心肌肥大起保护作用[10]。造成自噬在心肌肥大中作用不同,甚至相反的原因可能是疾病的诱因、损伤程度及自噬的水平不同。自噬的发生主要包括三个阶段:第一阶段,自噬诱导因素刺激内质网、高尔基体或细胞膜等形成自噬前体;第二阶段,在Atgs的参与下,自噬前体延伸,包裹需要降解的蛋白质和受损的细胞器,形成自噬体;第三阶段,自噬体与溶酶体结合形成自噬溶酶体,降解产物并参与机体代谢。从自噬前体的形成到内容物降解的整个流程即自噬流(autophagy flux)。在自噬的发展过程中,beclin-1是自噬启动阶段的关键因子,参与调控自噬前体的产生。在自噬被诱导后,由原位于胞质中的LC3I与磷脂酰乙醇胺(phosphatidyl ethanolamine,PE)偶合,形成始终稳定锚定在自噬体膜上的LC3II,标志着自噬体的形成,因此,研究者以往多以beclin-1、LC3蛋白的表达或者以绿色荧光蛋白标记LC3等方法间接反映自噬的活性。然而,自噬体数量的增加不能完全反映自噬的活性,因为造成自噬体数量增加的原因可能是自噬的激活,还可能是自噬溶酶体的降解障碍导致自噬体无法降解而堆积,所以新近研究多以自噬流评价自噬[11, 12]。本研究中,我们检测了自噬标志性蛋白LC3、beclin-1的表达,还检测了可以反映自噬流通畅性的自噬相关蛋白p62,以及通过观察CQ在溶酶体水平阻断自噬的降解后LC3的表达水平来评价自噬水平。结果显示,ET-1明显诱导LC3II/I、beclin-1蛋白表达的增加,促进p62蛋白的降解。并且,在用CQ阻断自噬降解后,LC3II/I的表达水平较未经CQ处理的细胞相比明显增加,提示ET-1诱导心肌肥大过程中明显伴随自噬水平的上调。为了进一步明确自噬在ET-1诱导的心肌细胞肥大过程中的作用,本研究观察了自噬抑制剂3-MA、CQ和自噬激动剂RAPA对ET-1诱导的心肌细胞肥大的影响。结果显示,3-MA、CQ抑制自噬可以明显改善ET-1诱导的心肌细胞肥大,而RAPA激活自噬则进一步促进ET-1诱导的心肌细胞肥大,提示自噬激活参与调节ET-1诱导的乳鼠心肌细胞肥大。
研究表明,Gq介导的磷脂酰肌醇信号通路在心肌肥大的发生、发展中发挥重要作用。DGK是磷脂酰肌醇信号通路的负调节因子,通过磷酸化DAG,可以削弱DAG对该信号通路的激活,在抑制心肌肥大发展过程中可能发挥关键作用,但其具体的胞内信号目前尚不完全清楚。有研究报道,DGK的抑制剂R59022能诱导神经细胞株NG108-15自噬[5]。我们对心肌纤维化的研究结果亦显示[13],DGK参与调节心肌成纤维细胞自噬和纤维化,提示DGK亦可能通过参与调节心肌细胞自噬,进而影响心肌肥大过程。因此,本研究首先观察了DGK的抑制剂R59022对心肌细胞肥大及自噬的影响。我们的结果显示,R59022预处理促进ET-1诱导的心肌细胞肥大,同时对ET-1诱导的自噬相关蛋白LC3II/I、beclin-1的表达水平的上调亦有促进作用,提示R59022可能通过促进心肌细胞自噬,从而促进了ET-1诱导的心肌细胞肥大。
目前已经明确的调控自噬的信号通路主要分为哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)依赖型途径和非mTOR依赖型途径。mTOR作为自噬启动阶段的关键调节因子,其活化后可抑制自噬的发生,是自噬的主要负调控因子[14]。目前认为mTOR信号通路上游的刺激因子主要是胰岛素、生长因子、营养因子、能量以及压力。生长因子和胰岛素的刺激可以激活PI3K,PI3K进一步活化其下游关键效应因子Akt,Akt直接磷酸化mTOR的Ser2448 位点,激活mTOR,从而抑制自噬。磷酸腺苷激活蛋白激酶(AMP-activated kinase,AMPK)则是细胞能量感受的总开关,通过mTOR信号通路和非mTOR信号通路如p53、ULK1[15]、avicin D[16]等调控细胞自噬与凋亡,在细胞的代谢调控中发挥重要作用。本研究结果显示,ET-1诱导乳鼠心肌细胞肥大过程中,Akt的磷酸化水平明显下调,R59022对此有促进作用,但是ET-1和R59022并不影响AMPK的磷酸化水平,提示R59022增强ET-1诱导的心肌细胞自噬促进心肌细胞肥大的机制可能与抑制Akt的激活,从而抑制mTOR通路的活化有关,而AMPK信号可能并不参与R59022的自噬促进作用,但其分子机制尚有待进一步明确。
| [1] | 林超,刘兆国,钱星,等. 自噬在心血管疾病中的作用研究进展[J].中国药理学通报, 2014,30(10):1347-9. Lin C, Liu Z G, Qian X, et al. Research progress on the role of autophagy in cardiovascular diseases[J]. Chin Pharmacol Bull, 2014,30(10):1347-9. |
| [2] | Oyabu J,Yamaguchi O,Hikoso S,et al.Autophagy-mediated degradation is necessary for regression of cardiac hypertrophy during ventricular unloading[J].Biochem Biophys Res Commun,2013,441(4):787-92. |
| [3] | Dai D F,Rabinovitch P.Mitochondrial oxidative stress mediates induction of autophagy and hypertrophy in angiotensin-II treated mouse hearts[J].Autophagy,2011,7(8):917-8. |
| [4] | Huang Y,Zhang H,Shao Z,et al.Suppression of endothelin-1-induced cardiacmyocyte hypertrophy by PPAR agonists:role of diacylglycerol kinase zeta[J].Cardiovasc Res,2011,90(2):267-75. |
| [5] | Takita T,Konuma T,Hanazato M,Inoue H.Diacylglycerol kinase inhibitor R59022-induced autophagy and apoptosis in the neuronal cell line NG108-15[J].Arch Biochem Biophys,2011,509(2):197-201. |
| [6] | Frey N,Olson E N.Cardiac hypertrophy:the good,the bad,and the ugly[J].Annu Rev Physiol,2003,65:45-79. |
| [7] | Li H,Gao S,Ye J,et al.COX-2 is involved in ET-1-induced hypertrophy of neonatal rat cardiomyocytes:role of NFATc3[J].Mol Cell Endocrinol,2014,382(2):998-1006. |
| [8] | 孔令雷,颜玲娣,宫泽辉.内皮素系统与心肌肥厚[J].中国药理学通报,2008,24(9):1127-30. Kong L L,Yan L D,Gong Z H.Endothelins system and myocardial hypertrophy[J].Chin Pharmacol Bull,2008,24(9):1127-30. |
| [9] | Rawat D K,Alzoubi A,Gupte R,et al.Increased reactive oxygen species,metabolic maladaptation,and autophagy contribute to pulmonary arterial hypertension-induced ventricular hypertrophy and diastolic heart failure[J].Hypertension,2014,64(6):1266-74. |
| [10] | Liu C,Xue R,Wu D,et al. REDD1 attenuates cardiac hypertrophy via enhancing autophagy[J].Biochem Biophys Res Commun,2014,454(1):215-20. |
| [11] | Lavandero S, Troncoso R,Rothermel B A,et al.Cardiovascular autophagy:concepts,controversies,and perspectives[J].Autophagy,2013,9(10):1455-66. |
| [12] | Zhang Y,Xu X,Ren J.MTOR overactivation and interrupted autophagy flux in obese hearts:a dicey assembly[J]?Autophagy,2013,9(6):939-41. |
| [13] | 邹刚玲,柳玉梅,张海宁.自噬对AngII诱导的心肌成纤维细胞增殖及迁移的影响及机制[J].广东药学院学报,2015,31(3):407-11. Zou G L,Liu Y M,Zhang H N.Effect of autophagy on AngⅡ-induced proliferation and migration of cardiac fibroblasts[J].J Guangdong Pharm Univ,2015,31(3):407-11. |
| [14] | Mizushima N,Levine B,Cuervo A M,Klionsky D J. Autophagy fights disease through cellular self-digest[J]. Nature,2008,451(7182):1069-75. |
| [15] | Wang S,Song P,Zou M H. AMP-activated protein kinase,stress responses and cardiovascular diseases[J].Clin Sci,2012,122(12):555-73. |
| [16] | Xu Z X,Liang J,Haridas V,et al.A plant triterpenoid,avicin D,induces autophagy by activation of AMP-activated protein kinase[J].Cell Death Differ,2007,14(11):1948-57. |

