


2. 天津市第一中心医院妇产科, 天津 300192
2. Dept of Obstetrics and Gynecology, Tianjin First Central Hospital, Tianjin 300192, China
心肌缺血/再灌注损伤(myocardial ischemia reperfusion injury,I/R)过程中除心肌细胞坏死、凋亡外,血管内皮细胞的损伤也发挥着重要作用。表现为内皮细胞屏障功能障碍、微血管通透性增加、粒细胞浸润、炎性介质释放;同时内皮细胞eNOS表达下降、一氧化氮(nitric oxide,NO)生成减少,导致微血管收缩,参与无复流现象的发生,心肌损伤加重[1]。
本实验室前期研究发现,1-磷酸鞘氨醇(sphingosine-1-phosphate,S1P)具有心血管保护作用,可抑制氧化应激状态下或炎症状态下(血小板活化因子)引起的在体大鼠微血管内皮细胞通透性增加,具有内皮细胞保护作用。S1P后适应抑制炎症反应、拮抗氧化应激、保护线粒体结构功能,减轻大鼠心肌缺血/再灌注损伤,亦可缓解心肌细胞缺氧/复氧(hypoxia/reoxygenation,H/R)损伤[2, 3]。其他实验室研究亦发现,离体大鼠心肌缺血后适应保护作用与内源性S1P有关[4]。但S1P是否对内皮细胞H/R损伤具有保护作用尚未见报道。本实验通过建立人脐静脉内皮细胞HUVEC缺氧/复氧损伤模型,以观察S1P对HUVEC H/R损伤是否具有保护作用,为临床用药提供依据。
1 材料HUVECs 人脐静脉内皮细胞株(上海艾研生物有限公司);S1P(美国Sigma,批号:032M4103V);超敏ECL化学发光试剂盒(批号:20130709)、BCA法蛋白定量试剂盒(批号:20140303)均购自江苏碧云天生物技术研究所;辣根过氧化物酶标记山羊抗兔抗体(批号:970380)、辣根过氧化物酶标记山羊抗小鼠抗体(批号:107724)均购自北京中衫金桥生物技术有限公司;兔抗人Bcl-2多克隆抗体(批号:L1311)、兔抗人Bax多克隆抗体(批号:B2812)、β-actin抗体(批号:E3012)、兔抗人NOS3多克隆抗体(批号:E1413)均购自Santa Cruz公司;Tubulin抗体(江苏碧云天生物技术研究所,批号:AT819-1);Annexin V-PI 双染色流式法细胞凋亡检测试剂盒(美国BD公司,批号:3337788);FACS Calibur型流式细胞仪(美国BD 公司);FV1000荧光显微镜(NIKON公司);ELx800吸收光酶标仪(BioTek公司)。
2 方法 2.1 细胞培养及实验分组HUVECs细胞常规用含10%胎牛血清的DMEM培养基培养于37℃、5% CO2培养箱内。取对数期生长的HUVECs细胞,调整细胞密度为1×108·L-1,均匀接种于板中,24 h后细胞融合至80% 左右。将培养的HUVECs细胞随机分为5组,即正常对照(Control)组、缺氧/复氧(H/R)组、S1P高、中、低剂量组。Control组换无血清的培养基。H/R组首先用模拟缺氧液(NaCl 139 mmol·L-1、KCl 4.7 mmol·L-1、CaCl2 1.0 mmol·L-1、MgCl2 0.5 mmol·L-1、HEPES 5 mmol·L-1、乳酸钠 20 mmol·L-1,pH 6.2)置换正常培养基,放入细胞厌氧培养装置密封,通入95% N2、5% CO2的混合气15 min,密封装置,置于37℃培养箱,缺氧处理16 h后,取出培养板,换用无血清培养基在95% O2+5% CO2的正常培养条件下培养4 h,建立H/R损伤模型。S1P低、中、高剂量组于复氧前加入含S1P(终浓度为2、4、6 μmol·L-1)的无血清培养基,余同H/R组。
2.2 测定指标 2.2.1 细胞存活率细胞缺氧/复氧损伤后,利用MTT法测定490 nm波长下每孔光吸收度值(OD 值),实验重复3次。并按下述公式计算细胞增殖率/%=(各实验组OD值-空白对照组OD值)/ (正常对照组OD值-空白对照组OD值)×100%。
2.2.2 SOD 活性、MDA 含量的检测收集各组HUVECs细胞,按试剂盒说明书操作收集细胞裂解液3 000×g×10 min离心,取上清液,比色法测定MDA含量及SOD活性。
2.2.3 细胞培养液中NO含量测定按实验分组,每组分别取细胞培养液0.1 mL,根据测定试剂盒说明书测NO含量,并按照下述公式计算:NO含量/μmol·L-1=[(测定管OD-空白管OD)/(标准管OD-空白管OD)]×标准品浓度×稀释倍数。
2.2.4 流式细胞仪检测细胞凋亡率各组缺氧/复氧细胞经胰酶消化后,采用Annexin V-PI 双染法对凋亡细胞进行染色,AnnexinV-FITC标记为绿色荧光,PI标记为红色荧光。流式细胞仪测定荧光强度,计算各组凋亡率。
2.2.5 荧光显微镜法检测线粒体膜电位实验结束后,弃培养液,加入JC-1染色工作液,充分混匀。细胞培养箱中37℃孵育20 min。在孵育期间,按照每1 mL JC-1染色缓冲液(5×)加入4 mL蒸馏水的比例,配制适量的JC-1染色缓冲液(1×),并放置于冰浴。37℃孵育结束后,吸除上清,用JC-1染色缓冲液(1×)洗涤2次。加入2 mL细胞培养液。荧光显微镜下观察,并计算红色荧光(激发波长:525 nm,发射波长:590 nm)及绿色荧光(激发波长490 nm,发射波长530 nm)荧光强度。在低膜电位时,JC-1以单体形式存在,产生绿色荧光;高膜电位时,JC-1形成聚合物,发射红色荧光。计算红、绿色荧光强度比值可反映线粒体膜电位变化。
2.2.6 Western blot检测实验结束后,用PBS洗涤细胞,并用适量胰酶消化、收集细胞。应用预冷裂解液冰上裂解细胞30 min,收集蛋白质样品,经BCA蛋白定量、电泳、转膜后用脱脂奶粉封闭2 h以上,加入一抗(tublin稀释度为1 ∶2 000,Bax、Bcl-2、eNOS、β-actin稀释度为1 ∶1 000),4℃摇床过夜,二抗(稀释度为1 ∶2 000)室温孵育1~2 h,再经显影、定影后观察结果并扫描,采用Quantitive软件分析条带的光密度值,计算Bcl-2/Bax、eNOS/tublin的比值。
2.3 统计学处理计量资料以 x±s 表示,采用SPSS 17.0软件对数据进行处理,均数间比较采用单因素方差分析(one-way ANOVA)。
3 结果 3.1 细胞存活率MTT数据显示,经缺氧/复氧处理后,与正常对照组比较,H/R组细胞存活率明显降低(P<0.01),而S1P各个浓度组存活率比H/R组有明显升高,其中中、高浓度组与H/R组比较差异具有显著性(P<0.05,P<0.01),且随S1P浓度增大,HUVEC细胞存活率逐渐上升,见Tab 1。
| ( x±s,n=6) | ||
| Group | Concentration/μmol·L-1 | Cell proliferation rate/% |
| **P<0.01 vs control group; #P<0.05, ##P<0.01 vs H/R group | ||
| Control | - | 100.00±0.00## |
| H/R | - | 68.89±3.56** |
| S1P(L) | 2 | 71.62±7.96** |
| S1P(M) | 4 | 76.68±7.69**# |
| S1P(H) | 6 | 81.88±7.29**## |
与正常对照组比较,H/R组的T-SOD、CuZn-SOD、Mn-SOD活性明显降低(P<0.01);与H/R组相比,S1P各个浓度组均明显升高T-SOD活性(P<0.01)、CuZn-SOD活性(P<0.01)、Mn-SOD活性(P<0.01),见Tab 2。
| ( x±s,n=3) | |||||
| Group | Concentration/μmol·L-1 | T-SOD/kU·L-1 | CuZn-SOD/kU·L-1 | Mn-SOD/kU·L-1 | MDA/nmol·L-1 |
| *P<0.05,**P < 0.01 0.01 vs control group; #P<0.05, ##P<0.01 vs H/R group | |||||
| Control | - | 24.78±1.56## | 11.90±0.73## | 12.87±1.48## | 1.48±0.099## |
| H/R | - | 10.38±1.07** | 5.63±0.37** | 4.76±0.96** | 2.96±0.148** |
| S1P(L) | 2 | 15.22±0.98**## | 8.36±0.93**## | 6.87±0.99**## | 2.52±0.160**# |
| S1P(M) | 4 | 16.19±1.48**## | 8.86±0.45**## | 7.33±1.27**## | 2.30±0.128**# |
| S1P(H) | 6 | 18.76±1.68**## | 9.83±0.57**## | 8.93±1.50**## | 1.70±0.173*## |
与正常对照组比较,H/R组的MDA含量明显升高(P<0.0l);与H/R组相比,S1P各个浓度组均明显降低MDA含量(P<0.05),见Tab 2。
3.4 细胞培养液中NO含量测定H/R组细胞经缺氧/复氧损伤后,NO含量明显降低(P<0.01)。与H/R组相比,S1P低、中、高各个浓度组均明显升高NO含量,且差异具有显著性(P<0.01),见Tab 3。
| ( x±s,n=3) | ||||
| Group | Concentration/μmol·L-1 | NO/μmol·L-1 | Apoptotic rate/% | Mitochondrial membrane potential(red/green) |
| *P<0.05,**P<0.01 vs control group; #P<0.05, ##P<0.01 vs H/R group | ||||
| Control | - | 24.20±1.81## | 8.16±1.27## | 1.27±0.15## |
| H/R | - | 0.93±0.07** | 25.84±4.11** | 0.30±0.07** |
| S1P(L) | 2 | 1.86±0.13**## | 21.48±5.04* | 0.49±0.08** |
| S1P(M) | 4 | 7.45±0.86**## | 17.24±3.84* | 0.62±0.10**# |
| S1P(H) | 6 | 13.04±1.42**## | 12.45±2.09## | 0.83±0.10*## |
与正常对照组比较,H/R组凋亡细胞数量明显增加(P<0.01)。S1P处理的不同浓度组可降低细胞凋亡率,其中高浓度组与H/R组比较差异具有显著性(P<0.01),见Tab 3及Fig 1。

|
| Fig 1 Effect of different concentrations of S1P on apoptosis of HUVECs cells A: Control group; B: H/R group; C: S1P (L) group; D: S1P (M) group; E: S1P (H) group |
荧光显微镜下观察,正常对照组正常细胞被JC-1染色后显示红色荧光,H/R组多数细胞呈绿色荧光,提示线粒体膜电位下降。细胞经S1P各个浓度组处理后,随着药物浓度的增加,HUVECs细胞红色荧光颗粒逐渐增强,绿色荧光颗粒逐渐减少,提高红绿色荧光比值,其中,中、高浓度组与H/R比较差异具有显著性(P<0.05,P<0.01),见Tab 3及Fig 2。
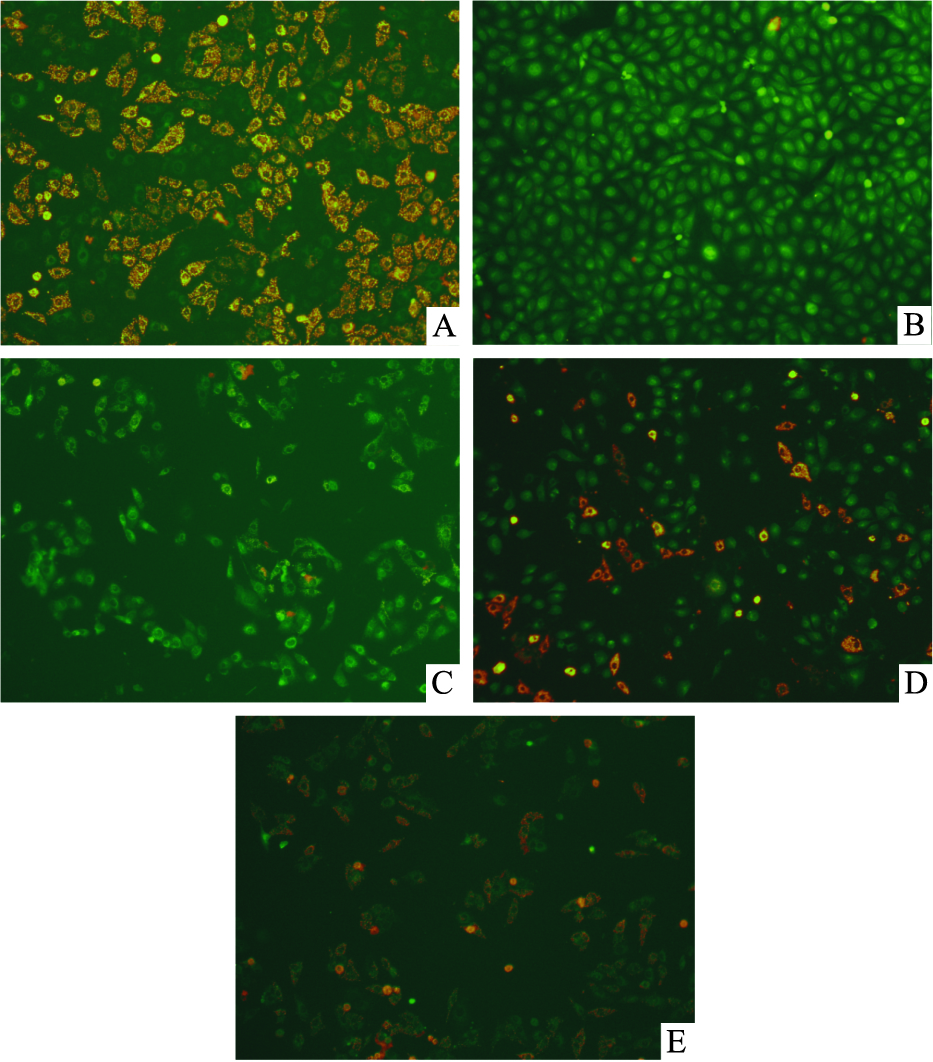
|
| Fig 2 Fluorescence image of HUVEC loaded with JC-1 to determine mitochondrial membrane potential A: Control group; B: H/R group; C: S1P (L) group; D: S1P (M) group; E: S1P (H) group |

|
| Fig 3 Effect of S1P on the expression of Bcl-2/Bax protein in HUVECs cells( x±s,n=3) *P<0.05, **P<0.01 vs control group; #P<0.05 vs H/R group |
与正常对照组比较,H/R组Bcl-2蛋白表达较低,而Bax条带密度较深,Bcl-2/ Bax比值较低。S1P各个浓度组可明显增加Bcl-2表达,降低Bax表达,提高Bcl-2/Bax,见Fig 3。与正常对照组比较,H/R组eNOS表达明显降低,S1P不同浓度组与H/R组比较,eNOS表达明显增多,见Fig 4。

|
| Fig 4 Effect of S1P on the expression of eNOS protein in HUVECs cells( x±s,n=3) *P<0.05, **P<0.01 vs control group;##P<0.01 vs H/R group |
心肌缺血/再灌注损伤过程中同时存在心肌细胞和内皮细胞损伤[1]。本实验前期研究已通过在体大鼠心肌缺血/再灌注损伤模型以及体外心肌缺氧/复氧损伤模型证实,S1P具有心肌细胞保护作用。本研究采用体外内皮细胞模型,观察了S1P对内皮细胞缺氧/复氧损伤的保护作用,研究证实,S1P可提高缺氧/复氧损伤细胞生存率,降低凋亡细胞数量。
eNOS在血管内皮细胞中高度表达,并催化NO的生成,发挥调节血管活性、抗凝血、抗血管增殖等作用。心肌缺血/再灌注时,内皮细胞功能障碍可导致eNOS水平下降、NO等扩血管物质减少,导致血管收缩、血小板黏附聚集,而进一步加重损伤[5]。Roviezzo等[6]研究发现,S1P处理牛胸主动脉后,能够引起Akt介导的eNOS表达上调以及NO的大量产生。本实验研究也证实,S1P处理后可上调内皮细胞eNOS表达水平,增加内皮细胞NO生成,减轻内皮细胞损伤。
内皮细胞缺氧/复氧损伤与多种因素密切相关,其中氧化应激是重要因素之一。细胞再给氧过程中,大量活性氧自由基(ractive oxygen species,ROS)产生超过了内源性抗氧化物质的清除能力,ROS可引起线粒体内细胞色素C释放,进而诱导凋亡发生[7, 8]。SOD为机体内源性抗氧化物质,可分为主要位于线粒体的Mn-SOD及位于胞质的Cu/Zn-SOD[9]。本研究证实,S1P可提高细胞3种SOD活性,并可降低细胞膜脂质过氧化反应的主要产物MDA含量,提示S1P的抗内皮细胞缺氧/复氧损伤作用可能与其抗氧化应激作用有关。
缺氧/复氧损伤过程中,内皮细胞发生明显凋亡现象。细胞凋亡的机制主要包括死亡受体途径以及线粒体途径两种。其中,线粒体发挥着重要的作用,细胞缺氧/复氧损伤过程中,氧化应激、钙超负荷可导致线粒体通透性转换孔开放、线粒体膜电位下降、线粒体肿胀、线粒体外膜破裂[10]。而细胞的存活与Bcl-2家族中抗凋亡成分与促凋亡成分的比率密切相关[11]。Bax是促凋亡基因,Bcl-2是抑制凋亡基因。后者主要作用为分布于线粒体外膜,抑制细胞色素C释放,并维持线粒体外膜完整性[12],同时也有研究证实,Bcl-2可通过抗氧化作用抑制氧化应激诱导的凋亡[13]。Bax正常情况下主要位于胞质,在凋亡信号诱导后易位至线粒体,诱导特异性通透孔道形成,导致促凋亡因子(细胞色素C、凋亡诱导因子等)释放增加,诱导凋亡形成[14]。本研究采用JC-1荧光染色方法观察了细胞线粒体膜电位的变化。该荧光的强弱或颜色变化可以反映线粒体膜电位的增高或降低[15]。研究表明,S1P可抑制缺氧/复氧损伤引起的线粒体膜电位下降。同时关于Bcl-2及Bax表达的检测证实,S1P可增加Bcl-2的表达,降低Bax的表达,提高Bcl-2/Bax的比率。
综上所述,S1P可能通过增强抗凋亡蛋白Bcl-2表达、抑制线粒体膜电位下降、抗氧化应激作用减少内皮细胞缺氧/复氧损伤。
| [1] | Akpinar T S, Ozkok A, Kose M, et al. Endothelial constitutive nitric oxide synthase, angiotensin converting enzyme, angiotensin II type 1 receptor gene polymorphisms adendothelial functions in healthy individuals[J]. Eur Rev Med Pharmacol Sci, 2014, 18(2):39-45. |
| [2] | 贺 苗, 赵 杰, 苏 健, 等. 1-磷酸鞘氨醇后适应对大鼠心肌缺血/再灌注损伤的保护作用[J]. 中国药理学通报, 2013, 29(10):1369-73.He M, Zhao J, Su J, et al. Protective effect of sphingosine 1-phosphate postconditioning on myocardial ischemia/reperfusion injury in rats[J]. Chin Pharmacol Bull, 2013, 29(10):1369-73. |
| [3] | 郑新彬, 温 克, 高卫真, 等. 1-磷酸鞘氨醇后适应对H9c2心肌细胞缺氧/复氧损伤的保护作用[J]. 中国现代应用药学, 2014, 31(1):1-5.Zheng X B, Wen K, Gao W Z, et al. Protective effects of sphingosine-1-phosphate postconditioning on hypoxia/reoxygenation injury in rat H9c2 cardiomyocytes[J]. Chin J Mod Appl Pharm, 2014, 31(1):1-5. |
| [4] | Vessey D A, Li L, Honbo N, et al. Sphingosine1-phosphateis an important endogenous cardioprotectant released by ischemic pre-and postconditioning[J]. Am J Physiol Heart Circ Physiol,2009, 297(4):H1429-35. |
| [5] | Xuan Y T, Tang X L, Qiu Y, et al. Biphasic response of cardiac NO synthase isoforms to ischemic preconditioning in conscious rabbits[J]. Am J Physiol Heart Circ Physiol, 2000, 279(5):H2360-71. |
| [6] | Roviezzo F, De Angelis A, De Gruttola L, et al. Involvement of proteinase activated receptor-2 in the vascular response to sphingosine 1-phosphate[J].Clin Sci (Lond), 2014, 26(8):545-56. |
| [7] | Jayakumar T, Chang C C, Lin S L, et al. Brazilin ameliorates high glucose-induced vascular inflammation via inhibiting ROS and cams production in human umbilical vein endothelial cells[J]. Bio Med Res Int, 2014, 403703. |
| [8] | Balasubramanian T, Senthilkumar G P, Karthikeyan M, et al. Protective effect of ethyl acetate fraction of stereospermum suaveolens against hepatic oxidative stress in STZ diabetic rats[J]. Tradit Complement Med, 2013, 3(3):175-81. |
| [9] | Brouwer M, Hoexum Brouwer T, Grater W, et al. Replacement of a cytosolic copper/zinc superoxide dismutase by a novel cytosolic manganese superoxide dismutase in crustaceans that use copper (haemocyanin) for oxygen transport[J]. Biochem,2003, 374(1):219-28. |
| [10] | Kadenbach B,Ramzan R,Moosdorf R,et al.The role of mitochondrial membrane potential in ischemic heart failure[J].Mitochondrion,2011, 11(5):700-6. |
| [11] | Juin P, Geneste O, Gautier F, et al. Decoding and unlocking the BCL-2 dependency of cancer cells[J]. Nat Rev Cancer, 2013, 13(7):455-65. |
| [12] | Ulukaya E, Acilan C, Yilmaz Y.Apoptosis:why and how does it occur in biology[J].Cell Biochem Funct,2011,29(6):468-80. |
| [13] | Hockenbery D M, Oltvai Z N, Yin X M, et al. Bcl-2 functions in an antioxidant pathway to prevent apoptosis[J]. Cell, 1993, 75(2):241-51. |
| [14] | Czabotar P E, Lessene G, Strasser A. Control of apoptosis by the BCL-2 protein family:implications for physiology and therapy[J]. Nat Rev Mol Cell Biol, 2014, 15(1):49-63. |
| [15] | Liu X, Sun C, Jin X, et al. Genistein enhances the radiosensitivity of breast cancer cells via G2/M cell cycle arrest and apoptosis[J]. Molecules, 2013, 18(11):13200-17. |

