


 , HAN Li-wen, WANG Xi-min, WANG Rong-chun, HOU Hai-rong, LIU Ke-chun
, HAN Li-wen, WANG Xi-min, WANG Rong-chun, HOU Hai-rong, LIU Ke-chun
 , PENG Wei-bing, SUN Chen, HAN jian
, PENG Wei-bing, SUN Chen, HAN jian
乳腺癌是发生在乳腺腺上皮组织的恶性肿瘤。全球乳腺癌发病率自20世纪70年代末开始一直呈上升趋势。据《2012中国肿瘤登记年报》公布的乳腺癌发病数据显示:全国肿瘤登记地区乳腺癌发病率位居女性恶性肿瘤的第1位,女性乳腺癌发病率(粗率)全国合计为42.55/10万。经过30多年的研究,斑马鱼已经成为一种公认的模式动物,由于其繁殖周期短、胚胎早期透明、并在系统的发育、功能及疾病模型方面取到了丰富的研究结果[1, 2],近几年斑马鱼的移植瘤动物模型在国际上刚刚兴起,尤其是移植瘤在肿瘤迁移机制的研究方面成为了广泛接受的模型。利用微量注射的方法,将人/鼠肿瘤移植入斑马鱼的腹腔中[3, 4],这种新模型在肿瘤增殖机制、肿瘤迁移基因研究、药物活性评价等方面都有报道,这些探索性的研究对高通量筛选提供了新的工具和新的研究思路,对新药的发掘具有重大的意义。本文研究建立以斑马鱼为动物载体,建立斑马鱼乳腺癌移植瘤模型,并对模型的生长特性、促血管生成、相关蛋白表达及抑制剂的作用进行初步的研究。
1 材料与方法 1.1 实验动物及瘤株实验瘤株:乳腺癌MCF-7由自中国海洋大学惠赠,乳腺癌T-47D与MDA-MB-231均为聊城大学惠赠,冻存细胞复苏后,传代,常规培养于细胞培养箱37℃备用。实验动物:选用野生型AB型斑马鱼与血管荧光转基因斑马鱼Tg(VEGFR2: GFP),系山东省科学院斑马鱼药物筛选平台提供。
1.2 实验仪器与耗材L-15、DMEM培养基与新鲜牛血清购自(GIBCO,批号分别为1300045、1122050;0.25%胰酶-EDTA购自GIBCO(批号为1535318),青霉素钠与链霉素购自上海生工,酪氨酸酶抑制剂PTK787(Vatalanib)及麻醉剂三卡因(A5040)购自SIGMA- ALDRICH;JAK抑制剂tofacitinib(S500105)购自Selleck,脱膜剂pronase E购自Solarbio,CM-DiL活细胞染色剂(C7000,Invitrogen);微量注射仪ZGENEBIO PCO-1500购自力钧生物科技有限公司,激光扫描共聚焦显微镜FV-1000来自OLYMPUS,伯乐 Chemiodc XPS化学发光凝胶成像系统,无菌操作台SW-CJ-2来自苏州AIRTECH,5804R离心机由Eeppendorf提供,体视显微镜选用重庆光学仪器公司ZSA302。
2 方法 2.1 斑马鱼胚胎的获取选用成熟♀♂斑马鱼分开喂养,照明14 h/黑暗10 h交替进行,定时饲喂混合饵料;采胚胎时,取性成熟斑马鱼,按照♀ ∶♂=1 ∶1~3放入交配缸中,于次日10时获得受精卵。对受精卵进行消毒和清洗后,加入斑马鱼胚胎培养用水中,置于28℃光照培养箱待用。
2.2 乳腺癌细胞系微量注射前准备在受精卵发育24 h时,使用1 g·L-1 Pronase E溶液脱去卵膜。在体视显微镜下挑选正常的斑马鱼胚胎,备用。无菌条件下将培养瓶中乳腺癌细胞除去培养基,PBS清洗2次后,加入胰酶消化,加入培养基终止消化,离心后换新的培养基,每毫升细胞悬液加入活细胞染色剂CM-DiL 7.5 μL,37℃孵育5 min,然后在冰箱4℃孵育15 min,离心除去上清液,PBS清洗2次后,加入无血清培养基复悬,镜下调整细胞密度达到3×108·L-1。
2.3 微量注射条件参照Yong-Teng的实验方法[5],选用新配制0.03%苯硫脲(抑制色素形成)孵育48 h pf的斑马鱼胚胎准备微量注射,加入适量三卡因轻度麻醉,放置在体视显微镜下,将不同浓度CM-dil染色后的乳腺癌细胞注射于胚胎卵黄囊后部,约0.05~0.2 μL,注射后斑马鱼用无菌水清洗,放入28℃培养箱。6 h后将死亡斑马鱼吸出,随机分为模型组(micro-injection,micro-IJ)与用药组,用药组分别加入血管生成抑制剂PTK787或者JAK抑制剂tofacitinib,药物处理48 h后,将幼鱼麻醉后在共聚焦镜下拍照,并用FV-10软件分析红色肿瘤细胞光密度(optical density,OD)。
2.4 统计学方法肠下静脉分析方法:参照文献方法改进[4],对肿瘤引起的对肠下静脉进行拍照,并用FV-10软件测量肠下静脉面积。移植瘤迁移评价方法:参照Ghotra等[6]的试验方法进行了改进,以斑马鱼卵黄囊后1/3处注射点为原点,按照周边移植瘤划出直线距离,利用软件Image J 1.43测量各个迁移细胞的迁移距离,计算总距离,数据用Graphpad prism 5.0处理。各组幼鱼逐条检测剔除失败样本。
2.5 Western blot分析在荧光镜下计数结束后,取出斑马鱼,鱼体粉碎匀浆,加入组织蛋白提取液,匀浆后冰浴静置20 min,然后4℃离心10 min,得上清液为蛋白提取液。分光光度计测定蛋白量,取30 μg蛋白提取液,按照体积1 ∶1加入上样缓冲液,进行SDS聚丙烯酰胺凝胶电泳。然后把分离后的蛋白质转移到PVDF膜上,5%的脱脂奶粉室温封闭1 h。与兔抗鼠HER2 抗体(1 ∶1 000) 4℃过夜孵育。TBST洗涤后,加入羊抗兔IgG二抗(1 ∶8 000)室温孵育1 h。TBST充分洗涤2次后,ECL显色,在化学发光成像系统拍照。利用Image J软件测条带灰度值,计算目的蛋白HER2的灰度比值。p53、VEGFa和β-actin的检测方法过程与HER2相同。
2.6 数据统计应用SPSS13.0对实验所得数据进行组间t检验。
3 结果 3.1 乳腺癌细胞斑马鱼移植瘤成瘤性的生长特点斑马鱼微量注射乳腺癌细胞48 h后,各组死亡率介于5%~15.7%,低于文献报道0.3~0.4[7];不同细胞系每个胚胎50~200个肿瘤细胞注射完毕后,移植成功率随数量增加而增加,在200/只时造模成功比例超过0.90。各模型呈现出不同的迁移规律:MCF-7呈现全身分布,在卵黄尾部与主动脉区域有分布;T-47D的分布较为局限,主要在卵黄区域及心脏分布;MDA-MB-231在斑马鱼胚胎全身均有分布,主要在循环系统附近分布。
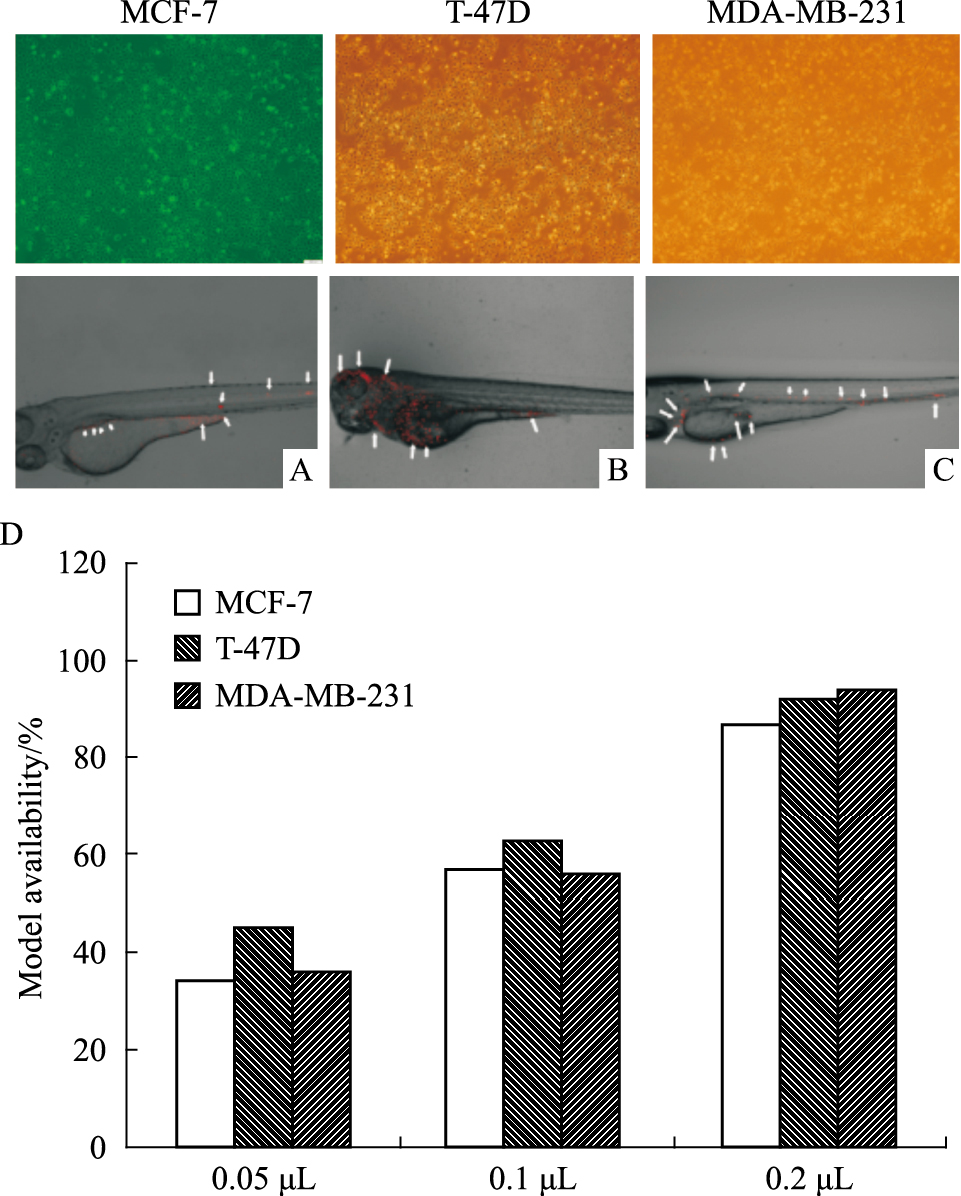
|
| Fig 1 Modeling of human breast cancer in zebrafish A:MCF-7 cell and xenograft larva;B:T-47D cell and xenograft larva;C:MDA-MB-231cell and xenograft larva;D:Model availability rate |
模型组在微注射48 h后,模型组镜下可见MB-231红色肿瘤细胞在胚胎各个器官均有分布,较集中于卵黄部、卵黄延伸部,少量分布于头部;用药组红色肿瘤细胞全身分布的情况消失,红色细胞量减少且分布区域局限,或者仅局限于卵黄延伸部(Fig 2C、D);OD值显示micro-IJ组与0.04/0.06 mmol·L-1 tofacitinib组比较在细胞数量及分布距离差异均具有显著性(P < 0.01)。
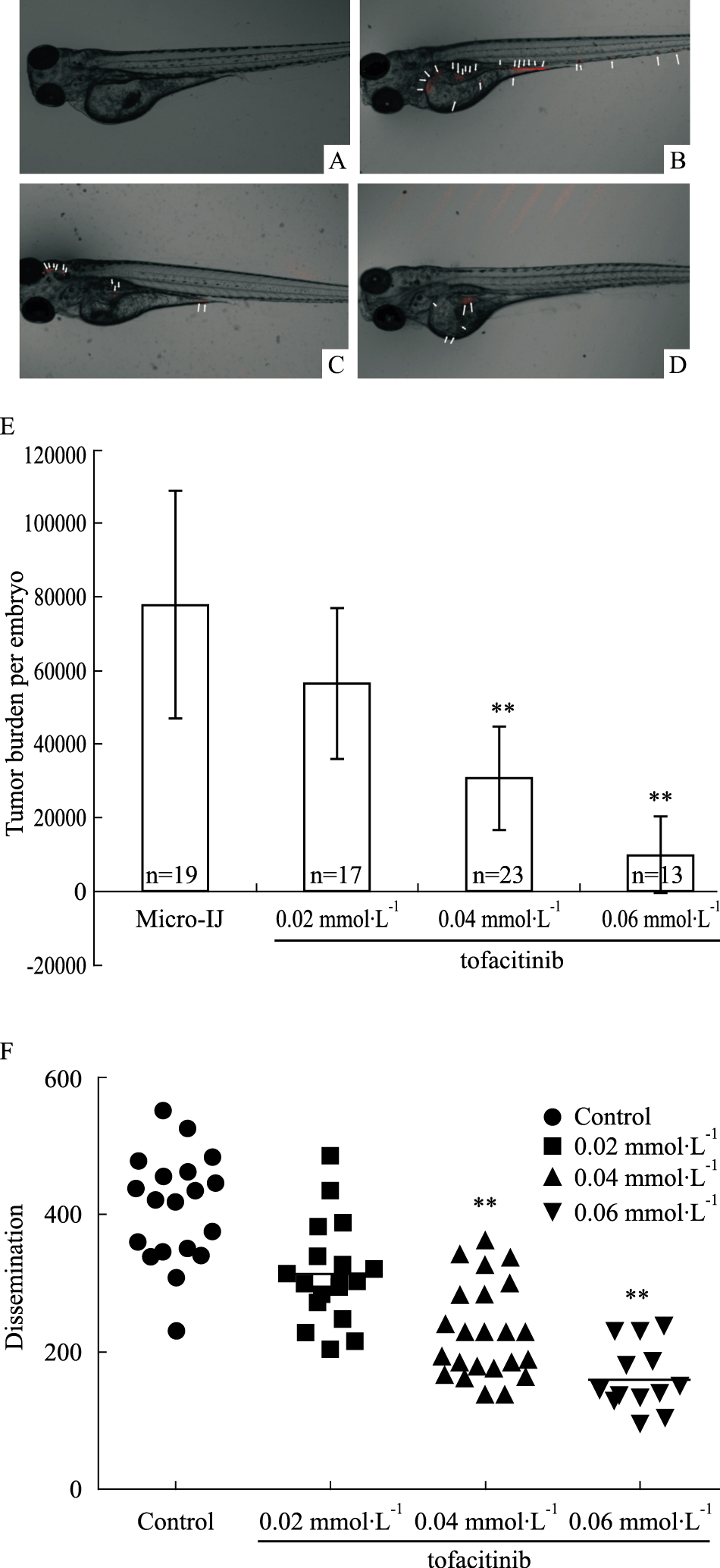
|
| Fig 2 Xenografts in zebrafish larva after treatmentwith different concentrations of tofacitinib(x±s) A:Zebrafish larva vehicle;B:Micro-IJ group;C,D:Xenograft larva treated with 10 mg·L-1/20 mg·L-1 tofacitinib. White arrow indicates MB-231 cell. E:Four group showed different tumor burden;F:Four groups dissemination was different from Micro-IJ; **P<0.01 vs micro-IJ group |
共聚焦镜下观察显示:正常对照组肠下静脉呈弓形,栅栏状,连续无分支,有少量出芽;微量注射模型组显示肠下静脉有明显增生,静脉弯曲延长,出现侧枝与分支,部分区域呈网状结构,同时可见鱼体内红色肿瘤细胞;与模型组比较,PTK787组肠下静脉丛OD明显减少,出芽及侧枝数量减少,用药组模型组与空白对照组、用药组比较差异有显著性(Fig 3D)。

|
| Fig 3 Lateral view of xenograft TG zebrafish showing SIVsafter treatment with PTK787 pass micro-IJ 48 h A:Vehicle-treated TG zebrafish at 120 hpf;B:Xenograft TG zebrafish larva at 120 hpf;C:Xenograft TG zebrafish larva treated with 4 mg·L-1 PTK787. White arrow indicates cancer cell, red arrow shows SIVs; **P<0.01 vs micro-IJ group |
Western blot结果显示,HER2高表达乳腺癌细胞T-47D细胞移植进入斑马鱼胚胎后,虽然AB胚胎在4 d自身有HER2表达,在T-47D细胞移植进入后,HER2表达量增加;MB-231细胞系移植后,VEGFa的量增加;在tofacitinib处理后的移植瘤胚胎,其p53表达量明显增加。
4 讨论目前采用的乳腺癌的小鼠/大鼠模型是最经典的动物疾病模型,但是其成本高,周期长,需要辅助雌激素缓释刺激成瘤,操作繁琐[8, 9];乳腺癌的体外实验虽然操作简便,成本低,但与肿瘤体内增殖,迁移的规律差异较大,作为在体实验的有益补充。斑马鱼移植瘤模型是近年来移植瘤模型研究热点,在药物研究中已经得到了广泛的应用[10, 11, 12],斑马鱼移植肿瘤模型具有成本较低、实验周期短(4~7 d),受精后1周内无明显免疫系统排异反应[13],移植癌细胞清晰可见等优点;目前斑马鱼肿瘤移植主要采用胚胎期的幼鱼,并多见于肿瘤细胞迁移相关基因功能研究与抗肿瘤的药物筛选研究[14];该模型兼顾了在体模型与体外实验的优势,减少了时间和成本,并满足了肿瘤在体微环境的要求。
在本研究发现不同类型的乳腺癌细胞在斑马鱼体内均能生长良好,但在迁移特性方面差异较大:MDA-231、MCF-7肿瘤细胞具有较强的迁移性,注射后48 h在胚胎多个部位有出现,与文献实验结果相似[15];而T-47D肿瘤细胞迁移则不明显,从本实验结果验证了移植瘤癌模型建立的成功率与细胞数量有关系,与较早的报道相同[16],细胞系自身特性对斑马鱼体内肿瘤细胞的的迁移有直接影响。
乳腺癌HER2高表达和乳腺癌低生存率间有显著的关联,HER2基因在乳腺癌细胞中的表达水平是乳腺癌的诊断指标和预后的一个重要标志物[17, 18]。而从Western blot实验结果发现,HER2在斑马鱼胚胎早期发育阶段有表达,从受精后10h至成年均有表达,而且在鱼鳍、神经系统及鳍再生中发挥重要作用[19],本实验结果提示HER2高表达的T-47D细胞移植后可增加斑马鱼HER2表达。同样人源肿瘤细胞的进入鱼体后促进SIVs的数量明显性的增加,并且VEGF的表达增强;同时斑马鱼模型的标记VEGFR2荧光血管数量增加,从而反应出VEGFR2表达也增强,说明移植瘤对VEGF配体/受体具有同时增强的作用,其对血管生成的促进作用强于单个促血管生成因子的实验作用,而且这种作用可被酪氨酸酶抑制剂PTK787抑制。研究发现JAK1或JAK2敲除的人源癌细胞在斑马鱼体内的迁移能力都会变弱[5],在本实验中发现JAK抑制剂确实能够抑制细胞的迁移,同时它可减少鱼体内移植肿瘤细胞数量,并增强p53表达,表明tofacitinib除了对JAK/stat3通路有抑制作用外,抑制在体肿瘤细胞的作用与p53通路有关。

|
| Fig 4 Western blot assay of zebrafish xenografts 48 h after injection A:Western blot assay of HER2 from AB and T-47D xenografts; B: Western blot assay of VEGFa from AB and MB-231 xenografts;C:Western blot assay of p53 from AB Zebrafish larva treated with tofacitinib |
斑马鱼移植瘤模型的制作方法简便、重复性佳、周期短,其自身比例0.80基因与人具有保守性[20],在多种癌细胞的迁移研究和药物活性评价方面有独特优势,虽然斑马鱼胚胎移植瘤无乳腺组织,无法做到组织器官发病,但肿瘤细胞在斑马鱼胚胎中的存活、促血管生成、迁移特征、及相关分子的表达都具有较高相似度;同时肿瘤标志物的相关因子如VEGF、HER2等重要靶点与人类有较高的保守性,对于靶点药物的评价展示了良好的适用性,因而在抗肿瘤的应用研究中得到认可,从目前的研究来看,随着该模型的不断深入研究,作为移植瘤模型其具有广阔的研究价值,并且在药物筛选方面具有独特的优势。
(致谢:本文所有试验均在山东省科学院生物研究所药物筛选室及生物公共实验平台完成并感谢中国海洋大学医药学院和聊城大学生物研究中心提供细胞系。)
| [1] | Rubinstein A L. Zebrafish:From disease modeling to drug discovery[J].Drug Discov Devel,2003,6(2):218-23. |
| [2] | Murphey R D,Zon L I. Small molecule screening in the zebrafish[J].Methods,2006,39(3):255-61. |
| [3] | van der Ent W, Burrello C, Feunisse A F,et al. Modeling of human uveal melanoma in zbrafish xenograft embryos[J].Invest Ophthalmol Vis Sci,2014, 55(10):6612-22. |
| [4] | Stefania N, Marco P. The zebrafish/tumor xenograft angiogenesis assay[J]. NAT protocols, 2007, 2(11):2918-23. |
| [5] | Yong T, Xie X Y, Steven W, et al. Evaluating human cancer cell metastasis in zebrafish[J].BMC Cancer,2013,13:453-65. |
| [6] | Ghotra V P, He S, de Bont H, et al. Automated whole animal bio-imaging assay for human cancer dissemination[J].PLoS One,2012,7:e31281. |
| [7] | Karni S M, Karine F L, Jamil H, et al. Discriminating different cancer cells using a zebrafish in vivo assay[J].Cancers,2011,3:4102-13. |
| [8] | Villanueva M T. A mouse model for metaplastic breast carcinoma[J].Nature Rev Cancer,2015,15(8):456-69. |
| [9] | Fantozzi A,Christofori G. Mouse models of breast cancer metastasis[J].Breast Cancer Res,2006,8(4):212. |
| [10] | Astin J W, Jamieson S M, Eng T C,et al. An in vivo antilymphatic screen in zebrafish identifies novel inhibitors of mammalian lymphangiogenesis and lymphatic-mediated metastasis[J].Mol Cancer Ther,2014,13(10):2450-62. |
| [11] | Bansal N, Davis S, Tereshchenko I,et al.Nrichment of human prostate cancer cells with tumor initiating properties in mouse and zebrafish xenografts by differential adhesion[J].Prostate,2014,74(2):187-200. |
| [12] | 陈锡强,程丽芳,徐新刚.熊果酸对斑马鱼血管生成及斑马鱼移植癌的抑制作用[J].中国药理学通报,2015,31(7):1004-8. Chen X Q, Cheng L F, Xu X G.et al. Inhibition of ursolic acid on angiogenesis and xenografts in zebrafish(danio rerio)[J].Chin Pharmacol Bull,2015,31(7):1004-8. |
| [13] | Lam S H,Chua H L,Gong Z, et al.Development and maturation of the immune system in zebrafish, Danio rerio:a gene expression profiling, in situ hybridization and immunological study[J].Dev Comp Immunol, 2004, 28:9-28. |
| [14] | Lee H W, Park Y M, Lee S J,et al.Alpha-smooth muscle actin (ACTA2) is required for metastatic potential of human lung adenocarcinoma[J].Clin Cancer Res,2013,19(21):5879-89. |
| [15] | van der Ent W, Burrello C, Teunisse A F,et al. Modeling of human uveal melanoma in zebrafis xenograft embryos[J].Invest Ophthamol Vis Sci,2014,55(10):6612-22. |
| [16] | Yang X J, Chen G L,Yu S C, et al.TGF-β1 enhances tumor-induced angiogenesis via JNK pathway and macrophage in ltration in an improved zebra sh embryo/xenograft glioma model[J].Intern Immunopharmacol,2013,15:191-8. |
| [17] | Olayioye M A,Neve R M,Lane H A.The erbb signaling network:receptor heterodimerization in development and cancer[J].EMBO,2000,19(13):3159-67. |
| [18] | Mai P, Hoang. M D, Aysegul A,et al. With HER2/neu protein overexpression and inter observer invasive breast carcinomar[J].Am J Clin Pathol, 2000,113(6):852-9. |
| [19] | Lyons D A,Pogoda H M,Voas M G, et al. erbb3 and erbb2 are essential for schwann cell migration and myelination in zebrafish[J].Curr Biol,2005,15(6):513-24. |
| [20] | Howe K, Clark M D, Torroja C F,et al.The zebrafish reference genome sequence and its relationship to the human genome[J].Nature,2013,496(7446):498-503. |