


2. 湖南省中药粉体与创新药物省部共建国家重点实验室培育基地, 湖南 长沙 410208
2. Training Bases, Hunan Key Laboratory of Chinese Materia Medica Powder and Innovative Drugs Established by Provincel and Ministry, Changsha 410208, China
近年国外研究表明[1, 2, 3, 4]:Nrf2/HO-1信号途径激活在血管新生中发挥重要作用,是一个新型调控血管新生的潜在靶点。补阳还五汤精简方是课题组在多年临床经验的基础上,遵循补阳还五汤之方义,基于益气祛瘀生新法精简方药,并且配合醇提、超临界CO2提取工艺制备而成。前期实验对精简方进行最佳给药剂量筛选,结果表明精简方中剂量(2.41 g·kg-1·d-1)可明显改善其神经功能缺失症状,恢复体质量,减小脑梗死面积,减轻脑组织水肿[5, 6]。本研究在前期研究基础上观察该剂量补阳还五汤精简方对大鼠脑缺血损伤后不同时点血管新生的作用,并从核转录因子E2相关因子2(Nrf2)/血红素加氧酶-1(HO-1)途径研究其作用机制。该研究为补阳还五汤精简方的后期新药申报工作奠定前期实验基础,为中药的药效分子机制研究思路提供参考。
1 材料 1.1 实验动物SPF级SD大鼠,体质量250~280 g,♂,北京维通利华实验动物技术有限公司,动物合格证号:SCXK(京)2012-0001。
1.2 药物补阳还五汤处方(生黄芪120 g、当归尾6 g、川芎3 g、红花3 g、赤芍4.5 g、桃仁3 g、地龙3 g)和补阳还五汤精简方处方(黄芪30 g、川芎9 g、地龙6 g)中所有原药材经鉴定均符合2010版《中国药典》的有关规定,补阳还五汤按传统水煎后浓缩干燥制备成干浸膏(每1 g干浸膏相当于原生药4.5 g),补阳还五汤精简方干浸膏由湖南中医药研究院中药所完成并提供(每1 g干浸膏相当于原生药4.7 g)。
1.3 主要试剂兔抗大鼠Nrf2多克隆抗体(批号:Ab137550) ,兔抗大鼠HO-1多克隆抗体(批号:Ab13248)购自Abcam公司。兔抗大鼠GAPDH多克隆抗体(批号:5471)购自上海拜力生物科技有限公司。兔抗大鼠vWF多克隆抗体(批号:0612)、辣根过氧化物酶标记的山羊抗兔IgG(批号:A0208)购自北京中杉金桥生物技术有限公司。SYBRGreenPCR试剂盒(批号F-415XL)、反转录试剂盒(批号#K1622)购自Thermo科技有限公司。
1.4 主要仪器Multiscan MK3酶标仪由芬兰雷勃公司提供,Finesse 325型石蜡切片机由英国Shando公司提供,Bx51光学显微镜及IPP6.0图像分析系统由日本Olympus公司生产提供。2400PCR 扩增仪(PE)、实时荧光定量PCR 仪、芬兰雷勃酶标仪(型号MK3)、电泳仪(型号mini protean 3 cell)由美国BIO-RAD 公司提供。
2 方法 2.1 模型制备参考改良Nagasawa等[7]线栓法复制大鼠局灶性脑缺血模型,假手术组仅切开皮肤、分离左侧颈总动脉后随即缝合。动物清醒2 h后参照Longal等[8]及Bedersont等[9]的5分制法进行神经功能评分,分值在1~3分者入组。评分越高,神经功能缺损越严重。剔除标准:评分低于1分;蛛网膜下腔出血;HE染色无脑缺血病理改变;未到时间点死亡。因大鼠死亡等致样本量不足时随机替补。
2.2 实验分组与处理除假手术组外,将造模成功后大鼠随机分为模型组、补阳还五汤组、补阳还五汤精简方组,每组30只,每组按3个时间点分别于首次给药后d 1、d 3、d 7处死,每个时间点10只。给药组于术后2 h给药,补阳还五汤组按成人等效剂量3.15 g·kg-1·d-1、补阳还五汤精简方组按2.41 g·kg-1·d-1药液灌胃。给药体积4 mL·kg-1。模型组和假手术组均给予等体积生理盐水。
2.3 免疫组化方法检测大鼠脑组织vWF表达及微血管密度(MVD)测定每组每个时间点5只大鼠,10%水合氯醛麻醉后断头取脑,4%多聚甲醛固定。各组组织切片一抗用兔抗大鼠vWF多克隆抗体(1 ∶100),阴性对照用PBS替代,4℃冰箱孵育过夜,用生物素标记的二抗在室温孵育30 min,DAB显色。每只动物取切片5张,最后采用Image pro-plus16.0成像分析系统分析光镜高倍(×400)下每张免疫组化切片相同部位拍照。vWF染色阳性表现为血管内皮细胞膜出现棕黄色颗粒者,1个血管计数以内皮细胞簇者为标准,管腔直径大于8个红细胞直径之和或肌层较厚的血管予以剔除。于缺血区内6个高倍视野(×400)镜下进行血管计数,其均数为该切片的微血管密度[10, 11]。
2.4 Real-Time PCR检测大鼠脑组织Nrf2及HO-1mRNA表达大鼠麻醉后断头处死,在冰盘上快速取出大鼠海马,按TRIzol试剂盒说明的步骤提取总RNA,通过紫外分光光度计测定RNA浓度,电泳查看RNA 的完整性。按照反转录试剂盒合成cDNA。将制备好的cDNA进行PCR扩增,PCR扩增所用的寡核苷酸物序列由上海生工生物工程公司合成。PCR 扩增反应体系(25 μL):SYBR Green Mix(12.5 μL)、上游引物F(0.5 μL)、下游引物R(0.5 μL)、ddH2O(9.5 μL)、cDNA 模板(2 μL)。反应条件:95℃、10 min;95℃、15 s;60℃、1 min;95℃、15 s;60℃、15 s(40个循环)。使用ABI 7500型荧光定量PCR仪采集待测基因及内参照GAPDH扩增各循环荧光信号引物。反应结束后确认实时荧光定量PCR的扩增曲线和融解曲线,进行PCR 定量时制作标准曲线,采用2-ΔΔCt计算目的基因的相对表达量。
| Gene | Accession No. | Primer sequence | Product length/bp |
| Nrf2 | NM_031789.2 | 5′ATATACGCAGGAGAGGGAAG 3′ | 222 |
| 5′ TCCCATCCTCATCACGTAAC 3′ | |||
| HO-1 | NM_012580.2 | 5′ GGGTCCTCACACTCAGTTTC 3′ | 228 |
| 5′ CCAGGCATCTCCTTCCATTC 3′ | |||
| GAPDH | NM_017008.3 | 5′ GTCGGTGTGAACGGATTTG 3′ | 181 |
| 5′ TCCCATTCTCAGCCTTGAC 3′ |
取100mg脑组织,按说明书提取并测定蛋白含量,取蛋白样品与4×SDS凝胶上样缓冲液混合后煮沸变性,SDS-PAGE电泳分离,湿转至PVDF膜上,用含5%脱脂奶粉的TBS溶解封闭。再分别与兔抗大鼠Nrf2多克隆抗体(1 ∶1 000)、兔抗大鼠HO-1多克隆抗体(1 ∶250)、兔抗大鼠GAPDH抗体(1 ∶1 500)4℃反应过夜,TBST溶液洗3次。然后与HRP 标记的二抗(1 ∶1 000)室温孵育,以增强型HRP-DAB 底物显色试剂盒显影。将膜进行扫描,图像分析软件测定目的条带的积分光密度值(IOD),以GAPDH为内参照,以目的条带IOD值与GAPDH条带IOD值的比值作为该蛋白的相对表达量。
2.6 统计学方法采用SPSS17.0统计软件进行分析。所有实验数据均经过方差齐性检验和正态性检验,计量资料用x±s表示,相同时间点的比较采用独立样本t检验或方差分析。
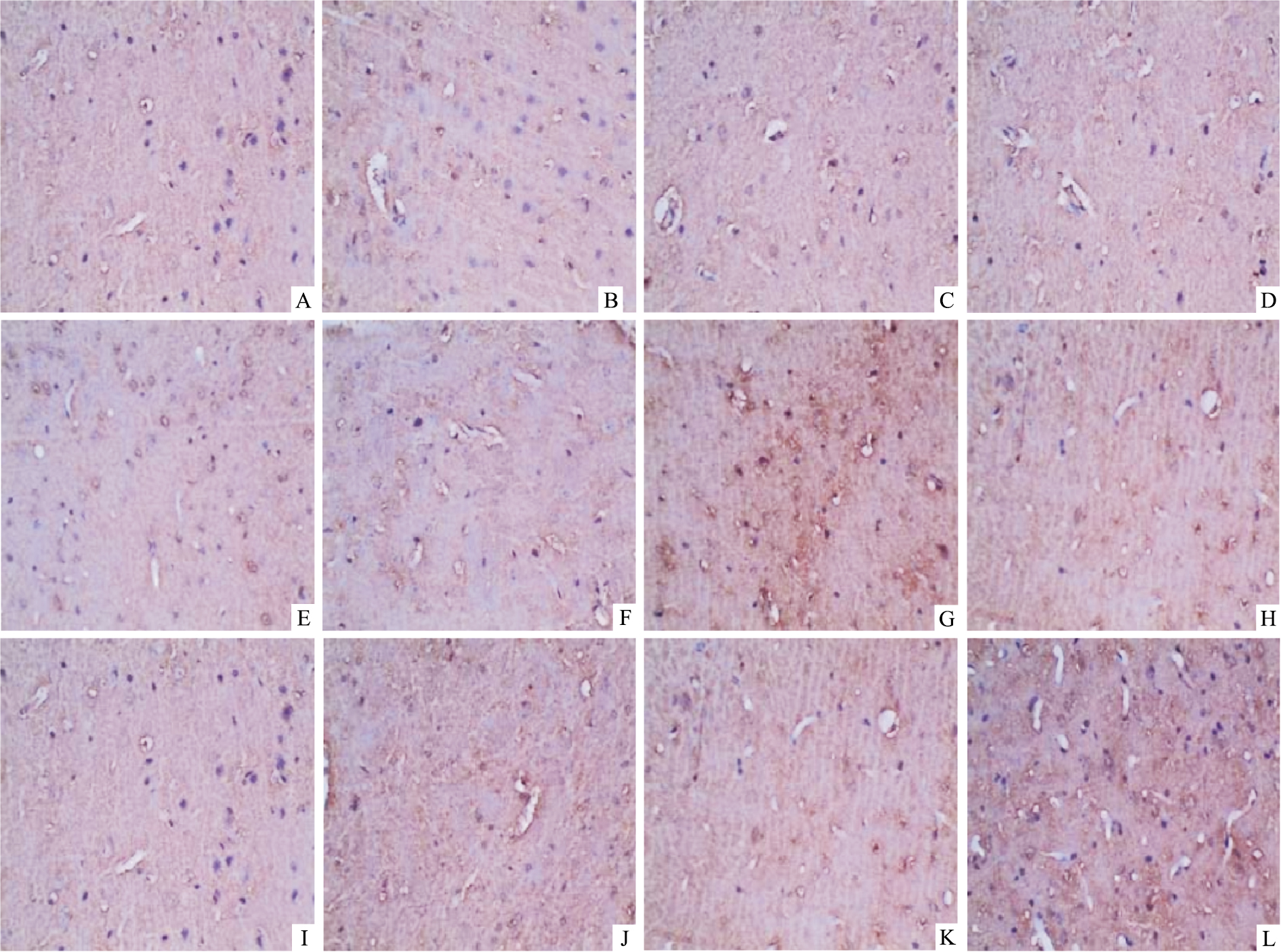
3 结果 3.1 补阳还五汤精简方对脑缺血大鼠不同时间点vWF表达及微血管密度(MVD)表达的影响vWF免疫组织化学染色结果显示:vWF标记血管内皮细胞,阳性细胞呈现棕黄色,微血管管腔由染成棕黄色的内皮细胞构成,形态不规则。在高倍显微镜下计数视野中vWF阳性细胞的数目以此来反映脑梗死区中平均微血管密度。假手术组vWF在微血管有极少量阳性表达,模型组vWF阳性表达微血管在d 1时无明显差异,d 3时表达明显升高(P < 0.05),随着动物生存时间延长,模型组vWF阳性表达呈现下降趋势。给药组d 7与模型组比较差异均有显著性(P < 0.05),给药组组间比较差异无显著性。见Tab 2。
|
| Fig 1 Expression of vWF in rats at different time points(×400) A:Sham(Day 1);B:Model(Day 1);C:Buyang Huanwu Decoction(Day 1);D: Thin Recipe of Buyang Huanwu Decoction(Day 1);E: Sham (Day 3);F: Model(Day 3);G: Buyang Huanwu Decoction (Day 3);H: Thin Recipe of Buyang Decoction (Day 3);I: Sham(Day 7);J: Model(Day 7);K: Buyang Huanwu Decoction (Day 7);L: Thin Recipe of Buyang Huanwu Decoction(Day 7) |
| Group | Day 1 | Day 3 | Day 7 |
| Sham | 13.22±2.18 | 12.39±1.96 | 13.41±2.35 |
| Model | 14.73±3.09 | 20.88±2.47 △ | 15.90±2.63 |
| Buyang HuanwuDecoction | 13.59±2.46 | 22.43±2.94 | 23.18±3.03 * |
| Thin Recipe of BuyangHuanwu Decoction | 14.25±1.85 | 21.67±1.79 | 24.46±2.15 * |
| △ P < 0.05 vs sham at the same time; * P < 0.05 vs model at the same time | |||
假手术组中Nrf2 mRNA、HO-1 mRNA呈少量表达,模型组Nrf2 mRNA表达略高,但与假手术组比较差异无统计学意义(P>0.05)。模型组HO-1 mRNA逐渐升高,d 7与假手术组比较差异有统计学意义(P < 0.05)。各给药组能不同程度上调Nrf2及HO-1 mRNA表达,其中Nrf2 mRNA在d 7上调最明显,HO-1 mRNA在d 3上调最明显,与同时段模型组比较差异具有统计学意义(P < 0.05)。见Tab 3、4。
| Group | Day 1 | Day 3 | Day 7 |
| Sham | 0.221±0.022 | 0.219±0.024 | 0.220±0.034 |
| Model | 0.234±0.025 | 0.221±0.036 | 0.228±0.011 |
| Buyang HuanwuDecoction | 0.240±0.031 | 0.259±0.029 | 0.292±0.038 * |
| Thin Recipe of BuyangHuanwu Decoction | 0.238±0.040 | 0.263±0.035 | 0.288±0.036 * |
| * P < 0.05 vs model at the same time | |||
| Group | Day 1 | Day 3 | Day 7 |
| Sham | 0.256±0.029 | 0.249±0.044 | 0.251±0.038 |
| Model | 0.251±0.045 | 0.257±0.028 | 0.319±0.043 △ |
| Buyang HuanwuDecoction | 0.258±0.036 | 0.321±0.051 * | 0.323±0.039 |
| Thin Recipe of BuyangHuanwu Decoction | 0.253±0.038 | 0.318±0.037 * | 0.337±0.035 |
| △ P < 0.05 vs sham at the same time; * P < .05 vs model at the same time | |||
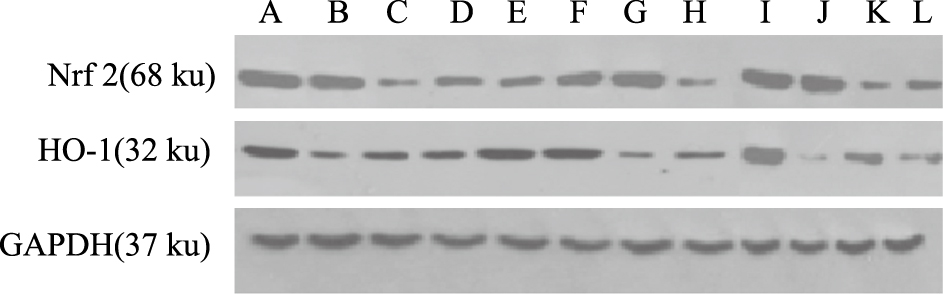
|
| Fig 2 Expression of Nrf2,HO-1protein in rats at different time points A: Thin Recipe of Buyang Huanwu Decoction(Day 1);B: Buyang Huanwu Decoction(Day 1);C: Model(Day 1);D: Sham(Day 1);E: Thin Recipe of Buyang Huanwu Decoction(Day 3);F: Buyang Huanwu Decoction (Day 3);G: Model(Day 3);H: Sham(Day 3);I: Thin Recipe of Buyang Huanwu Decoction(Day 7) ;J: Buyang Huanwu Decoction (Day 7);K: Model(Day 7);L: Sham(Day 7) |
Western blot结果显示:Nrf2蛋白定位于68 ku,HO-1蛋白定位于32 ku,内参照物GAPDH定位于37 ku,假手术组中Nrf2、HO-1蛋白呈少量表达,模型组d 3 Nrf2蛋白、d 7 HO-1蛋白表达与假手术组比较差异有统计学意义(P < 0.01,P < 0.05)。各给药组能不同程度上调Nrf2、HO-1蛋白表达,其中d 1及d 7 Nrf2蛋白表达与同时段模型组比较差异具有统计学意义(P < 0.01),补阳还五汤组d 3及补阳还五汤精简方组d 3、d 7 HO-1蛋白表达与同时段模型组比较差异具有统计学意义(P < 0.01)。见Tab5、6。
| Group | Day 1 | Day 3 | Day 7 |
| Sham | 0.319±0.038 | 0.278±0.033 | 0.368±0.042 |
| Model | 0.306±0.024 | 0.845±0.051 △△ | 0.259±0.045 |
| Buyang HuanwuDecoction | 0.695±0.047 ** | 0.745±0.043 | 0.631±0.057 ** |
| Thin Recipe of BuyangHuanwu Decoction | 0.721±0.052 ** | 0.612±0.048 | 0.845±0.061 ** |
| △△ P < 0.01 vs sham at the same time; ** P < 0.01 vs model at the same time | |||
| Group | Day 1 | Day 3 | Day 7 |
| Sham | 0.425±0.059 | 0.373±0.023 | 0.369±0.041 |
| Model | 0.491±0.060 | 0.382±0.034 | 0.411±0.037 △ |
| Buyang HuanwuDecoction | 0.523±0.044 | 0.867±0.042 ** | 0.218±0.043 |
| Thin Recipe of BuyangHuanwu Decoction | 0.542±0.037 | 0.824±0.033 ** | 0.904±0.058 ** |
| △ P < 0.05 vs sham at the same time; ** P < 0.01 vs model at the same time | |||
脑组织在缺血缺氧损伤作用下,缺血半暗带神经元发生一系列神经功能缺损形态学变化,这种脑组织缺血性神经功能损伤在一定时限内是可逆性的,主要取决于缺血区血供情况。血管新生通过启动损伤区微血管网重建,改善缺血区周围的组织灌流,为损伤神经元的修复、突触重建和神经发生创造良好的微环境[12, 13, 14]。然而,脑缺血后血管新生是一系列相互衔接、精密调控的过程,诸多调控因子参与其中,相关调控机制仍未完全明确。
研究表明[1, 2, 3, 4],Nrf2/HO-1信号途径在血管新生中发挥重要的调控作用。静息情况下Nrf2存在于细胞质中,半衰期较短,在胞质中与肌动蛋白结合蛋白Keapl结合而处于失活状态,且被泛素蛋白酶体途径迅速降解。当受到来源于亲电子物质或活性氧的信号攻击后,Nrf2从Keapl-Nrf2复合物中解离,Nrf2的半衰期明显延长,然后稳定状态的Nrf2转位进入细胞核,与ARE特异性位点结合,启动ARE调控的二相酶及抗氧化酶的基因表达[15, 16]。
补阳还五汤精简方由黄芪、川芎等组成,遵循补阳还五汤之方义,秉承“瘀血不去,新血不生”和“不破不立,瘀祛新生”的观念而发展起来的。并且配合醇提、超临界CO2提取工艺制备而成,旨在寻找一种物质基础明确、药效相当甚至更优于原方的新型复方。本实验研究结果显示:与模型组比,补阳还五汤精简方组大鼠脑缺血区vWF阳性表达较模型组明显增多,微血管密度增加,并随着动物生存时间延长,vWF表达维持在较高水平,说明药物的干预弥补了自身血管新生的不足,这也可能是补阳还五汤精简方减轻缺血脑区病理损伤,改善缺血后神经行为学障碍的因素之一。从分子生物水平,Nrf2蛋白表达水平在脑缺血损伤d 1即开始升高,d 3到达高峰,随后逐渐下降,证明Nrf2在缺血性损伤早期即被激活,但Nrf2mRNA在脑缺血损伤后各时间点无明显变化的表达,这与Nrf2蛋白的表达不相一致,这提示Nrf2调控并非发生于基因转录水平,HO-1蛋白及mRNA早期表达不明显,表达升高在Nrf2表达高峰之后的d 7,因此推测下游调控的抗氧化和解毒酶HO-1的表达在Nrf2诱导下发生。补阳还五汤精简方上调了Nrf2的表达且促进了其下游基因H0-1的表达,且作用时间与血管新生的时相基本一致,推测该方通过激活Nrf2/HO-1信号途径发挥对脑缺血后血管新生调控作用。该实验结果显示补阳还五汤精简方与补阳还五汤原方药效学之间差异无统计学意义,这可能是由于补阳还五汤精简方采用的现代制备工艺和设备能更大程度的将药材中的有效成分溶出,在不改变药效药理作用的前提下具有有效节约中药资源,改善传统水煎液的服用不便等优势,为中药现代化发展方向提供参考。
(致谢:本实验完成于湖南省中药粉体与创新药物省部共建国家重点实验室培育基地,实验过程中得到该实验室全体老师的指导及同学的协助,在此表示感谢。)
| [1] | Afonyushkin T,Oskolkova O V, Philippova M, et al.Oxidized phospholipids regulate expression of ATF4 and VEGF in endothelial cells via NRF2-dependent mechanism novel point of convergence between electrophilic and unfolded protein stress pathway[J].Arterioscler Thromb Vasc Biol, 2010; 30(5):1007-13. |
| [2] | Uno K, Prow T W, Bhutto I A, et al.Role of Nrf2 in retinal vascular development and the vaso-obliterative phase of oxygen-induced retin-opathy[J].Exp Eye Res, 2010;90(7):493-500. |
| [3] | Tongers J,Knapp J W,Korf M, et al.Haeme oxygenase promotes progenitor cell mobilization,neovascularization and functional recovery after critical hindlimb ischaemia in mice[J].Cardiovasc Res, 2008,78(9):294-300. |
| [4] | Ryter S W,Morse D,Chol A M.Carbon monoxide and bilirubin:potential therapies for Pulmonary for pulmonary/vascular injury and disease[J].Am J Respir Cell Molbiol, 2007,36(2):175-82. |
| [5] | 夏相宜,刘芳,佘颜,等.脑健胶囊对MCAO大鼠脑水肿及梗死面积的影响[J].中医学报,2014,29(4):532-4. Xia X Y,Liu F,She Y,et al. Effect of Naojian Capsule on Encephaledema,Area of Cerebral Infarction and Body Quality in MCAO Rats[J].China J Chin Med,2014,29(4):532-4. |
| [6] | 刘青萍.补阳还五精简方脑健片治疗脑缺血后脑损伤的谱效关系和药代动力学数学模型研究[D].长沙:湖南中医药大学,2014,5. Liu Q P.Thin recipe of Buyang Huanwu Decoction(NAOJIAN tablets) in the treatment of cerebral ischemia injury spectrum effect relationship and pharmacokinetics mathematical model Research[D].Changsha:Hunan University of Chinese Medicine.2014,5. |
| [7] | Nagasawa H, Kogure K. Correlation between cerebral blood and histologic changes in a new rat model of cerebral artery occlusion stroke[J].Stroke,1989,20(6):1037. |
| [8] | Longa E Z, Weinstein P R, Carlson S, et al.Reversible middle cerebral artery occlusion without craniectomy in rats[J].Stroke,1989,20(1):84-91. |
| [9] | Bederson J B, Pitts L H, Tsuji M, et al.Rat middle cerebral artery occlusion:evaluation of the model and development of a neurologic examination[J].Stroke,1986,17(3):472-6. |
| [10] | 李灵娟.microRNA-376b-5p对脑缺血后血管新生的调控作用及机制研究[D].长沙:中南大学湘雅医学院, 2014,5. Li L J.The regulation role of microRNA-376b-5p on angiogenesis after cerebral ischemia and mechanism[D].Changsha:Central South University,2014,5. |
| [11] | 孙笑.血管增生促进缺血损伤脑内神经血管单元重构的细胞机制研究[D].上海:复旦大学,2013,5. Sun X. Cellular mechanisms of vascular proliferation in the reconstruction of nerve cells in the brain of ischemic injury[D].Shanghai:Fudan University,2013,5. |
| [12] | Wei L,Fraser J L,Lu Z Y,et al.Transplantation of hypoxia preconditioned bone marrow mesenchymal stem cells enhances angiogenesis and neurogenesis after cerebral ischemia in rat[J].Neurobiol Dis,2012,46(3):635-45. |
| [13] | 常丽萍,张秋燕,韩建科,等.通心络超微粉对缺血性脑卒中大鼠微血管新生影响的实验研究[J].中国药理学通报,2012,28(7):1015-8. Chang L P,Zhang Q Y,Han J K,et al.Experimental study on the interventional effects of Tongxinluo supermicropowder on angiogenesis of ischemic stroke rats[J].Chin Pharmacol Bull,2012,28(7):1015-8. |
| [14] | Ergul A, Alhusban A, Fagan S C. Angiogenesis:A harmonized target for recovery after stroke[J].Stroke,2012,43(8):2270-4. |
| [15] | Dhakshinamoorthy S,Jaiswal A K.Functional characterization and role of Nrf2 in antioxidant response element-mediated expression and antioxidant induction of NAD(P)H:quinine oxidoreductasel gene[J].Oncogene,2001,20(29):3906-17. |
| [16] | Ogborne R M,Rushworth S A,O'Connell M A.Epigallocatechin activates haem oxygenase-1 expression via protein kinase C deta and Nrf2[J].Biochem Biophys Res Commun,2008,373(9):584-8. |

