


2. 福建医科大学附属漳州市医院血液科, 福建 漳州 363000;
3. 福建医科大学药学院, 福建 福州 350004
2. Dpet of Hematology, Zhangzhou Affiliated Hospital of Fujian Medical University, Zhangzhou Fujian 363000, China;
3. School of Pharmacy, Fujian Medical University, Fuzhou 350004, China
DNA甲基化反应是由DNA甲基转移酶(DNMT)催化的,目前发现的DNMTs家族包括:DNMT1、DNMT2、DNMT3A、DNMT3B以及DNMT3L,其中DNMT1是一种持续性DNA甲基转移酶,维持有丝分裂期DNA的甲基化状态[1, 2]。DNA甲基化不仅参与基因表达调控,而且参与肿瘤的发生发展过程,是肿瘤常见表观遗传学改变之一[3],DNMT成为一个重要的分子靶标,在疾病的治疗和预防中发挥重要作用[4]。有实验证明,在急性白血病患者和白血病细胞株中,DNMT基因异常高表达[5]。这些高表达的DNMT可能诱导某些相关基因,尤其是一些抑癌基因异常甲基化,最终可能导致白血病发生。因此,通过靶向性沉默DNMT1基因,重新启动基因转录,阻滞细胞周期,抑制肿瘤细胞增殖,诱导肿瘤细胞凋亡。
目前去甲基化治疗已成为肿瘤诱导分化、抑制增殖的新方法,为探讨靶向沉默DNMT1对急性淋巴细胞白血病的作用,本研究通过人工化学合成针对DNMT1基因的siRNA片段,以LipofectamineTM 2000为介导,靶向沉默Molt-4细胞DNMT1基因的表达,探讨其对Molt-4细胞增殖、凋亡以及对组蛋白调控的影响,研究白血病靶向基因治疗。
1 材料与方法 1.1 实验仪器细胞培养箱(3111,美国Thermo公司),低温离心机(J2-21型 Beckman公司),常温离心机(上海医疗器械公司),倒置显微镜(Model-U-LH 100HG,日本OLYMPUS产品),全自动凝胶成像系统(GeneGenius,英国Syngene公司),UV2100紫外分光光度仪(上海谱析公司),PCR扩增仪(AG22331,德国Eppendorf公司),迷你垂直电泳槽(美国BIO-RAD公司),脱色摇床(北京东方仪器厂)。
1.2 试剂RPMI 1640培养基(美国 Gibco公司);LipofectamineTM2000 转染试剂、RNA提取试剂盒、RT-PCR试剂盒及Opti-MEM试剂(美国Invitrogen公司);DNMT1 siRNA及PCR引物(上海吉玛制药技术有限公司);细胞凋亡检测试剂盒(美国BD公司);二甲基亚砜及MTT(浓度为5 g·L-1)(美国Sigma公司);BCA蛋白定量试剂盒(Thermo公司);β-actin、DNMT1、procaspase-3、BCL-2、P15单克隆抗体及Goat anti-mouse with HRP conjugate、 Goat anti-rabbit with HRP conjugate 二抗(美国Santa Cruz公司);Anti-acetyl-Histone H3、Anti-trimethyl-Histone H3 (Lys9)、Anti-trimethyl-Histone H3 (Lys4)(美国Upstate 公司)。
1.3 细胞培养取人类急性T淋巴细胞性白血病Molt-4细胞株(中国科学院上海细胞库),培养于含 15%胎牛血清、青霉素100 kU·L-1+链霉素100 kU·L-1的 RPMI 1640 培养液,置于 37℃、饱和湿度、5%CO2培养箱培养,每2~3天传代 1 次,选择对数生长期细胞进行实验。
1.4 Molt-4细胞转染和转染效率检测依据Reynolds等总结的设计siRNA 原则,针对DNMT1区域选择作用靶点的小干扰RNA片段,委托上海吉玛公司合成。DNMT1 siRNA序列Sense 5′-GCACCU CAUUUGCCGAAUATT-3′,Antisense5′-UAUUCGGCA AAUGAGGUGCTT -3′,同时合成标有荧光标记的通用随机阴性序列作为对照。转染前取对数生长期Molt-4细胞,悬浮于无抗生素的培养液中,调整细胞浓度为(8~16)×105。以LipofectamineTM 2000为载体进行转染,步骤参照说明书。
1.5 RT-PCR法检测Molt-4细胞DNMT1 mRNA表达选择对数生长期的Molt-4细胞,接种在6孔板上,DNMT1 siRNA浓度分别为0、30、60、120 nmol·L-1,每孔总体积为2 mL。转染后培养24 h,TRIzol法提取总RNA,经紫外分光光度法鉴定定量,A260/A280比值均在1.8~2.0之间,经逆转录为cDNA。以反应制备所得的cDNA进行PCR扩增。设计PCR引物序列如下:DNMT1上游引物:5′-AGGTTGATGTCTGCGTGGTAGC-3′,下游引物5′-CCGAGTTGGTGATGGTGTGTAC-3′;β-actin上游引物:5′- CAGGAGGAGCAATGATCTTGATCT-3′,下游引物5′- TCATGAAGTGTGACGTGGACATC-3′。PCR反应条件:95℃ 5 min预变性,95℃ 45 s变性,49℃ 45 s退火,72℃ 45 s延伸,40个循环,72℃ 10 min再延伸。最后将PCR产物经16 g·L-1琼脂糖凝胶电泳,于凝胶图像分析仪上自动分析成像。
1.6 MTT法绘制细胞生长曲线将对数生长期的Molt-4细胞接种于96孔培养板中,2×104个/孔,DNMT1 siRNA浓度分别为0、30、60、120 nmol·L-1。终体积为200 μL,每组设6个平行孔。细胞转染后置于37℃、5% CO2饱和湿度的培养箱中继续培养24、48和72 h,于实验结束前4 h取出一块板,加5 g·L-1 MTT 20 μL,继续培养4 h,离心,吸去上清,加入二甲基亚砜150 μL,震荡10 min,使结晶物充分溶解,酶标仪单波长492 nm 测吸光度(A 值),计算细胞增殖率。细胞增殖率/%=(A实验-A空白) / (A对照-A空白)×100%。实验重复 3 次。以时间为横坐标,细胞增殖率为纵坐标绘制细胞增殖曲线。
1.7 流式细胞仪检测细胞早期凋亡将Molt-4细胞悬液接种于6孔板上,终体积为2 mL,DNMT1 siRNA浓度分别为0、30、60、120 nmol·L-1,转染后培养24 h,离心收集细胞。依据BD公司Annexin V和PI双染试剂盒说明书进行处理,应用流式细胞仪检测。
1.8 Western blot检测DNMT1蛋白、凋亡相关蛋白及组蛋白调控影响DNMT1 siRNA转染24h后,收集上述各处理组细胞,预冷的PBS洗涤2次后,按照 1×106 细胞加入100 μL 裂解液和1 μL 酶抑制剂的比例充分裂解细胞。于低温(4℃)下,12 000 r·min-1离心15 min后,收集蛋白,-20℃保存备用。BCA法进行蛋白定量,取备用蛋白,以12%SDS-PAGE电泳分离后,电转移法转膜,室温下水平摇床上缓慢摇动,封闭1 h;放入TBS 1 ∶400稀释的一抗中,4℃过夜。TBS洗涤液洗膜3次后,分别放入辣根过氧化物酶标记的二抗,室温下水平摇床上缓慢摇动1 h;洗膜后化学发光法显色,X射线胶片扫描后,以β-actin为内参,应用AlphaDigiDoc图像分析软件分析比较。
1.9 统计学处理应用SPSS 17.0软件处理。计量资料数据以x± s 表示。单变量两组资料比较采用t检验,多组资料比较采用单因素方差分析。
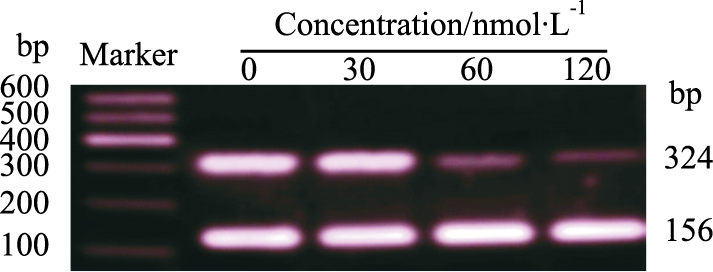
2 结果 2.1 DNMT1 siRNA对DNMT1 mRNA表达的影响DNMT1 siRNA转染Molt-4细胞24 h后,提取mRNA进行RT-PCR,与对照组比较可见,DNMT1 siRNA组的mRNA条带亮度明显减弱,而且随着DNMT1 siRNA浓度的增加,亮度呈递减趋势,其中120 nmol·L-1组亮度减弱最明显,表现出浓度依赖性(Fig 1)。0、30、60、120 nmol·L-1组DNMT1扩增条带灰度值与β-actin 比值分别为:0.99±0.18、0.85±0.15、0.20±0.07和0.09±0.01,与对照组相比,各处理组差异均有统计学意义(P < 0.05)。
|
| Fig 1 Expression of DNMT1 mRNA in Molt-4 cells after transfection with DNMT1 siRNA for 24 h |
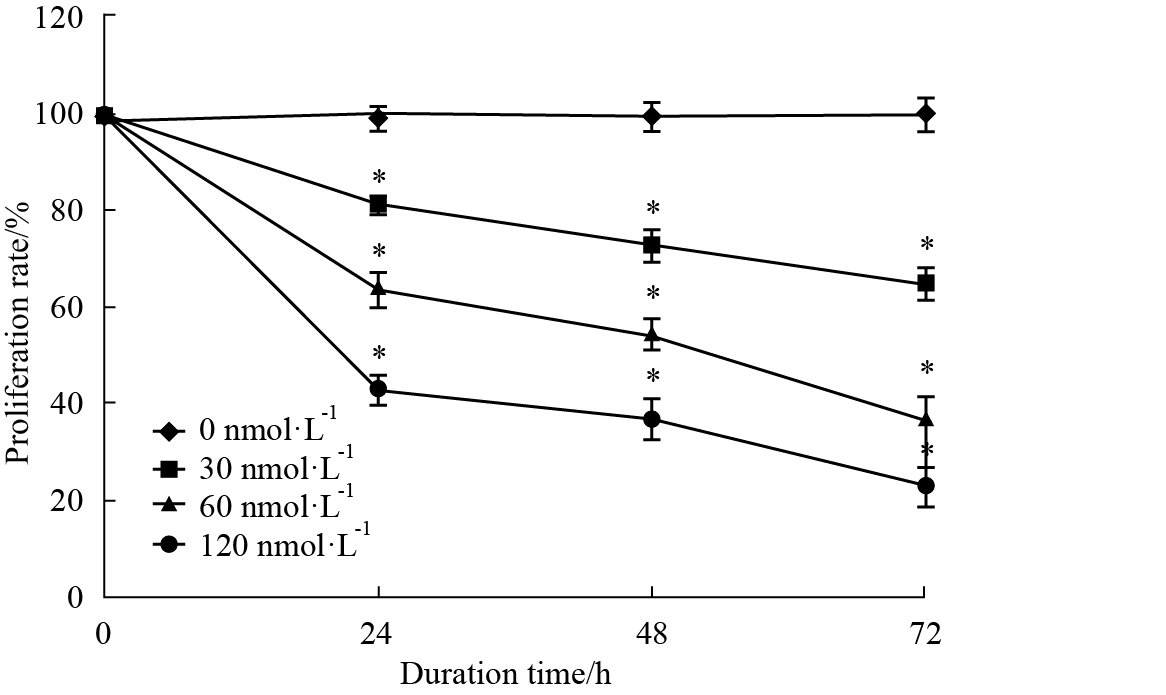
MTT法检测DNMT1 siRNA对Molt-4细胞增殖率的影响,经0、30、60、120 nmol·L-1的DNMT1 siRNA作用24、48、72 h后,Molt-4细胞的增殖率变化见Tab 1。结果显示,细胞的增殖率随着DNMT1 siRNA浓度的增加而逐渐下降;而且随着DNMT1 siRNA作用时间的延长,增殖率逐渐下降,说明其作用具有浓度依赖性和时间依赖性(Fig 2),与对照组细胞增殖率相比,各处理组差异均有统计学意义(P < 0.05)。
| (x± s ) | |||
| Concentration/ nmol·L-1 | Proliferation rate/% | ||
| 24 h | 48 h | 72 h | |
| 0 | 98.23±1.84 | 99.02±2.51 | 99.91±3.52 |
| 30 | 82.01±1.73* | 72.03±2.73* | 63.15±3.49* |
| 60 | 62.12±1.96* | 54.76±1.86* | 31.06±3.73* |
| 120 | 41.11±2.24* | 34.23±3.54* | 20.83±3.54* |
|
| Fig 2 Proliferation rates of Molt-4 cells after transfection with DNMT1 siRNA for 24,48 and 72 h *P < 0.05 vs 0 nmol·L-1 |
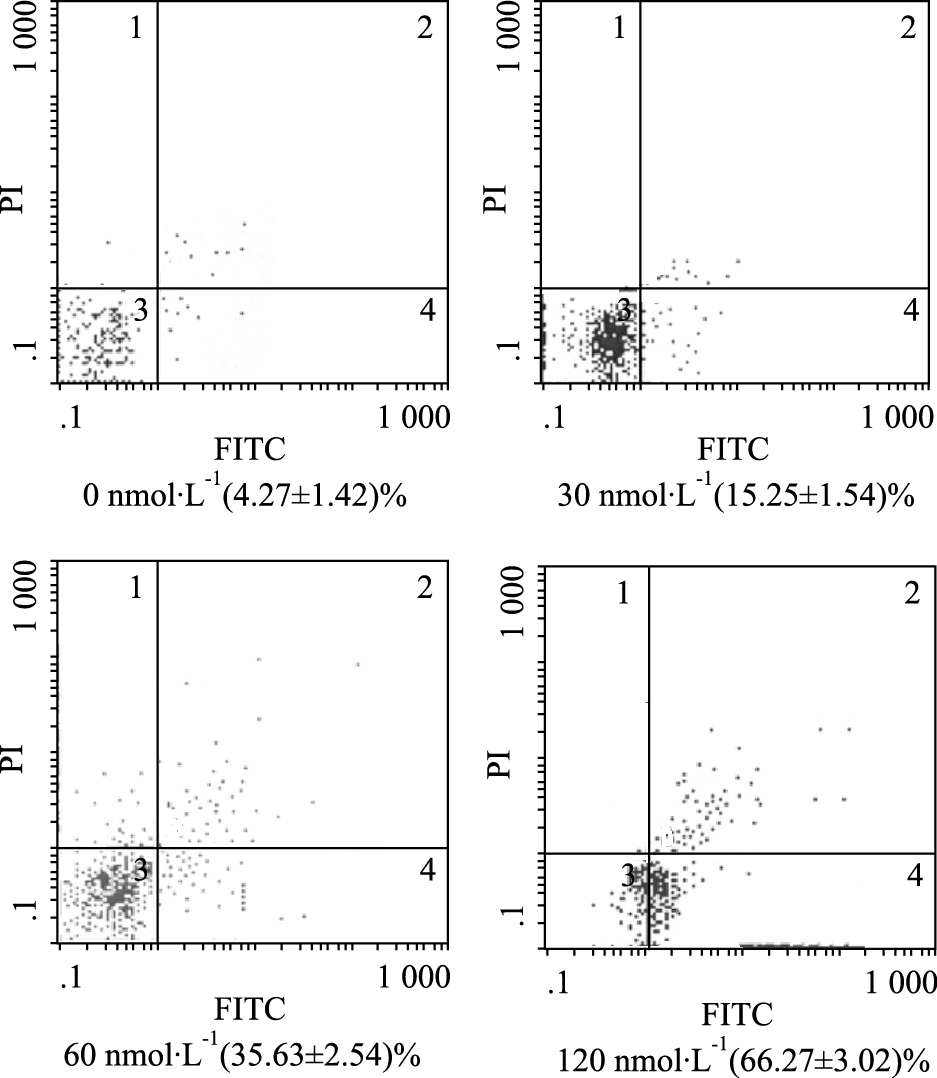
经DNMT1 siRNA作用24 h后,0、30 、60、120 nmol·L-1 siRNA组细胞凋亡率分别为(4.27±1.42)%、(15.25±1.54)%、(35.63±2.54)%、(66.27±3.02)%,结果显示:细胞凋亡率随着siRNA浓度增加而逐渐上升,说明其作用具有浓度依赖性。DNMT1 siRNA组与对照组凋亡率比较,差异有统计学意义(P < 0.05),见Fig 3。
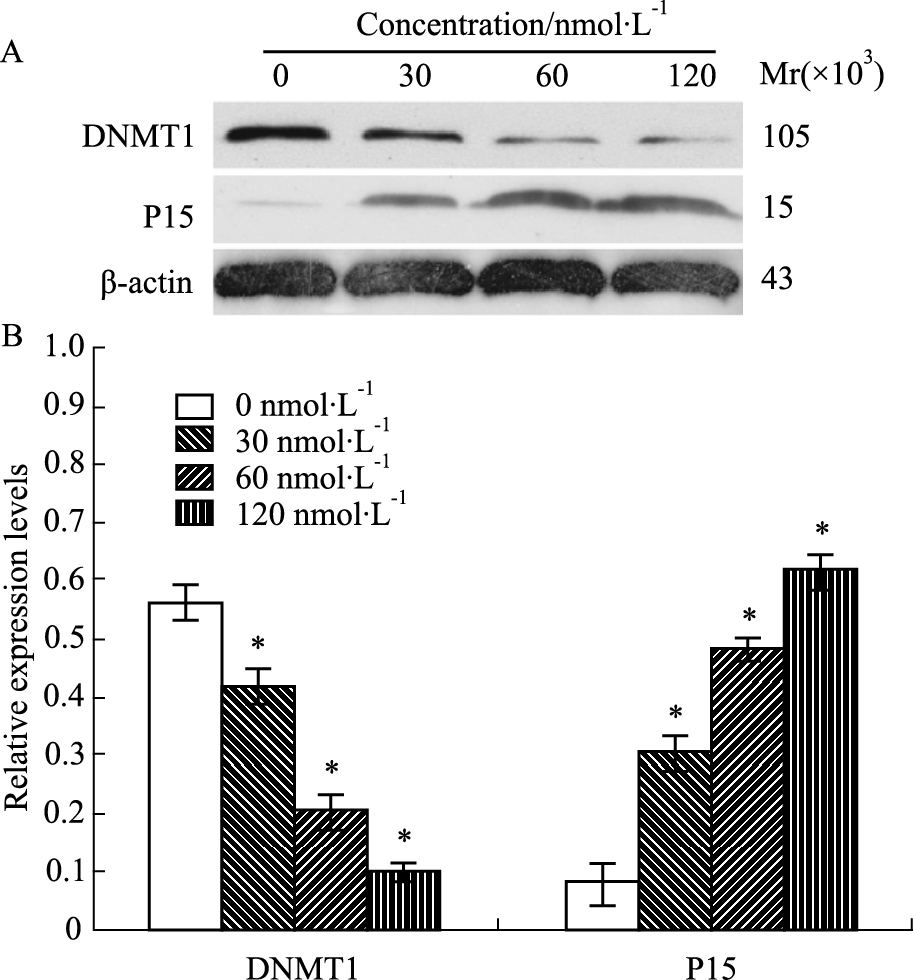
2.4 DNMT1 siRNA对Molt-4细胞P15、DNMT1表达的影响经0、30、60、120 nmol·L-1DNMT1 siRNA作用Molt-4细胞24 h后,Western blot法检测结果显示,随着DNMT1 siRNA浓度递增,抑癌蛋白 P15的表达量呈现递增趋势;而DNMT1蛋白表达量呈现递减趋势。AlphaDigiDoc图像分析软件分析比较,各组条带灰度值与β-actin及对照组比较,差异有统计学意义(P < 0.05),见Fig 4。
|
| Fig 3 Apoptotic rates of Molt-4 cells after transfection with DNMT1 siRNA for 24 h |
|
| Fig 4 Alteration of DNMT1,P15 protein in Molt-4 cells after transfection with DNMT1 siRNA for 24 h A: Protein electrophoresis; B: Proteins relative density. *P < 0.05 vs 0 nmol·L-1 |
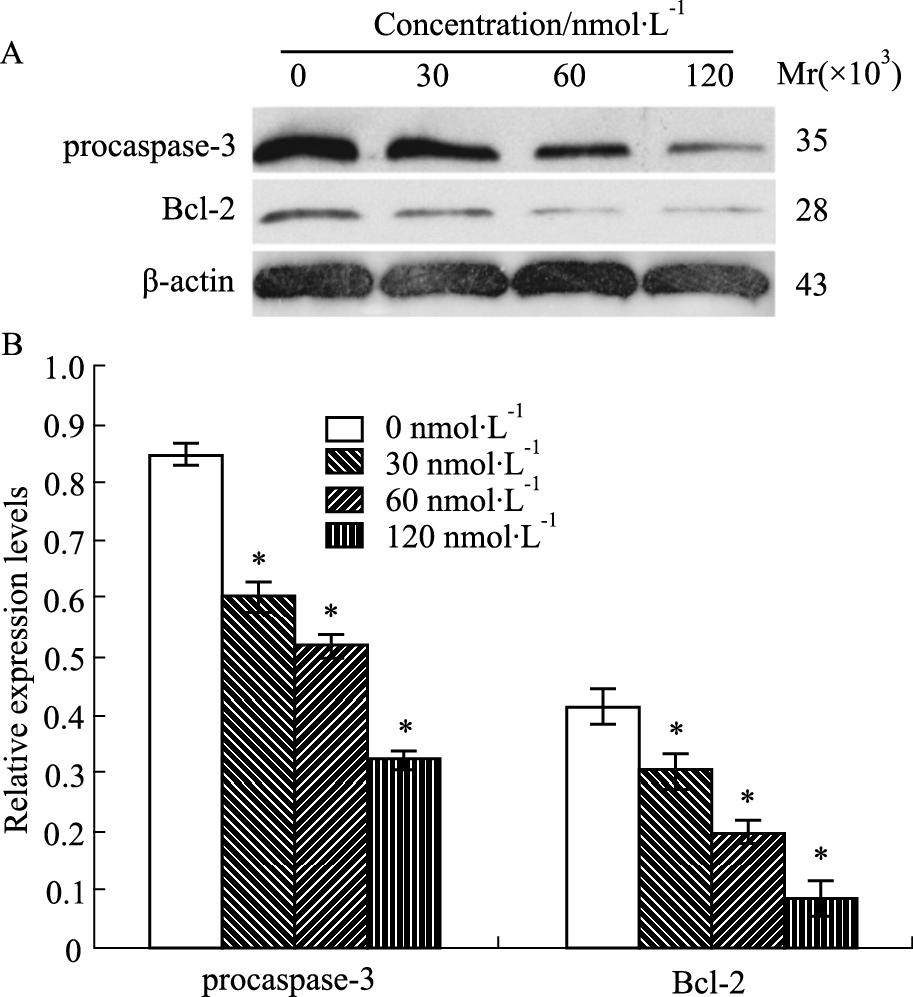
经上述不同浓度的DNMT1 siRNA处理Molt-4细胞24 h后,结果显示:抗凋亡蛋白Bcl-2和胱天蛋白酶procaspase-3的表达量随着DNMT1 siRNA浓度的增加而递减,呈现浓度依赖性(P < 0.05),差异有统计学意义(Fig 5)。
|
| Fig 5 Alteration of apoptosis-related proteins in Molt-4 cells after transfection with DNMT1 siRNA for 24 h A:Protein electrophoresis;B:Proteins relative density. *P < 0.05 vs 0 nmol·L-1 |
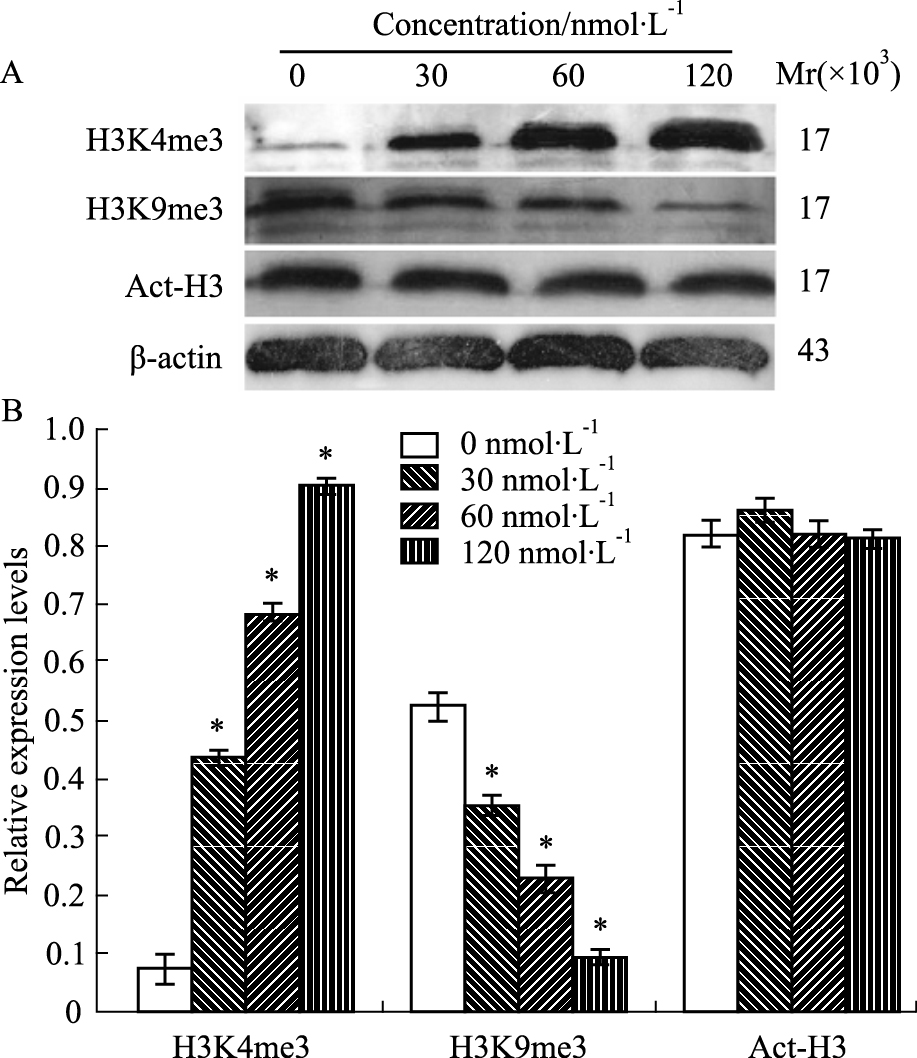
经上述不同浓度的DNMT1 siRNA处理Molt-4细胞24 h后,H3K4甲基化水平随siRNA处理浓度增加而表达逐渐增强,H3K9甲基化水平随着siRNA处理浓度的增加而逐渐降低;P < 0.05,差异有统计学意义。而组蛋白H3乙酰化水平未见明显变化,差异无统计学意义(P>0.05),见Fig 6。
|
| Fig 6 Alteration of histone-related proteins in Molt-4 cells after transfection with DNMT1 siRNA for 24 h A:Protein electrophoresis; B: Proteins relative density. *P < 0.05 vs 0 nmol·L-1 |
DNMT1是人体发育过程中必需的基因,定位于人类19pl3.2-19pl3.3,是人体内最早发现且最为重要的甲基转移酶[6],主要维持DNA甲基化。DNMT1 基因的高表达参与或影响恶性肿瘤的形成过程,启动子甲基化异常导致的转录失活是多种肿瘤发病的共同机制之一[7]。研究发现:在胃癌、肝癌、卵巢癌、肺癌等多种肿瘤临床样本中均检测到DNMT1蛋白的高表达[8],DNA甲基转移酶抑制剂(DNMTis)对于治疗基因启动子区存在高甲基化的癌症有重要的意义[9]。因此,本研究通过DNMT1 siRNA降低DNMT1基因的表达,从而逆转肿瘤抑制基因的高甲基化状态,抑制肿瘤的发生发展。
Kurita 等[10]构建DNMT1 siRNA及 DNMT3b siRNA 转染肝癌细胞,发现siRNA抑制肝癌细胞的增殖及促进细胞凋亡。本研究显示:Molt-4细胞经不同浓度的DNMT1 siRNA作用后,增殖率逐渐下降,表现出时间依赖性和浓度依赖性,说明DNMT1 siRNA可阻滞细胞周期,抑制细胞增殖。研究还发现:DNMT1 siRNA可上调抑癌蛋白P15表达。p15基因作为细胞周期的负性调控因子,如果p15 基因失活,则P15 蛋白不能正常表达,细胞增殖失去控制,导致细胞癌变。p15基因缺失、突变、失活等在恶性血液病中容易发生,而且p15基因甲基化与血液病的疗效及预后也有关系[11] 。本研究采用的急性T淋巴细胞性白血病Molt-4细胞株,其p15基因高度甲基化,p15基因弱表达,对正常细胞周期不能发挥负性调控功能,导致细胞生长周期失调,细胞癌变。通过转染DNMT1 siRNA,上调p15基因和P15蛋白的表达水平,从而抑制肿瘤细胞增殖。
本研究显示,DNMT1 siRNA可诱导Molt-4细胞凋亡,随着DNMT1 siRNA浓度增加,Molt-4细胞凋亡率逐渐增高;同时procaspase-3及Bcl-2表达量逐渐递减,具有明显的浓度依赖性。推测沉默DNMT1可通过线粒体介导的通路(内在通路)发挥对Molt-4细胞株凋亡的调控,Bcl-2家族中促凋亡蛋白,诱发细胞色素C从线粒体释放入胞质,激活caspase-9前体,活化的caspase-9继而激活下游的caspase-3,引发caspases级联反应,诱导细胞凋亡发生,启动内源性凋亡通路。亦不排除受体介导的外源性凋亡通路参与的凋亡过程,其作用机制有待进一步研究。本研究通过DNMT1 siRNA转染Molt-4细胞,结果p15基因表达增加,Bcl-2表达降低,抑制细胞增殖,并诱导细胞凋亡,推测DNMT1 siRNA通过增加p15基因表达,降低Bcl-2表达,参与细胞周期调控过程。
本研究发现:DNMT1 siRNA可下调组蛋白H3K9甲基化水平,上调组蛋白H3K4的甲基化水平。DNMT1 siRNA抑制H3K9甲基化,解除对抑癌基因的转录抑制作用,从而使p15基因转录活性增加、表达水平增加,发挥细胞周期负性调控作用促使细胞周期停滞;Bcl-2表达水平下降,启动线粒体介导的通路,诱导细胞进入凋亡程序。DNMT1 siRNA干扰DNMT1基因表达,H3K4 甲基化水平升高,说明在基因沉默机制中,H3K9甲基化与DNA甲基化正相关,而H3K4甲基化与DNA甲基化负相关,具体机制有待进一步研究证实。由此可见,DNA 甲基化与组蛋白修饰之间存在密切的联系,DNMT1的N端与HDAC1、HDAC2结合,引起组蛋白去乙酰化;亦可招募赖氨酸特异性脱甲基酶1 (LSDl)和组蛋白甲基化酶Suv39hl,导致组蛋白不同的氨基酸去甲基化或甲基化。另外,组蛋白低乙酰化状态促进DNA甲基化,而组蛋白高乙酰化状态抑制DNA甲基化[12]。有研究报道:DNA甲基转移酶抑制剂5-氮杂-2’脱氧胞苷能改变组蛋白乙酰化状态[13],而本研究显示转染DNMT1 siRNA后,组蛋白H3乙酰化水平无明显变化,因此推测在DNA甲基化与组蛋白乙酰化相互之间的调控可能存在多样性。
本研究证实采用RNA干扰技术沉默DNMT1基因后,通过调控组蛋白的甲基化,重新启动基因转录,上调p15基因表达,裂解Bcl-2,激活caspase-3,启动线粒体介导的凋亡途径,抑制肿瘤细胞增殖,诱导细胞凋亡。因此,在今后临床治疗中,有望通过siRNA沉默DNMT1基因,发挥抑癌作用,成为癌症基因治疗的有效手段。
(致谢:本文实验在闽南师范大学菌物产业工程技术中心实验室完成,感谢实验室的老师对本实验的支持。)
| [1] | Gu H, Bock C,Mikkelsen T S, et al. Genome-scale DNA methylation mapping of clinical samples at single-nucleotide resolution[J]. Nat Meth,2010,7(2):133-6. |
| [2] | Song J, Teplova M, Ishibe-Murakami S, Patel D J. Structure-based mechanistic insights into DNMT1-mediated maintenance DNA methylation[J]. Science,2012,335(6069):709-12. |
| [3] | Christensen B C,Kelsey K T,Zheng S,et al. Breast cancer DNA methylation profiles are associated with tumor size and alcohol and folate intake[J]. PLoS Genet,2010,6(7):e1001043. |
| [4] | Ben G R, Ben A O, Ziadi S,et al.Methylation of miR-124a-1,miR-124a-2,and miR-124a-3 genes correlates with aggressive and advanced breast cancer disease[J].Tumour Biol,2014,35(5):4047-56. |
| [5] | 乔淑凯,徐世荣,郭晓楠,等.急性白血病患者甲基转移酶基因的表达其及临床意义[J]. 中国实验血液学杂志,2005,13(2):260-5.Qiao S K,Xu S R,Guo X N, et al. Clinical significance of the expression of DNA methyltransfearse genes(DNMT)in acute leukemia patients[J].J Exp Hematol,2005,13(2):260-5. |
| [6] | Armstrong C A, Jones G D, Anderson R, et al. DNMTs are required for delayed genome instability caused by radiation[J]. Epigenetics,2012,7(8):892-902. |
| [7] | Bian E B,Zhao B,Huang C,et al. New advances of DNA methylation in liver fibrosis,with special emphasis on the crosstalk between microRNAs and DNA methylation machinery[J].Cell Signal,2013,25(9):1837-44. |
| [8] | Zhang Y,Chen F Q,Sun Y H, et al. Effects of DNMT1 silencing on malignant phenotype and methylated gene expression in cervical cancer cells[J]. J Exp Clin Cancer Res,2011,30(98):1-8. |
| [9] | 张玲,盛树力,秦川. 表观遗传学药物的研究进展[J].中国药理学通报,2013,29(3):297-302.Zhang L,Sheng S L,Qin C.Research progress in the epigenetic drug[J]. Chin Pharmacol Bull,2013,29(3):297-302. |
| [10] | Kurita S,Higuchi H,Saito Y,et al.DNMT1 and DNMT3b silencing sensitizes human hepatoma cells to TRAIL-mediated apoptosis via up-regulation of TRAIL-R2/DR5 and caspase-8[J], Cancer Sci, 2010,101(6):1431-9. |
| [11] | Galm O,Wilop S, Lüders C, et al. Clinical implications of aberrant DNA methylation patterns in acute myelogenous leukemia[J]. Ann Hematol, 2005, 1(84):39-46. |
| [12] | Hellebrekers D M,Jair KW, Viré E, et al. Angiostatic activity of DNA methyltransferase inhibitors[J]. Mol Cancer Ther, 2006,5(2):467-75. |
| [13] | Oda M,Kumaki Y,Shigeta M,et al.DNA methylation restricts lineage-specific functions of transcription factor Gata4 during embryonic stem cell differentiation[J].PLoS Genet,2013,9(6):e1003574. |

