


2. 张家口市宣化皇城医院功能科, 河北 宣化 075100;
3. 河北北方学院, 河北 张家口 075000;
4. 河北北方学院生命科学研究中心, 河北 张家口 075000
2. Dept of Function, Huangcheng Hospital, Zhangjiakou, Hebei 075100, China;
3. Hebei North University, Zhangjiakou Hebei 075000, China;
4. Experiment center, Heber North University, Zhangjiakou Hebei 075000, China
青蒿琥酯(artesunate,ART)作为一种高效、低毒的抗疟药已广为人知,近来又有研究发现,ART还有抗肿瘤功效,但其作用机制尚未明确。而侵袭和转移是大肠癌患者死亡的主要原因,近年研究发现,包括大肠癌在内的多种肿瘤组织中高迁移率族蛋白(high mobility group protein,HMG蛋白)过表达,有可能通过激活下游基质金属蛋白酶(matrix metalloproteinases,MMPs)来促进肿瘤的侵袭转移。本实验通过ART干预大肠癌Lovo细胞,观察对细胞侵袭能力的影响,并检测细胞内HMGB1和侵袭迁移相关基因 MMP-2表达情况,来探讨其作用机制。
1 材料与方法 1.1 主要材料人大肠癌Lovo细胞购于中国医学科学院基础医学研究所北京协和医学院细胞资源中心,青蒿琥酯购于桂林南药股份有限公司(批号H10930195)。培养基F12K购于Sigma公司;BCA蛋白分析试剂盒购于Pierce公司;Transwell小室购于Coster公司;基底膜胶(Matrigel)购于BD公司; HMGB1 抗体、MMP-2抗体、β-actin抗体均购于Santa Cruz公司。
1.2 方法 1.2.1 细胞培养人大肠癌Lovo细胞株采用F12K培养基,常规培养于含5%CO2的37℃温箱中,待细胞进入对数生长期后,用不同浓度(20、80、160 μmol·L-1)的青蒿琥酯处理Lovo细胞,不加药物组为阴性对照,进行以下实验。
1.2.2 软琼脂集落形成实验参照文献方法[1],取对数生长期的各组细胞5 000个,接种于含下层5 g·L-1琼脂糖和上层3.5 g·L-1琼脂糖的6孔板中,37℃和5% CO2实验条件下培养14 d后,倒置相差显微镜下计数大于10个细胞的集落数,并计算细胞集落抑制率。集落抑制率/%=(1-给药组集落数/对照组集落数)×100%
1.2.3 Transwell小室侵袭实验参照文献方法[2]进行以下实验。Transwell小室的上室底部为孔径8 μm的聚碳酸酯膜,膜上铺匀1 ∶4稀释的基底膜胶(matrigel)。下室加预先制备的Lovo细胞培养上清液600 μL,上室加入100 μL不含胎牛血清的培养液,然后按照1×105个细胞的密度在上室加入ART(20、80、160 μmol·L-1)处理后的细胞悬液30 μL,每组4个复孔。37℃、5%CO2温箱中培养24 h,取出滤膜,用棉签擦尽膜上Matrigel及未穿过的细胞,甲醇固定5 min,HE染色。光镜200倍,随机计数5个视野的穿膜细胞数,取每个视野的平均数表示肿瘤细胞侵袭能力。
1.2.4 HMGB1和MMP-2蛋白水平检测提取各组Lovo细胞总蛋白,对蛋白定量后进行常规Western blot法检测各组蛋白水平,与内参照β-actin的测定结果相对比,利用Kodak Digital Science ID Image Analysis Software (Eastman Kodak Company,USA)测定各条带净灰度值。
1.2.5 统计学方法采用SPSS 13.0统计软件对数据进行统计学分析。对计量单位,用x± s 表示,样本均数比较采用单因素方差分析(one way ANOVA)。
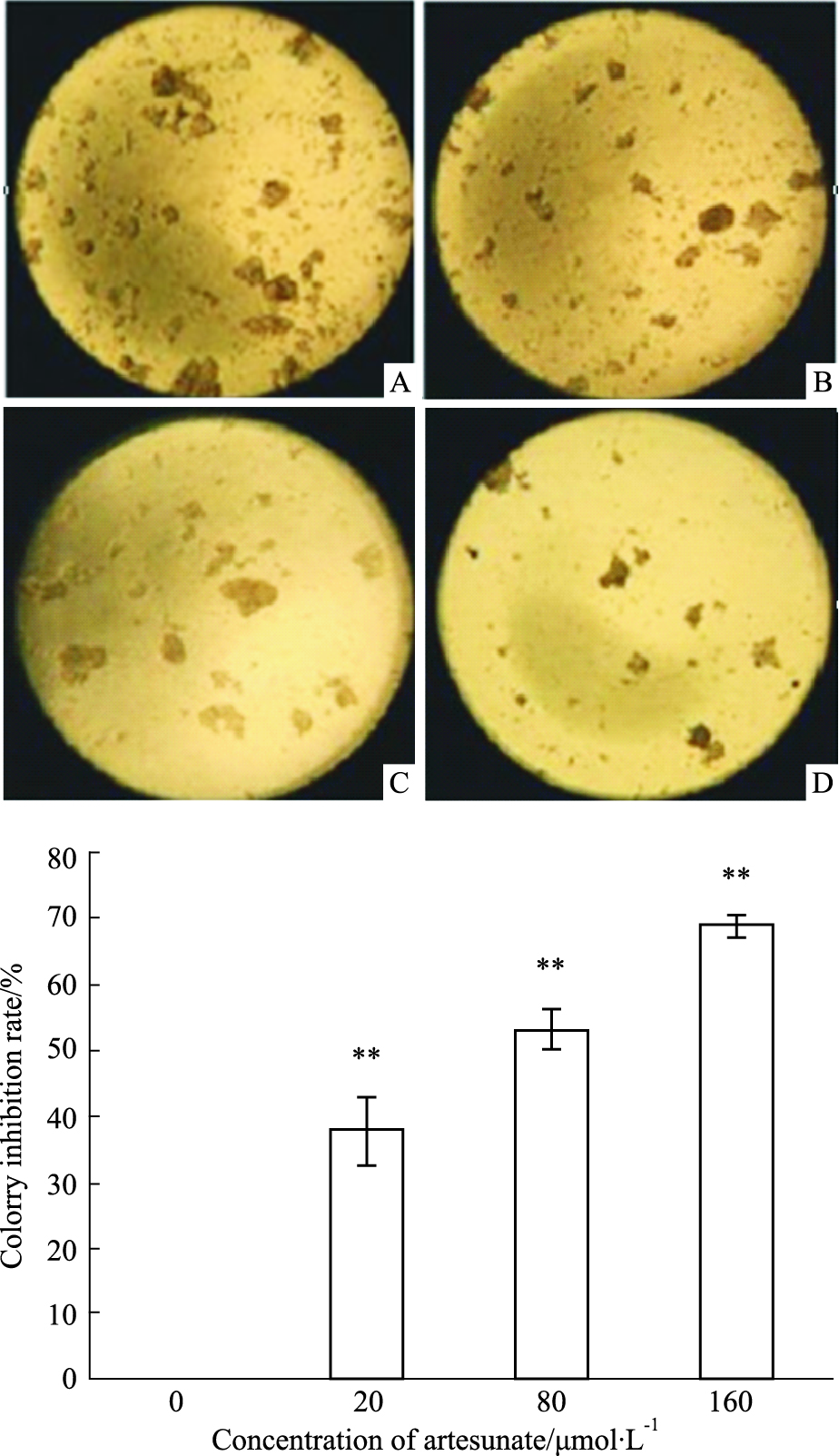
2 结果 2.1 青蒿琥酯对大肠癌Lovo细胞软琼脂集落形成的影响人大肠癌Lovo细胞可自发形成集落。经青蒿琥酯处理48 h后发现,青蒿琥酯处理组(20 μmol·L-1)即出现Lovo细胞集落生成减少;与对照组相比,青蒿琥酯由低到高浓度处理组集落形成抑制率分别为(38.01±5.12)%、(53.05±2.92)%和(69.37±1.84)%,呈剂量依赖性(P < 0.01,Fig 1)。
|
| Fig 1 Influence of soft-agar colony formation of the artesunate on Lovo cells (n=5) A: Blank control, B: 20μmol·L-1 ART, C: 80μmol·L-1, D: 160μmol·L-1 ART. **P < 0.01 vs control(0 μmol·L-1) |
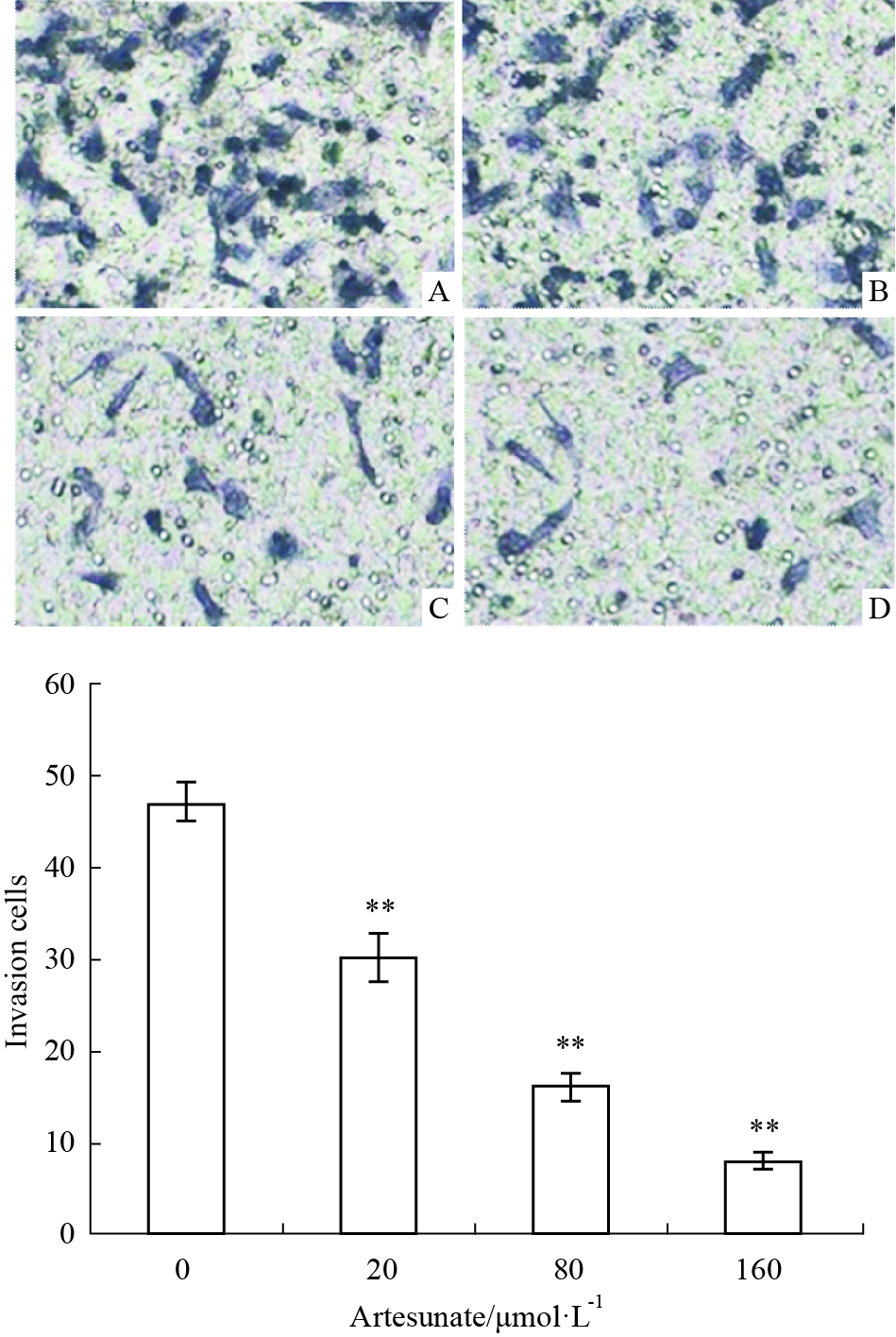
与对照组比较,随青蒿琥酯浓度增高,Lovo细胞穿过滤过膜的细胞数分别为30.33±2.52、15.67±1.53,8.00±1.00,呈明显下降趋势,与对照组(47.00±2.00)相比,差异有统计学意义(P < 0.01,Fig 2)。
|
| Fig 2 Effect of artesunate on invasion of Lovo cells detected by Matrigel contained transwell chamber assay (n=5) A:Blank control, B~D: 20, 80, 160 μmol·L-1 ART. **P < 0.01 vs control(0 μmol·L-1) |
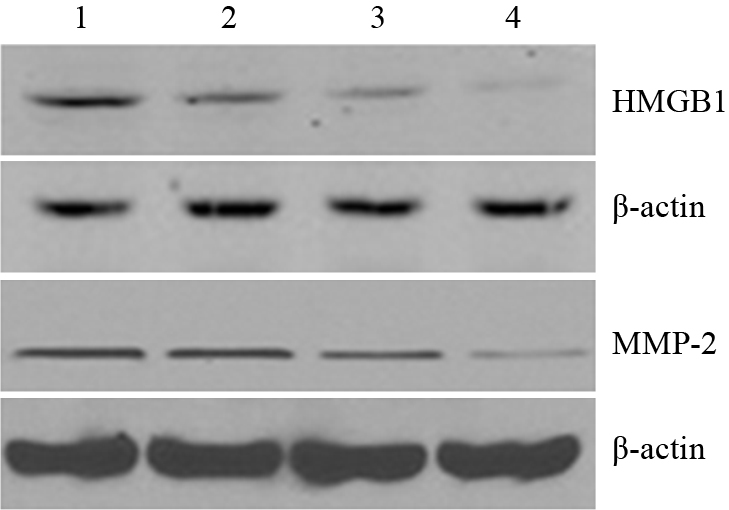
青蒿琥酯处理细胞后,于48 h收集细胞,进行Western blot检测,结果发现,与对照组相比,处理组HMGB1和MMP-2蛋白水平均随浓度升高而降低(Tab 1,Fig 3)。
|
| Fig 3 Effects of artesunate on expression of HMGB1 and MMP-2 in Lovo cells 1: Control; 2~4:20, 80, 160 μmol·L-1 ART |
| (n=3) | ||||
| Group | HMGB1 | MMP2 | ||
| Protein expression | Inhibition rate/% | Protein expression | Inhibition rate/% | |
| Control | 1.07±0.02 | 1.05±0.02 | ||
| 20 μmol·L-1 ART | 0.87±0.09** | 18.69 | 0.97±0.03 | 7.62 |
| 80 μmol·L-1 ART | 0.49±0.01** | 54.21 | 0.56±0.07** | 46.67 |
| 160 μmol·L-1 ART | 0.24±0.06** | 77.57 | 0.28±0.04** | 73.33 |
ART作为一种中药提取成分,广泛应用于抗疟治疗,近几年,人们发现它也有抗肿瘤功效,但对肿瘤的抑制作用研究仍不深入。大肠癌是常见的消化道恶性肿瘤之一,临床研究发现,20%的患者在诊断时就已经发生了转移,另外早期诊断为大肠癌的患者,有半数最终也发生了远处转移[3],所以控制肿瘤细胞的侵袭转移刻不容缓。大多数正常的真核细胞(除成熟红细胞外),只有黏附在特定的细胞外基质上才能存活,称为锚着依赖性(anchorage dependence)。而肿瘤细胞其恶性程度可以利用其锚着不依赖性检测肿瘤细胞的主动移动能力。软琼脂中的克隆形成率则反映细胞的群体依赖性和增殖能力,是反映肿瘤细胞的恶性度的重要指标。研究发现,软琼脂形成集落的多少与肿瘤恶性程度呈正相关[4]。癌细胞侵袭能力越强,软琼脂上形成的集落数目越多且集落体积越大[5]。本研究发现,大肠癌细胞经不同浓度的青蒿琥酯处理后,软琼脂集落数明显减少,且呈浓度依赖性(P < 0.01),提示青蒿琥酯可在某种程度上抑制大肠癌细胞的恶性增殖能力。
肿瘤细胞的侵袭转移的关键环节之一是通过侵袭细胞外基质来实现[6]。目前常用的基质胶matrigel主要成分由层黏连蛋白、Ⅳ型胶原、巢蛋白、硫酸肝素糖蛋白等组成,还包含生长因子和基质金属蛋白酶等,与细胞外基质的成分非常相近,能有效地模拟肿瘤细胞在体外的侵袭过程。黄伟炜等[7]以人结肠癌细胞HCT-8为模型,采用软琼脂集落培养试验发现青蒿琥酯可明显抑制结肠癌HCT-8细胞的侵袭,其抑制作用与减少肿瘤新生血管有关。本研究发现,大肠癌Lovo细胞有较强的侵袭能力,而经过青蒿琥酯处理后,穿过聚碳酸脂膜的细胞数呈浓度依赖性减少(P < 0.01),提示青蒿琥酯可抑制大肠癌细胞的侵袭能力,本研究进一步从降解细胞外基质的途径探讨青蒿琥酯侵袭抑制机制。
基质金属蛋白酶(matrix metalloproteinases,MMPs)几乎能降解细胞外基质的所有成分,在肿瘤细胞侵袭转移中占重要位置[8]。其中MMP-2是该家族的重要成员之一,在许多肿瘤如肝细胞癌[9]、子宫内膜癌[10]、肺癌[11]、结肠癌[12]、胃癌[13]等组织中过表达,而在正常组织中表达很低或不表达也得到证实。近来有学者发现,MMP-2基因作为肿瘤标志物,与某些癌细胞侵袭有关,在肿瘤的诊断、治疗和预后发挥作用[14]。高迁移率族蛋白B1(high mobility group protein B1,HMGB1)因其在聚丙烯酰胺凝胶电泳中的高迁移率而得名。研究发现HMGB1通过与晚期PAGE结合,激活MAPK、p38、JNK等信号通路,引起MMPs等肿瘤相关因子的激活[15],降解细胞外基质,从而促进肿瘤的浸润和转移。同时,也有研究发现大肠癌细胞侵袭转移能力增强与HMGB1的高表达密切相关[16]。本研究以不同浓度青蒿琥酯处理大肠癌Lovo细胞后,应用Western blot法检测HMGB1和MMP-2蛋白水平。结果发现,青蒿琥酯处理组HMGB1和MMP-2蛋白水平均明显下调,提示青蒿琥酯影响HMGB1与相应受体结合,抑制细胞核外的相关信号通路,导致MMP-2表达下降,阻碍细胞外基质的降解,减少细胞向远处侵袭转移的可能性。
综上所述,青蒿琥酯在体外培养中证实能抑制大肠癌细胞增殖和侵袭,有可能成为一个有较好前景的抗肿瘤中成药,其抑制侵袭作用通过何种信号通路仍有待进一步研究。
(致谢:本文实验在河北北方学院生命科学研究中心完成。)
| [1] | 张明芳, 郭亚, 齐元麟, 等. RNAi沉默Notch1基因对人胶质瘤U251细胞增殖能力的影响[J].中国药理学通报, 2010,26(2):199-203.Zhang M F, Guo Y, Qi Y L, et al. Effect of silencing Notch1 gene expression by RNA interference on proliferation of human glioma U251 cells[J]. Chin Pharmacol Bull, 2010,26(2):199-203. |
| [2] | 陈美娟, 赵若琳, 郭园园, 等. 麦冬皂苷B对A549细胞株体外黏附、侵袭及迁移的抑制作用及机制研究[J].中国药理学通报, 2015,31(5):660-4.Chen M J, Zhao R L, Guo Y Y, et al. Inhibitory effect of ophiopogonin-B on adhesion, invasion and migration of A549 cells in vitro[J]. Chin Pharmacol Bull, 2015,31(5):660-4. |
| [3] | Zhang W,Zhang T,Jin R,et al. MicroRNA-301a promotes migration and invasion by targeting TGFBR2 in human colorectal cancer[J]. J Exp Clin Cancer Res,2014,33(1):113. |
| [4] | Thapa N, Choi S, Hedman A,et al. Phosphatidylinositol phosphate 5-kinase Iγi2 in association with Src controls anchorage-independent growth of tumor cells[J]. J Biol Chem, 2013,288(48):34707-18. |
| [5] | Huang W S,Wang T B,He Y,et al. Phosphoinositide-3-kinase, catalytic, alpha polypeptide RNA interference inhibits growth of colon cancer cell SW948[J]. World J Gastroenterol, 2012,18(26):3458-64. |
| [6] | Hsu H H,Kuo W W,Ju D T, et al. Estradiol agonists inhibit human Lovo colorectal cancer cell proliferation and migration through p53[J]. World J Gastroenterol, 2014,20(44):16665-73. |
| [7] | 黄伟炜, 牛红军, 刘宁. 青蒿琥酯对人结肠癌HCT-8细胞侵袭能力影响及机制研究[J].中成药, 2011,33(12):2062-4.Huang W W, Niu H J, Liu N. Artesunate inhibiting invasion induced by human colon cancer HCT-8 cells and its mechanism[J]. Chin Tradit Patent Med, 2011,33(12):2062-4. |
| [8] | Zhu J, Liang L, Jiao Y,et al. Enhanced invasion of metastatic cancer cells via extracellular matrix interface[J]. PLoS One, 2015,10(2):e0118058. |
| [9] | Suh Y G,Lee E J,Cha H,et al. Prognostic values of vascular endothelial growth factor and matrix metalloproteinase-2 in hepatocellular carcinoma after radiotherapy[J]. Dig Dis, 2014,32(6):725-32. |
| [10] | Yi K W,Kim S H,Ihm H J, et al. Increased expression of p21-activated kinase 4 in adenomyosis and its regulation of matrix metalloproteinase-2and-9 in endometrial cells[J]. Fertil Steril, 2015,103(4):1089-97. |
| [11] | Fa K N, Yang C M, Chen P C, et al. Anti-metastatic effects of antrodan, the Antrodia cinnamomea mycelia glycoprotein, in lung arcinoma cells[J]. Int J Biol Macromol, 2015,74:476-82. |
| [12] | Kostova E, Slaninka-Miceska M, Labacevski N,et al. Expression of matrix metalloproteinases 2, 7 and 9 in patients with colorectal cancer[J]. Vojnosanit Pregl, 2014,71(1):52-9. |
| [13] | Gurgel D C, Valença-Junior J T, Dornelas C A,et al. Immunoexpression of metalloproteinases 2 and 14 and TIMP-2 inhibitor in main types of primary gastric carcinomas and lymph node metastasis[J]. Pathol Oncol Res, 2015,21(1):73-81. |
| [14] | Kamyab-Hesari K,Mohtasham N,Aqhazadeh N, et al. The expression of MMP-2 and Ki-67 in head and neck melanoma, and their correlation with clinic-pathologic indices[J]. J Cancer Res Ther, 2014,10(3):696-700. |
| [15] | Ohmori H,Luo Y,Kuniyasu H. Non-histone nuclear factor HMGB 1 as a therapeutic target in colorectal cancer[J].Expert Opin Ther Tarqets, 2011,15(2):183-93. |
| [16] | Süren D,Yildirim M,Demirpençe Ö, et al. The role of high mobility group box 1(HMGB1) in colorectal cancer[J].Med Sci Monit,2014,20:530-7. |

