


TGR5,也称M-BAR、GPBAR或者GPR131。由330 个氨基酸组成,包含7 个跨膜结构域,属于G蛋白偶联受体家族成员,是一种新型胆汁酸受体[1]。近年研究发现,激活TGR5可以减少巨噬细胞炎症反应,抑制单核细胞中促炎症因子的表达[2, 3],另外,还可以促进胰高血糖素样肽-1(GLP-1)的分泌,使胰岛素水平增加[4],调控能量代谢相关基因的表达,改善胰岛素抵抗等[5]。TGR5在炎症、糖脂代谢等方面均有非常重要的调节作用,但目前尚未见它在糖尿病肾病方面的报道。
糖尿病肾病(diabetic nephropathy,DN)是糖尿病常见的微血管并发症,是终末期肾病发生的主要原因。病理特征主要表现为肾脏纤维化、系膜细胞增生、细胞外基质的堆积以及系膜区增宽等[6]。纤维连接蛋白(fibronectin,FN)是细胞外基质的重要组成部分,能有效反映其堆积程度[7, 8];而转化生长因子TGF-β1可以促进胞外基质的合成,加速肾脏纤维化[9, 10],两者都是糖尿病肾病的重要指标。
为此,实验以大鼠肾小球系膜细胞为研究对象,予以高糖刺激模拟糖尿病肾病的体内环境,检测了TGR5的表达情况,并运用特异性激动剂INT-777激活TGR5,或者使用过表达、干扰TGR5的方法,检测FN、TGF-β1的变化,进而探索TGR5在糖尿病肾病中发挥的作用。
1 材料与方法 1.1 细胞的传代和培养大鼠肾小球系膜细胞的原代分离培养按以前的实验方法进行[11]。细胞鉴定后,取5~12代的细胞进行实验。培养于含10% 胎牛血清的DMEM培养基中,37 ℃,5% CO2,每2~3 d使用5% 胰酶消化传代。细胞生长至汇合时,用无血清培养基处理24 h,之后再予以不同的分组处理。
1.2 实验试剂D-( + )-葡萄糖和胰蛋白酶(Sigma);胎牛血清(HyClone);DMEM培养基(Gibco);识别FN,TGR5的抗体(Santa Cruz Biotechnology),识别TGF-β1的抗体(Cell Signaling Technology)和识别α-tubulin的抗体(Sigma);辣根过氧化物酶偶合的兔、鼠二抗(Promega);INT-777(MedChem Express)。
1.3 质粒的转染质粒TGR5以及空载购自Origene。将系膜细胞接种至培养皿中常规培养,细胞生长近融合至60%~80%时,即可开始转染实验。转染试剂按LipofectamineTM LTX & Plus Reagent(Life Technologies)的说明书进行使用。转染24 h后,无血清培养24 h,使细胞同步化,再给予高糖和INT-777刺激24 h,收集细胞用于Western blot检测。
1.4 TGR5干扰实验消化重悬的系膜细胞接种至培养皿中常规培养,细胞生长近融合至60%~80%时即可开始干扰实验。干扰序列购自Genepharma,正义链5′-GCUUCUUUCUAAGCCUACUTT-3′;反义链5′-AGUAGGCUUAGAAAGAAGCTT-3′。干扰试剂按 LipofectamineTM RNAiMAX Transfection Reagent(Life Technologies)的说明书进行使用。48 h后收集细胞用于Western blot检测。
1.5 Werstern blot检测大鼠肾小球系膜细胞FN以及TGF-β1的蛋白水平细胞终止培养后,弃培养基,在冰上用预冷的PBS漂洗2次,弃去PBS,加去污裂解液,刮下细胞收集裂解液至1.5 mL EP管,裂解完毕后离心取上清,用BCA法测定蛋白含量。之后将提取蛋白进行凝胶电泳,每个泳道上样量为20 μg总蛋白。电泳结束后,电转至PVDF膜或者NC膜(Millipore)上。一抗4 ℃孵育12~16 h,之后分别用对应的辣根过氧化物酶标记的二抗室温孵育1 h。洗膜后曝光,显影。利用图像分析软件Quantity One(Bio-Rad)确定目的条带的光密度值。
1.6 统计学分析数据采用Graphpad Prism 5.0进行分析,组间比较、组内比较用t检验,多组比较用方差分析(单因素方差分析、LSD法),结果用 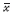 ± s表示。
± s表示。
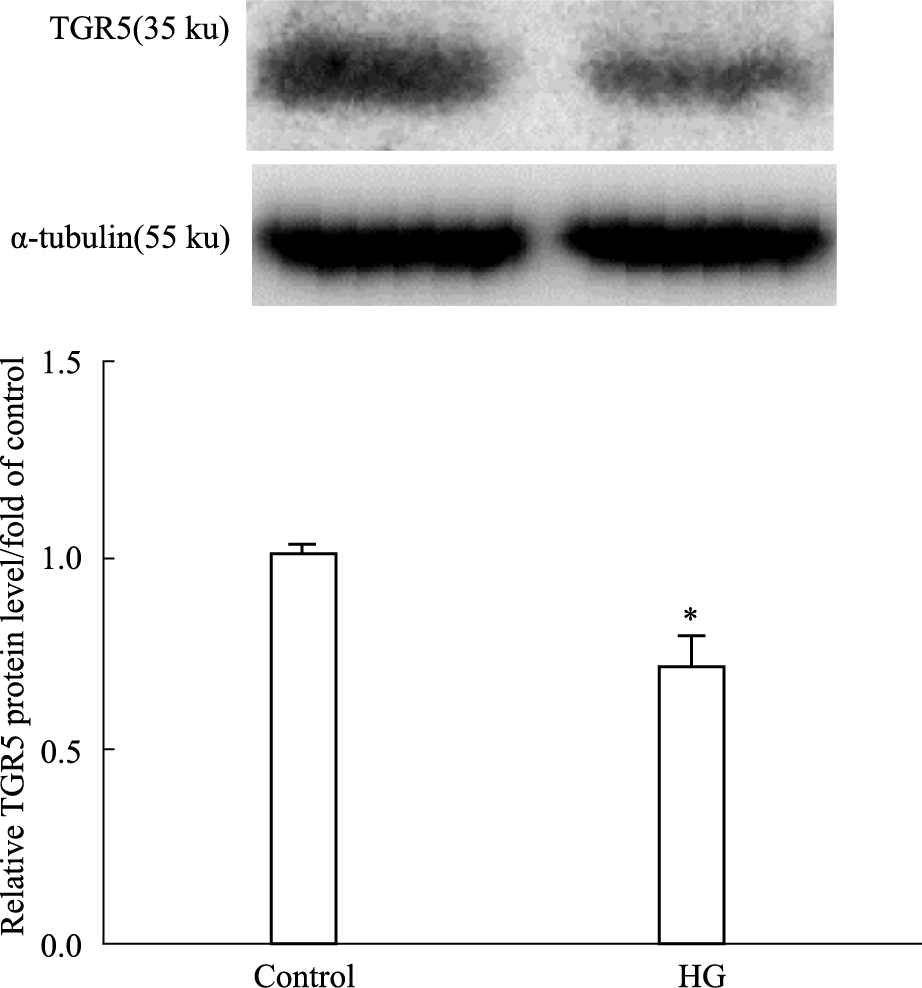
从Fig 1可以看出,大鼠肾小球系膜细胞中存在TGR5的表达,为进一步实验提供了基础。与正常对照组相比,高糖组TGR5的蛋白表达水平下降,提示TGR5可能参与了糖尿病肾病的发展进程,具体作用有待进一步探讨。
|
| Fig 1 Protein level of TGR5 in rat glomerular mesangial cells *P < 0.05 vs control |
INT-777是TGR5的一种特异性激动剂[12]。如Fig 2所示,与正常对照组相比,高糖组的FN及TGF-β1蛋白水平均明显上升。在此基础上加入特异性激动剂INT-777(终浓度为10 μmol·L-1)处理,FN蛋白水平下调(P < 0.01),TGF-β1的表达也明显减少(P < 0.05)。由此可见,激动TGR5可以抑制由高糖引起的FN、TGF-β1蛋白水平的异常升高。

|
| Fig 2 Effects of INT-777 on protein expression of FN and TGF-β1 in high glucose-treated rat glomerular mesangial cells *P < 0.05, **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs HG |
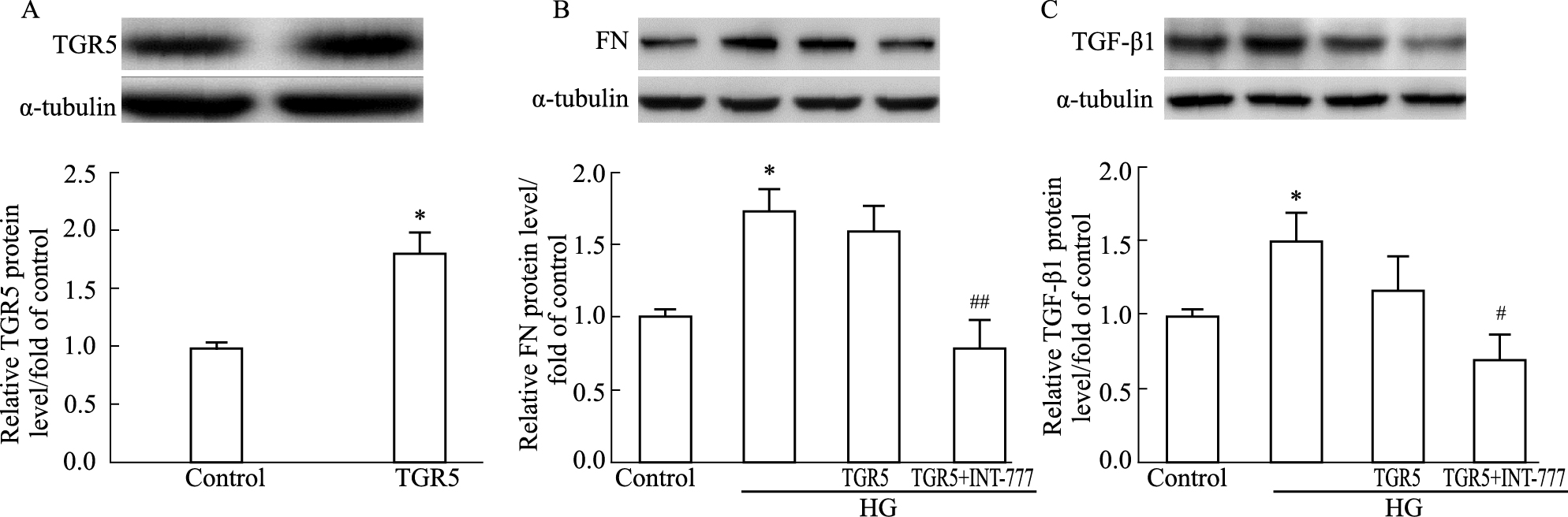
为进一步确定TGR5发挥的作用,采用TGR5过表达的方法,并于过表达后进一步予以INT-777刺激来检测FN及TGF-β1的表达情况。从Fig 3A可以看出,与对照组相比,过表达组的TGR5蛋白表达明显升高(P < 0.05)。如Fig 3B-C所示,与高糖组相比,TGR5过表达组的FN、TGF-β1的蛋白水平已经有下降的趋势。在此基础上予以INT-777刺激,FN与TGF-β1的蛋白水平均更进一步下调(P < 0.01,P < 0.05)。
|
| Fig 3 Effects of TGR5 overpression on protein expression of FN and TGF-β1 in high glucose-treated rat glomerular mesangial cells *P < 0.05 vs control; #P < 0.05, ##P < 0.01 vs HG |
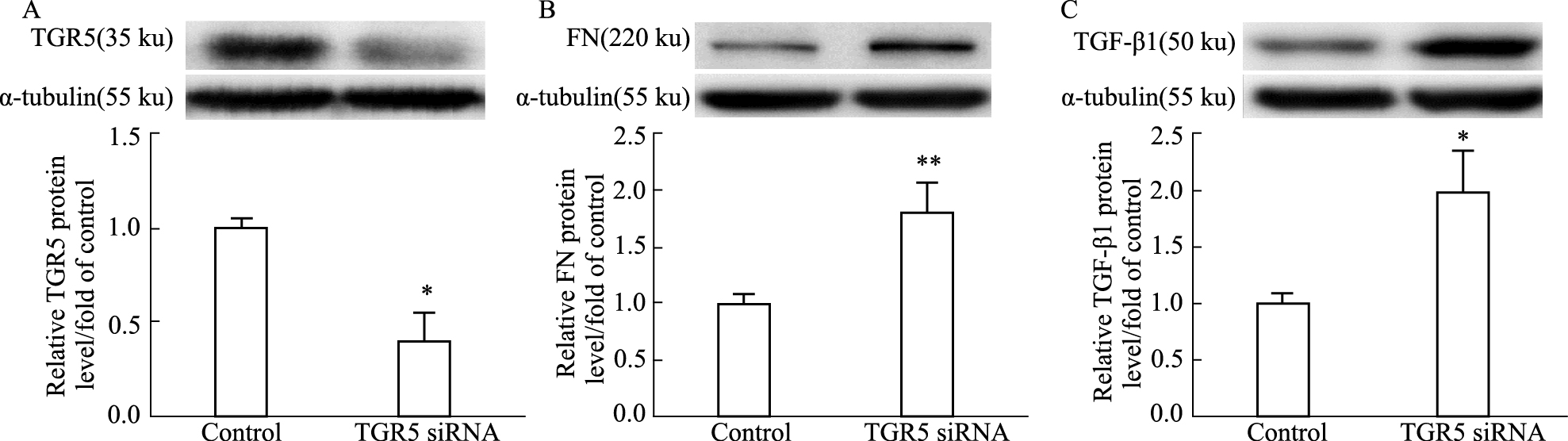
另一方面,对TGR5进行干扰,以验证它对于FN及TGF-β1的调控作用。从Fig 4A中可以看出,TGR5干扰序列的干扰效率达到70%。如Fig 4B-C所示,与对照组相比,干扰TGR5后,FN及TGF-β1的蛋白水平均异常升高(P < 0.01,P < 0.05),远高于正常水平,说明TGR5在肾小球系膜细胞中确实可以阻止FN、TGF-β1的蛋白异常表达。
|
| Fig 4 Effects of TGR5 knockdown on protein expression of FN and TGF-β1 in rat glomerular mesangial cells *P < 0.05, **P < 0.01 vs control |
大量研究表明,高糖可以导致转化生长因子的增加,促进胞外基质的堆积,是糖尿病肾病发生的重要原因[9, 13]。大鼠肾小球系膜细胞是肾小球的主要功能细胞[14],细胞外基质的产生、细胞因子的分泌等都与之有关,在肾脏的生理功能和组织结构的维护中有着重要作用[8]。在糖尿病状态下,大鼠肾小球系膜细胞中转化生长因子TGF-β1等细胞因子的表达增加、FN等细胞外基质的大量积聚,促进肾脏纤维化,导致系膜区扩张,促成了糖尿病肾病的病理变化[7, 9]。本研究利用高糖培养大鼠肾小球系膜细胞,FN及TGF-β1的蛋白水平相对于正常对照组明显上升,成功模拟了体内糖尿病肾病的环境。
TGR5可以被一定浓度范围内的鹅去氧胆酸(CDCA),石胆酸(LCA),胆酸(CA),脱氧胆酸(DCA)等激活,但均无较好的特异性[15]。本研究采用半合成胆酸衍生物INT-777作为TGR5的激动剂,它毒性低,有较高的效价和选择特异性,可以排除胆汁酸核受体FXR的影响[12]。此外,我们使用了过表达的方法,并在此基础上再次使用该激动剂,进一步增强了TGR5的功能,有效地降低了由高糖引起的FN、TGF-β1蛋白水平升高,而干扰TGR5引起这些指标的异常上升则从功能缺失的角度更好地突显了TGR5对于FN、TGF-β1蛋白表达的抑制作用。
对于糖尿病肾病的治疗,目前多采取控制血糖、调节血脂等方法进行综合治疗,缺乏特异有效的方法。采取有针对性的方法阻止糖尿病肾病的发生,探讨其有效靶点,具有重要的意义。近年来发现,胆汁酸受体不仅参与胆汁酸的合成与代谢,而且在糖脂代谢以及能量消耗中也发挥着重要的调节作用[1]。TGR5作为一种新型胆汁酸膜受体,其发挥的生理功能有待积极探索。本研究在大鼠肾小球系膜细胞中检测到了TGR5的表达,并在使用不同方法干预TGR5之后,检测了糖尿病肾病进程中的重要指标FN、TGF-β1的表达变化,证实了TGR5可以抑制高糖状态下这两者的异常升高,在糖尿病肾病进程中可能发挥着重要的保护作用,有望成为该疾病的新靶标,为治疗提供了新的思路。
(致谢:本研究在中山大学药学院药理与毒理学实验室完成,实验室老师和同学在课题的设计、实验的具体操作上均给予了大力的支持与帮助,在此表示衷心的感谢!)
| [1] | Pols T W, Noriega L G, Nomura M, et al. The bile acid membrane receptor TGR5 as an emerging target in metabolism and inflammation[J]. J Hepatol, 2011, 54(6):1263-72. |
| [2] | Pols TW, Nomura M, Harach T, et al. TGR5 activation inhibits atherosclerosis by reducing macrophage inflammation and lipid loading[J]. Cell Metab, 2011, 14(6):747-57. |
| [3] | Hogenauer K, Arista L, Schmiedeberg N, et al. G-protein-coupled bile acid receptor 1(GPBAR1, TGR5) agonists reduce the production of proinflammatory cytokines and stabilize the alternative macrophage phenotype[J]. J Med Chem, 2014, 57(24):10343-54. |
| [4] | Thomas C, Gioiello A, Noriega L, et al. TGR5-mediated bile acid sensing controls glucose homeostasis[J]. Cell Metab, 2009, 10(3):167-77. |
| [5] | Watanabe M, Houten S M, Mataki C, et al. Bile acids induce energy expenditure by promoting intracellular thyroid hormone activation[J]. Nature, 2006, 439(7075):484-9. |
| [6] | Kanwar Y S, Sun L, Xie P, et al. A glimpse of various pathogenetic mechanisms of diabetic nephropathy[J]. Annu Rev Pathol, 2011, 6:395-423. |
| [7] | 李学娟, 陈泽彬, 魏红, 等. 大黄素对高糖培养的GMC增殖、FN表达及p38MAPK的影响[J]. 中国药理学通报, 2014, 30(2):233-8. Li X J, Chen Z B, Wei H, et al. Effects of emodin on cell proliferation, FN expression and p38MAPK pathway in rat mesangial cells cultured under high glucose[J]. Chin Pharmacol Bull, 2014, 30(2):233-8. |
| [8] | Huang K, Huang J, Xie X, et al. Sirt1 resists advanced glycation end products-induced expressions of fibronectin and TGF-beta1 by activating the Nrf2/ARE pathway in glomerular mesangial cells[J]. Free Radic Biol Med, 2013, 65:528-40. |
| [9] | Xie X, Xia W, Fei X, et al. Relaxin inhibits high glucose-induced matrix accumulation in human mesangial cells by interfering with TGF-beta1 production and mesangial cells phenotypic transition[J]. Biol Pharm Bull, 2015, 38(10):1464-9. |
| [10] | 余敏, 周宏灏, 刘昭前. 糖尿病肾病相关基因研究进展[J]. 中国药理学通报, 2008, 24(11):1419-22. Yu M, Zhou H H, Liu Z Q. Progress in related genes of diabetic nephropathy[J]. Chin Pharmacol Bull, 2008, 24(11):1419-22. |
| [11] | Geoffroy K, Wiernsperger N, laqarde M, E1 Bawab S. Bimodal effect of advanced glycation end products on mesangial cell proliferation is mediated by neutral ceramidase regulation and endogenous sphingolipids[J]. J Biological Chem, 2004, 279(33):34343-52. |
| [12] | Pellicciari R, Gioiello A, Macchiarulo A, et al. Discovery of 6alpha-ethyl-23(S)-methylcholic acid (S-EMCA, INT-777) as a potent and selective agonist for the TGR5 receptor, a novel target for diabesity[J]. J Med Chem, 2009, 52(24):7958-61. |
| [13] | 刘慰华, 刘世明, 林双峰, 等. 黄连素通过S1P2-MAPK信号通路抗糖尿病肾纤维化作用机制研究[J]. 中国药理学通报, 2013, 29(5):723-728. Liu W H, Liu S M, Lin S F, et al. Role of berberine in fibronectin expression via S1P2-MAPK signaling pathway in diabetic nephropathy[J]. Chin Pharmacol Bull, 2013, 29(5):723-8. |
| [14] | Cove-Smith A, Hendry B M. The regulation of mesangial cell proliferation[J]. Nephron Exp Nephrol, 2008, 108(4):e74-9. |
| [15] | Stepanov V, Stankov K, Mikov M. The bile acid membrane receptor TGR5:a novel pharmacological target in metabolic, inflammatory and neoplastic disorders[J]. J Recept Signal Transduct Res, 2013, 33(4):213-23. |

