


2. 安徽华星化工股份有限公司, 安徽 合肥 230088
2. Anhui Huaxing Chemical Industry Co. LTd, Hefei 230088, China
EILDVP(Glu-Ile-Leu-Asp-Val-Pro)是细胞外基质纤维黏连蛋白(NF)与极迟抗原-4(very late antigen-4,VLA-4;整合蛋白α4β1)结合的配体的CS-1区序列,其中LDV(Leu-Asp-Val)序列为其关键的三肽[1]。VLA-4广泛分布于淋巴细胞、中性和嗜酸性粒细胞等炎症细胞表面,其与NF、血管细胞黏附分子-1(VCAM-1)的结合和相互作用是炎症启动和发展过程中炎性细胞黏附、迁移至血管外组织的关键步骤。研究表明,EILDVP等含LDV序列肽可竞争抑制炎细胞与NF、VCAM-1的结合和相互作用,干扰类风湿关节炎、哮喘等慢性炎症和自身免疫性疾病的病理过程[2, 3, 4, 5, 6]。但是,与其它肽类分子性质相似,现有以LDV序列为基础结构的VLA-4拮抗肽由于分子量小,易被清除和酶解破坏,其体内代谢时间短,较大的治疗剂量和较短的给药时间间隔可能成为其应用的障碍。利用目前国际公认的聚乙二醇(polyethlene glycol,PEG)修饰增加蛋白质和多肽药物稳定性、延长血浆半衰期等药物性能改善特点,我们对EILDVP肽进行了聚乙二醇修饰[5, 6, 7]。本文比较了125I标记2 ku和20 ku分子质量直链甲氧基聚乙二醇(mPEG2000和mPEG20000)修饰EILDVP肽的小鼠血药浓度和相关药代动力学参数,实验结果报告如下。
1 材料与方法 1.1 受试化合物与试剂化合物A:EILDVP-Tyr-NH2、化合物B(mPEG2000修饰肽):EILDVP-Cys(mPEG2000-MAL)-Tyr-NH2、化合物C(mPEG20000修饰肽):EILDVP-Cys (mPEG20000 -MAL)-Tyr-NH2,为本实验室采用Fmoc固相方法合成,RP-HPLC方法纯化,质量分数分别为0.995、0.959和0.992;MS鉴定,化合物A分子质量为847.6 u,化合物B在3 050.0 u附近有一组相差44的峰,化合物C在21 050.7 u附近有一组相差44的峰,与预期相符。委托北方生物技术研究所采用氯胺T法对3种化合物进行125I标记,并经PR-HPLC方法分离纯化;标记化合物A放射性比活性为1.005 Bq·g-1、化合物B为0.344 Bq·g-1、化合物C为0.264 Bq·g-1;3种125I标记肽放化纯度(质量分数) 均高于0.95;生理盐水稀释至使用浓度。碘化钠(NaI)、三氯乙酸(TCA)为天津大茂化学试剂厂产品,分析纯;其余试剂为国产分析纯;实验用水为超纯水。
1.2 主要仪器γ 计数器:MF-1000型,西安凯普公司产品;低温冷冻离心机:KDC-2046型,科大创新股份有限公司中佳分公司产品。
1.3 实验动物及其分组给药KM小鼠,清洁级,体质量20~25 g,由河北省实验动物中心提供,合格证编号810145。以上小鼠随机分为125I标记的化合物A、B、C 3组。实验前12 h,各小鼠im质量浓度20 g·L-1 NaI生理盐水溶液0.25 mL饱和甲状腺,禁食不禁水,参考预实验计算的3种125I标记肽半衰期(T1/2)和初始血药浓度(C0),进一步按给药后0.08、0.25、0.5、1、2、4、6、8、24、32、48和72 h采血时间点,将小鼠随机分为A组0.08~6 h组、B组0.08~32 h组、C组0.08~72 h组,每组5只小鼠,♀♂兼用(♀3只♂2只,或♀2只♂3只),按5 mL·kg-1容积分别尾静脉注射3.441GBq·L-1浓度的3种125I标记肽。
1.4 血样样品处理[8]各组单次给药后,分别在各采血时间点,于动物眼眶取血0.2 mL,肝素抗凝,全血在4℃条件下6 000×g离心10 min,取血浆-20℃保存备用。检测时取25 μL血浆样品,加入175 μL纯水,混匀后,加入等容积质量浓度200 g·L-1的TCA溶液沉淀蛋白,4℃条件下6 000×g离心10 min后弃上清,测定酸沉淀部分的放射性,换算为μmol·L-1。
1.5 标准曲线制备[8]分别将3种125I标记肽以纯水配制成3.75、7.5、15、30、60、120、240、480 μg·L-1浓度的标准液。分别取以上标准液10 μL,加入小鼠空白血浆25 μL、纯水165 μL,混匀后加入等容积质量浓度200 g·L-1的TCA溶液沉淀蛋白,每个浓度做3个平行管,“1.4”方法测定沉淀部分放射性,换算为μmol·L-1。以测定样品125I标记肽浓度为横坐标,放射性为纵坐标,分别做3种125I标记肽的标准曲线。
1.6 样品在血浆中回收率、精密度测定[8]按照标准曲线中溶液的配制方法,将3种125I标记肽分别配制为15、60、240 μg·L-1浓度,分别进行回收率和精密度测定。回收率的测定:取3个浓度3种125I标记肽稀释液,测定其总放射性,用等容积质量浓度200 g·L-1的TCA沉淀后,测定其沉淀放射性,计算沉淀放射性占总放射性的百分比。精密度的测定:3种125I标记肽每个浓度设6个平行管,同批测定,评价批内精密度。
1.7 实验动物血药浓度的测定和药代动力学参数计算各组小鼠按“1.3”方法尾静脉注射3种125I标记肽,按“1.4”方法取样并测定沉淀物放射性,测定并换算数据分别代入相应标准曲线方程,求出各时间点血药浓度。3P97药动学统计软件对取得的血药浓度-时间数据进行处理,计算药代动力学参数。
2 结果 2.1 125I标记EILDVP及其聚乙二醇修饰肽的标准曲线、回收率和精密度3.75~480 μg·L-1测定浓度范围内,125I标记的EILDVP-Tyr-NH2、EILDVP-Cys(mPEG2000-MAL)-Tyr-NH2和EILDVP-Cys(mPEG20000-MAL)-Tyr-NH2肽(化合物A、B、C)的放射数值与肽浓度均呈良好线性关系,回归方程分别为:=25.73X+61.02(r=0.995)、=33.06X+79.71(r=0.992)、=46.07X+2.62(r=0.994);3种125I标记肽在浓度为15、60和240 μg·L-1时,回收率在88.92%~106.66%之间,日内变异系数(RSD) < 10%(Tab1)。
( ± s,n=6) ± s,n=6) |
||||||
| Group/μg·L-1 | A | B | C | |||
| Recovery/% | RSD/% | Recovery/% | RSD/% | Recovery/% | RSD/% | |
| 240 | 97.48 | 8.08 | 104.66 | 4.49 | 88.92 | 3.55 |
| 60 | 101.86 | 4.43 | 97.78 | 7.81 | 106.66 | 8.32 |
| 15 | 104.86 | 5.21 | 94.82 | 9.18 | 94.69 | 9.54 |
| EILDVP-Tyr-NH2,EILDVP-Cys(mPEG2000-MAL)-Tyr-NH2 and EILDVP-Cys(mPEG20000-MAL)-Tyr-NH2 peptide labeled by 125I are separately A,B,C. | ||||||
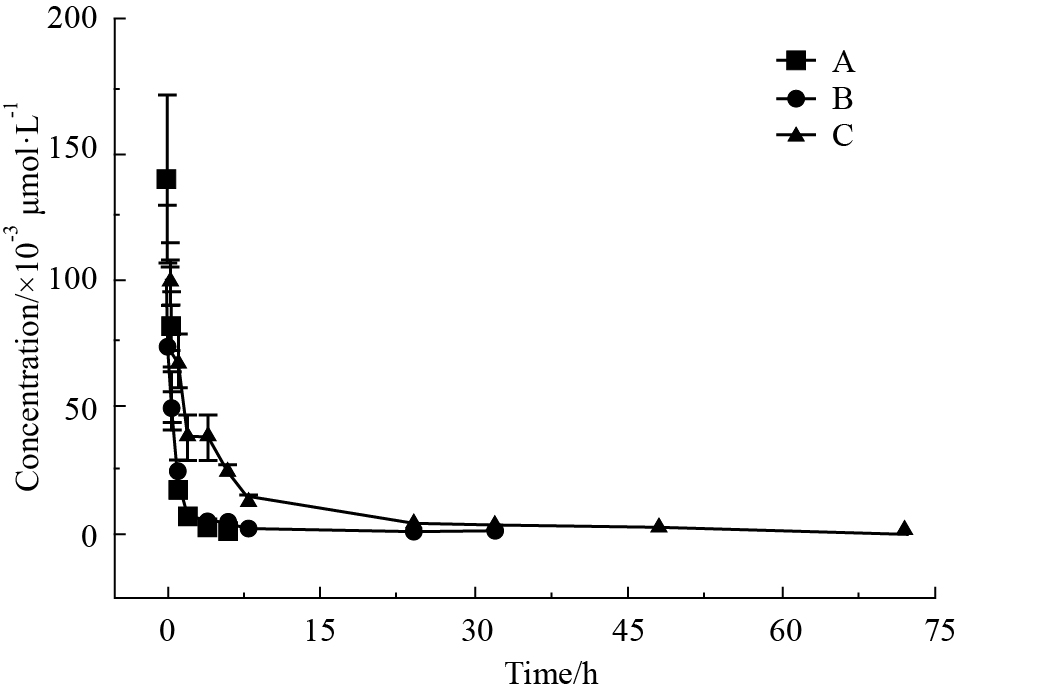
小鼠尾静脉注射3.441 GBq·L-1浓度(5 mL·kg-1容积)3种125I标记肽后,不同时间点血浆经TCA沉淀后测定放射性,测定并换算数据分别代入相应标准曲线方程,取得血药浓度-时间数据(Fig1),经3P97药动学统计软件分析房室数为1,计算主要药代动力学参数(Tab2);其中mPEG20000修饰肽的血浆半衰期(T1/2)明显高于原型肽(化合物A)、清除率(Cl)明显低于原型肽;125I标记EILDVP-Cys (mPEG20000-MAL)-Tyr-NH2(化合物C)组小鼠血浆,在0.08 h时因125I剂量致放射性测量值溢出仪器的读出范围,未影响3P97软件对本组药代动力学参数的计算。
|
| Fig 1 Blood drug concentration-time curve of EILDVP peptide labeled by 125I and modified by polyethylene glycol EILDVP-Tyr-NH2,EILDVP-Cys(mPEG2000-MAL)-Tyr-NH2 and EILDVP-Cys(mPEG20000-MAL)-Tyr-NH2 peptide labeled by 125I are separately A,B,C. |
( ± s,n=5) ± s,n=5) |
||||
| Parameter | Unit | A | B | C |
| Co | μmol·L-1 | 0.16±(5.94×10-3) | 0.11±(2.64×10-3) | 0.10±(6.42×10-3) |
| Ke | 1·h-1 | 2.44±(1.70×10-1) | 1.59±(7.85×10-2) | 0.36±(5.11×10-2) |
| V | mL·kg-1 | 87.05 | 108.33 | 23.99 |
| T1/2 | h | 0.28 | 0.43 | 1.94 |
| AUC | (μmol·L-1)·h | 0.07 | 0.07 | 0.28 |
| Cl | mL·(kg·h)-1 | 212.26 | 172.64 | 8.59 |
| EILDVP-Tyr-NH2,EILDVP-Cys(mPEG2000-MAL)-Tyr-NH2 and EILDVP-Cys(mPEG20000-MAL)-Tyr-NH2 peptide labeled by 125I are separately A,B,C. | ||||
相关研究资料和我们既往实验结果提示,EILDVP(Glu-Ile-Leu-Asp-Val-Pro)等含LDV(Leu-Asp-Val)关键序列的VLA-4拮抗肽具有治疗类风湿关节炎、慢性哮喘等免疫性炎症的潜在药用价值,并且聚乙二醇修饰可通过增加体内稳定性、延长半衰期等机制增强肽类分子药理活性[2, 3, 4, 5, 6, 7]。本实验在EILDVP-Cys(mPEG2000-MAL)-Tyr-NH2等肽结构中设计加入Tyr,是为EILDVP肽提供原结构中缺乏的125I标记部位[9];利用某些mPEG衍生物特异修饰Cys的特性,在短肽C端加入Cys以提供mPEG定点巯基修饰部位,预期防止随机修饰可能发生的修饰物对短肽生物活性部位的屏蔽[10]。
3.2 修饰物mPEG的分子质量本实验以预期提高被修饰物体内稳定性、半衰期,并较大程度保留原型化合物活性为目的,依据被修饰蛋白质或肽类分子在体内的作用时间与偶联的PEG数量和相对分子质量成正比、生物活性与PEG相对分子质量成反比的蛋白质和肽类药物化学修饰的基本规律[11],参考既往2 ku分子质量 mPEG延长约0.5 ku分子质量短肽半衰期2倍以上的实验结果[7],选择分子质量分别为2 ku和20 ku的直链甲氧基聚乙二醇(mPEG2000和mPEG20000)为修饰物,主要观察和比较mPEG20000对短肽的修饰效果。
3.3 结果分析本实验药代动力学参数显示,125I标记的mPEG2000和mPEG20000修饰肽较原型EILDVP-Tyr-NH2肽的血浆半衰期(T1/2)分别延长1.54倍和6.93倍,清除率(Cl)分别降低1.23倍和24.71倍;3种受试化合物表观分布容积(V)均较小,数据提示主要分布在血浆,原因是否与其血浆蛋白结合率有关,尚待直接测试验证;受单一给药途径限制,因125I 标记量及仪器测量范围所致3种受试化合物动物单位体质量给药剂量差异,不能分析本文mPEG20000修饰肽曲线下面积(AUC)数值与另2种受试化合物的差异。
本实验单剂量3种受试化合物的小鼠体内药代动力学分析结果提示,适宜分子质量的直链甲氧基聚乙二醇(mPEG)修饰有利于延长EILDVP肽在体内的维持时间,从而保证有效浓度药物分子产生活性,对提高药效具有积极意义;在实验涉及分子质量范围内,分子质量较大(20 ku)的mPEG对EILDVP肽修饰效果较好。以上结果与我们既往mPEG修饰含LDV序列肽抗炎作用增强的药效实验结果吻合[6]。
| [1] | Chen L L, Lobb R R, Cuervo J H, et al. Identification of ligand binding sites on integrin α4β1 through chemical cross-linking[J]. Biochemistry,1998,37(24):8743-53. |
| [2] | Dutta A S, Gormley J J, Coath M, et al. Potent cyclic peptide inhibitors of VLA-4 (α4β1 integrin) mediated cell adhesion. Discovery of compounds like cyclo (MePhe-Leu-Asp-Val-D-Arg-D-Arg) (ZD7349)compatible with depot formulation[J]. J Pept Sci, 2000, 6(8):398-412. |
| [3] | Gloria C, Kashmira S, Gloria J, et al. A small molecule very late antigen-4 antagonist can inhibit ovalbumin-induced lung inflammation[J]. Am J Respir Crit Care Med,2003,167(10):1400-9. |
| [4] | Vanderslice P, Biediger R J, Woodside D G,et al. Small molecule agonist of very late antigen-4 (VLA-4) integrin induces progenitor cell adhesion[J]. J Biol Chem,2013,288(27):19414-28. |
| [5] | Pepinsky R B,Lee W C,Cornebise M,et al. Design,synthesis,and analysis of a polyethelene glycol-modified(PEGlyated)small molecule inhibitor of integrin α4β1 with improved pharmaceutical properties[J]. J Pharmacol Exp Ther, 2005, 312(2):742-50. |
| [6] | 甄晓兰.不同分子量聚乙二醇化的VLA-4拮抗肽对致敏性哮喘小鼠肺组织Eotaxin和CCR3表达的影响[D]. 承德医学院,2010.Zhen X L. Effects of the VLA-4 antagonist peptides modified by different molecular weights PEG in mice lung tissue expression of Eotaxin and CCR3 on allergic asthma models[D]. Chengde Medical College,2010. |
| [7] | 赵铁华,文 曙,邓淑华,等.聚乙二醇化脑啡肽的镇痛药效和体内分布[J].中国药理学通报,2013,29(5):703-7. Zhao T H, Wen S, Deng S H, et al. Analgesic activity and biodistribution of polyethylene glycol conjugation to enkephalin[J].Chin Pharmacol Bull,2013,29(5):703-7. |
| [8] | 鹿晓晶,李丽琴,张瑞华,等.125I-相思子毒素P2在小鼠体内的血药浓度及其生物利用度[J].中国药理学通报,2010,26(12):1665-9. Lu X J, Li L Q, Zhang R H, et al.Plasma concentration and bioavailability of 125I-abrin P2 in mice[J].Chin Pharmacol Bull,2010,26(12):1665-9. |
| [9] | 尹伯元.放射性碘标记[M]//尹伯元. 放射免疫测定基础.天津:天津科技出版社,1985:177-8. Yin B Y.Radio-iodinated labelling[M]//Yin B Y.Basis of radio immunity assay. Tianjin:Tianjin Science & Technology Publishing Corp,1985:177-8. |
| [10] | Yu P Z, Zheng C Y, Chen J, et al. Investigation on PEGylation strategy of recombinant human interleukin-1 receptor antagonist[J]. Bioorg Med Chem,2007, 15(16):5396-405. |
| [11] | Bowen S, Tare N, Inoue T, et al. Relationship between molecular mass and duration of activity of polyethylene goycol conjugated granulocyte colony-stimulating factor mutein[J]. Exp Hematol, 1999,27(3):425-32. |

