


2. 辽宁医学院附属第一医院肿瘤科, 辽宁 锦州 121001
2. Dept of Oncology, First Affiliated Hospital, Liaoning Medical College, Jinzhou Liaoning 121001, China
恶性肿瘤已经成为严重威胁人类健康的疾病之一。恶性肿瘤细胞可以通过多种方式破坏机体的组织学屏障,随血液、淋巴液转移和扩散,进而侵犯正常组织和器官[1]。舌鳞状细胞癌(tongue squamous cell carcinoma,TSCC)与其他口腔恶性肿瘤相比,其恶性程度高,生长快,浸润性强。由于舌部血供丰富,运动频繁,导致TSCC常发生早期的颈淋巴结转移,且转移率较高。近年来一些研究显示,补骨脂乙素(isobavachalcone,IBC)具有促进肿瘤细胞凋亡、抑制肿瘤细胞转移等生物学活性。尤其是作为一种毒副作用小,来源经济的新型抗癌药物,IBC的临床应用价值日益引起人们的重视。但是,IBC对舌癌细胞的侵袭和转移是否有影响,尚未见报道。本研究将不同浓度的IBC作用于人舌鳞状细胞癌Tca8113细胞,观察其对细胞迁移以及侵袭的影响,同时还观察IBC对侵袭相关蛋白MMP-2、MMP-9及其上游Akt蛋白磷酸化表达的影响。
1 材料与方法 1.1 药品、主要试剂IBC(纯度>0.98)购自上海同田生物技术有限公司。MTT、Annexin V-FITC/PI双染凋亡试剂盒购于南京凯基生物科技发展有限公司。Transwell小室、基质胶购于美国Sigma公司。所有抗体均购自美国Santa Cruz公司。
1.2 主要仪器二氧化碳培养箱(日本,MCO-20AIC,三洋电机);细胞涂片离心机(日本,Cyto-Tek Centrifuge,樱花精机株式会社);4℃高速离心机(日本,CF16RXⅡ,hitachi koki co.,ltd);全波段酶标仪(瑞士,M200,TECAN公司);倒置显微镜(日本,IX51,OLYMPUS公司);流式细胞仪(美国,FACCSVERSE,Becton Dickinson公司);凝胶成像系统(美国,IMAGE QUANT LAS 4000,GE HEALTHCARE公司);半干转机(美国,170-3940,BIO-RAD公司)。
1.3 细胞及细胞培养人舌鳞状细胞癌Tca8113细胞株购自上海中科院细胞库。Tca8113细胞用RPMI 1640培养基(含0.1的胎牛血清、1×105 IU·L-1青霉素和100 mg·L-1链霉素)培养于37℃、0.05 CO2的培养箱中。
1.4 MTT分析将Tca8113细胞接种于96孔板中,每孔100 μL,大约5 000个细胞/孔。每组设5个复孔。待细胞贴壁后加入不同浓度的IBC,37℃、0.05 CO2条件下继续培养12、24和48 h,终止培养前4 h每孔加入MTT溶液20 μL,到预定时间后小心吸去上清,避免蓝色结晶脱落。随后每孔加入150 μL DMSO,低速振荡摇匀10 min。用酶标仪于490 nm波长条件下测定吸光度值。细胞增殖抑制率/%=1-(实验组OD值-空白组OD值)/(对照组OD值-空白组OD值)×100 %。计算IC50(药物抑制50%细胞增殖时的药物浓度)及绘制出细胞增殖抑制曲线。本次实验重复3次,取平均值。
1.5 划痕实验细胞接种于6孔板,每孔5×105个细胞,设定3个复孔。待细胞贴壁后进行划痕,加入不同浓度无血清的IBC培养液继续培养24 h。在0 h及24 h取样并拍照。迁移率/%=(原始划痕平均距离-24 h划痕平均距离)/ 原始划痕平均距离×100%。
1.6 Transwell实验Matrigel胶通过无血清培养基进行1 ∶6稀释。将稀释后的Matrigel胶30 μL加入transwell上室,轻轻摇匀使其均匀铺满上室底部,放入培养箱30 min使其凝固,做成人工基底膜。将不含血清的培养基和5×104/细胞(总体积为100 μL)加入上室,并加入不同浓度不含血清的IBC混匀。下室加入600 μL含0.10胎牛血清的培养基,37℃培养箱内培养。24 h后取出小室,吸干上室内液体,PBS冲洗后放入4%甲醛中固定15 min,加入0.1%结晶紫染液中染色15 min。用棉签擦拭掉上室Matrigel凝胶及残余细胞。高倍镜下( ×400) 随机取6个视野计数,取平均值作为穿过人工基底膜的细胞数。
1.7 Western blot分析将0、10、20和40 μmol·L-1的IBC 作用Tca8113细胞24 h后,胰酶消化收集细胞。本实验的裂解液采用含有蛋白酶抑制剂(100 mg·L-1 PMSF,2 mg·L-1 Aprotitin)的强RIPA裂解液(0.1% SDS,1% Triton-100,150 mmol·L-1 NaCl,1 mmol·L-1 EDTA(pH 8.0),10 mmol·L-1 Tris-HCl (pH 7.5))。将收集到的细胞中加入适量裂解液冰上裂解30 min后,超声震碎10 s,13 000 r·min-1 4℃离心20 min。根据实验需要选用12%的SDS-聚丙烯凝胶,将20 μL蛋白样品加入上样孔中,电泳约2 h,然后转印至PVDF膜上。用5 %脱脂奶粉封闭1 h后,分别加入Akt、p-Akt、MMP-2、MMP-9及β-actin抗体,4℃孵育过夜。TBST摇晃清洗3次后加入辣根过氧化物酶标记的二抗作用1 h,凝胶图像分析系统拍照。
1.8 统计学分析本研究的所有实验数据均为3次独立实验的结果,统计学结果通过SPSS 16.0进行分析,进行t检验。数据变量以 ± s表示。
± s表示。
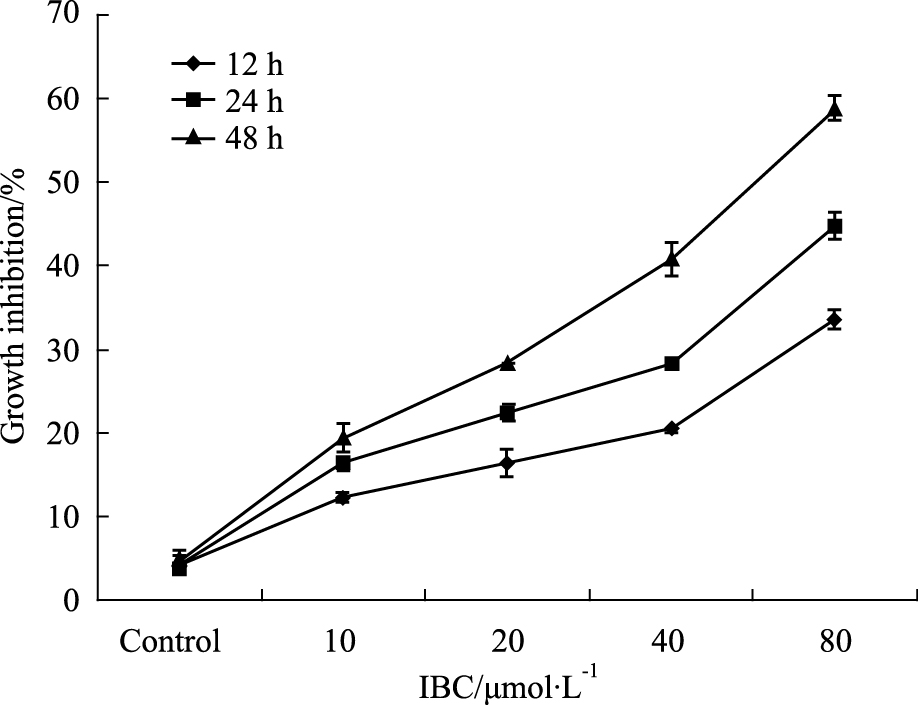
用0、10、20、40、80 μmol·L-1 IBC分别处理舌癌Tca8113细胞12、24、48 h,通过MTT法检测各组吸光度值。实验结果显示,不同浓度IBC对Tca8113细胞均有增殖抑制作用(Fig1)。IBC作用12、24和48 h的IC50分别为(280.22±7.45)、(128.31±6.83)和(56.37±6.75) μmol·L-1。12、24和48 h的IC50值相比,3组差异均具有统计学意义(P < 0.05)。以上结果表明,IBC可呈时间-剂量依赖性抑制Tca8113细胞的增殖。
|
Fig 1
Effects of IBC on Tca8113 cell proliferation ( ± s, n=3) ± s, n=3)
|
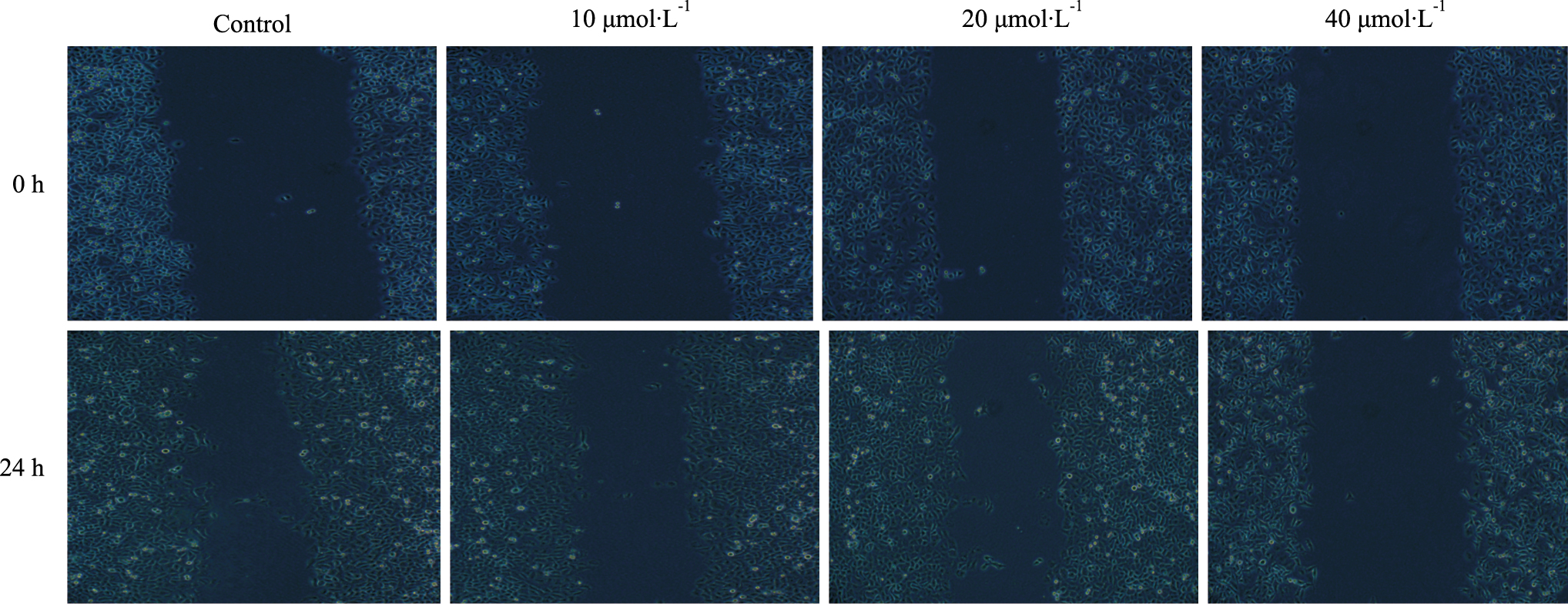
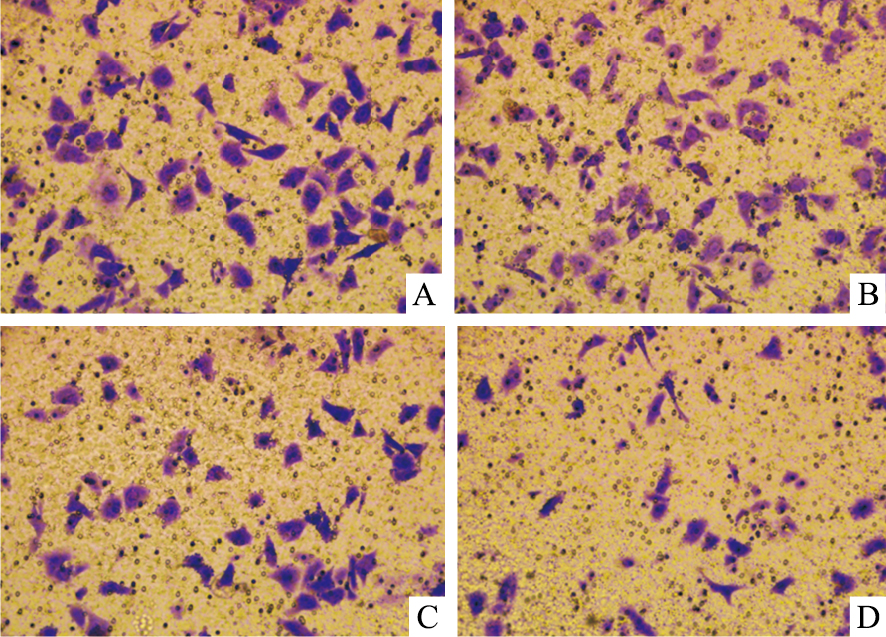
为了明确IBC是否影响创伤修复,将采用了划痕实验和Transwell实验进行观察。本次实验选用时间点为24 h,IBC处理浓度为10、20和40 μmol·L-1,是为了排除细胞凋亡对细胞迁移和侵袭的影响。20和40 μmol·L-1 IBC作用于舌癌Tca8113细胞24 h后,划痕愈合速度及侵袭性明显低于对照组(P < 0.05)(Fig2、3)。这表明不同浓度的IBC可抑制Tca8113细胞的迁移和侵袭能力。
|
| Fig 2 IBC decreased invasion of Tca8113 cells(×200) Tca8113 cells were detected by an optical microscope |
|
| Fig 3 IBC decreased migration of Tca8113 cells(×400) Tca8113 cells were detected by a optical microscope.A: Control group; B~D: 10, 20, 40 μmol·L-1 IBC treated group |
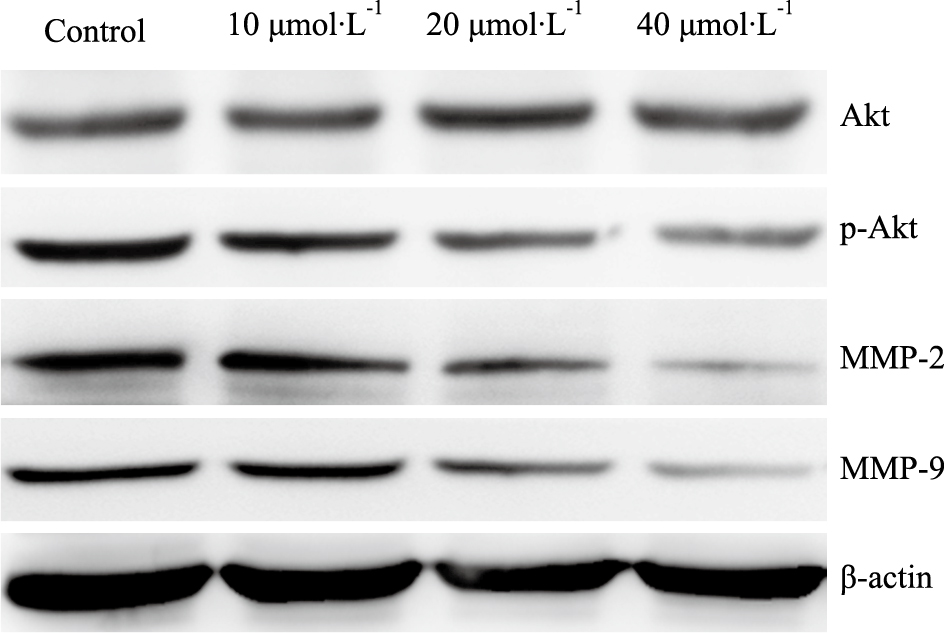
为探讨IBC抑制Tca8113细胞迁移和侵袭的作用机制,本次通过Western blot观察0、10、20、40 μmol·L-1 IBC处理舌癌细胞24 h后MMP-2、MMP-9蛋白的变化。实验结果发现,20和40 μmol·L-1 IBC可明显下调MMP-2和MMP-9蛋白表达,与对照组相比差异具有统计学意义(P < 0.05)。进一步观察发现,IBC具有明显抑制Akt磷酸化的作用(Fig4)。
|
| Fig 4 Effects of IBC on protein expression of Akt,p-Akt, MMP-2 and MMP-9 in Tca8113 cells At 24 h after incubation with IBC, the expression levels of all proteins were analyzed by Western blot. |
侵袭和转移是癌症最致命的特征,其占癌症相关死亡率的90%以上[1]。由于舌部解剖学特征以及肿瘤筛查检测灵敏性和特异性相对较低等原因,导致一部分TSCC患者确诊时已出现颈部淋巴结转移或远处转移,这使得治疗难以达到预期治疗效果。目前TSCC最有效的治疗方法为手术切除。然而,过度的手术切除常严重影响TSCC患者的口腔功能及术后生活质量。放疗、化疗、免疫治疗作为辅助性治疗手段,使TSCC患者的生存率得到很大的改善,但仍没有达到满意的效果[2]。
补骨脂作为中药材,在我国广泛分布。现代药理学研究表明,补骨脂具有扩张冠状动脉、增强免疫力、抗菌及抗肿瘤等生理活性[3, 4]。IBC最早是由Bhalla等[5]于1968年从补骨脂的果实中提取出来的一种活性成分。IBC属查尔酮类,具有抗炎、抗菌、抗氧化等生物学活性。Nishimura等[6]研究表明,IBC通过线粒体途径诱导人神经母细胞瘤凋亡,而对正常小脑颗粒细胞无细胞毒性。Jing等[7]也发现,IBC促进肿瘤细胞OVCAR-8、PC3、A549、MCF-7的凋亡,同时又对正常细胞L-02、HUVEC无毒性作用。以上研究结果提示,IBC在对肿瘤细胞具有杀伤作用的同时对血管内皮细胞及正常肝细胞无明显杀伤作用,也就意味着其对血管和肝脏无明显毒副作用,这说明IBC有可能作为低毒高效的抗肿瘤药物应用于临床。近期研究发现,IBC可抑制胃癌细胞的迁移以及侵袭。这表明IBC除了具有促进肿瘤细胞凋亡的作用,还具有抑制肿瘤细胞侵袭和转移的能力。
本研究通过划痕实验观察IBC对Tca8113细胞迁移能力的影响。实验结果发现,随着药物浓度的增加,Tca8113细胞的迁移能力逐渐减弱。然而,肿瘤的侵袭和转移是一个复杂的过程。肿瘤细胞通过降解细胞外基质(extracellular matrix,ECM)进入血液或淋巴循环系统,并最终到达靶器官形成新的转移灶。在本研究中,通过Transwell实验观察IBC对舌癌细胞侵袭能力的影响。Transwell小室上铺盖了Matrigel胶,进而模拟ECM。实验结果发现,对照组的Tca8113细胞可以突破Matrigel胶进入下室。随着IBC药物浓度的增高,Tca8113细胞逐渐失去穿透Matrigel胶的能力。以上结果表明,IBC呈剂量依赖性抑制舌癌细胞迁移和侵袭的能力。
为了侵袭并扩散到周围的正常组织中,肿瘤细胞分泌以基质金属蛋白酶(MMPs)为主的多种酶类,后者是一群锌依赖性的内肽酶,可以降解几乎所有细胞外基质的成分[8]。Aparna等[9]的研究发现,MMP-2和MMP-9的高水平表达是舌癌患者肿瘤局部复发的危险因素。此外,MMP-9还与舌癌远处转移及生存期密切相关。因此,MMPs是肿瘤细胞侵袭和转移的关键蛋白,尤其是MMP-2、MMP-9蛋白的高水平表达在一定程度上代表了舌癌细胞的高侵袭性[10]。本研究通过Western blot法证实,IBC明显降低Tca8113细胞胞质中MMP-2、MMP-9蛋白的表达。这表明IBC通过下调MMP-2和MMP-9的蛋白表达从而抑制了舌癌细胞的侵袭性。一些研究表明,异常活化的Akt信号通路可激活一系列胞质蛋白(如MMP-2、MMP-9),促进肿瘤细胞的侵袭和转移[11, 12]。本实验发现IBC作用于Tca8113细胞可引起p-Akt蛋白表达的明显降低。因此,抑制异常激活的Akt蛋白表达可能是IBC抑制舌癌Tca8113细胞侵袭性的机制之一。
本次研究证实了IBC通过下调MMP-2和MMP-9的蛋白表达及其上游磷酸化Akt的蛋白表达从而抑制TSCC细胞迁移以及侵袭能力。然而,IBC通过何种通路抑制舌癌细胞的迁移和侵袭,还有待进一步研究。总之,IBC具有较明确的抑制舌鳞癌细胞迁移以及侵袭的作用,为IBC的进一步药物研发及临床应用提供了理论基础。
(本实验完成于辽宁医学院附属第一医院肿瘤中心实验室,在此对实验室的各位老师以及同学的帮助表示由衷的感谢!)
| [1] | Jin X, Zhu Z, Shi Y. Metastasis mechanism and gene/protein expression in gastric cancer with distant organs metastasis[J].Bull Cancer, 2014, 101(1):E1-12. |
| [2] | 黄晓斌, 杨宏宇, 徐志英, 杨辉俊. 68例舌癌的治疗与预后分析[J].海南医学, 2011, 22(10):116-7. Huang X B, Yang H Y, Xu Z Y, Yang H J. Clinical analysis of treatment and prognosis of 68 patients with tongue cancer[J].Hainan Med J, 2011, 22(10):116-7. |
| [3] | Akihisa T, Tokuda H, Hasegawa D, et al. Chalcones and other compounds from the exudates of Angelica keiskei and their cancer chemopreventive effects[J].J Nat Prod, 2006, 69(1):38-42. |
| [4] | 沈丽霞, 董晓华, 李 炜, 等. 槲皮素、补骨脂素对乳腺癌细胞株MCF-7增殖的影响[J].中国药理学通报, 2009, 25(5):601-5. Shen L X, Dong X H, Li W, et al. Effect of quercetin and psoralen on proliferation in MCF-7 cells[J].Chin Pharmacol Bull, 2009, 25(5):601-5. |
| [5] | Bhalla V X, Nayak U R, Dev S. Some new fiavonoids from Psoralea Corylifolia[J].Tetrahedron Lett, 1968, 20(1):2401-6. |
| [6] | Nishimura R, Tabata K, Arakawa M, et al. Isobavachalcone, a chalcone constituent of Angelica keiskei, induces apoptosis in neuroblastoma[J].Biol Pharm Bull, 2007, 30(10):1878-83. |
| [7] | Jing H, Zhou X, Dong X, et al. Abrogation of Akt signaling by Isobavachalcone contributes to its anti-proliferative effects towards human cancer cells[J].Cancer Lett, 2010, 294(2):167-77. |
| [8] | AO J S. Molecularmechanisms of glioma invasiveness:the role of proteases[J].Nat Rev Cancer, 2003, 3(7):489-501. |
| [9] | Aparna M, Rao L, Kunhikatta V, et al. The role of MMP-2 and MMP-9 as prognostic markers in the early stages of tongue squamous cell carcinoma[J].J Oral Pathol Med, 2015, 44(5):345-52. |
| [10] | 韩成敏, 陈 鑫, 吴东辉. 基质金属蛋白酶MMP-2、MMP-9表达同舌癌侵袭和转移相关性研究[J].吉林医学, 2006, 27(5):476-7. Han C M, Chen X, Wu D H. The relationship between the expression of matrix metalloproteinase-2, 9 and invasion or metastasis of tongue carcinoma[J].Jilin Med J, 2006, 27(5):476-7. |
| [11] | Cheng C Y, Hsieh H L, Hsiao L D, et al. PI3-K/Akt/JNK/NF-kappaB is essential for MMP-9 expression and outgrowth in human limbal epithelial cells on intact amniotic membrane[J].Stem Cell Res, 2012, 9(1):9-23. |
| [12] | 陈美娟, 赵若琳, 郭园园, 等. 麦冬皂苷B对A549细胞株体外黏附、侵袭和迁移的抑制作用及机制研究[J].中国药理学通报, 2015, 31(5):660-4. Chen M J, Zhao R L, Guo Y Y, et al. Inhibitory effect of ophiopogonin-B on adhesion, invasion and migration of A549 cells in vitro[J]. Chin Pharmacol Bull, 2015, 31(5):660-4. |

