


2. 蚌埠医学院第一附属医院肿瘤内科, 安徽 蚌埠 233003
刘浩(1979-),男,博士,教授,硕士生导师,研究方向:生化药理学,通讯作者,Tel:0552-3175323,E-mail:liuhao6886@foxmail.com
2. Dept of Medical Oncology, the first Affiliated Hospital of Bengbu Medical College, Bengbu Anhui 233003, China
三阴乳腺癌(triple negative breast cancer,TNBC)指是雌激素受体(estrogen receptor,ER)、孕激素受体(progesterone receptor,PR)和人类表皮生长因子受体-2(human epidermal growth factor receptor-2,Her-2)均为阴性表达的乳腺癌[1]。TNBC恶性程度高、侵袭性强,易复发转移,预后差,由于缺乏内分泌治疗和针对Her-2的靶向治疗,临床治疗以蒽环类和紫杉类传统化疗药为主[2]。阿霉素(adriamycin,ADM)作为蒽环类抗癌药物,是经典的乳腺癌化疗药物,对TNBC也表现出较高的敏感性[2, 3]。但是剂量依赖的毒性作用及耐药性的产生,限制了其应用。靶向治疗因具有靶向性好、副作用小、患者耐受性好等优点成为目前关注的热点。靶向治疗药物西妥昔即西妥昔单抗(cetuximab,C225)为特异性表皮生长因子受体(epidermal growth factor receptor,EGFR)单克隆抗体,能够与EGFR 的内源性配体EGF、TGF-α竞争性地结合EGFR 胞外配体区,抑制EGFR自身磷酸化,阻断下游信号转导通路,抑制肿瘤的生长、转移。临床研究表明,大部分TNBC患者EGFR表达较高,可能会受益于西妥昔的治疗。因此,课题组将西妥昔与ADM联合应用于MDA-MB-231 TNBC细胞株,通过测定细胞的活性、凋亡率、线粒体膜电位及相关蛋白表达,探讨西妥昔联合阿霉素抗TNBC的作用及机制,为西妥昔与ADM联合治疗TNBC提供实验室与理论依据。
1 材料与方法 1.1 试剂三阴乳腺癌细胞株MDA-MB-231细胞: 蚌埠医学院生化药理研究室提供。DMEM培养基为Gibco 公司生产,新生牛血清、胰蛋白酶均为Gibco 公司生产。阿霉素由浙江海正药业股份有限公司生产。西妥昔德国默克里昂制药公司生产。噻唑蓝(methyl thiazolyl tetrazolium,MTT)、JC-1染色试剂盒、碘化吡啶(pyridine iodide ,PI)购自Sigma公司;GRP78、Bcl-2、Caspase-3抗体及β-actin 抗体均购自Santa Cruz 公司;山羊抗兔及抗鼠IgG 购自中杉金桥生物技术有限公司;Immobilon Western Chemiluminescent HRP Substrate(Millipore公司)。
1.2 仪器与设备AccuriC6流式细胞仪(美国BD公司);垂直电泳仪、DYC-Z4013 电转移槽及凝胶成像系统(美国BIO-RAD公司);BioTek酶联免疫检测仪(SynergyHT公司);U-HGLGPS 荧光显微镜(日本奥林巴斯);Revco超低温冰箱(美国REVCO公司);4239R高速低温离心机(意大利ALC公司)。
1.3 方法 1.3.1 药物溶液的配制阿霉素先用0.9%生理盐水溶解为浓度10 g·L-1的溶液,再用DMEM培养基稀释成浓度为100、50、25、12.5 μmol·L-1的药液。西妥昔原液(5 g·L-1)用DMEM 稀释成浓度为2 250、1 500、750、250、83 mg·L-1的药液。磷酸盐缓冲液(phosphate buffer solution,PBS): NaCl 137 mmol·L-1,KCl 2.7 mmol·L-1,Na2HPO4 10 mmol·L-1,KH2PO4 2 mmol·L-1,pH 7.2~7.4。MTT粉末以PBS 配成浓度为5 g·L-1的药液。PI缓冲液:2 mg PI、0.1 g NaC6H5、100 mL Triton-100、100 mL ddH2O,浓度为10 mg·L-1。
1.3.2 细胞培养MDA-MB-231细胞接种于含10%新生小牛血清、青霉素(1×105 U·L-1)、链霉素(100 mg·L-1)和NaHCO3(3.7 g·L-1)的DMEM培养液中,体积分数0.05 CO2、饱和湿度、37 ℃培养箱中培养 。
1.3.3 MTT法检测细胞存活率收集指数生长期的MDA-MB-231细胞,用DMEM稀释成2.5×107个每升的单细胞悬液,接种于96孔板,每孔200 μL。共分为ADM 1.25、2.5、5、10 μmol·L-1 4个浓度组;西妥昔8.3、25、75、225 mg·L-1 4 个浓度组;对照组;调零组(只加培养液,无细胞),每组3个复孔。培养24 h,吸弃培养液,加入含血清的DMEM 180 μL,各组分别加入相应的药物溶液20 μL,其中合用组分别加入1 500 mg·L-1西妥昔和50 μmol·L-1 ADM 各10 μL。加药后使单用ADM各组药物终浓度分别为1.25、2.5、5、10 μmol·L-1;单用西妥昔各组药物终浓度8.3、25、75、22 mg·L-1;合用组西妥昔终浓度为75 mg·L-1、ADM终浓度为 2.5 μmol·L-1。对照组、调零组加入等体积的培养液。加药后各组MDA-MB-231细胞分别培养12、24、48 h,加入15 μL MTT,培养箱中继续培养4 h,吸弃培养液,每孔加入150 μL DMSO,37℃孵育30 min,酶标仪570 nm测定吸光度(A)值,计算细胞存活率/%。实验重复3次。细胞存活率/%=(实验组A值-调零组A值)/(对照组A值-调零组A值)×100%。
1.3.4 PI染色检测细胞凋亡收集指数生长期的细胞,用DMEM稀释成单细胞悬液,接种于6孔细胞培养板,每孔细胞数3×105个。培养24 h,弃培养液,加入新鲜培养液1.8 mL及对应浓度药物的溶液0.2 mL,使终浓度为ADM组为2.5 μmol·L-1、西妥昔组为75 mg·L-1,合用组为西妥昔75 mg·L-1、ADM 2.5 μmol·L-1,对照组加入2 mL新鲜DMEM培养液。培养24 h,收集细胞,2 500 r·min-1,离心5 min,75%预冷乙醇固定,4℃过夜。PBS洗涤2遍,PI染色,室温避光孵育30 min,流式细胞仪检测。实验重复3次。
1.3.5 JC-1染色测定线粒体膜电位的变化将贴壁生长的细胞用胰酶消化制成细胞悬液,以3×105个/孔的密度接种于6孔培养板,贴壁培养过夜,弃培养液,加入新鲜的含药培养液,培养24 h,吸弃药液,按JC-1说明书加入JC-1染色液,37℃避光孵育30 min,JC-1染色缓冲液洗2次,加入2 mL新鲜的培养液,荧光显微镜下观察拍照。据JC-1染色试剂盒说明书,JC-1可由完整的线粒体膜进入线粒体内部形成多聚体,发出红色荧光,当线粒体膜电位降低时JC-1难进入线粒体内,而以JC-1单体的形式停留在细胞质内发出绿色荧光,因此,当线粒体膜电位降低时红色荧光减弱,绿色荧光增强。
1.3.6 Western blot检测蛋白将细胞制成细胞悬液后,以每孔4×106个的密度接种于6孔培养板,贴壁过夜,吸弃培养液,加入药物处理24 h,收集细胞,提取细胞总蛋白,BCA试剂盒进行蛋白定量。10% SDS-PAGE 电泳,PVDF膜,50 V 转2 h;用含50 g·L-1脱脂奶粉的TPBS室温封闭2 h,一抗4 ℃ 孵育过夜;二抗室温孵育2 h。Immobilon Western Chemiluminescent HRP Substrate显色,实验重复3次。
1.4 统计学方法 应用SPSS 17.0统计软件对数据进行分析,近似正态分布的计量资料以 ± s表示,组间比较采用方差分析及Dunnette-t检验。
± s表示,组间比较采用方差分析及Dunnette-t检验。
MTT结果显示:西妥昔对MDA-MB-231细胞的抑制作用具有浓度依赖性,随药物浓度的增加,MDA-MB-231细胞的存活率呈下降趋势,而在同一浓度不同时间点间,西妥昔对MDA-MB-231细胞的抑制作用没有明显增强。而ADM对MDA-MB-231细胞的抑制作用则具有浓度依赖性与时间依赖性,随着药物浓度的增加和作用时间的延长,MDA-MB-231细胞的存活率均呈明显的下降趋势;与单用ADM组比较,西妥昔与ADM合用可明显降低细胞的存活率。相同作用时间,合用组细胞的存活率明显低于西妥昔组(P < 0.01)与ADM组(P < 0.05或20151220),见Fig1A、1B、1C。

|
Fig 1
Cetuximab and/or adriamycin inhibited proliferation of MDA-MB-231 cells( ± s,n=3)
*P < 0.05 vs ADM group;**P < 0.01 vs ADM group; △△P < 0.01 vs cetuximab group ± s,n=3)
*P < 0.05 vs ADM group;**P < 0.01 vs ADM group; △△P < 0.01 vs cetuximab group
|
PI结果显示,西妥昔与ADM均可诱导MDA-MB-231细胞凋亡,细胞凋亡率分别为(11.03±1.32)%,(17.13±1.37)%,二者合用可明显增加MDA-MB-231细胞的凋亡率(43.93±3.59) %,与西妥昔组、ADM组相比,差异均有统计学意义(P < 0.01),见Fig2。

|
|
Fig 2
Apoptosis induced by cetuximab and/or
adriamycin in MDA-MB-231cells
A: Control; B: Cetuximab (75 mg·L-1); C: Adriamycin (2.5 μmol·L-1); D: Cetuximab (75 mg·L-1 ) combined adriamycin (2.5 μmol·L-1). **P < 0.01 vs A; ## |
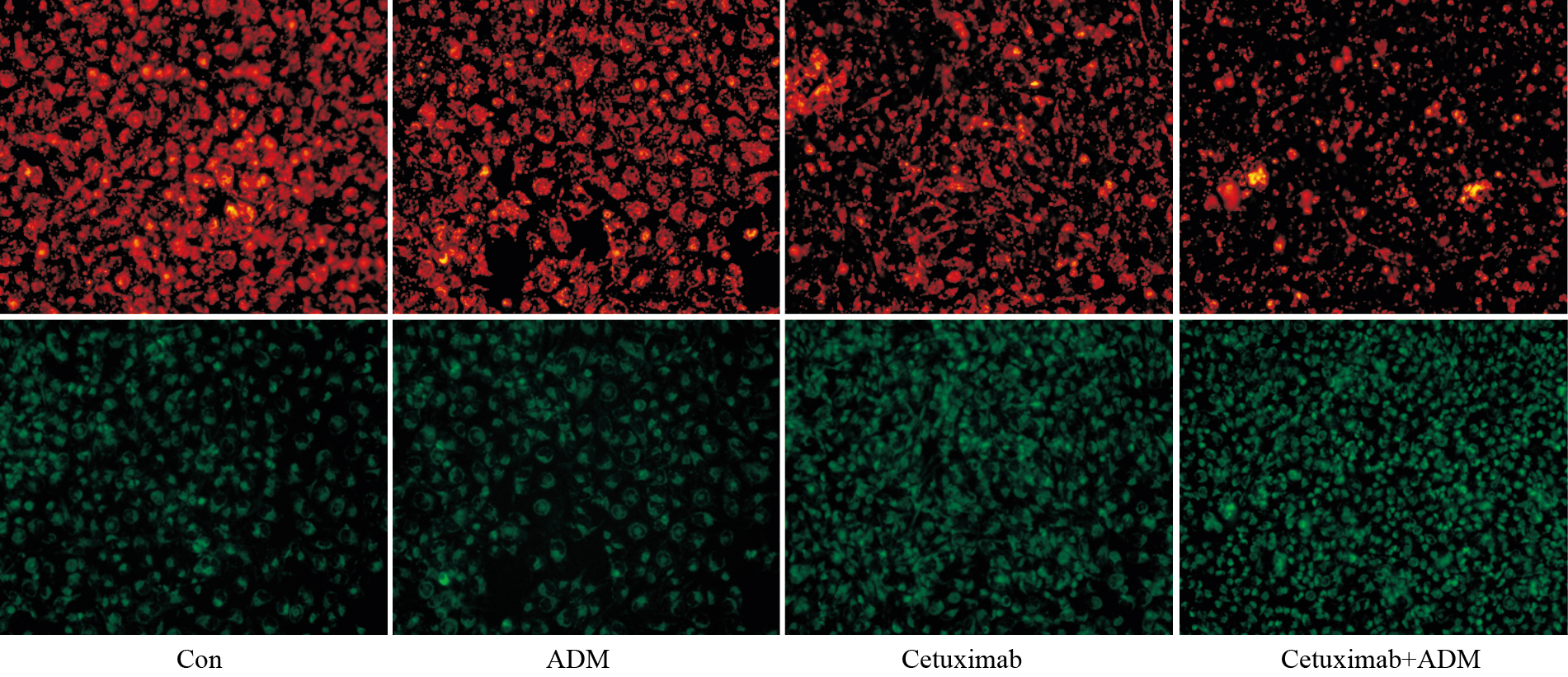
JC-1染色结果显示,西妥昔组、ADM组与对照组相比红色荧光减弱,绿色荧光增强,联合用药组的改变更明显,见Fig3。JC-1染色结果表明西妥昔和ADM单用均可降低线粒体膜电位,而合用组的作用更强。
|
| Fig 3 Cetuximab and/or adriamycin reduced MMP in MDA-MB-231 cell |
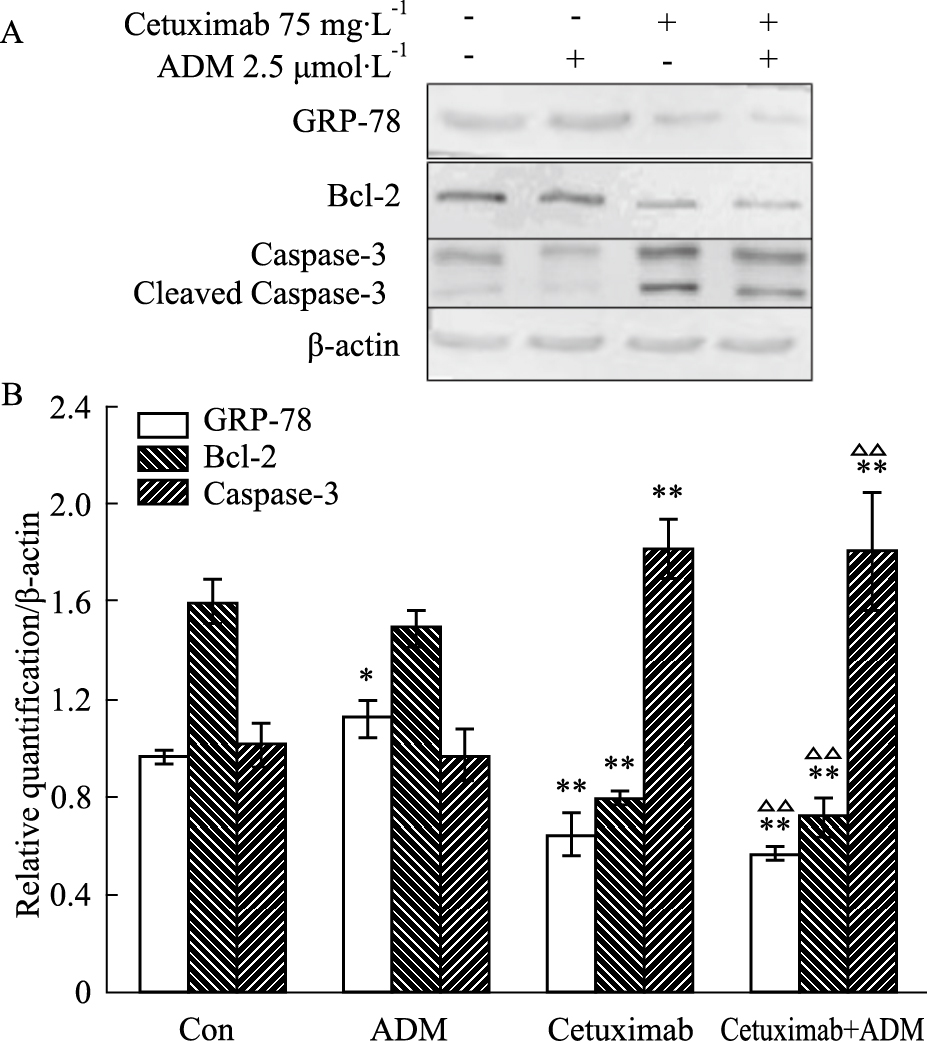
西妥昔能减少GRP-78、Bcl-2表达,激活Caspase-3。ADM对Bcl-2及Caspase-3的表达无明显影响,可增加GRP-78的表达。二者合用可明显降低GRP-78、 Bcl-2的表达,增加Caspase-3激活,见Fig4。
|
| Fig 4 Effect of cetuximab and/or adriamycin on GRP-78/ Bcl-2/Casepase-3 in MDA-MB-231cells A: The experession of GRP-78, Bcl-2 and Caspase-3 in MDA-MB-231 cells which treated with cetuximab (75 mg·L-1 ) combined adriamycin (2.5 μmol·L-1) for 24 hours; B: The result of the experession of GRP-78, Bcl-2 and Caspase-3 analysed by BandScan 5 software. The data were presented as the mean ± SD of three independent experiments.*P < 0.05, **P < 0.01 vs control group;△△P < 0.01 vs ADM group. |
传统化疗药物的毒性大大限制了临床应用。西妥昔是由德国默克公司开发的一种EGFR单克隆抗体,主要用于EGFR表达阳性的直肠癌的治疗。因西妥昔是特异性EGFR的阻断剂,具有肿瘤靶向性强、毒副作用小等优点,受到广泛的研究和关注。近年将西妥昔与传统化疗药联合治疗其他恶性肿瘤的研究取得不错的进展。有些方案已进入Ⅱ期临床研究阶段。阿霉素作为治疗乳腺癌的一线药物,未见与西妥昔联合治疗TNBC的报道。本试验将阿霉素与西妥昔联合用于TNBC细胞株MDA-MB-231,结果显示西妥昔与阿霉素合用可明显抑制三阴乳腺癌细胞株MDA-MB-231的增殖。
内质网应激与细胞凋亡及肿瘤的发生、发展密切相关。细胞应激时GRP-78的高表达是细胞的一种防御机制,通过这种机制延长细胞在各种不利因素刺激下的生存期。肿瘤形成及实体瘤微环境的改变,可作为诱导因素致内质网应激,诱导GRP-78 表达。高度表达GRP-78的肿瘤细胞可降低毒性T细胞对其的杀伤力;同时对抗针对G1期和S期产生毒性的化疗药物[4],减少肿瘤细胞凋亡,通过影响凋亡效应的作用来阻断化学药物对细胞的杀伤性,促进肿瘤细胞的增殖和抗药性的产生[5, 6, 7],报道显示,TNBC恶性程度高、易复发、转移,与内质网应激有着密切的关系[8]。试验中阿霉素作用于三阴乳腺癌细胞株24 h后,细胞内GRP-78表达增加,与文献[9]报道一致,其机制为肿瘤细胞产生了内质网应激,诱导GRP-78表达,保护细胞免于受到该化疗药物的伤害,这也是肿瘤产生耐药性的机制之一[10]。西妥昔对内质网应激的调节作用,尚无文献报道,但内质网应激的产生需要多种信号传导通路的参与[11],而西妥昔可通过竞争结合EGFR,抑制PI3K/AKT/ERK等多种传导通路[12],试验中西妥昔降低GRP-78表达,可能是与其通过抑制信号传导通路,下调了内质网应激水平有关。
线粒体在多种肿瘤细胞的凋亡中扮演着重要的作用。线粒体功能障碍诱导的细胞凋亡主要通过两条途径实现[13]即:(1)线粒体通过释放凋亡蛋白如细胞色素C及凋亡诱导因子到细胞之中,最终启动Caspase凋亡通路;(2)降低线粒体膜电位,改变线粒体膜的通透性。Bcl-2蛋白家族是线粒体膜蛋白家族的一员,其可通过Bcl-2/Bax的比值变化调节线粒体膜的通透性,研究表明 Bcl-2/Bax比值降低时,可增加线粒体膜的通透性,降低线粒体膜电位,启动Caspase凋亡通路,诱导细胞凋亡[14]。Maya、Janmaat等[15, 16]研究发现西妥昔具有抑制EGFR,降低线粒体膜电位激活线粒体通路,诱导肺癌及结肠癌细胞死亡的作用。试验结果显示西妥昔能够抑制TNBC细胞的Bcl-2的表达,降低线粒体膜电位,激活并上调Caspase-3,合用组更明显。结果表明西妥昔及联合用药诱导MDA-MB-231细胞的凋亡是通过阻断EGFR,进而抑制Bcl-2,降低线粒体膜电位,激活线粒体凋亡通路实现。
总之,本研究发现西妥昔与阿霉素联合应用能增强对TNBC细胞增殖的抑制作用,其机制可能是西妥昔阻断EGFR下游的信号传导通路,下调内质网应激水平,去除内质网对细胞的保护作用,进而减少Bcl-2表达,降低线粒体膜电位,激活线粒体凋亡通路,促进细胞凋亡。本研究为西妥昔联合阿霉素作为TNBC的治疗方案提供了一个实验基础。本研究仅为体外培养的TNBC细胞株的疗效,进一步的体内外药效及机制有待于进一步的研究。
(致谢:本文所涉及实验均在安徽省生化药物工程技术研究中心完成,感谢中心各位老师的支持与帮助。)
| [1] | Yuan N, Meng M, Liu C, et al. Clinical characteristics and prognostic analysis of triple-negative breast cancer patients[J]. Mol Clin Oncol, 2014,2(2):245-51. |
| [2] | 李永霞,刘 磊,李 平,等.三阴乳腺癌的内科治疗进展[J].华西医学,2012,27(1):141-4.Li Y X, Liu L, Li P,et al. The development in the treatment of three negative breast cancer[J]. West China Med J, 2012,27(1):141-4. |
| [3] | 高会霞,王 彬,周希山.三阴性乳腺癌的临床特征及治疗现状[J].中国实用医学,2013, 8(29):231-3. Gao H X, Wang B, Zhou X S,et al. Clinical feature and current treatment status of triple negative breast cancer[J]. China Prac Med, 2013, 8(29):231-3. |
| [4] | 吉海杰,周 蕾,陈乃宏.依达拉奉对硝普钠诱导PC12细胞氧化应激的保护作用[J].中国药理学通报,2011,27(9):1201-4. Ji H J, Zhou L,Chen N H. Neuroprotective effects of edaravone against oxidative stress on sodium nitroprusside-induced PC12 cells[J]. Chin Pharmacol Bull, 2011,27(9):1201-4. |
| [5] | 范丽梅,张立会,崔松花,等.特异性下调GRP78基因表达对卵巢癌细胞耐药性的影响[J]. 吉林大学学报(医学版),2011,37(2):255-9.Fan L M, Zhang L H, Cui S H,et al. Effect of GRP78 gene expression down-regulation on cisplatin resistance of human ovarian cancer SKOV3/DDP cell[J]. J Jilin Univ(Med Ed), 2011,37(2):255-259. |
| [6] | Cook K L,Clarke P A, Clarke R. Targeting GRP78 and antiestrogen resistance in breast cancer[J]. Future Med Chem,2013,5(9):1047-57. |
| [7] | Roller C,Maddalo D. The molecular Chaperone GRP78/BiP in the development of chemoresistance:Mechanism and possible treatment[J]. Front Pharmacol,2013,4(10):1-5. |
| [8] | Bernardi R, Gianni L. Hallmarks of triple negative breast cancer emerging at last[J].Cell Res, 2014, 24(8):904-5. |
| [9] | Li Y, Liu H, Huang Y Y, et al. Suppression of endoplasmic reticulum stress-induced invasion and migration of breast cancer cells through the downregulation of heparanase[J]. Int J Mol Med, 2013, 31:1234-42. |
| [10] | Chen J, Wei H, Xie B, et al. Endoplasmic reticulum stress contributes to arsenic trioxide-induced apoptosis in drug-sensitive and -resistant leukemia cells[J]. Leuk Res, 2012,36:1526-35. |
| [11] | Cláudio N, Dalet A, Gatti E,et al.Mapping the crossroads of immune activation and cellular stress response pathways[J].EMBO J, 2013,32:1214-24. |
| [12] | Simpson D R,Mell L K,Cohen E E.Targeting the PI3K/AKT/mTOR pathway in squamous cell carcinoma of the head and neck[J].Oral Oncol,2015,51(4):291-8. |
| [13] | Akl H, Vervloessem T, Kiviluoto S, et al. A dual role for the anti-apoptotic Bcl-2 protein in cancer:mitochondria versus endoplasmic reticulum[J]. Biochim Biophys Acta, 2014, 1843(10):2240-52. |
| [14] | Volkmann N, Marassi F M, Newmeyer D D, et al. The rheostat in the membrane:BCL-2 family proteins and apoptosis[J]. Cell Death Differ, 2014,21, 206-15. |
| [15] | Maya S,Sarmento B,Lakshmanan V K,et al. Actively targeted cetuximab conjugated gamma-poly(glutamic acid)-docetaxel nanomedicines for epidermal growth factor receptor over expressing colon cancer cells[J]. J Biomed Nanotechnol, 2014,10(8):1416-28. |
| [16] | Janmaat M L,Kruyt F A,Rodriguez J A,et al.Response to epidermal growth factor receptor inhibitors in non-small cell lung cancer cells:limited antiproliferative effects and absence of apoptosis associated with persistent activity of extracellular signal-regulated kinase or Akt kinase pathways[J]. Clin Cancer Res,2003,9(6):2316-26. |

