


黄仁彬(1955-),男,博士,教授,博士生导师,研究方向:心血管病药物,E-mail:huangrenbin518@163.com
减轻心肌缺血/再灌注损伤(myocardial ischemia/reperfusion injury,MI/RI)是冠心病防治中亟待解决的问题。MI/RI与钙超载、能量代谢、炎症反应及程序性细胞死亡等过程密切相关[1]。凋亡和自噬是两种常见的程序性细胞死亡方式,参与了MI/RI的形成和发展[2, 3]。研究表明[4],3-磷脂酰肌醇激酶—丝/苏氨酸激酶(PI3K/Akt)通路调控凋亡,影响代谢,调节自噬,在MI/RI中发挥重要作用。玉郎伞(又称龙眼参)是广西壮族的一种习用草药,为蝶形花科植物疏叶崖豆Millettia pulchra Kurz var. laxior(Dunn)Z. Wei的块根,具有补气、补血、提高免疫力、抗衰老和抗应激等功能。17-甲氧基-7-羟基-苯并呋喃查尔酮(17-methoxyl-7- hydroxyl-benzofuran chalcone),简称玉郎伞查尔酮—YLSC,是由本课题组从玉郎伞中提取的黄酮单体[5]。前期研究证实[6, 7, 8],YLSC能够抑制大鼠心肌缺血/再灌注诱导的细胞凋亡,减轻缺氧/复氧及垂体后叶素所致的心肌损伤。上述作用涉及多个PI3K/Akt信号通路靶点,如ATPase、TNF-α、eNOS、Bcl-2家族、Caspase家族等,而YLSC是否通过PI3K/Akt途径发挥抗MI/RI作用尚未见报道。因此,本研究通过构建大鼠MI/RI的动物模型,从心肌细胞凋亡和自噬等方面观察YLSC对MI/RI的影响,同时探讨其对PI3K/Akt信号通路的调控作用,为进一步研发新药提供实验依据。
1 材料 1.1 动物SPF级SD大鼠,♂,体质量(260±20) g,由广西医科大学实验动物中心提供,许可证: SCXK(桂)2014-0003。
1.2 药物与试剂YLSC(本室提供,高效液相显示其纯度为98%,DMSO溶解备用);PI3K抑制剂wortmannin(WM,美国Sigma公司,货号:9951S);肌酸激酶同工酶(CK-MB,货号:E006)、乳酸脱氢酶试剂盒(LDH,货号:A020-2)、一氧化氮(NO,货号:A012)试剂盒购于南京建成生物工程研究所;肿瘤坏死因子试剂盒(TNF-α,货号:E-30633)购于北京诚林生物科技有限公司;单克隆抗体p-Akt(货号:4060P)、t-Akt(货号:4691P)、LC3-Ⅱ(货号:3868P)均购于美国CST公司;总RNA 提取试剂(货号:9180)、cDNA合成试剂盒(货号:RR047A)、Real time染料法实时荧光定量试剂盒(RR820A)及引物均由TaKaRa公司提供。
1.3 主要仪器MS4000U- 1C 型生物信号分析系统(广州市龙飞达科技有限公司);动物呼吸机器(上海奥尔科特生物科技有限公司);722S型可见分光光度计(上海精密科学仪器有限公司);TGL-16G-A型高速冷冻离心机(上海安享科学仪器厂);LX-100型电动匀浆机(江苏海门市其林贝尔仪器制造有限公司);7300型实时荧光定量 PCR 仪(美国Applied Biosystems公司);Power pac 基础电泳仪(美国 Bio-Rad 公司)。
2 方法 2.1 动物分组造模及给药将50只SD大鼠,随机分为假手术组、模型组、YLSC(5 mg·kg-1)组、WM(24 μg·kg-1)组、YLSC+WM组(n=8)。各组均于造模前10 min从舌下静脉给药。假手术组和模型组给予0.5% DMSO的生理盐水。按文献方法[8]建立大鼠心肌缺血/再灌注模型(缺血30 min/再灌注2 h),以左室前壁发绀、ST段抬高为缺血成功标志;复灌后,上述变化消失即为再灌注成功。
2.2 指标检测 2.2.1 血清CK-MB、LDH、NO及TNF-α含量测定造模结束,各组动物经腹主动脉取血5 mL,3 000 r·min-1离心10 min,取上清,按试剂盒说明书检测血清CK-MB、LDH、NO和TNF-α含量。
2.2.2 FQ-PCR检测相关基因的表达用试剂盒提取心肌总RNA,测定260 nm和280 nm处的吸光度比值及其完整性,逆转录合成cDNA后,用7300型荧光定量PCR仪进行实时定量PCR分析相关基因表达量。引物序列见Tab1。
| Gene | Sense primer | Anti-sense primer |
| eNOS | 5′-CTGTGTGACCCTCACCGATACAA-3′ | 5′-AGCACAGCCACGTTAATTTCCA-3′ |
| Caspase-3 | 5′-GAGACAGACAGTGGAACTGACGATG-3′ | 5′-GGCGCAAAGTGACTGGATGA-3′ |
| Beclin1 | 5′-GAAACTGGACACGAGCTTCAAGA-3′ | 5′-ACCATCCTGGCGAGTTTCAATA-3′ |
| GAPDH | 5′-GGCACAGTCAAGGCTGAGAATG-3′ | 5′-ATGGTGGTGAAGACGCCAGTA-3′ |
FQ-PCR反应条件:第1步,95 ℃预变性30 s;第2步,95℃变性5 s、60℃退火31 s,72 ℃延伸45 s,共40个循环。采用7300实时PCR系统SDS软件,根据2-ΔΔCT法计算mRNA的相对表达量。
2.2.3 Western blot 测定 t-Akt、p-Akt和LC3-Ⅱ的蛋白表达取左心室缺血心肌50 mg,加入500 μL裂解液,匀浆,收集上清,进行蛋白定量后煮沸,SDS-PAGE电泳,恒压转膜,5%脱脂牛奶封闭 1 h,蛋白一抗封闭,4 ℃过夜;二抗37 ℃孵育1 h,ECL发光,X线片显影、定影,UVP 凝胶图像处理系统分析其灰度值。
2.3 统计学处理应用SPSS 21.0统计软件进行数据处理,计量资料以 ± s表示,组间比较采用方差分析,组内比较采用t检验。
± s表示,组间比较采用方差分析,组内比较采用t检验。
从Tab2可见,与假手术组对比,模型组大鼠血清中CK-MB、LDH及TNF-α含量明显升高(P < 0.05或P < 0.01),NO含量明显降低(P < 0.05);与模型组相比,YLSC能降低CK-MB、LDH及TNF-α含量(P < 0.05),升高NO水平(P < 0.05);YLSC+WM 组和WM组分别与YLSC组比较,CK-MB、LDH以及TNF-α的含量明显提高(P < 0.05),NO含量明显减少(P < 0.05);模型组、YLSC+WM 组和WM组之间差异无统计学意义。
( ± s,n=8) ± s,n=8) |
|||||
| Group | Dose | CK-MB/U·L-1 | LDH/U·L-1 | NO/μmol·L-1 | TNF-α/ng·L-1 |
| Sham | - | 11.15±4.74 | 2016.73±189.53 | 30.16±6.03 | 189.63±88.87 |
| Model | - | 19.11±3.75# | 4298.22±499.27## | 20.78±6.99# | 561.20±128.85## |
| YLSC | 5 mg·kg-1 | 14.28±4.33* | 3645.18±421.83* | 33.65±9.82* | 393.20±107.98* |
| WM | 24 μg·kg-1 | 19.54±3.65Δ | 4246.91±479.01Δ | 21.36±8.57Δ | 568.87±120.42Δ |
| YLSC+WM | 5 mg·kg-1+24 μg·kg-1 | 19.86±3.78Δ | 4259.46±473.47Δ | 20.33±7.64Δ | 573.91±126.78Δ |
| *P < 0.05 vs model;#P < 0.05,##P < 0.01 vs sham;ΔP < 0.05 vs YLSC | |||||
与假手术组比较,模型组心肌eNOS表达下调(P < 0.05),caspase-3和Beclin1表达均明显上调(P < 0.05);YLSC组eNOS表达水平高于模型组(P < 0.05),而caspase-3和Beclin1表达水平均低于模型组(P < 0.05);与YLSC组比较,WM组和YLSC+WM组大鼠心肌eNOS表达量减少(P < 0.05),caspase-3和Beclin1基因表达量均明显增加(P < 0.05),与模型组比较差异无统计学意义。见Tab3。
( ± s,n=5) ± s,n=5) |
||||
| Group | Dose | eNOS/GAPDH | Caspase-3/GAPDH | Beclin1/GAPDH |
| Sham | - | 1.39±0.06 | 0.40±0.02 | 0.38±0.05 |
| Model | - | 0.85±0.05## | 0.94±0.05# | 0.79±0.07# |
| YLSC | 5 mg·kg-1 | 1.15±0.04* | 0.72±0.08* | 0.61±0.04* |
| WM | 24 μg·kg-1 | 0.82±0.07Δ | 0.95±0.07Δ | 0.76±0.05Δ |
| YLSC+WM | 5 mg·kg-1+24 μg·kg-1 | 0.84±0.06Δ | 0.96±0.03Δ | 0.77±0.0.6 Δ |
| *P < 0.05 vs model;#P < 0.05,##P < 0.01 vs sham;ΔP < 0.05 vs YLSC | ||||
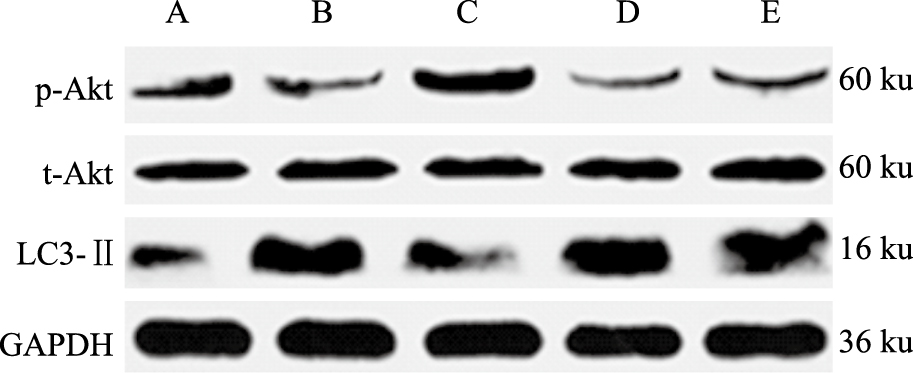
与假手术组比较,模型组大鼠心肌p-Akt蛋白表达量降低(P < 0.05),LC3-Ⅱ蛋白表达明显增高(P < 0.05),而t-Akt表达无明显变化。YLSC预处理后,p-Akt蛋白表达明显升高(P < 0.05),同时LC3-Ⅱ蛋白表达量明显降低(P < 0.05)。与YLSC组比较,WM组和YLSC+WM组大鼠p-Akt表达量减少,LC3-Ⅱ表达增高(P < 0.05),但与模型组比较差异无统计学意义。见Fig1和Tab4。
|
Fig 1
Protein expression of p-Akt andLC3-Ⅱ in five groups( ± s,n=5)
A: Sham; B: Model; C: YLSC; D: WM; E: YLSC+WM ± s,n=5)
A: Sham; B: Model; C: YLSC; D: WM; E: YLSC+WM
|
( ± s,n=5) ± s,n=5) |
|||
| Group | Dose | p-Akt/t-Akt | LC3-Ⅱ/GAPDH |
| Sham | - | 0.64±0.12 | 0.38±0.08 |
| Model | - | 0.42±0.13# | 0.88±0.20# |
| YLSC | 5 mg·kg-1 | 0.86±0.22* | 0.61±0.14* |
| WM | 24 μg·kg-1 | 0.42±0.20Δ | 0.86±0.19Δ |
| YLSC+WM | 5 mg·kg-1+24 μg·kg-1 | 0.47±0.16Δ | 0.85±0.15Δ |
| *P < 0.05 vs model;#P < 0.05 vs sham;ΔP < 0.05 vs YLSC | |||
心肌细胞死亡是缺血/再灌注损伤导致心梗患者预后不佳的主要原因[9],凋亡是最常见的程序性细胞死亡方式。对凋亡的研究,最初多从中性粒细胞聚集、脂质过氧化、线粒体钙超载等被动途径着手。随着研究的深入,人们发现在导致严重后果之前,心肌细胞内的“自我保护机制”已经发生作用,其中最重要的是PI3K/Akt信号通路[10]。
PI3K/Akt 信号通路是一条重要的抗凋亡/促增殖信号途径。许多研究发现[10, 11],心肌缺血/再灌注时激活PI3K/Akt通路,使Akt在Ser473位点磷酸化成p-Akt,作用于多个下游靶点,能够减少MI/RI,发挥保护心肌功能。本课题组前期实验证明[7, 8],YLSC能提高ATPase活性,下调Bax蛋白,增加Bcl-2/Bax比值;上调NF-κB,降低TNF-α含量,从而减轻MI/RI,上述作用涉及到多个PI3K/Akt通路靶点。那么,YLSC对心肌损伤的保护作用是否与激活PI3K/Akt 信号通路有关? 基于此思路,本研究采用PI3K特异性抑制剂wortamannin,进一步观察YLSC对MI/RI保护作用与PI3K/Akt 信号通路的关联。
内皮型一氧化氮合酶(eNOS)是PI3K/Akt通路的一个重要靶点,其产生的NO作为信号分子在缺血/再灌注损伤过程中发挥重要作用[12]。内源性NO能扩张冠状动脉,增加血流供应,缩小梗死范围及改善能量代谢,从而减轻MI/RI[13]。此外,磷酸化Akt活化激活下游的eNOS,合成并释放NO后,可以抑制线粒体通透性转换孔的开放,抑制线粒体释放促凋亡因子而减少细胞凋亡[13]。PI3K/Akt通路也可调控半胱氨酸天冬氨酸蛋白酶(Caspase)家族参与抗细胞凋亡的心肌保护作用[10]。Caspase家族是细胞凋亡发生机制中最关键的环节之一,其中caspase-3与细胞凋亡的关系最为密切,参与多种因素诱导的细胞凋亡[14]。本实验中,与模型组比较,YLSC预处理上调心肌p-Akt与eNOS表达,升高血清NO含量,下调caspase-3表达,联合应用PI3K抑制剂wortmannin后上述作用均消失,表明YLSC能够抑制MI/RI诱导的细胞凋亡,其作用机制可能与PI3K/Akt信号通路的活化有关。
除凋亡外,自噬[15]是亚细胞膜结构发生变化并经溶酶体介导对细胞内蛋白质和细胞器降解的过程,对维持细胞内环境稳态及其生长、发育具有积极意义,然而,过度自噬则会导致细胞死亡。研究表明[16],缺血/再灌注时自噬异常增加,会导致严重的心肌损伤。Beclin1是调节细胞自噬过程的关键基因,其通过增加自噬相关蛋白的表达而促进自噬;微管相关蛋白轻链3蛋白-II(LC3-Ⅱ)是公认的自噬标志物,两者在心肌表达高低直接反映MI/RI自噬的发生程度[17]。本研究发现MI/RI时Beclin-1及LC3-Ⅱ表达水平上升,提示自噬发生。与模型组相比,YLSC能下调Beclin-1基因及LC3-Ⅱ蛋白表达,表明其抑制自噬而产生抗MI/RI作用。研究发现当细胞受饥饿、缺氧等因素刺激时PI3K/Akt通路能负性调节细胞的自噬[18]。本实验观察到YLSC抑制自噬的同时Akt的磷酸化水平也升高,并且该作用能够被PI3K/Akt通路阻断剂所阻断。因此,推测YLSC通过激活PI3K/Akt信号通路从而抑制细胞过度自噬,抑制缺血/再灌注损伤。
MI/RI发生时,由于氧化应激激活NF-κB,进而刺激心肌细胞分泌大量的炎症因子,如TNF-α,加重心肌细胞凋亡[19]。CK-MB和LDH是最常见和应用最广泛的心肌损伤标志物,其血清含量的增高提示心肌受到严重损伤,且损伤程度和心肌梗死程度呈正相关[20]。本实验结果显示,给予YLSC后,大量存在于心肌细胞中的CK-MB和LDH的漏出减少,TNF-α的释放减少,表明 YLSC可增加细胞存活,减轻MI/RI,对缺血心肌具有保护作用。
综上所述,YLSC能够减少缺血/再灌注引起的心肌酶漏出和炎症因子的释放,抑制心肌细胞凋亡和过度自噬。Wortmannin作为PI3K特异性抑制剂,下调p-Akt的表达,继而抑制了上述YLSC对MI/RI心肌的保护效应;单独应用wortmannin,心肌p-Akt表达下调,但对MI/RI没有影响。上述结果提示YLSC可能通过激活PI3K/Akt信号通路,对MI/RI产生保护作用,而激活后的Akt具体如何发挥保护效应还需进一步研究。
(致谢:本实验在广西医科大学医学科学实验中心及药学院实验中心完成,感谢黄仁彬教授、黄建春老师及唐静芝、黄婉苏同学的指导及帮助。)
| [1] | Hausenloy D J, Yellon D M. Myocardial ischemia-reperfusion injury:A neglected therapeutic target[J].J Clin Invest,2013,123(1):92-100. |
| [2] | Jennings R B. Historical perspective on the pathology of myocardial ischemia/reperfusion injury[J].Circ Res,2013,113(4):428-38. |
| [3] | Przyklenk K, Dong Y, Undyala V V, Whittaker P. Autophagy as a therapeutic target for ischaemia/reperfusion injury? Concepts, controversies, and challenges[J].Cardiovasc Res,2012,94(2):197-205. |
| [4] | Yao H, Han X, Han X. The cardioprotection of the insulin-mediated PI3K/Akt/mTOR signaling pathway[J].Am J Cardiovasc Drugs,2014,14(6):433-42. |
| [5] | 简 洁,张士军,邱 莉,等. 壮药玉郎伞查尔酮类成分的研究[J].中国医院药学杂志,2010,30(20):1734-7.Jian J, Zhang S J, Qiu L, et al. Study on chemical constituents of chalcones from Millettia Pulchra[J].Chin J Hospital Pharm,2010,30(20):1734-7. |
| [6] | 覃斐章,简 洁,焦 杨,黄仁彬. 17-甲氧基-7-羟基-苯并呋喃查尔酮对垂体后叶素致大鼠心肌缺血的保护作用[J].中国实验方剂学杂志,2012,18(01):145-8. Qin F Z, Jian J, Jiao Y, Huang R B. Protective effect of 17-methoxyl-7-hydroxyl-benzofuran chalcone on myocardial ischemia induced by pituitri n in rats[J].Chin J Exp Tradit Med Formul,2012,18(01):145-8. |
| [7] | 简 洁,刘 曦,黄仁彬,蒋伟哲. 玉郎伞两种黄酮单体对心肌细胞缺氧/复氧损伤的保护作用[J].中国药理学通报,2009,25(7):942-5. Jian J, Liu X, Huang R B, Jiang W Z. Protection and its mechanism of two flavone morphons from Yulangsan on hypoxia-reoxygenation induced injury in myocardial cells[J].Chin Pharmacol Bull,2009,25(7):942-5. |
| [8] | 梁杏梅.17-甲氧基-7-羟基-苯并呋喃查尔酮对心肌缺血/再灌注损伤大鼠NF-κB信号通路的调控作用及其机制研究[D].广西医科大学,2014. Liang X M. Study on the regulation and its mechanim of 17-methoxyl-7-hydroxy-benzene-furanchalcone on NF-κB signaling pathway in myocardial ischemia reperfusion injury rats[D].Guangxi Med Univ,2014. |
| [9] | Liu H, Guo X, Chu Y, Lu S. Heart protective effects and mechanism of quercetin preconditioning on anti-myocardial ischemia reperfusion(IR) injuries in rats[J].Gene,2014,545(1):149-55. |
| [10] | Wu H, Ye M, Yang J, et al. Nicorandil protects the heart from ischemia/reperfusion injury by attenuating endoplasmic reticulum response-induced apoptosis through PI3K/Akt signaling pathway[J].Cell Physiol Biochem,2015,35(6):2320-32. |
| [11] | The cardioprotective effect of icariin on ischemia-reperfusion injury in isolated rat heart:potential involvement of the PI3K-Akt signaling pathway[J].Cardiovasc Ther,2015,33(3):134-40. |
| [12] | Yan S,Chen L,Wei X, et al. Tetramethylpyrazine analogue CXC195 ameliorates cerebral ischemia-reperfusion injury by regulating endothelial nitric oxide synthase phosphorylation via PI3K/Akt signaling[J].Neurochem Res,2015,40(3):446-54. |
| [13] | 何东伟,刘新伟,庞 勇,刘 柳. 白藜芦醇对大鼠缺血/再灌注心肌细胞凋亡的抑制作用与PI3K-Akt信号通路的关系[J].中国中药杂志,2012,37(15):2323-6.He D W, Liu X W, Pang Y, Liu L. Inhibitory effect of resveratol on ischemia reperfusion-induced cardiocyte apoptosis and its relationship with PI3K-Akt signaling pathway[J].China J Chin Mater Med,2012,37(15):2323-6. |
| [14] | Zhu L, Wei T, Gao J,et al. The cardioprotective effect of salidroside against myocardial ischemia reperfusion injury in rats by inhibiting apoptosis and inflammation[J].Apoptosis,2015,20(11):1433-43. |
| [15] | Wei K, Wang P, Miao C Y. A double-edged sword with therapeutic potential:an updated role of autophagy in ischemic cerebral injury[J].CNS Neurosci Ther,2012,18(2):879-86. |
| [16] | 孙 瑶,张 婵,简 洁. 九龙藤总黄酮调控自噬对抗心肌缺血/再灌注损伤的实验研究[J].中国药理学通报,2015,31(2):232-6.Sun Y, Zhang C, Jian J. Experimental study of Bauhinia championii flavones on adjusting autophagy in myocardial ischemia/reperfusion injury[J].Chin Pharmacol Bull,2015,31(2):232-6. |
| [17] | Jain K, Paranandi K S, Sridharan S, Basu A. Autophagy in breast cancer and its implications for therapy[J].Am J Cancer Res,2013,3(3):251-65. |
| [18] | Singh B N, Kumar D, Shankar S, Srivastava R K. Rottlerin induces autophagy which leads to apoptotic cell death through inhibition of PI3K/Akt/mTOR pathway in human pancreatic cancer stem cells[J].Biochem Pharmacol,2012,84(9):1154-63. |
| [19] | 邵 莹,吴启南,周 婧,等. 淡竹叶黄酮对大鼠心肌缺血/再灌注损伤的保护作用[J].中国药理学通报,2013,29(2):241-7. Shao Y, Wu Q N, Zhou J, et al. Protective effects of total flavones from Lophatherum gracile on myocardial ischemia-reperfusion injury in rats[J].Chin Pharmacol Bull,2013,29(2):241-7. |
| [20] | 吴春艳,吴志刚,余光勇. 传统心肌酶谱检测在诊断急性心肌梗塞(AMI)的临床意义[J].中国医药导刊,2013,15(04):713-4. Wu C Y, Wu Z G, Yu G Y. Detection of traditional myocardial enzymes clinical significance in the diagnosis of acute myocardial infarction(AMI)[J].Chin J Med Guide,2013,15(04):713-4. |
