


2. 浙江医学高等专科学校基础医学部, 浙江 杭州 310053;
3. 浙江省人民医院病理科, 浙江 杭州 310046
2. Dept of Basic Medicine, Zhejiang Medical College, Hangzhou 310053, China;
3. Dept of Pathology, People's Hospital of Zhejiang Province, Hangzhou 310046, China
急性肺损伤(acute lung injury,ALI)/急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)是临床上常见的呼吸系统急危重症之一,具有发病急、进展快、病情凶险、病死率高等特点[1]。我国人口日趋老龄化,老年ALI的发病率是我国总人口发病率的110多倍,严重危害老年患者的身体健康。大量临床资料分析发现,革兰阴性杆菌感染是引起ALI,并导致死亡的主要原因之一。内毒素是革兰阴性杆菌细胞外膜成分之一,主要致病物质是脂多糖(LPS)。抗生素可杀灭侵入机体的细菌,但对细菌释放的内毒素无作用,应用抗生素使细菌裂解和死亡后,可释放更多的LPS[2]。MAPKs和NF-κB是LPS引起炎症的两条主要信号通路。MAPKs家族成员主要包括p42/44ERK、JNK和p38MAPK[3],均参与机体炎症反应的发生发展。NF-κB是重要的核內转录因子,在ALI病变过程中可引起多种炎症因子的大量释放。因此,以MAPKs和NF-κB为靶点的ALI治疗药物成为当前的研究热点。本研究旨在探讨三叶青黄酮对ALI的保护作用及其在MAPKs和NF-κB信号通路上的可能作用机制。
1 材料与方法 1.1 材料实验动物: 采用22月龄C57BL/6J小鼠(购自上海斯莱克实验动物有限公司),体质量45~50 g,随机分为4组:对照组、模型组、低剂量组、高剂量组,每组14只。实验试剂:LPS(L2880,大肠杆菌055:B5) 购自美国Sigma公司;Bradford蛋白定量试剂盒购自江苏碧云天生物技术公司;小鼠炎症因子和MAPKs信号分子ELISA检测试剂盒购自上海艾莱萨生物科技有限公司;核蛋白抽提和NF-κB活性检测试剂盒购自美国Active Motif公司。
1.2 三叶青总黄酮的制备称取三叶青(购自浙江中医药大学附属医院药房)饮片粗粉50 g,置于烧瓶中,加入5倍量的体积分数为0.6的乙醇溶液,水浴提取2次,每次提取1.5 h,趁热抽滤,滤渣按上述操作重复提取1次。合并提取液,三叶青总黄酮得率为33.2 mg·g-1。旋蒸除去乙醇,得到粗提物浓缩液,溶于水,利用HPD826吸附树脂对三叶青总黄酮粗提取物进行纯化,收集洗脱液,旋蒸,真空干燥得三叶青纯化物。称取一定量的纯化物,用乙醇定容于容量瓶中,得到三叶青纯化物中总黄酮纯度为516.2 mg·g-1。
1.3 ALI模型的诱导及给药参考前人方法[4],用400 μg·g-1的水合氯醛小鼠腹腔注射,麻醉后仰卧于45°倾斜的平板上。镊子轻轻拉出小鼠的舌,移液枪吸取1 g·L-1的LPS,以2.5 μg·g-1体重的剂量,滴于小鼠咽后壁,马上捏住小鼠鼻子。20 s后,松开舌及鼻,放于笼中让其自然苏醒。实验组同时灌胃给予三叶青黄酮40 μg·g-1(低剂量组)和80 μg·g-1 (高剂量组),对照组分别给予相等剂量的生理盐水。持续给药3 d。
1.4 支气管肺泡灌洗液(BALF)及肺组织匀浆的获得给药3 d后,7只小鼠行颈部手术分离气管进行插管,以0.5 mL PBS灌洗3次,收集灌洗液,离心BALF,上清于-80 ℃保存,待ELISA检测。沉淀用PBS悬起,血细胞计数仪计算白细胞总数,用瑞氏-吉姆萨染色进行细胞分类。取出另7只小鼠肺组织,左肺于40 g·L-1多聚甲醛磷酸盐缓冲液固定待病理切片检查。右肺用组织匀浆器研磨后,分别提取组织总蛋白和核蛋白,保存于-80 ℃冰箱中,用于信号分子表达和活性测定。
1.5 肺组织切片及HE染色肺组织固定12 h以上,常规石蜡包埋,4 μm连续切片。常规脱蜡至水,苏木精染色5 min,伊红染色1 min,梯度乙醇脱水,二甲苯透明,中性树胶封片。最后由经验丰富的医生根据炎症细胞浸润、肺水肿、出血和肺泡壁增厚等病理变化程度进行组织学评分。每个指标分5个等级:0:最小损伤,1:轻微损伤,2:中度损伤,3:严重损伤,4:最大损伤。
1.6 ELISA测定按照ELISA试剂盒说明书操作,检测BALF中的炎症因子和肺组织匀浆中MAPKs信号蛋白分子的表达。
1.7 核蛋白的提取和NF-κB p65的活性测定根据试剂盒说明,方法简述如下:96孔板中固定NF-κB p65的保守结合位点(5′-GGGACTTCC-3′),加入核蛋白提取液,封板,室温孵育、洗涤;依次加入NF-κB p65抗体、HRP-标记的二抗孵育、洗涤。最后加入显色剂,室温避光孵育2~10 min终止反应(由蓝色变为黄色),5 min内450 nm 波长测其吸光度值。
1.8 Western blot检测NF-κB p65蛋白的表达配制PAGE胶,取肺组织总蛋白提取物上样,电泳。冷却后电转印到PVDF膜上,洗膜,阻断液封闭。一抗为NF-κB p65兔抗人IgG,二抗为HRP标记的羊抗兔IgG,依次孵育洗涤后,感光,ECL显色,以GAPDH作内参。用密度比值表示目的蛋白量。
1.9 统计学处理实验结果以  ± s表示,用Prism 软件分析、作图。进行多组结果比较时采用单因素方差分析,进一步采用q检验法进行两组间的比较分析。
± s表示,用Prism 软件分析、作图。进行多组结果比较时采用单因素方差分析,进一步采用q检验法进行两组间的比较分析。
与对照组相比,模型组的白细胞总数和中性粒细胞数明显升高(P < 0.01),而三叶青总黄酮可明显降低老年ALI小鼠肺组织的白细胞渗出(P < 0.01),结果见Tab1。
( ± s,n=7) ± s,n=7) |
||
| Group | Leukocyte number (×105) | Neutrophil number (×105) |
| Control | 3.64±0.26 | 1.68±0.18 |
| Model | 19.05±1.20## | 18.77±1.48## |
| RTFs Low dose | 12.91±1.10** | 9.56±0.91** |
| High dose | 8.08±0.81** | 5.66±0.52** |
| ##P < 0.01 vs control;**P < 0.01 vs model group. | ||
ELISA法定量检测BALF中IL-1β、IL-6、IL-12p40、TNF-α和sTNF-R1的分泌水平(Fig1)。与对照组相比,支气管滴注LPS明显提高了小鼠BALF中各种促炎因子的分泌水平(P < 0.01)。给予三叶青黄酮后,上述炎症因子的分泌明显减少(P < 0.01),可能和肺组织中巨噬细胞、上皮细胞和内皮细胞的活性受到抑制有关。

|
| Fig 1 Secretion of inflammatory factors in BALF ##P < 0.01 vs control; **P < 0.01 vs model group. |
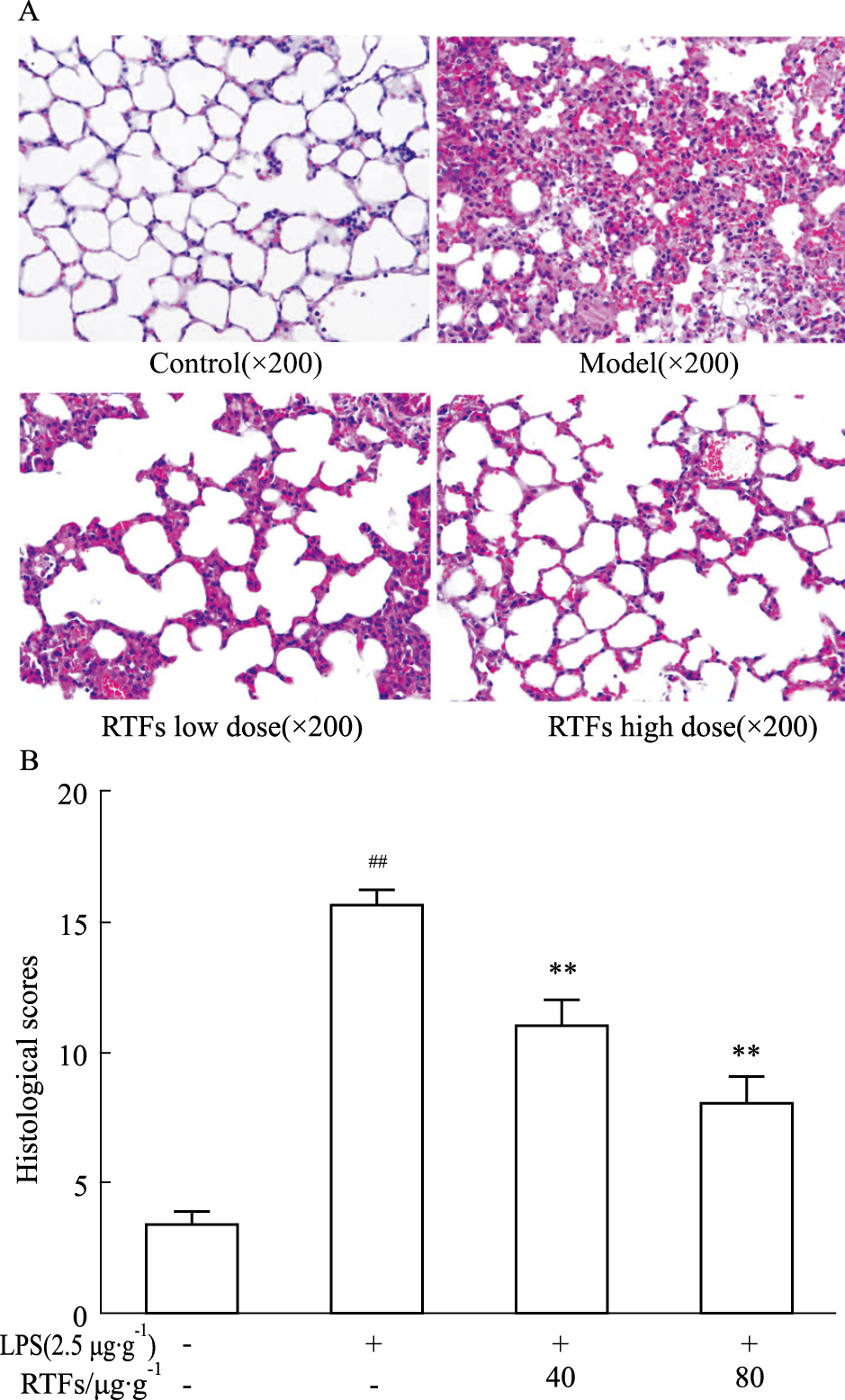
如Fig2所示,对照组老年小鼠肺组织结构清晰,无明显病理变化。炎症模型组小鼠肺组织结构严重破坏,血管扩张充血严重,肺泡腔出血,中性粒细胞等白细胞弥漫浸润,肺泡壁明显增厚,但给予三叶青黄酮后,病变明显改善。组织学评分进一步以半定量的方式证明了三叶青黄酮对ALI老年小鼠的肺组织病理损伤的逆转效果。
|
| Fig 2 Histopathologic examination and score of HE-stained lung tissues ##P < 0.01 vs control;**P < 0.01 vs model group. |
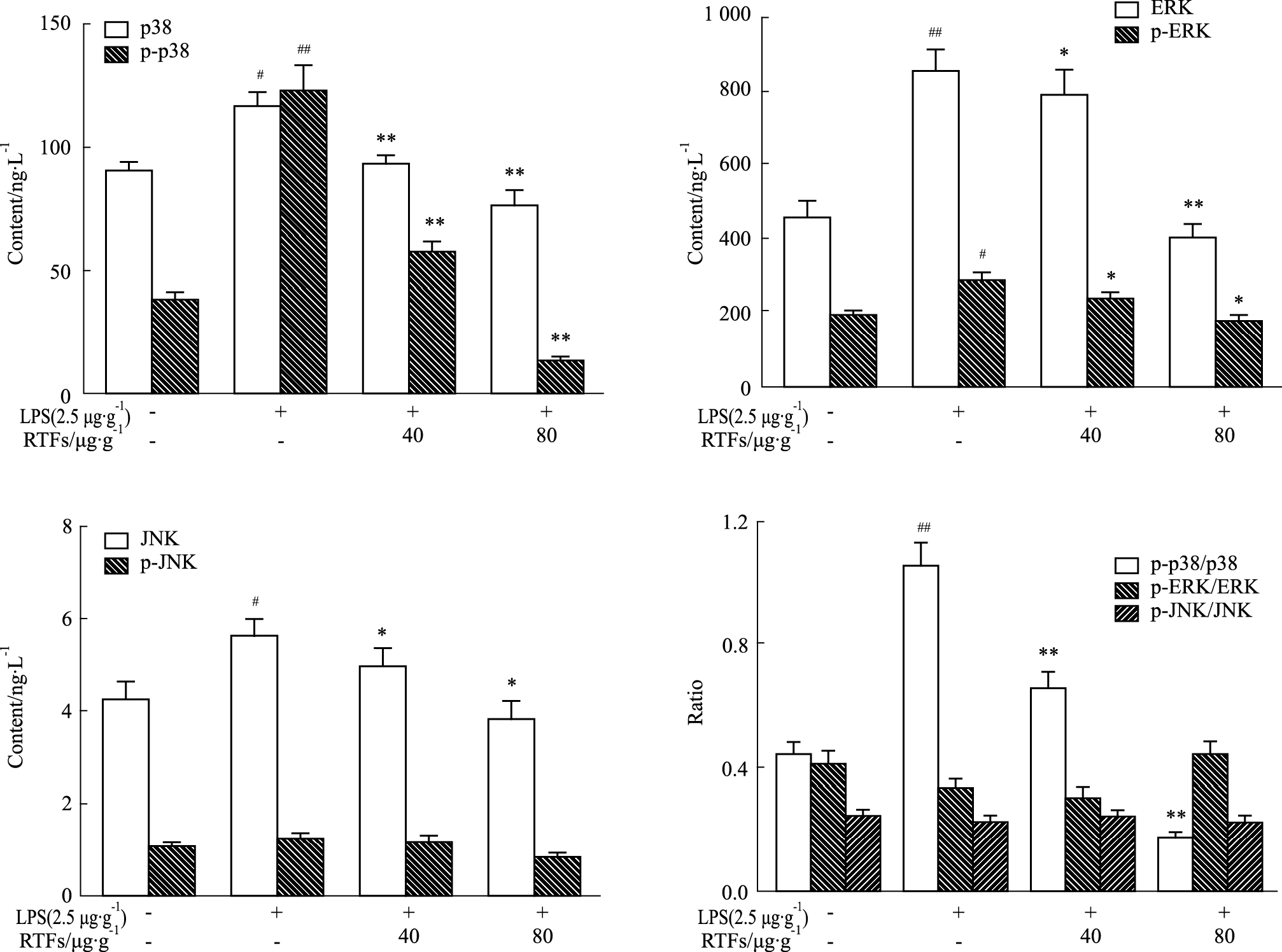
如Fig3所示,模型组肺组织中 p38MAPK、ERK、JNK及其磷酸化蛋白的表达水平明显升高,但与对照组比较,仅p38MAPK分子的磷酸化水平大幅升高(P < 0.01)。给予三叶青黄酮可明显降低p38MAPK分子的磷酸化水平(P < 0.01),而ERK和JNK的磷酸化水平改变不明显。
|
| Fig 3 Expression of MAPKs in lung tissues #P < 0.05,##P < 0.01 vs control; *P < 0.05,**P < 0.01 vs model group. |
与对照组相比,LPS刺激使NF-κB的表达水平、磷酸化水平和DNA结合活性都明显升高(P < 0.01)。但随着三叶青黄酮给药剂量的增加,NF-κB p65的表达水平、磷酸化水平以及DNA结合活性均逐渐降低(P < 0.01,Fig4)。

|
| Fig 4 Expression and DNA binding activity of NF-κB p65 in lung tissues A: Relative expression of NF-κB p65 and p-p65 detected by Western blot; B: DNA binding activity of NF-κB detected with TransAM kit. #P < 0.05,##P < 0.01 vs control; *P < 0.05,**P < 0.01 vs model group. |
三叶青是我国民间常用中草药之一,具有抗肿瘤[5]、免疫调节、抗病毒、抗炎等作用,且毒副作用小。近年来,三叶青的消炎功效日益成为人们研究的焦点,三叶青对Ⅱ型胶原所致实验性关节炎小鼠有一定的治疗作用[6]。三叶青提取物具有较好的抗炎、镇痛及解热作用,与相关的中医临床功效及主治相符。三叶青以块根入药,黄酮是三叶青根提取物中具有抗炎生物活性的主要成分之一。通过超高效液相色谱串联三重四级杆质谱法(UPLC-MS/MS)已测定三叶青根中10种黄酮类成分的含量[7]。
支气管滴注内毒素LPS可诱导ALI动物模型。LPS刺激促使白细胞,尤其是中性粒细胞向感染病灶的迁移,加速对免疫反应的调节[8]。同时,LPS通过单核巨噬细胞趋化因子-1(MCP-1)的分泌,趋化并激活静止的肺泡巨噬细胞,引起炎症和ALI。本研究发现,老年小鼠支气管滴注LPS后,肺间质充满了活化的肺泡巨噬细胞和中性粒细胞,但三叶青黄酮给药后BALF中白细胞数量明显减少,表明三叶青黄酮可抑制LPS引起的白细胞浸润和向病灶的迁移。另外,LPS刺激后肺组织充血水肿严重,肺泡间隔增厚,肺组织评分也快速升高,但三叶青黄酮给药可逆转这一损伤性变化,可见三叶青黄酮对LPS引起的肺损伤有明显疗效。
血管内皮损伤在ALI的发作中有重要作用,气—血屏障的破坏,促进中性粒细胞的游出和肺泡腔的炎性渗出。LPS诱导的IL-1β、IL-6、IL-12p40和TNF-α的过量释放,增加了肺组织血管的渗透性,引起血管内皮细胞损伤[9]。三叶青黄酮灌胃给药可明显减少上述炎症因子的产生,可见三叶青黄酮对ALI血管内皮损伤具有保护作用和抗炎效果。
此外,三叶青黄酮除了抑制IL-1β、IL-6、IL-12、p40、TNF-α等促炎因子的分泌外,还影响sTNF-R1的产生。TNF的所有生物学功能都依赖于TNFR,TNFR主要有两种亚型:TNF-R1和TNF-R2。膜结合型TNFR(mTNFR)在蛋白酶等作用下,可裂解成sTNF-R1 和sTNF-R2等亚型,释放到血液或组织液中[10]。sTNFR仍有结合TNF的活性,从而调节TNF的生物学功能。当TNF释放时,sTNFR也迅速释放,这可能作为一种反馈保护机制,以减少直接发挥作用的TNF及细胞表面的mTNFR数量。三叶青黄酮抑制TNF表达的同时,也降低了sTNFR的水平,使两者保持着动态平衡,从而阻碍了炎症的过度发展,促进组织微环境的稳定。
LPS通过MAPKs和NF-κB信号级联途径调节炎症介质的表达和释放。其中,NF-κB是宿主抗感染反应的重要转录因子。静息状态下,NF-κB存在于细胞质中,和IκB聚合形成异源三聚体。受LPS刺激后,IκB发生降解并释放出NF-κB异源二聚体,NF-κB转移至细胞核内,启动各种炎症因子基因的转录和翻译,发挥转录水平的调控作用,促进ALI的病变发展[11]。因此,阻断NF-κB的活化有望缓解ALI。本研究证实,三叶青黄酮灌胃可明显抑制老年ALI小鼠肺组织NF-κB的表达和磷酸化,降低核内NF-κB的DNA结合活性,并呈现浓度依赖性。NF-κB的活性变化和下游炎症因子的分泌水平完全一致。因此,NF-κB是三叶青黄酮拮抗LPS所致小鼠ALI炎症的重要作用靶点。
MAPKs信号通路是介导细胞反应的重要信号转导系统,MAPKs家族成员均可对炎症进行调控。当受到LPS刺激后,细胞内的ERK、JNK 和p38MAPK被激活,作用于各自的底物,从而影响转录因子的活性,调控包括IL-1β、IL-6、IL-12p40、TNF-α等多种细胞因子的表达。而这些细胞因子又能激活MAPKs,最终调控其它炎症介质的生成[12]。本实验结果显示,三叶青黄酮明显抑制p38MAPK的表达和磷酸化,且这种抑制作用呈剂量依赖性,而对JNK和ERK无明显影响。p38MAPK的磷酸化水平和NF-κB的磷酸化及DNA结合活性呈正相关。有研究指出,在MAPK信号通路中,与NF-κB的激活关系最为密切的是p38MAPK,若p38MAPK的表达受到抑制,NF-κB的激活也会受到影响[13]。因此,p38MAPK和NF-κB都是抗炎机制中的重要环节,是抗炎药物作用的重要靶点。
综上所述,本研究证实三叶青黄酮对LPS诱导的老年小鼠ALI具有明显抗炎效果,减轻病变,改善肺功能。p38MAPK和NF-κB信号通路是三叶青黄酮发挥抗炎作用的主要途径。其对ALI小鼠肺内巨噬细胞、内皮细胞、上皮细胞等细胞水平的影响还有待进一步深入研究。
(致谢:感谢浙江中医药大学中药药理实验室、动物实验中心和浙江医学高等专科学校科研实验中心提供的大力支持。)
| [1] | Gotts J E, Matthay M A. Treating ARDS:new hope for a tough problem[J]. Lancet Respir Med, 2014, 2(2):84-5. |
| [2] | Gutsmann T,Schromm A B,Brandenburg K. The physicochemistry ofendotoxins in relation to bioactivity[J].Intern J Med Microbiol, 2007, 297(5):341-52. |
| [3] | Arndt P G, Young S K, Lieber J G, et al. Inhibition of c-Jun N-terminal kinase limits lipopolysaccharide-induced pulmonary neutrophil influx[J]. Am J Respir Crit Care Med, 2005, 171(9):978-86. |
| [4] | 郭 玲, 李文静, 徐明江, 王 宪. 吸入脂多糖诱导小鼠急性肺炎模型的建立[J]. 北京大学学报(医学版), 2009, 141(2):226-9.Guo L, Li W J, Xu M J, Wang X. A mouse model of acute lung inflammation induced by lipopolysaccharide inhalation[J]. J Peking Univ(Health Sci), 2009, 141(2):226-9. |
| [5] | 钟良瑞, 魏克民. 三叶青黄酮对肺癌A549细胞生长抑制与MAPKs通路关系的研究[J]. 中国药理学通报, 2014, 30(1):101-4. Zhong L R, Wei K M. Radix tetrastigma hemsleyani flavone suppresses human lung carcinoma A549 cell by regulating MAPKs pathway[J]. Chin Pharmacol Bull, 2014, 30(1):101-4. |
| [6] | 吴安安, 倪荷芳. 三叶青对小鼠Ⅱ型胶原关节炎的影响[J]. 南京中医药大学学报, 2007, 23(5):307-9.Wu A A,Ni H F.Effect of Tetrstigma Hemsleyanum on type Ⅱcollagen arthritis[J].J Nangjing TCM Univ,2007,23(5):307-9. |
| [7] | 许 文, 傅志勤, 林 婧, 等. UPLC-MS/MS法同时测定三叶青中10种黄酮类成分[J]. 药学学报, 2014,49(12):1711-7.Xu W, Fu Z Q, Lin J, et al. Rapid simultaneous determination of ten major flavonoids in Tetrastigma hemsleyanum by UPLC-MS/MS[J]. Acta Pharm Sin, 2014, 49(12):1711-7. |
| [8] | 梁家红, 张水娟, 姚 立. 丹酚酸B对肺上皮细胞凋亡和急性肺损伤的影响[J]. 中国药理学通报, 2013, 29(4):531-4.Liang J H, Zhang S J, Yao L. Effects of salvianolic acid B on lung epithelial cell apoptosis and acute lung injury[J]. Chin Pharmacol Bull, 2013, 29(4):531-4. |
| [9] | Vandenbroucke E, Mehta D, Minshall R, Malik A B. Regulation of endothelial junctional permeability[J]. Ann N Y Acad Sci, 2008, 1123:134-45. |
| [10] | Ijiri Y, Kato R, Sadamatsu M, et al. Chronological changes in circulating levels of soluble tumor necrosis factor receptors 1 and 2 in rats with carbon tetrachloride-induced liver injury[J]. Toxicology,2014, 316:55-60. |
| [11] | Galani V,Tatsaki E, Bai M,et al. The role of apoptosis in the pathophysiology of acute respiratory distress syndrome (ARDS):an up-to-date cell-specific review[J]. Pathol Res Pract, 2010, 206(3):145-50. |
| [12] | Moreira-Tabaka H, Peluso J, Vonesch J L, et al. Unlike for human monocytes after LPS activation, release of TNF-α by THP-1 cells is produced by a TACE catalytically different from constitutive TACE[J]. PloS One, 2012, 7(3):e34184. |
| [13] | Nick J A, Avdi N J, Young S K, et al.Selective activation and functional significance of p38 alpha mitogen-activated protein kinase in lipopolysaccharide stimulated neutrophils[J].J Clin Invest, 1999, 103(6):851-8. |

