


2. 宁夏医科大学基础医学院, 宁夏 银川 750001;
3. 宁夏医科大学药学院, 宁夏 银川 750001
2. School of Basic Medical Science, Yinchuan 750001, China;
3. School of Pharmacy, Yinchuan 750001, China
神经病理性疼痛(neuropathic pain,NP)是由于外周或中枢神经系统受到损伤或产生病变而导致的疼痛,严重危害人类健康和影响生活质量,是最常见、最顽固、最难治的慢性疼痛[1, 2]。由于其病因多样,发病机制至今尚未彻底阐明,目前仍缺乏有效的治疗措施。NP不仅严重影响了患者的生活质量、精神状态和社会功能,还给社会带来了巨大的经济负担。随着新型动物模型的不断涌现,对NP 病理生理学研究的日趋深入,更多的受体被发现参与到NP 发生发展的过程,这些受体的表达及其介导的细胞内信号传导系统与镇痛效应存在较高的相关性,为新型镇痛药的开发提供了新的作用靶点。
近年来,用于治疗NP的治疗药物主要是抗癫痫药、抗抑郁药及阿片类镇痛药。由于这些药物具有毒、副作用以及疗效不确定等特点,因此从植物中提取有效成分并开发新药越来越受到人们重视。天然药物具有作用机制的多靶点和低毒性的特点,已被广泛用于慢性疼痛的研究与开发,所以从天然植物中寻找并开发高效、低毒、低成瘾性的新型镇痛药的研究一直受到国内外医药学界的关注。氧化苦参碱(oxymatrine,OMT)是宁夏特色植物苦豆子中的一种生物碱,传统中医主要用于清热、祛风燥湿、止痛杀虫等[3]。近年来,国内外的研究发现氧化苦参碱在抗心律失常、抗肿瘤、抗动脉粥样硬化、保肝利胆、治疗湿疹和带状疱疹等方面具有一定的药理活性[3, 4],并且有研究表明OMT具有镇痛作用[5]。本研究采用坐骨神经结扎致神经病理性痛小鼠模型,观察氧化苦参碱对神经病理性痛小鼠行为学的变化以及脊髓水平CaMK Ⅱ的表达情况,探讨氧化苦参碱在神经病理性痛的镇痛作用及其作用机制,为OMT应用于临床疼痛治疗提供理论依据。
1 材料与方法 1.1 实验动物ICR小鼠[宁夏医科大学实验动物中心,合格证号:SYXK(宁)2013-0001],体质量18~22 g,♂。
1.2 实验材料OMT(宁夏药物研究所,纯度98%);戊巴比妥钠(Sigma-Aldrich公司,批号:20091011);KN-93(Sigma-Aldrich公司,批号:139298-40-1);AIP(Sigma-Aldrich公司,批号:167114-91-2);氯化钠注射液(宁夏启元国药有限公司,批号:101121-1)。4-0医用铬制肠线(上海浦东金环医疗用品有限公司);Von Frey Filaments(Danmic Global,USA)。
1.3 坐骨神经结扎动物模型的制备参照Bennett和Xie[6]方法建立坐骨神经慢性缩窄性损伤模型,小鼠称重,经腹腔注射0.9%戊巴比妥钠麻醉后,取侧卧位,备皮,用碘伏消毒皮肤,切开右下肢股部皮肤后,顺肌纹钝性分离股二头肌和臀肌,暴露右侧坐骨神经中上段,于坐骨神经分成3支前的主干部位处,游离神经7 mm左右。用4-0医用铬制肠线间隔1 mm松结扎3处,为了预防强度过大,结扎线的松紧以引起右后肢出现轻微的颤动为宜,从而保护神经外膜的血运。结扎完毕后逐层缝合肌肉层和皮肤。假手术组只暴露右侧坐骨神经,不结扎该神经。
1.4 观察OMT的镇痛作用 1.4.1 分组与给药将小鼠随机分为假手术组(sham)组、模型(CCI)组、OMT(160、80、40 mg·kg-1)剂量组,每组10只。假手术组只暴露右侧坐骨神经,不给与结扎。模型组和给药组如上所述进行右侧坐骨神经的结扎。术后d 8,假手术组和模型组腹腔注射生理盐水;给药组分别注射高、中、低剂量OMT,给药容量均为0.01 mL·g-1,连续给药7 d。在术前,术后d 7和给药后1、3、5、7 d进行各个行为学指标的测定。
1.4.2 机械缩足反射阈值的测定在安静的环境下,将小鼠置于2 mm×2 mm的金属网垫上,用有机玻璃盒约束小鼠,待其适应30 min后,采用Chaplan[7]等的up-down方法测定小鼠的机械缩足反射阈值(PWT)。使用不同折力的Von Frey Filaments(vFFs)刺激小鼠的第3、4趾间的皮肤,观察小鼠的缩足反应。当vFFs弯曲至90°时,小鼠仍不抬足,视为无反应。从0.4 g开始,如果vFFs不能引起缩足反应,则给予相邻的大一级的vFFs;如果有反应,则更换相邻的小一级的vFFs,每次间隔10 s,直到找到10次中引起50%抬足反应时的vFFs,最大折力为4.0 g,记录压力值,即为机械缩足反射阈值(g)。
1.4.3 冷缩足反射次数的测定在安静的环境下,将小鼠置于表面温度为(4±1)℃的冷盘上,用有机玻璃盒约束小鼠,待其适应5 min后,按照Jasmin等[8]的方法观察小鼠5 min,记录小鼠右后肢抬足次数。
1.5 观察OMT与相关工具药的作用 1.5.1 分组及给药小鼠制备成CCI模型后,随机分为4组:对照组:NS(ip)+NS(ith)组、OMT组:OMT(ip)+NS(ith)组、工具药组:NS(ip)+工具药(ith)、复合组:OMT(ip)+各工具药(ith),每组10只。OMT采用腹腔注射(ip)给药,工具药采用鞘内注射(ith)给药。从术后d 8开始,连续给药7 d,d 7给药时各组ip OMT或NS 45 min后,再ith给予工具药或NS。OMT:ip容量为0.1 mL/10 g;相关工具药:KN-93 1.25 μg/只、AIP 0.02 μg/只,ith容量为5 μL/只。各组鞘内注射工具药或NS 15 min后,测定小鼠手术侧机械缩足反射阈值。
1.6 OMT对CCI小鼠脊髓组织CaMK Ⅱ受体蛋白表达的影响 1.6.1 分组及给药ICR ♂小鼠21只,随机分为:假手术组、模型组、OMT(160 mg·kg-1)组,每组7只。假手术组只暴露右侧坐骨神经,不给予结扎。模型组和OMT组进行右侧坐骨神经的结扎。各组分别于d 7给药后60 min后,脱颈处死取腰膨大处脊髓置于-80℃冰箱中备用。
1.6.2 提取各组脊髓组织总蛋白用BCA试剂盒测定蛋白浓度。取总蛋白50 μg制备蛋白样品,经10% SDS-PAGE分离,电转到硝酸纤维膜上后,将膜封闭2 h,加一抗(兔源抗-pCaMK Ⅱ抗体、兔源抗-CaMK Ⅱ抗体或兔源抗-β-actin抗体),于4℃过夜,TBST洗涤(5 min×3),加二抗(HRP标记的羊抗兔IgG抗体),室温下孵育2 h。TBST洗涤(5 min×3),加入化学发光底物进行曝光、显影及图像采集。对蛋白条带进行光密度的比值表示pCaMK Ⅱ和CaMK Ⅱ蛋白的相对含量。
1.7 统计学处理应用SPSS 13.0统计软件进行数据处理分析,各数值用 ± s表示。两样本均数间比较采用t检验,多样本均数间比较采用One-way ANOVA检验。
± s表示。两样本均数间比较采用t检验,多样本均数间比较采用One-way ANOVA检验。
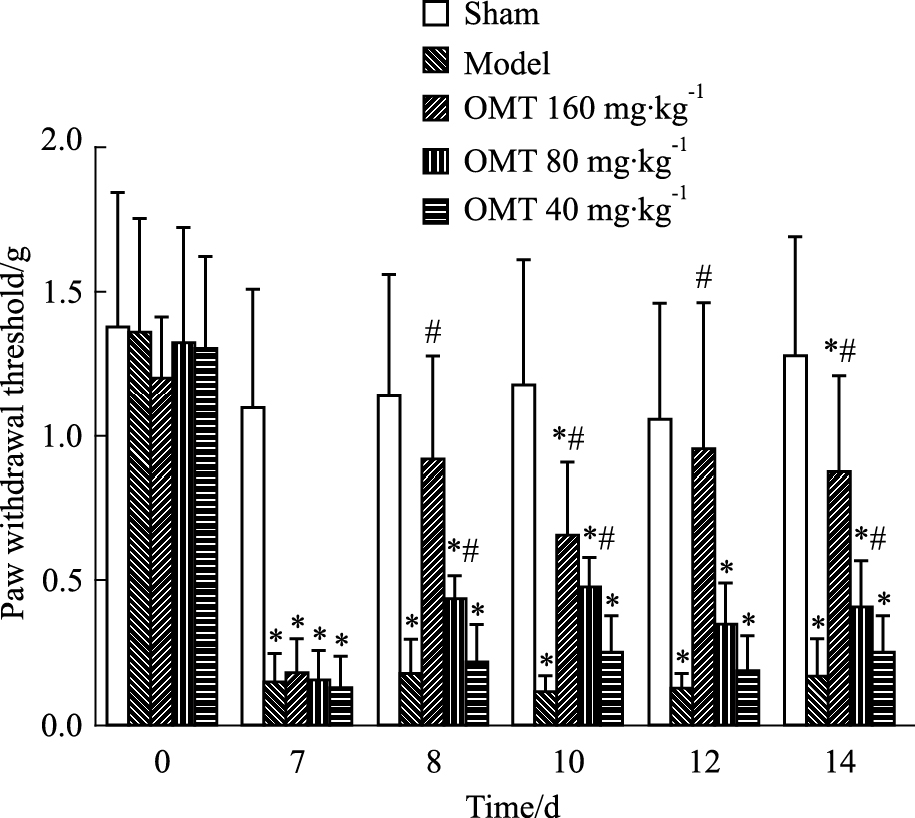
手术前,各组小鼠的基础痛阈值比较差异无显著性(P>0.05)。手术后,与假手术组比较,其它各组的PWT明显降低(P < 0.05),说明CCI模型制备成功。与模型组比较,CCI+OMT(160 mg·kg-1)组给药后1、3、5、7 d的PWT明显增高(P < 0.05);CCI+OMT(80 mg·kg-1)组给药后1、3、7 d的PWT明显增高(P < 0.05);而CCI+OMT(40 mg·kg-1)组给药后各时间点的PWT差异无显著性(P>0.05),见Tab1、Fig1。
| Sham | - | 1.38±0.46 | 1.10±0.41# | 1.14±0.42# | 1.18±0.43# | 1.06±0.40# | 1.28±0.41# |
| Model | - | 1.36±0.39 | 0.15±0.10* | 0.18±0.12* | 0.12±0.05* | 0.13±0.05* | 0.17±0.13* |
| CCI+OMT | 160 | 1.20±0.21 | 0.18±0.12* | 0.92±0.36# | 0.66±0.25*# | 0.96±0.50# | 0.88±0.33*# |
| CCI+OMT | 80 | 1.32±0.40 | 0.16±0.10* | 0.44±0.08*# | 0.48±0.10*# | 0.35±0.14* | 0.41±0.16*# |
| CCI+OMT | 40 | 1.30±0.32 | 0.13±0.11* | 0.22±0.13* | 0.25±0.13* | 0.19±0.12* | 0.25±0.13* |
| *P < 0.05 vs sham group;#P < 0.05 vs CCI group | |||||||
|
| Fig 1 Effects of OMT on mechanical allodynia test in hind paw ipsilateral on chronic constrictive injury (CCI) of sciatic nerve in mice *P < 0.05 vs sham group;#P < 0.05 vs CCI group |
手术前,各组小鼠的基础痛阈值比较差异无显著性(P>0.05)。手术后,与假手术组比较,模型组小鼠冷缩足反射次数明显增高(P < 0.05),说明模型制备成功。与模型组比较,CCI+OMT(160、80、40 mg·kg-1)组给药后各个时间点的冷缩足反射次数均明显降低(P < 0.05),见Tab2,Fig2。
| Group | Dose/mg·kg-1 | Paw withdrawal threshold/g | |||||
| Preoperation | 7 d postoperation | After administration/d | |||||
| 1 | 3 | 5 | 7 | ||||
| Sham | - | 13.5±2.99 | 15.8±2.44# | 14.7±4.55# | 15.8±4.83# | 15.6±4.33# | 17.6±4.48# |
| Model | - | 15.5±1.84 | 51.9±7.54* | 44.3±9.48* | 49.2±6.40* | 43.7±6.90* | 46.1±4.15* |
| CCI+OMT | 160 | 14.1±2.08 | 53.1±5.67* | 19.1±4.61# | 19.7±2.06*# | 19.1±4.91# | 18.5±4.25# |
| CCI+OMT | 80 | 13.8±2.15 | 51.8±6.81* | 30.2±4.34*# | 27.8±2.90*# | 27.2±3.16*# | 26.8±4.40*# |
| CCI+OMT | 40 | 14.4±2.37 | 48.3±8.41* | 34.8±6.91*# | 33.2±4.08*# | 31.9±2.64*# | 32.3±3.77*# |
| *P < 0.05 vs sham group;#P < 0.05 vs CCI group | |||||||

|
| Fig 2 Effects of OMT on cold allodynia test in hind paw ipsilateral on chronic constrictive injury (CCI) of sciatic nerve in mice *P < 0.05 vs sham group;#P < 0.05 vs CCI group |
KN-93是实验研究中最常用的CaMK Ⅱ抑制剂。在本实验中,NS(ip)+NS(ith)组、OMT(35 mg·kg-1,ip)+NS(ith)组、NS(ip)+KN-93(ith)组和OMT(35 mg·kg-1,ip)+KN-93(ith)组术后d 7的PWT差异无显著性(P>0.05)。与NS(ip)+NS(ith)组比较,OMT(35 mg·kg-1,ip)+NS(ith)组和NS(ip)+KN-93(ith)组给药后d 7的PWT差异无显著性(P>0.05);OMT(35 mg·kg-1,ip)+ KN-93(ith)组给药后d 7的PWT明显升高(P < 0.01)。 与OMT(35 mg·kg-1,ip)+ NS(ith)组比较,OMT(35 mg·kg-1,ip)+KN-93(ith)组给药后d 7的机械缩足反射阈值明显升高(P < 0.01)。阈下剂量的KN-93能明显增强阈下剂量OMT的镇痛作用,提示:KN-93对阈下剂量的OMT的镇痛作用有协同作用(Tab3、Fig3)。
| Group | Administrationroute | Paw withdrawal threshold/g | |
| 7 d postoperation | 7 d after administration | ||
| NS+NS | ip+ith | 0.18±0.12 | 0.16±0.13 |
| OMT(35 mg·kg-1)+NS | ip+ith | 0.20±0.15 | 0.17±0.13 |
| NS+KN-93 | ip+ith | 0.20±0.10 | 0.13±0.04 |
| OMT(35 mg·kg-1)+KN-93 | ip+ith | 0.19±0.11 | 0.70±0.21**## |
| **P<0.01 vs NS+NS group;##P<0.01 vs OMT+NS group | |||

|
| Fig 3 Effects of KN-93 on antinociception of OMT **P<0.01 vs NS+NS group;##P<0.01 vs OMT+NS group |
AIP亦是一种CaMK Ⅱ抑制剂。在本实验中,NS(ip)+NS(ith)组、OMT(35 mg·kg-1,ip)+ NS(ith)组、NS(ip)+AIP(ith)组和OMT(35 mg·kg-1,ip)+AIP(ith)组术后d 7的PWT差异无显著性(P>0.05)。与NS(ip)+NS(ith)组比较,OMT(35 mg·kg-1,ip)+NS(ith)组和NS(ip)+AIP(ith)组给药后d 7的PWT差异无显著性(P>0.05);OMT(35 mg·kg-1,ip)+ AIP(ith)组给药后d 7的PWT明显升高(0.46±0.10)(P < 0.01)。 与OMT(35 mg·kg-1,ip)+NS(ith)组比较,OMT(35 mg·kg-1,ip)+ AIP(ith)组给药后d 7的机械缩足反射阈值明显升高(P < 0.01)。阈下剂量的AIP能明显增强阈下剂量OMT的镇痛作用,提示:AIP对阈下剂量的OMT的镇痛作用有协同作用(Tab4、Fig4)。
| Group | Admin-istrationroute | Paw withdrawal threshold/g | |
| 7 d postoperation | 7 d afteradministration | ||
| NS+NS | ip+ip | 0.18±0.12 | 0.16±0.13 |
| OMT(35 mg·kg-1)+NS | ip+ip | 0.20±0.15 | 0.17±0.13 |
| NS+AIP | ip+ip | 0.16±0.10 | 0.19±0.12 |
| OMT(35mg·kg-1)+AIP | ip+ip | 0.18±0.12 | 0.46±0.10**## |
| **P<0.01 vs NS+NS group;##P<0.01 vs OMT+NS group | |||

|
| Fig 4 Effects of AIP on antinociception of OMT **P<0.01 vs NS+NS group;##P<0.01 vs OMT+NS group |
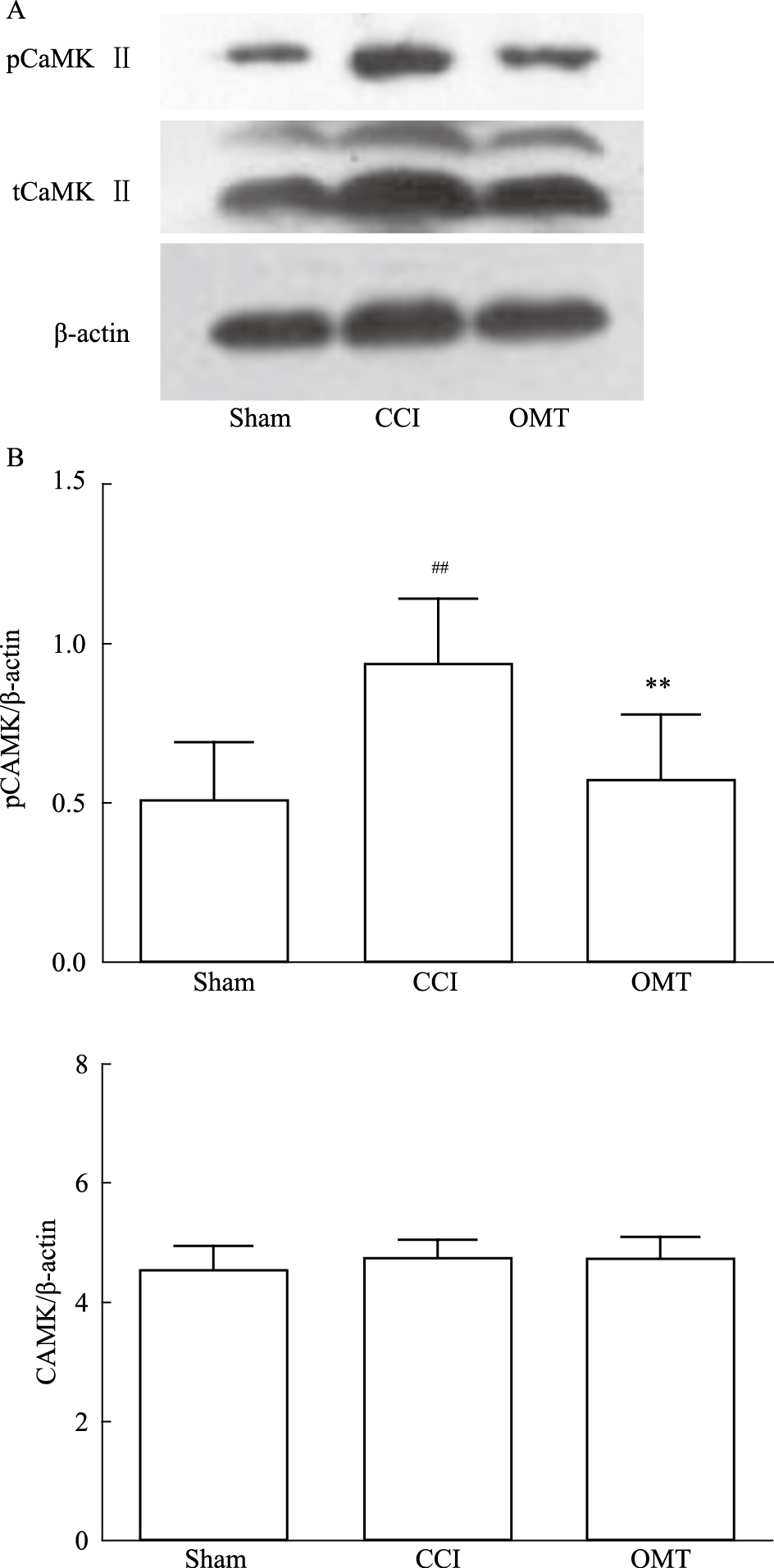
结果显示:模型组小鼠的pCaMK Ⅱ蛋白表达较假手术组明显升高(P < 0.01);与模型组比较,OMT(160 mg·kg-1)组可明显降低pCaMK Ⅱ蛋白的表达(P < 0.01);而各组小鼠的CaMK Ⅱ蛋白表达均无明显差异(Fig5)。
|
| Fig 5 Effects of OMT on the expressionof CaMK Ⅱprotein of mice with CCI A:Representative of immunoblot bands;B:Data summary.**P < 0.01 vs sham group;##P < 0.01 vs CCI group |
神经病理性疼痛属于难治性疼痛,目前只有40%~60%的病人能够得到部分的缓解[9]。
已有文献证实氧化苦参碱对于化学刺激、物理性热刺激、肿瘤转移性疼痛、神经性、炎性等引起的疼痛具有明显的镇痛作用[10, 11, 12, 13]。刘芬等[10]提出,氧化苦参碱可对抗热板和冰醋酸所致的小鼠疼痛反应。陈霞等[5]通过小鼠热板法也证明了,氧化苦参碱可剂量相关地升高小鼠的痛阈值。张娟等[11]研究还发现,氧化苦参碱可以抑制由福尔马林引起的急性疼痛和和继发性炎性反应。近年来,姜静[12]、吕晓强等[13]通过研究证实氧化苦参碱对肿瘤转移性、神经病理性、化学性及物理刺激性疼痛均有抑制作用。目前,对于氧化苦参碱的镇痛作用机制的研究,主要可能是与神经递质相关。
疾病的机制研究在很大程度上依赖于动物模型,近年来,多种急性、慢性疼痛动物模型的建立为人类了解自身的神经病理性疼痛的发病机制作出了巨大的贡献,同时也为观察药物的作用机制及疗效提供方便[7, 8]。CCI模型是由Bennett和Xie于1988年首创的,该模型容易操作,成功率高,创伤小,而且并发症少[6],CCI模型常被用于慢性神经病理性疼痛发生机制及药物治疗的研究,是最常用的慢性神经病理性疼痛的动物模型。通过CCI模型机械缩足反射法观察OMT对神经病理性疼痛具有较好的镇痛作用。
而神经病理性疼痛的发生机制十分复杂,目前,疼痛与CaMK Ⅱ受体的激活之间的关系越来越受到人们的重视。CaMK Ⅱ,是一种多功能的丝氨酸/苏氨酸蛋白激酶[14]。它能参与各种神经元功能,如基因表达、合成和释放神经递质、神经递质受体的调节、离子通道和突触的可塑性[15]。在慢性疼痛中发现,细胞内明显增加的钙离子通过结合到它的钙离子结合位点从而激活钙调蛋白,一旦激活它将发生自身磷酸化,之后它的活动将不再依赖于钙离子。已被证实CaMK Ⅱ的自身磷酸化存在于与疼痛传导相关的脊髓背角浅层和背根神经节[16],这表明CaMK Ⅱ在疼痛中的调节作用逐渐被认识。文中运用CaMK Ⅱ的拮抗剂KN-93和AIP能协同OMT对CCI小鼠的镇痛作用,提示OMT可能通过CaMK Ⅱ受体发挥作用。KN-93是实验研究中最常用的CaMK Ⅱ抑制剂,能够直接阻断外来的伤害性刺激。Fang等[17]研究发现在大鼠足底皮下注射辣椒素15 min后,行为学测试发现大鼠的探索行为明显减少,如鞘内给予CaMKII抑制剂KN-93,则可以恢复大鼠的探索行为。Ogawa等[18]在切断SD大鼠下牙槽神经所形成的三叉神经痛研究中发现,神经切断后30 min,CaMK Ⅱ和pCaMK Ⅱ在脑干的三叉神经亚核表达即增加,鞘内给予KN-93即可缓解下牙槽神经切断后的痛觉过敏。本实验结果显示,与OMT(35 mg·kg-1,ip)+NS(ith)组比较,KN-93与阈下剂量OMT合用时,CCI小鼠的机械缩足反射阈值明显提高。AIP是一种新合成的多肽类物质,其抑制作用不受Ca2+/CaM存在与否的影响,1 μmol·L-1的AIP就可完全抑制CaMK Ⅱ的活性但不影响cAMP反应元件结合蛋白、蛋白激酶C及CaMKIV的活性[19]。与此研究结果相似,本实验发现,与OMT(35 mg·kg-1,ip)+NS(ith)组比较,鞘内注射AIP与阈下剂量OMT合用时,CCI小鼠的机械缩足反射阈值明显提高。上述表明氧化苦参碱对神经病理性疼痛的镇痛作用与受体CaMK Ⅱ的调节作用。另外,与模型组比较,OMT高剂量组能明显降低小鼠脊髓pCaMK Ⅱ受体的蛋白表达,进一步证实OMT能够通过调节CaMK Ⅱ受体的活性来发挥镇痛作用。
(致谢:本实验是在宁夏回药现代化工程技术研究中心药理实验室完成,感谢研究中心各位老师的指导和帮助!)
| [1] | Campbell J N, Meyer R A. Mechanisms of neuropathic pain[J]. Neuron, 2006, 52(1):77-92. |
| [2] | Leung L,Cahill C M.TNF-α and neuropathic pain-a review[J].Neuroinflammation, 2010; 7(27):1- 11. |
| [3] | Zhou J J,Yang G,Jin S J, et al.Oxymatrine-carbenoxolone sodium inclusion compound induces antinociception and increases the expression of GABAAα1 receptors in mice[J].Eur Pharm,2010, 626:244-9. |
| [4] | 陶丽君,高进贤,金少举,等.甘珀酸钠苦参素包合物对小鼠中枢的抑制作用[J].第四军医大学学报,2009,30(9):823-6.Tao L J,Gao J X,Jin S J,et al. Inhibitory effects of oxymatrine-carbenoxolone sodium inclusion complex on central nervous system in mice[J].J Fourth Milit Med Univy, 2009,30(9):823-6. |
| [5] | 陈 霞,刘 芬,吕文伟,等.氧化苦参碱的镇痛作用及其机制研究[J].中草药,2006,37(2):255-7. Chen X,Liu F,Lv W W,et al. Study on the analgesic effect and mechanism of the oxidation of Matrine[J].Chin Tradit Herbal Drugs, 2006,37(2):255-7. |
| [6] | Bennett C J,Xie Y K.A peripheral mononeuropathy in rat that produces disorders of pain sensation like those seen in man[J]. Pai,1988,33:87-107. |
| [7] | Chaplan S R, Bach F W, Pogrel J W, et al. Quantitative assessment of tactile allodynia in the rat paw[J].J Neurosci Methods, 1994, 53(1):55-63. |
| [8] | Jasmin L, Kohan L, Franssen M, et al. The cold plate as a test of nociceptive behaviors:description and application to the study of chronic neuropathic and inflammatory pain models[J]. Pain, 1998, 75(2-3):367-82. |
| [9] | Dworkin R H, O'Connor A B, Backonja M, et al.Pharmacologic management of neuropathic pain:evidence-based recommendations[J].Pain,2007,132(3):237-51. |
| [10] | 刘 芬,刘 洁,陈 霞,等.氧化苦参碱的镇痛作用及其机制[J].吉林大学学报(医学版),2005,31(6):883-5. Liu F,Liu J,Chen X,et al. Analgesic action of oxymatrine and its mechanism[J].J Jilin Univ(Med Ed), 2005,31(6):883-5. |
| [11] | 张 娟,肖鲁伟,戴体俊,等.氧化苦参碱对脊髓c-fos表达和对阿片受体的作用研究[J].中华中医药学刊,2009,27(5):1077-9. Zhang J,Xiao L W,Dai T J,et al. Research the effect of oxymatrine on C-fos expression in the dorsal horn of the spinalCord and opiodi receptor[J].Chin Arch Tradit Chin Med, 2009,27(5):1077-9. |
| [12] | 姜 静,冯建伟,陈靖,等.氧化苦参碱的镇痛作用[J].中药药理与临床,2012,28(6):50-2. Jiang J,Feng J W,Chen J,et al.Analgesic effect of oxymatrine in different pain models[J]. Pharmacol Clin Chine Mat Med, 2012,28(6):50-2. |
| [13] | 吕晓强,邓扬鸥,杨 丽,等.氧化苦参碱镇痛作用及其阿片受体非相关性[J].中华中医药杂志,2014,29(2):564-7. Lyu X Q,Deng Y O,Yang L,et al. Analgesic effect of oxymatrine and its non-correlation with opioid receptors[J]. China J Tradit Chine Med Pharm, 2014,29(2):564-7. |
| [14] | 周 静,杨建平,王丽娜.信号转导通路在病理性疼痛中的研究进展[J].国际麻醉学与复苏杂志,2011,3(21):105-8. Zhou J,Yang J P,Wang L N. Research progress of signal transduction pathway in pathological pain[J]. Intern J Anesthesiol Resuscit, 2011,3(21):105-8. |
| [15] | 马传庚, 陈志武. 钙离子对疼痛调控的影响[J].中国药理学通报,1992, 8(1):78-80. Ma C G,Chen Z W. Effects of calcium ion on pain regulation[J]. Chin Pharmacol Bull, 1992, 8(1):78-80. |
| [16] | Ichikawa H, Gouty S, Regalia J, et al. Ca2+/Calmodulin-dependent protein kinase II in the rat cranial sensory ganglia[J]. Brain Res,2004,1005(1-2):36-43. |
| [17] | Fang L, Wu J,Lin Q, et al. Calcium/calmodulin-dependent protein kinase II contributes to spinal cord central sensitization[J]. Neurosci, 2002,22:4196-204. |
| [18] | Ogawa A, Dai Y, Yamanaka H, et al. Ca2+/calmodulin-protein kinaseII a in the trigeminal subnucleus caudalis contributes to neuropathic pain following inferior alveolar nerve transaction[J]. Exp Neurol,2005,192:310-9. |
| [19] | Ishda A, Kameshita I, Okuno S, et al. A novel highly specific and potent inhibitor of calmodulin-dependent protein kinase Ⅱ[J]. Biochem Biophys Res Commun, 1995, 212(3):806-12. |

