


2. 上海中医药大学中药研究所中药标准化教育部重点实验室, 中药新资源与质量标准综合评价国家中医药管理局重点研究室, 上海市复方中药重点实验室, 上海 201203
季莉莉(1976-),女,博士,研究员,博士生导师,研究方向:中药药理与毒理学,Tel:021-51322517,E-mail:lichenyue1307@126.com
2. The MOE Key Laboratory for Standardization of Chinese Medicines, the SATCM Key Laboratory for New Resources and Quality Evaluation of Chinese Medicines, and the Shanghai Key Laboratory of Complex Prescription, Institute of Chinese Materia Medica, Shanghai University of Traditional Chinese Medicine, Shanghai 201203, China
金银花为忍冬科植物Lonicera japonicae Thunb. 的干燥花蕾或带初开的花,自古被誉为是清热解毒的良药,常用于治疗热毒疮痈、咽喉肿痛、发热、发疹、发斑等各种热性病。已有研究表明,金银花具有抗菌、抗炎、抗病毒、保肝等诸多药效活性[1],其所含的主要活性成分为酚酸类、黄酮类等多酚类化合物[2]。
至2014年,全球约有3.87亿人罹患糖尿病,并且有预计糖尿病患者的数量在2030年将达到5.5亿(http://www.eatlas.idf.org/)。糖尿病一般可以分为两种类型:1型(胰岛素依赖型)和2型(胰岛素非依赖型),这两种类型的患者都将具有高血糖的症状。一项研究报告称大约1/3的糖尿病患者都患有DR,其中1/10的患者甚至有视力危险性视网膜疾病[3]。DR是一种常见的糖尿病微血管并发症,通常根据视网膜的病变程度主要分成两个阶段:早期糖尿病视网膜病即NPDR、晚期糖尿病视网膜病即增殖性DR (PDR)[4]。大约有35%~60%的DR患者最终都会发展成PDR,并在患病10年左右丧失视力[5]。本论文主要在STZ诱导NPDR小鼠动物实验模型上,观察了金银花水提物 (FL) 对STZ诱导小鼠NPDR进程中BRB渗漏、视网膜组织中炎性相关NF-κB信号通路的激活,以及神经小胶质细胞活化等的影响,从而探讨FL改善DR活性及其机制。
1 材料与试剂 1.1 试剂 Streptozotocin(链脲霉素,STZ),柠檬酸,柠檬酸三钠,多聚甲醛(均购自国药试剂);血糖试纸(Life Scan);IL-6/IL-1β ELISA试剂盒(RapidBio,CA);Iba1抗体 (GeneTax,CA),其它抗体均来自Cell Signaling Technology公司,二抗则购自Jackson Immuno Research;胞质/胞核蛋白抽提试剂盒、BCA试剂盒 (Thermo Scientific);化学发光液、PVDF膜均购自Millipore公司;其它试剂购自Sigma公司。金银花水提物是实验室前期制备所得,具体方法见文献[6]。
1.2 动物SPF级C57BL/6小鼠,♂,体质量18~22 g,购自中国科学院上海实验动物中心。动物合格证编号:SCXK(沪)2012-0002。饲养于上海中医药大学SPF级动物房,饲养1周后使用。温度(22±1)℃,湿度55%±5%,12 h光暗循环,饲料与水消毒后自由摄取。实验严格按照国家和上海中医药大学动物中心动物使用管理条例进行。
2 方法 2.1 STZ诱导小鼠糖尿病视网膜病模型的建立将0.1 mol·L-1柠檬酸溶液与柠檬酸三钠溶液以14 ∶11的比例混匀,调pH至4.3~4.5,待用。称取适量STZ粉末,避光溶解配成一定浓度后立即腹腔注射(1 mL·kg-1) 给予已禁食12 h的小鼠,STZ的最终剂量为55 mg·kg-1,连续注射5 d,另有一组腹腔注射溶媒对照作为正常对照组。1周后测小鼠血糖浓度,血糖值≥16.7 mmol·L-1(2 500 mg·L-1)视为糖尿病造模成功。将造模成功的小鼠随机分为3组:模型组,FL (50 mg·kg-1),FL (100 mg·kg-1)。每周检测体重变化,每两周检测血糖变化。STZ腹腔注射2个月后,每组取6只进行伊文氏蓝实验,其他剩余10只小鼠用戊巴比妥钠(30 mg·kg-1,腹腔)麻醉,从腹主动脉取血,并摘取眼球,迅速剥离视网膜组织后冷冻储存备用。
2.2 伊文氏蓝实验检测BRB渗漏情况配制0.2 g·L-1的伊文氏蓝溶解于PBS中,小鼠腹腔注射 (10 μL·g-1)伊文氏蓝溶液,注射后2 h用PBS灌注小鼠左心室彻底去除血管内残留的伊文氏蓝染料,然后摘取眼球,剥离视网膜组织置离心管中,将视网膜组织冷冻干燥后称取重量,接下来将视网膜组织与120 μL甲酰胺70℃孵育18 h提取伊文氏蓝染料,将该提取液在10 000×g,4℃离心2次,小心吸取上清,使用分光光度计在620 nm测定上清液的吸光度值。伊文氏蓝染料在甲酰胺提取物中的量是根据预先制作的标准曲线计算所得,结果以伊文氏蓝含量除以干燥视网膜重量的形式表达。
2.3 蛋白胞质胞核的提取使用胞质/胞核蛋白抽提试剂盒提取视网膜组织胞质和胞核部分的蛋白,同时使用BCA试剂盒测定蛋白浓度,并将所有样品统一到相等的蛋白浓度。
2.4 Western blot实验蛋白样本通过SDS-PAGE胶进行电泳,将胶上蛋白转印至PVDF膜,用含5%脱脂牛奶的TBST溶液封闭1 h后,加入一抗,4 ℃孵育过夜。洗去一抗后,与二抗室温孵育1 h,TBST洗去过量抗体后,加入化学发光液进行显像,结果用GeneTools图像分析软件进行定量。
2.5 ELISA实验全血于室温静置2 h后,于4℃,4 000×g离心15 min,分离上层血清,按照试剂盒说明书对血清中IL-6、IL-1β的含量进行测定。
2.6 数据分析实验数据均用  ± s表示,采用SPSS 16.0统计软件进行分析,以One-Way ANOVA 方式进行方差分析,两两比较采用LSD法。
± s表示,采用SPSS 16.0统计软件进行分析,以One-Way ANOVA 方式进行方差分析,两两比较采用LSD法。
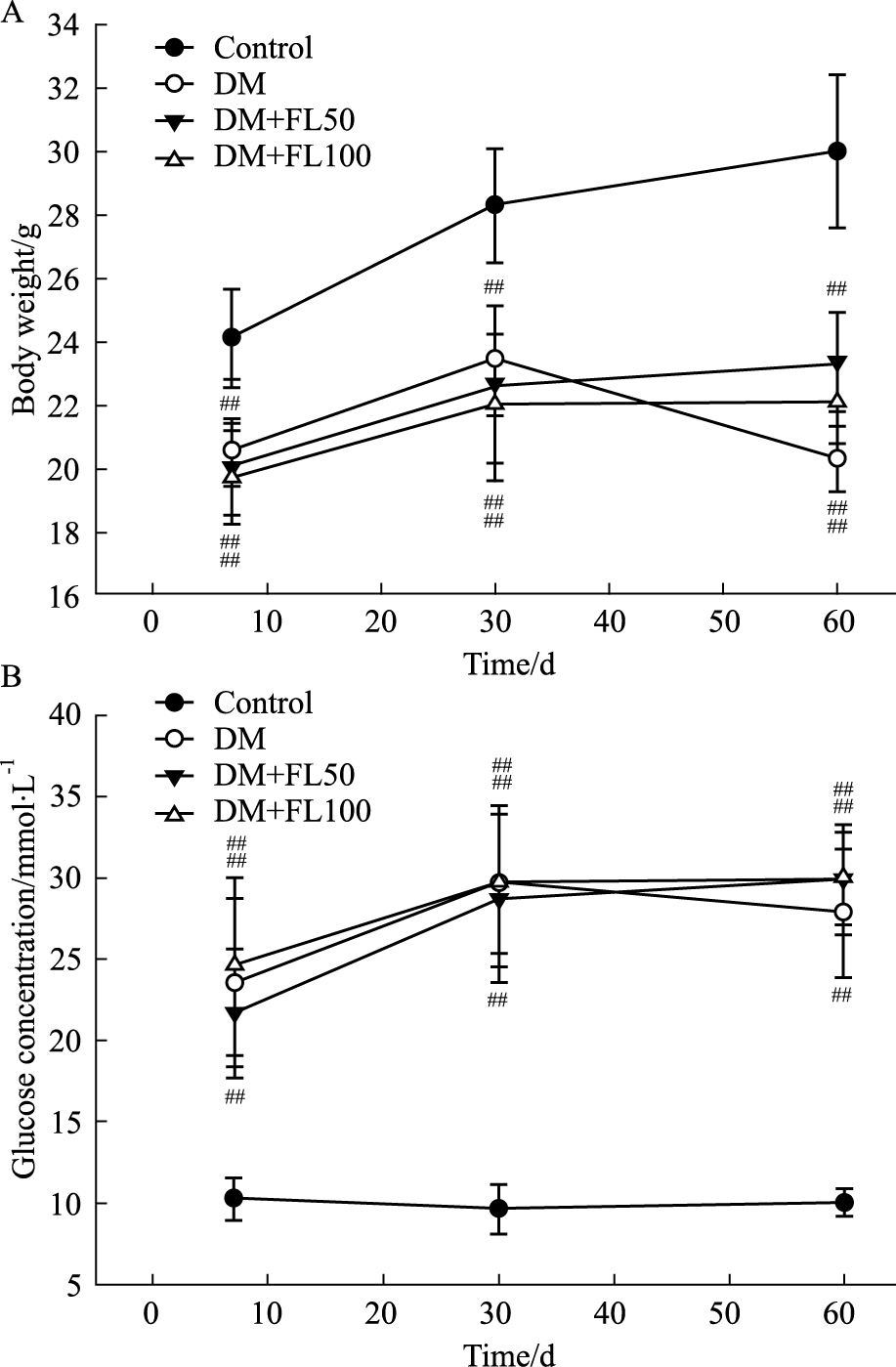
如Fig1A所示,除正常组以外其他组小鼠体重均有所下降,与正常组相比差异有显著性(P < 0.01),FL (50、100 mg·kg-1) 给药并不能逆转糖尿病小鼠降低的体重。Fig1B为不同组别小鼠血糖检测情况,由图可见除正常组以外,其他组小鼠的血糖均有所上升且与正常组相比差异均有显著性 (P < 0.01),FL (50、100 mg·kg-1) 给药并不能降低糖尿病小鼠升高的血糖值。
|
Fig 1
Effect of FL on body weight (A) and blood glucose contents (B) in STZ-induced diabetic mice(  ± s, n=10)
##P < 0.01 vs control. ± s, n=10)
##P < 0.01 vs control.
|
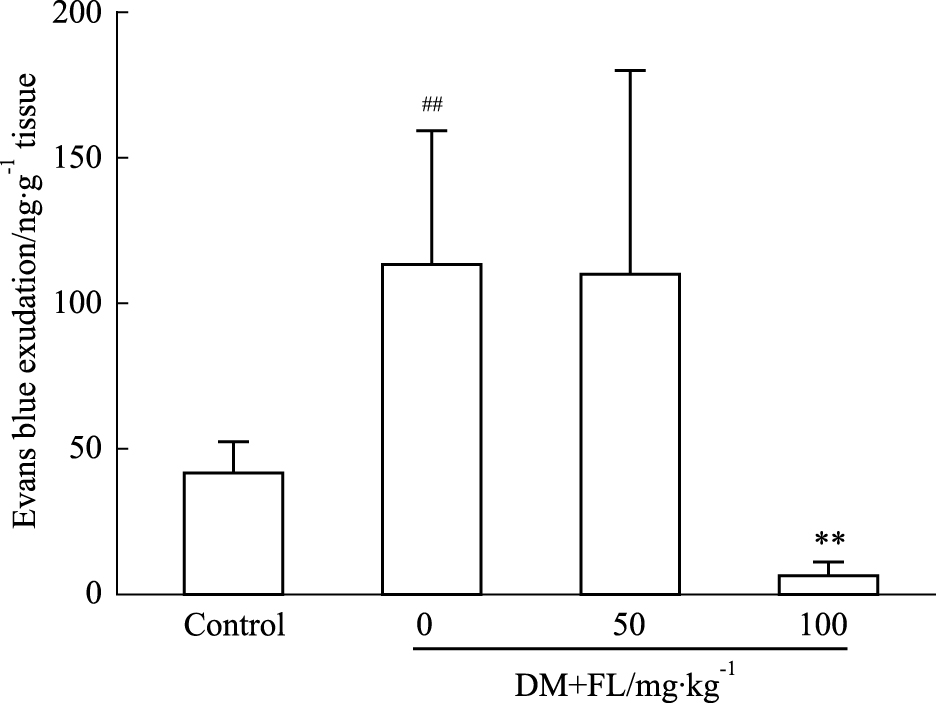
如Fig2所示,STZ诱导糖尿病小鼠出现BRB渗漏且与正常组相比差异有显著性(P < 0.01),而FL (100 mg·kg-1) 给药后能明显抑制BRB的渗漏(P < 0.01),FL (50 mg·kg-1) 给药则没有明显影响。
|
Fig 2
Effect of FL on BRB breakdown in STZ-induced
diabetic mice( ± s, n=6)
##P < 0.01 vs control; **P < 0.01 vs DM without FL. ± s, n=6)
##P < 0.01 vs control; **P < 0.01 vs DM without FL.
|
如Fig3A-B所示,STZ诱导糖尿病小鼠视网膜组织中NF-κB p65亚单位的表达在细胞核中明显增加 (P < 0.05),而FL (100 mg·kg-1)可以抑制增加的p65核转位 (P < 0.01)。但p65在视网膜组织胞质中的表达未发生变化。

|
Fig 3
Effect of FL on activation of retinal NF-κB signaling pathway in STZ-induced diabetic mice( ± s, n=4-6)
A:Effect of FL on NF-κBp65 translocation from cytoplasm into nucleus in retinas from STZ-induced diabetic mice. The representative blots of six independent experiments; B:Quantitative densitometric analysis of NFκBp65 in cytoplasm and nucleus; C:Effect of FL on the phosphorylation of p65, IκB, IKK in retinas from STZ-induced diabetic mice. The representative blots of at least four independent experiments; D:Quantitative densitometric analysis of phosphorylated p65, IκB, IKK in retinas. #P < 0.05, ##P < 0.01 vs control; *P < 0.05,**P < 0.01 vs DM without FL. ± s, n=4-6)
A:Effect of FL on NF-κBp65 translocation from cytoplasm into nucleus in retinas from STZ-induced diabetic mice. The representative blots of six independent experiments; B:Quantitative densitometric analysis of NFκBp65 in cytoplasm and nucleus; C:Effect of FL on the phosphorylation of p65, IκB, IKK in retinas from STZ-induced diabetic mice. The representative blots of at least four independent experiments; D:Quantitative densitometric analysis of phosphorylated p65, IκB, IKK in retinas. #P < 0.05, ##P < 0.01 vs control; *P < 0.05,**P < 0.01 vs DM without FL.
|
Fig3C-D的结果进一步表明,STZ诱导的糖尿病小鼠视网膜组织中p65,IKK,IκB发生磷酸化激活,与正常组比较差异有显著性(P < 0.05,P < 0.01),而FL (50、100 mg·kg-1) 均能不同程度的抑制NF-κB,IKK,IκB的磷酸化激活 (P < 0.05,P < 0.01)。
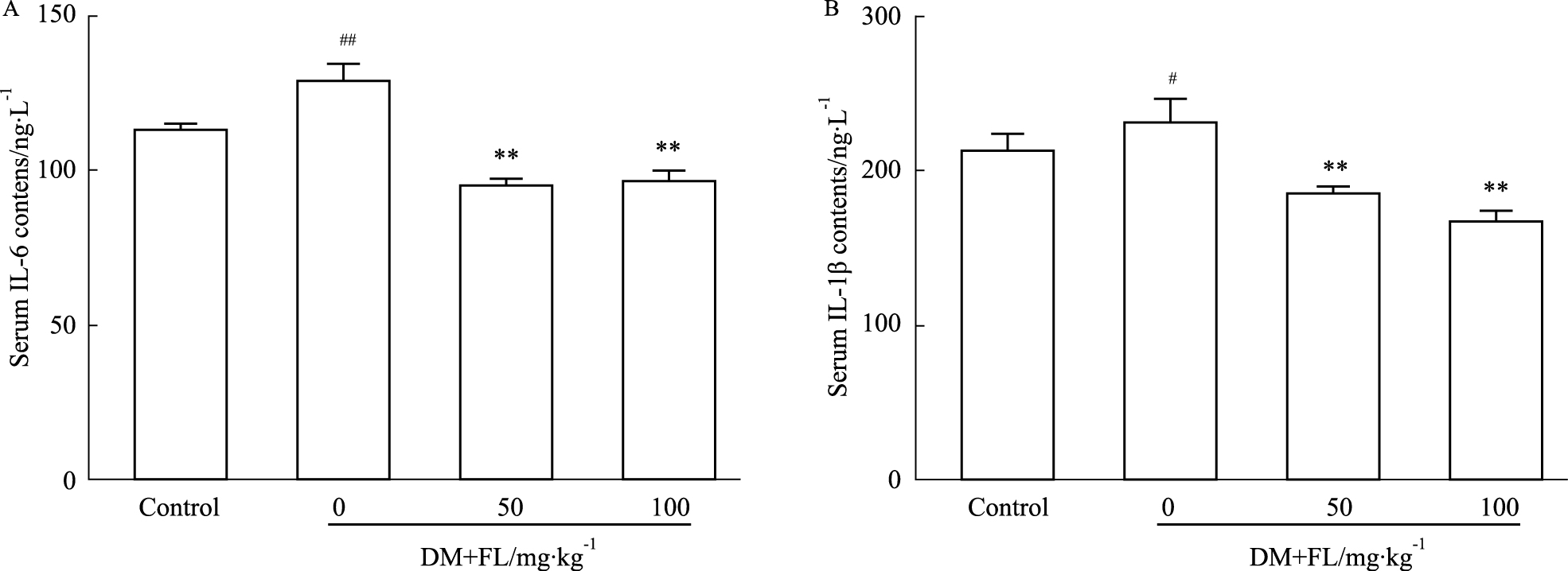
3.4 FL对STZ诱导糖尿病小鼠血清中炎性因子的影响如Fig4所示,STZ诱导糖尿病小鼠血清中IL-6和IL-1β的含量均明显上调 (P < 0.05,P < 0.01),而FL (50、100 mg·kg-1) 均能明显抑制血清中升高的IL-6和IL-1β的含量 (P < 0.01)。
|
Fig 4
Effect of FL on serum IL-6 and IL-1β contents in STZ-induced diabetic mice( ± s, n=8)
A: IL-6 contents; B: IL-1β contents. #P < 0.05, ##P < 0.01 vs control; **P < 0.01 vs DM without FL. ± s, n=8)
A: IL-6 contents; B: IL-1β contents. #P < 0.05, ##P < 0.01 vs control; **P < 0.01 vs DM without FL.
|
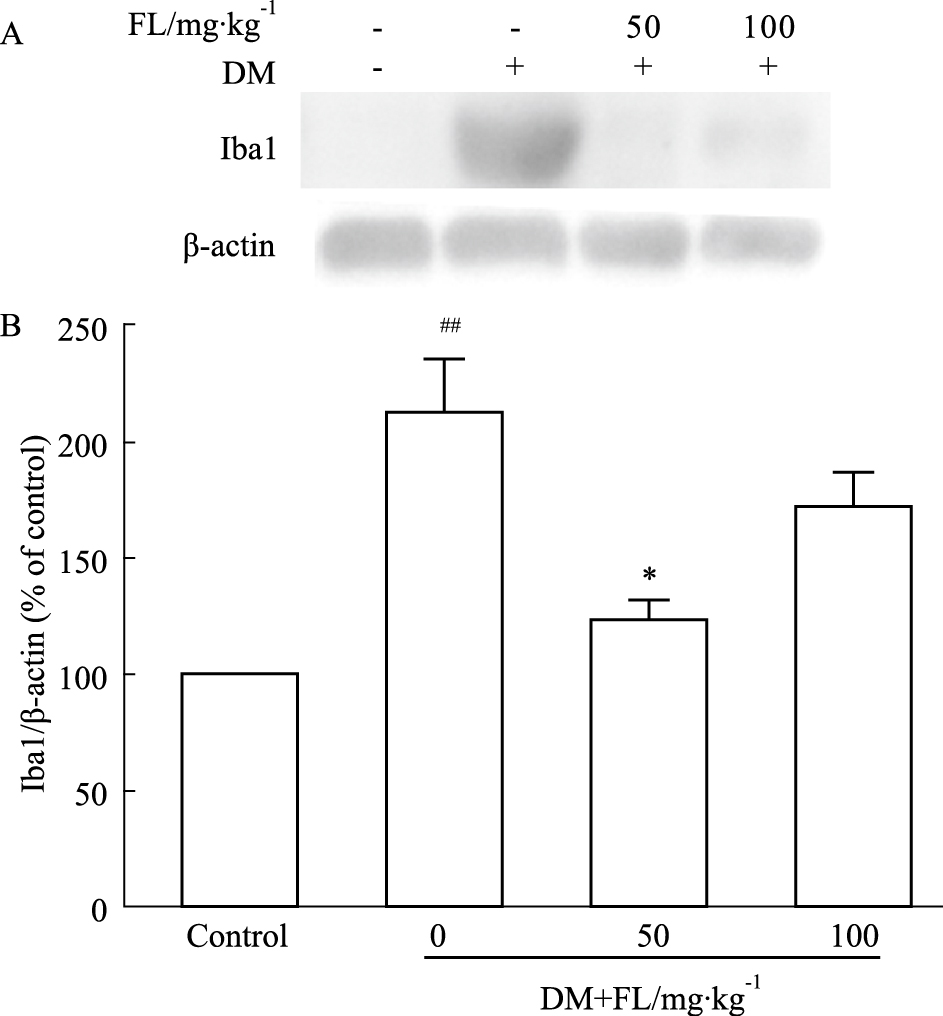
如Fig5A-B所示,STZ诱导糖尿病小鼠视网膜组织中Iba1表达明显增加,与正常组比较差异具有显著性(P < 0.01),而FL (50 mg·kg-1) 能降低升高的Iba1表达 (P < 0.05),FL (100 mg·kg-1) 也具有降低Iba1表达的趋势。
|
Fig 5
Effect of FL on retinal Iba1 expression in STZ-induced
diabetic mice( ± s, n=3)
A:The representative blots of three independent experiments;B:Quantitative densitometric analysis of Iba1 in retinas.
##P < 0.01 vs control; *P < 0.05 vs DM without FL. ± s, n=3)
A:The representative blots of three independent experiments;B:Quantitative densitometric analysis of Iba1 in retinas.
##P < 0.01 vs control; *P < 0.05 vs DM without FL.
|
我们的实验结果显示,FL给药后对STZ诱导糖尿病小鼠升高的血糖和降低的体重均没有明显逆转,说明FL给药对糖尿病病程中血糖和体重的改变无明显改善。DR是糖尿病最常见的并发症,属于微血管疾病的一种[7]。糖尿病视网膜病的早期会发生BRB的损伤,导致视网膜发生渗漏并引起黄斑水肿,这是造成DR患者失明的主要原因[8]。我们的研究发现,FL可以改善STZ诱导糖尿病小鼠BRB的渗漏,提示FL可以缓解DR的进程。
已有的研究发现,视网膜的炎性损伤在DR病程中发挥了重要的作用,特别是在糖尿病视网膜病的早期阶段即NPDR中具有重要调控作用[9]。转录因子NF-κB介导的炎性损伤信号通路是已知的调控炎症最重要的信号通路[10]。我们的结果发现FL可以抑制STZ诱导小鼠视网膜组织中NF-κB p65亚单位的核转位,说明FL可以抑制NF-κB的激活。IκB是NF-κB的抑制蛋白,其磷酸化激活可以导致NF-κB的激活,而IKK则可以诱导IκB的磷酸化,因此两者都参与调控了NF-κB的激活[11, 12]。我们的实验还发现FL可以抑制STZ诱导糖尿病小鼠视网膜组织中p65、IKK、IκB的磷酸化激活,从而进一步证实了FL可以抑制视网膜组织NF-κB炎性信号通路的激活。同时,我们的实验还发现FL可以降低糖尿病小鼠血清中升高的促炎因子IL-6,IL-1β的含量,这可能是因为FL抑制了NF-κB炎性信号通路所导致。已有研究认为促炎因子表达过量将会导致白细胞瘀滞,从而引发BRB的渗漏[9]。我们的实验发现FL可以降低促炎因子的表达,这将有助于改善BRB的渗漏。
Iba1蛋白是小胶质细胞的标志物,其表达增加预示了小胶质细胞的激活[13]。已有研究发现小胶质细胞会在DR的病程中发生活化激活,并在炎性损伤中发挥重要调控作用[14, 15]。我们的研究发现FL可以明显抑制STZ诱导糖尿病小鼠视网膜组织中升高的Iba1表达,提示FL可以抑制DR病变过程中神经小胶质细胞的活化。
综上所述,我们的研究发现FL可能通过抑制神经小胶质细胞的活化,抑制NF-κB介导的炎性信号通路,缓解视网膜的炎性损伤和BRB的渗漏,从而发挥改善DR的药效活性。本研究结果为清热解毒中药金银花用于DR的预防和治疗奠定了良好的实验依据。
(致谢:本论文的全部研究工作在上海中医药大学中药研究所季莉莉研究员课题组实验室完成,在此予以感谢。)
| [1] | Shang X, Pan H, Li M, et al. Loniceria japonica Thunb:ethnopharmacology, phytochemistry andpharmacology of an important traditional Chinese medicine[J]. J Ethnopharmacol, 2011, 138 (1):1-21. |
| [2] | 张小娜,童 杰,周衍晶,等. 忍冬属药材药效成分及药理作用研究进展[J]. 中国药理学通报,2014,36(8):1049-51. ZHANG X N, TONG J,ZHOU Y J,et al. Studies on medicinal ingredients and pharmacological effects of Lonicera[J]. Chin Pharmacol Bull,2014,36(8):1049-51. |
| [3] | Saaddine J B. Projection of diabetic retinopathy and other major eye diseases among people with diabetes mellitus:United States, 2005-2050[J]. Arch Ophthalmol, 2008, 126 (12):1740-7. |
| [4] | Wilkinson C P, Ferris III F L, Klein R E, et al. Global Diabetic Retinopathy Project Group, Proposed international clinical diabetic retinopathy and diabetic macular edema disease severity scales[J]. Ophthalmology, 2003, 110 (9):1677-82. |
| [5] | Wong T Y. Rates of progression in diabetic retinopathy during different time periods:a systematic review and meta-analysis[J]. Diabetes Care, 2009, 32 (12):2307-13. |
| [6] | Jiang P, Sheng Y C, Chen Y H, et al. Protection of Flos Lonicerae against acetaminophen-induced liver injury and its mechanism[J]. Environ Toxicol Pharmacol, 2014, 38(3):991-9. |
| [7] | Antonetti D A. Diabetic retinopathy[J]. N Engl J Med, 2012, 366(13):1227-39. |
| [8] | Cheung N, Mitchell P, Wong T Y. Diabetic retinopathy[J]. Lancet, 2010, 376 (9735):124-36. |
| [9] | Adamis A P. Is diabetic retinopathy an inflammatory disease[J]? Br J Ophthalmol, 2002, 86 (4):363-5. |
| [10] | Baeuerle P A, Henkel T. Function and activation of NF-kappa B in the immune system[J]. Annu Rev Immunol, 1994, 12:141-79. |
| [11] | Baeuerle P A, Baltimore D. I kappa B:a specific inhibitor of the NF-kappa B transcription factor[J]. Science, 1988, 242(4878):540-6. |
| [12] | Dyson H J, Komives E A. Role of disorder in IκB-NFκB interaction[J]. IUBMB Life, 2012, 64 (6):499-505. |
| [13] | Imai Y, Ibata I, Ito D, et al. A novel gene iba1 in the major histocompatibility complex class III region encoding an EF hand protein expressed in a monocytic lineage[J]. Biochem Biophys Res Commun, 1996, 224 (3):855-62. |
| [14] | Chen X, Zhou H, Gong Y, et al. Early spatiotemporal characterization of microglial activation in the retinas of rats with streptozotocin-induced diabetes[J]. Graefes Arch Clin Exp Ophthalmol, 2015, 253 (4):519-25. |
| [15] | Grigsby J G, Cardona S M, Pouw C E, et al. The role of microglia in diabetic retinopathy[J]. J Ophthalmol, 2014, 2014:705783. |

